替硝唑中杂质亚硝酸根的离子色谱法测定
2021-08-11潘波刘丽娟陈玉双郑玉林
潘波 刘丽娟 陈玉双 郑玉林

摘 要 目的:建立替硝唑原料药中杂质亚硝酸根的测定方法。方法:采用离子色谱法测定,Dionex IonPac AS19,3.5 mm×250 mm色谱柱,KOH溶液梯度洗脱。结果:亚硝酸根与替硝唑可达到基线分离。亚硝酸根在0.025~1.000 mg/ml范围内线性关系良好,检测限(LOD)为0.010 mg/ml,定量限(LOQ)为0.025 mg/ml。结论:该法操作简便,重现性好,结果准确可靠,可以用于替硝唑原料药中基因毒性杂质亚硝酸根的测定。
关键词 替硝唑 亚硝酸根 离子色谱法
中图分类号:R978.19; R917 文献标志码:A 文章编号:1006-1533(2021)11-0078-03
Determination of impurity nitrite in tinidazole by ion chromatography
PAN Bo1*, LIU Lijuan2, CHEN Yushuang2, ZHENG Yulin2**
(1. Shanghai Sinopharm Holding Co., Ltd., Shanghai 200023, China; 2. Shanghai Fenglin Biological Technology Co., Ltd., Shanghai 201210, China)
ABSTRACT Objective: To establish a method for the determination of nitrite in tinidazole bulk drug. Methods: The ion chromatography (IC) was carried out on a Dionex IonPac AS19 column with KOH solution as gradient elution. Results: Nitrite could be completely separated from tinidazole and its stranded curve showed good linearization over the range of 0.025-1.000 mg/ml with detection limit 0.010 mg/ml and quantitation limit 0.025 mg/ml. Conclusion: This method is simple, reproducible and accurate and can be used for the determination of nitrite in tinidazole bulk drug.
KEy WORDS tinidazole; nitrite; ion chromatography
基因毒性杂质或遗传毒性杂质(genotoxic impurity,GTI)可直接或间接损伤细胞中的DNA,诱发基因突变,具有致癌可能或者倾向。各国的法规机构,如人用药品注册技术要求国际协调会(International Conference on Harmonization of Technical Requirements for Registration of Pharmaceutical for Human Use,ICH)[1]、美国卫生与人类服务部 (U.S. Department of Health and Human Services,DHHS)[2]、欧洲药品管理局(EMA)[3]等都对基因毒性杂质进行了明确要求,众多制药企业在新药研发过程中也越来越关注基因毒性杂质的控制和检测。
替硝唑是一种硝基咪唑类抗菌药,用于治疗各种厌氧菌感染,如败血症、骨髓炎、腹腔感染、盆腔感染、肺支氣管感染、肺炎、鼻窦炎、皮肤蜂窝组织炎、牙周感染及术后伤口感染,也可作为结肠直肠手术、妇产科手术及口腔手术等的术前预防用药及肠道外阿米巴病、阴道滴虫病、贾第虫病、加得纳菌阴道炎等的治疗[4-6]。替硝唑的合成过程中用到硝酸,因此在替硝唑原料药生产贮存过程中有可能生成亚硝酸根,须严格控制其毒理学关注阈值 (threshold of toxicological concern,TTC)[1]。ICH发布基因毒性杂质的最大摄取量为1.5 mg/d。
目前亚硝酸根的检测方法通常有紫外分光光度法[7],重氮偶联反应双模式方法[8],离子色谱法[9-10]等。这些方法各有优缺点,但大多不仅费时费力,还会造成环境污染,如紫外分光光度法作为经典方法需要盐酸萘乙二胺衍生,会引入重金属污染物镉,对环境危害很大。重氮偶联反应双模式方法,比色法专属性差,会有离子干扰。离子色谱法[9]通过选择高容量阴离子交换柱,增大进样体积,以检测水中的亚硝酸盐,但通过增大本底量,容易引入氯离子和其他离子干扰;而武伦玮等[10]报道的离子色谱改进方法,前处理复杂,需要加入乙酸锌和亚铁氰化钾,会引入重金属污染物。为了克服以上困难,本研究建立了简便准确的离子色谱法,可准确灵敏地测定原料药中基因毒性杂质亚硝酸根的含量。
1 材料和方法
1.1 仪器与试药
AQ1200离子色谱仪、Dionex IonPac AS19色谱柱(3.5 mm×250 mm,4 μm)(赛默飞公司)。
原料药(X制药有限公司,含量99.9%、99.9%和100.1%,批号F-20190801、F-20190802和F-20190803);国家标准样品GSB 04-2839-2011、亚硝酸根单元素标准溶液(1 000 mg/ml),购自国家标准物质中心网。
1.2 方法
1.2.1 溶液配制
1)工作标准液 精密移取亚硝酸根标准溶液0.5 ml或0.1 ml置10 ml容量瓶中,加超纯水至刻度,摇匀,配制成亚硝酸根质量浓度为50 mg/ml或10 mg/ml的工作标准液1和2。
2)供试品溶液 精密称量供试品0.25 g置于50 ml量瓶中,加入40 ml超纯水,超声(500 W,400 kHz)15 min并放冷至室温,重复超声操作5次后用超纯水稀释至刻度,摇匀,过滤,取续滤液作为供试品溶液(2.5 mg/ml)。
3)线性溶液 精密量取工作标准液,用超纯水配制成质量浓度分别为0.025、0.050、0.100、0.250、0.500、1.000 mg/ml的溶液,分别作为10%(定量限浓度)~ 400%限度水平检测用对照品溶液。
4)准确度溶液 精密称定供试品0.25 g 3份,分别置50 ml量瓶中,加入0.20、0.25、0.30 ml工作标准液1溶液,加入40 ml超纯水,超声15 min并放冷至室温,重复超声操作5次,用超纯水稀释至刻度,摇匀,过滤,取续滤液分别作为80%、100%、120%限度水平检测用准确度溶液。
5)稳定性溶液 精密称定供试品0.25 g,置50 ml量瓶中,加入0.25 ml工作标准液1溶液,加入40 ml超纯水,超声15 min并放冷至室温,重复超声操作5次,用超纯水稀释至刻度,摇匀,过滤,作为稳定性检测用溶液。
1.2.2 色谱条件
淋洗液:KOH溶液;梯度程序见表1。流速1.0 ml/min,柱温30 ℃,进样量25 μl。
2 结果
2.1 线性
以浓度为横坐标,峰面积为纵坐标,按最小二乘法进行线性回归,得回归方程为y=0.885 2x-0.006 5,相关系数r为0.999 9。结果表明,亚硝酸根在0.025~1.000 mg/ml范围内线性关系良好,亚硝酸根检测限(LOD)为0.010 mg/ml,定量限(LOQ)为0.025 mg/ml。
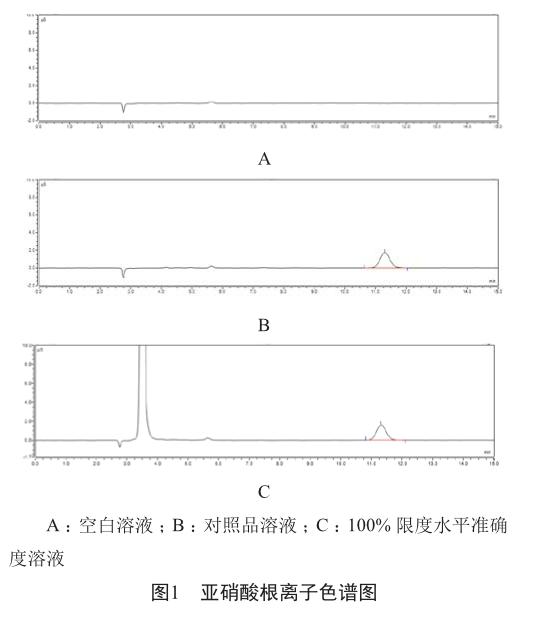
2.2 专属性试验
色谱图显示,空白溶液中亚硝酸根出峰处无干扰;供试品溶液中亚硝酸根出峰处无杂质干扰;0.250 mg/ml线性标准溶液连续6针进样,峰面积RSD为0.2%。系统适用性(峰面积RSD≤2.0%)和专属性均符合要求。
2.3 准确度试验
按准确度试验要求,对3个限度水平的准确度溶液进行离子色谱测定,计算得平均回收率(n=9)为97%,RSD为4.9%。符合回收率90%~110%、RSD<15%的要求。
2.4 精密度、重复性和稳定性试验
按精密度、重复性和稳定性试验要求,各制备6份供试品溶液进行离子色谱测定,其中精密度和重复性测试的RSD分别为4.8%和5.2%,符合<15.0%的要求。工作标准液2(10 mg/ml)及稳定性溶液于室温放置8 h内较稳定。
2.5 样品测定
从3批原料药中取样测定,计算得3批样品中亚硝酸根检出量分别为0.027、0.032 和0.036 mg/ml。
3 讨论
亚硝酸根限度值:按亚硝酸钠CPDB(潜在致癌物数据库)毒性数据计算(TD50线性外推法)[9],取大鼠的限度值167 mg/(kg·d),计算亚硝酸根限度,则替硝唑中亚硝酸根限度为55.68 mg/ml。按此标准判断,所选用的原料中亚硝酸根检出量远远小于限度。
本研究建立的方法与传统的亚硝酸根测定方法(比色法、紫外分光光度法)比较,灵敏度更高,测试更准确。与已报道的离子色谱法相比,前处理简单,环保,准确度和灵敏度更适用于药物中的基因毒性杂质研究;本研究只对一种替硝唑的基因毒性杂质进行了研究,今后会根据合成路线,对多种基因毒性杂质开展研究。
参考文献
[1] ICH guideline M7 on assessment and control of DNA reactive(mutagenic) impurities in pharmaceuticals to limit potential carcinogenic risk[EB/OL]. (2015-08-25)[2020-09-29]. https:// www.ich.org/page/multidisciplinary-guidelines#7-2.
[2] Guidance for Industry Genotoxic and Carcinogenic Impurities in Drug Substances and Products: Recommended Approaches- Guidance[EB/OL]. (2008-12-03)[2020-09-29]. https:// downloads.regulations.gov/FDA-2008-D-0629-0002/ attachment_1.pdf.
[3] EMEA. Guidelines on the limits of genotoxic impurities[EB/ OL]. (2006-06-28)[2020-09-29]. https://www.ema.europa.eu/ en/documents/scientific-guideline/guideline-limits-genotoxicimpurities_en.pdf.
[4] 柏干榮. 替硝唑的药理与临床应用进展[J]. 中国药房, 1998(1): 42-43.
[5] 王忠, 于淮, 张林, 等. 复方替硝唑喷雾制剂的制备及临床应用[J]. 中国医院药学杂志, 2000(12): 54-55.
[6] 董勤, 宁兰, 郭治. 替硝唑的临床应用及制剂发展[J]. 中国新药与临床杂志, 2001, 12(5): 394-395.
[7] 袁艳丽, 韩衍青, 李新丽, 等. 分光光度法测定口服补液盐散中亚硝酸根含量[J]. 山东化工, 2020, 49(22): 71-73.
[8] 蔡荣源, 陆德婵, 翁婷炜, 等. 利用重氮偶联反应双模式快速检测痕量亚硝酸盐[J]. 福建师范大学学报(自然科学版), 2021, 37(3): 48-53.
[9] 王文雷, 曹燕燕, 岳太星. 熟水中超痕量亚硝酸盐含量测定[J]. 质量安全与检验检测, 2020, 30(4): 19-21.
[10] 武伦玮, 胡雪, 段国霞, 等. 离子色谱法测定乳制品中亚硝酸盐和硝酸盐含量的方法改进[J]. 乳业科学与技术, 2020, 43(6): 20-25.
