可注射型富血小板纤维蛋白对人根尖牙乳头干细胞生物学行为的影响
2021-08-11曹子蔚蒋备战
潘 菁,曹子蔚,管 贇,蒋备战
年轻恒牙易受龋病、外伤、感染等因素影响导致牙髓坏死甚至是根尖周炎。牙髓再生作为治疗年轻恒牙牙髓坏死的新方法,有诱导根管壁增厚、根尖闭合、神经血管再生等优势,可以获得较为理想的治疗效果[1]。
富血小板纤维蛋白(platelet rich fibrin,PRF)是二代血小板浓缩产品,具有调节免疫应答和促进组织愈合的作用,Choukroun等[2]在此基础上提出可注射型富血小板纤维蛋白(injectable platelet rich fibrin,iPRF)。iPRF的三维纤维蛋白网中富含血小板、白细胞、Ⅰ型胶原蛋白、骨钙素和多种生长因子,可成为促进软硬组织愈合的良好载体[3]。
本实验拟探究iPRF的生长因子含量及其对根尖牙乳头干细胞的增殖、迁移和成骨/成牙向分化的影响,为后续的牙髓再生治疗提供实验基础。
1 材料与方法
1.1 主要材料和仪器
胰酶、α-MEM不完全培养基、青霉素/链霉素、PBS、茜素红染色液(凯基,中国);胎牛血清(Gibco,美国);细胞培养皿、离心管、细胞培养板、Transwell板(Coring,美国);CCK-8试剂盒(翊圣,中国);ELISA试剂盒(博士德,中国);倒置显微镜(Nikon,日本);细胞总RNA提取试剂盒、实时定量荧光聚合酶链反应(quantitative real time polymerase chain reaction,qRT-PCR)试剂盒(TaKaRa,日本);胶原酶、地塞米松、抗坏血酸、β-甘油磷酸钠(Sigma,美国)。
1.2 细胞培养
收集因阻生拔除的第三磨牙(根尖孔未闭合),剪碎根尖部软组织并用胰蛋白酶消化处理,置于37 ℃、5% CO2的培养箱中培养获得人根尖牙乳头干细胞(human stem cells from apical papilla, hSCAPs)。培养基由10%胎牛血清、1%青霉素/链霉素和α-MEM不完全培养基制成。本实验所获取的hSCAPs已经过课题组前期鉴定[4],选取第4代hSCAPs用于后续实验。
1.3 可注射型富血小板纤维蛋白提取液(injectable platelet rich fibrin extracts,iPRFe)的制备
本实验经过同济大学伦理委员会批准(伦理审查编号:2018-012),所有志愿者知情同意。选取健康男性8例,年龄25~40岁,血常规示血小板计数正常。分别抽取志愿者10 mL静脉血,以700 r/min的速率低温离心3 min,上层即为iPRF,吸取上层液体状物质冻干成膜,研磨成粉,浸入50 mL α-MEM不完全培养基中,24 h后通过0.22 μm滤器过滤,得到液体定义为1×iPRFe,放入-20 ℃冰箱待用。
1.4 ELISA法测定iPRFe相关因子含量
取出待用iPRFe,按ELISA试剂盒说明书分别检测iPRFe中血小板衍生生长因子-BB(platelet derived growth factor-BB,PDGF-BB)、胰岛素样生长因子1(insulin-like growth factor 1,IGF1)和转化生长因子β1(transforming growth factor β1,TGFβ1)的含量。测定450 nm吸光度值,并根据曲线计算相应结果。
1.5 iPRFe对hSCAPs增殖的影响
将1×iPRFe用α-MEM不完全培养基分别稀释至1/2×、1/4×和1/8×浓度,并加入10%胎牛血清和1%青霉素/链霉素制成条件培养液,对照组不含iPRFe。将hSCAPs以2×103个/孔接种于96孔板,待细胞贴壁24 h后换用条件培养液。每组设置6个复孔,每孔200 μL液体,于37 ℃、5% CO2培养箱中培养,隔天换液。分别于第1、3、5天取出检测,弃去原培养液,PBS清洗3次,加入含有10% CCK-8试剂的100 μL PBS,孵育1 h后取出,酶标仪测定各孔450 nm处吸光度值,记录结果。选取促进hSCAPs增殖最佳浓度的iPRFe进行后续实验的比较。
1.6 Transwell实验检测iPRFe对hSCAPs迁移的影响
实验分为2组:对照组(由10%胎牛血清、1%青霉素/链霉素和89% α-MEM不完全培养基制成的培养基培养)和iPRFe组(含10%胎牛血清、1%青霉素/链霉素和促进增殖最佳浓度的iPRFe培养液培养)。常规将hSCAPs细胞悬液以2×105个/mL的密度接种至6孔Transwell板的上室,下室加入各组条件培养基,于37 ℃、5%的CO2培养箱中培养24 h。取出Transwell小室,PBS冲洗,4%多聚甲醛溶液固定,棉拭子擦去膜上面未迁移的细胞,PBS冲洗,0.1%结晶紫染色。显微镜观察并拍照。3%醋酸溶液脱色,酶标仪测定各孔570 nm处吸光度值,记录结果。
1.7 茜素红检测iPRFe对hSCAPs矿化的影响
配制矿化诱导条件培养基(osteogenic medium,OM):α-MEM不完全培养基、10%胎牛血清、1%青霉素/链霉素、终浓度分别为10 mmol/L的β-甘油磷酸钠、0.05 mmol/L的抗坏血酸和0.1 μmol/L的地塞米松。实验分为3组:对照组(空白细胞培养液)、OM组(仅含OM)和iPRFe组(OM+iPRFe)。将hSCAPs接种至6孔细胞培养板内,待细胞融合至80%,分别加入各组诱导培养基,每2 d换液,分别培养7、14、21 d。取出细胞培养板,PBS冲洗,4%多聚甲醛溶液固定,茜素红染色,PBS冲洗,拍照。1 mmol/L氯化十六烷基吡啶脱色,紫外分光光度仪检测562 nm处吸光度值,记录结果。
1.8 qRT-PCR检测成骨/成牙向分化相关基因的表达
实验分组同1.7。按1.7方法矿化诱导培养7、14、21 d后用TRIzol分别提取OM组、iPRFe组与对照组hSCAPs的总RNA,逆转录合成cDNA。检测碱性磷酸酶(alkaline phosphatase,ALP)、牙本质基质蛋白1 (dentin matrix protein 1,DMP1)、牙本质涎磷蛋白(dentin sialophosphoprotein,DSPP)和骨钙素(osteocalcin, OCN)的mRNA表达情况。所用引物由生工生物工程(上海)股份有限公司合成,引物序列见表1。
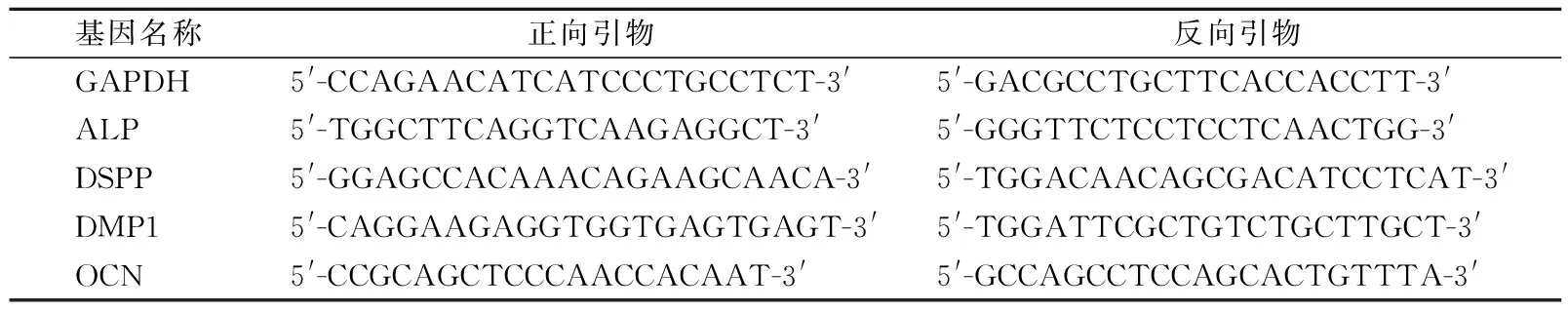
表1 GAPDH、ALP、DSPP、DMP1、OCN引物序列Tab.1 Primer sequences of GAPDH, ALP, DSPP, DMP1, OCN
1.9 统计分析
相同实验重复3次,实验数据为均值±标准差,由SPSS 20.0软件进行单因素方差分析,P<0.05为差异具有统计学意义。
2 结 果
2.1 iPRFe的因子含量
ELISA结果显示,iPRFe中有PDGF-BB、TGFβ1和IGF1等细胞因子,且TGFβ1和IGF1的含量较高,而PDGF-BB的含量则相对较低(图1)。
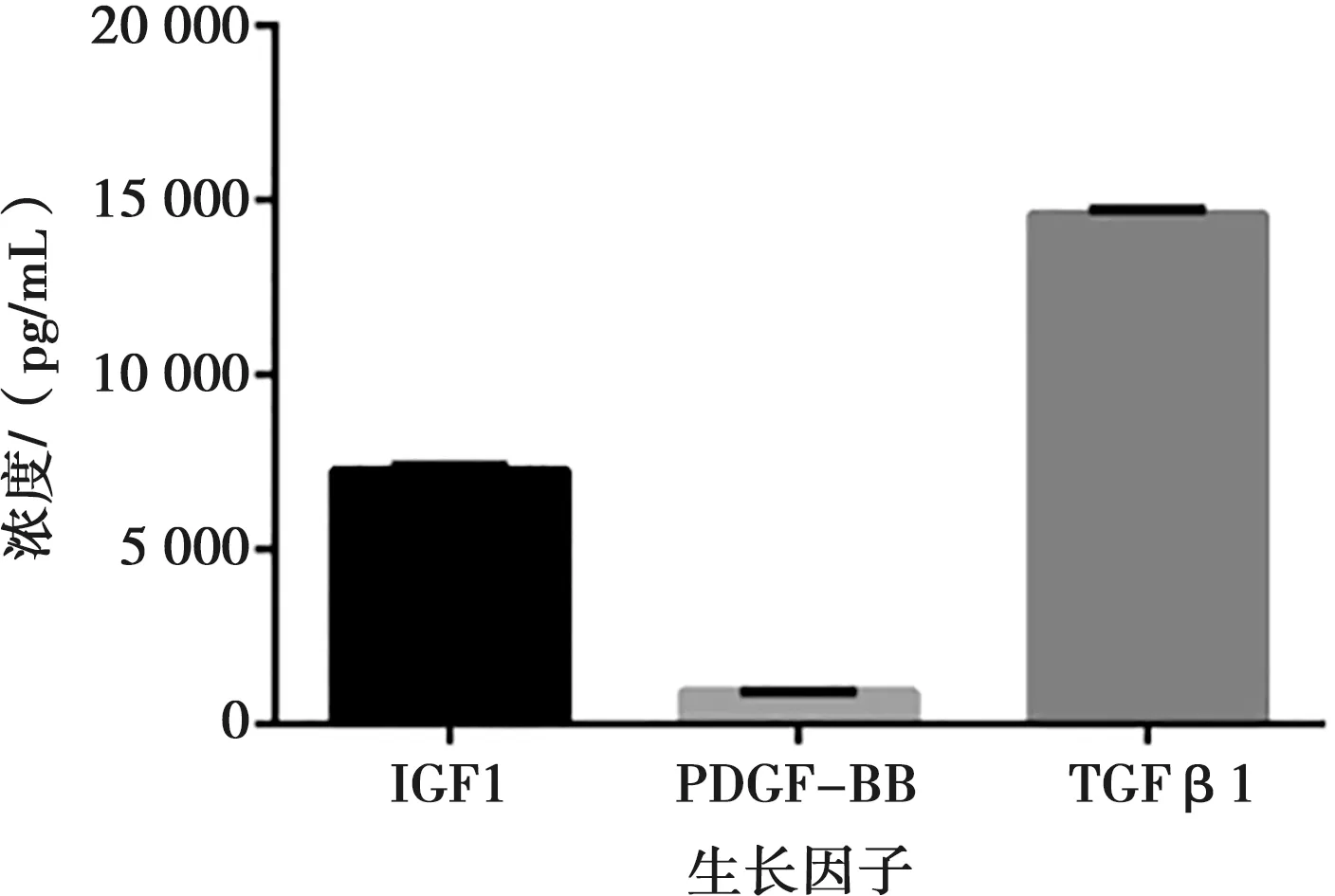
图1 iPRFe生长因子含量Fig.1 The content of growth factors in iPRFe
2.2 iPRFe对hSCAPs增殖的影响
将hSCAPs培养1、3、5 d后发现,所有浓度的iPRFe均明显促进细胞增殖;与对照组相比,浓度为1×组明显促进细胞增殖,但低于1/4×组(P<0.05),与其余组间无差异(P>0.05)。1 d和5 d时,在iPRFe浓度1/4×时,细胞增殖量较浓度为1/2×明显增加(P<0.05);而浓度为1/8×时,细胞增殖量比浓度为1/4×时稍低,差异有统计学意义(P<0.05)。因此在所有浓度中,1/4×iPRFe对hSCAPs的增殖促进效果最佳(图2)。
2.3 iPRFe对hSCAPs迁移的影响
将hSCAPs置于1/4×浓度的iPRFe中培养24 h,观察细胞迁移量。结果可见iPRFe组(图3B)细胞迁移数目明显多于对照组(图3A)。定量结果显示,iPRFe组的细胞迁移量明显高于对照组,差异具有统计学意义(P<0.05)(图3C)。
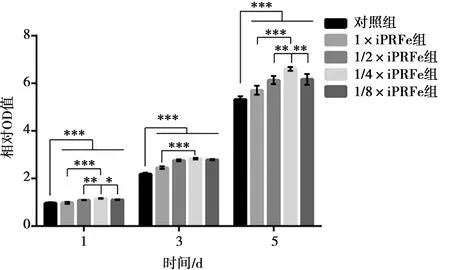
*:P<0.05,**:P<0.01,***:P<0.001
2.4 iPRFe对hSCAPs矿化的影响
hSCAPs在经过矿化诱导培养后,7 d可见iPRFe组的矿化结节染色均比对照组和OM组的更深。随着时间推移,OM组的染色逐渐变深,且比对照组明显;iPRFe组的矿化结节染色比对照组和OM组的深染更明显。定量结果显示,7、14、21 d时OM组和iPRFe组的染色均明显高于对照组,差异具有统计学意义(P<0.05),且相同时间点,iPRFe组比OM组深染(图4)。
2.5 iPRFe对成骨/成牙向分化相关基因表达的影响
hSCAPs经过矿化诱导7 d,OM组和iPRFe组的ALP、DMP1和DSPP的表达均升高,iPRFe组的OCN表达明显升高,但OM组OCN表达与对照组相比无明显差异;除DSPP和OCN外,iPRFe组的升高量明显高于OM组(P<0.05)。诱导培养中后期14 d及21 d时,iPRFe组的ALP、DMP1、DSPP和OCN的表达均明显升高,且高于OM组(P<0.05)(图5)。
3 讨 论
成功的牙髓再生,离不开三个基本要素,即种子细胞(干细胞)、支架材料和生长因子。目前已有多种血小板浓缩制品,包括PRF、浓缩生长因子等,含有各种活性因子,同时具有三维网状支架结构,且无需添加任何其他生物来源制剂,避免了伦理道德争议和疾病传播的风险,可以作为牙髓再生较为理想的选择。研究表明,PRF和浓缩生长因子均能促进牙髓再生[5-6]。PRF是凝胶状,应用于根管内需要经过一定的修剪,而iPRF在具有PRF和浓缩生长因子相似优点的同时,临床操作的便利性大大提升。
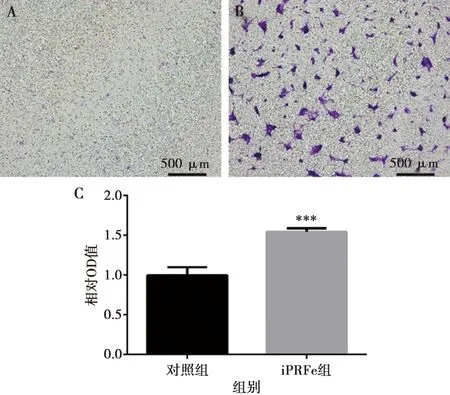
A:对照组Transwell结果;B:iPRFe组Transwell结果;C:对照组和iPRFe组hSCAPs细胞迁移结果分析;***:与对照组相比,P<0.001
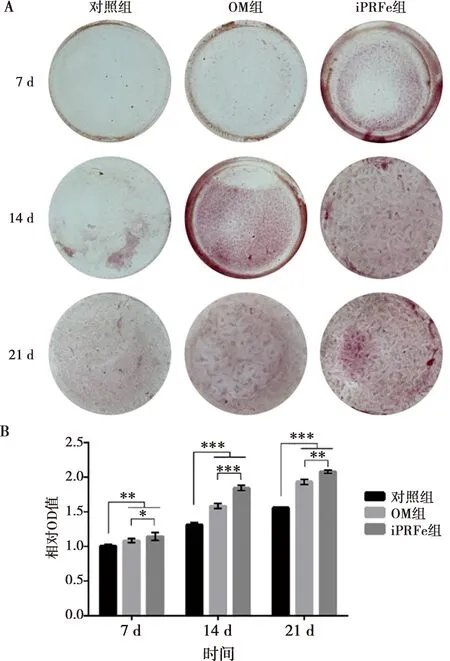
A:不同培养液培养hSCAPs茜素红染色结果;B:茜素红染色结果的矿化水平分析,*:P<0.05,**:P<0.01,***:P<0.001

A:ALP表达水平;B:DMP1表达水平;C:DSPP表达水平;D:OCN表达水平;*:P<0.05,**:P<0.01,***:P<0.001
hSCAPs是基于内源性细胞归巢模式牙髓再生治疗中的主要干细胞来源之一,存在于未发育完全的恒牙根尖周组织中,是一种具有自我更新能力和多向分化潜能的成体间充质干细胞。与其他牙源性干细胞相比,hSCAPs的增殖率高于人牙髓干细胞和人牙周膜干细胞[7-8]。基质细胞衍生因子-1、TGFβ1等趋化因子可促进hSCAPs的迁移,在基于细胞归巢再生的根管治疗中均可能得到临床应用[9-10]。因此,本实验研究了iPRFe对hSCAPs增殖、迁移和矿化的影响,结果表明iPRF在牙髓再生中可能有较为理想的效果。
PDGF-BB是一种重要的促有丝分裂因子,对单核细胞、中性粒细胞、间充质干细胞及成骨细胞产生趋化作用,促进组织愈合。IGF1是牙体及骨组织修复的关键生长因子,可调控间充质干细胞的成牙及成骨向分化[11]。TGFβ1作为骨形成和吸收的调节因子,可通过上调ALP水平促进钙化沉积[12],也能促进细胞进一步分泌细胞外基质相关成分。本实验中,iPRFe含有较高浓度的TGFβ1和IGF1,推测其与iPRFe促进hSCAPs的成牙及成骨向分化有关,但PDGF-BB含量相对较低,提示hSCAPs的增殖、迁移可能还与其他生长因子相关。
在本实验中,iPRF能促进hSCAPs的增殖和迁移。1、5 d时,1/8×浓度的iPRFe促增殖效果低于1/4×浓度的iPRFe,可能与VEGF、PDGF、碱性成纤维细胞生长因子等生长因子含量下降有关[13]。在所选浓度中,浓度为1/4×的促增殖效果最佳,表明生长因子的含量并非越高越好,而是在一个合适的浓度的情况下,作用效果最佳。有学者猜测血小板浓缩制品浓度过高产生的抑制作用是因为其不仅含有促进组织愈合的生长因子,也含有一些炎症因子,如血小板反应蛋白、血小板因子4等,浓度过高时则会反向抑制[14]。总之,iPRF含有多种细胞因子,作用复杂多样,其作用机制还有待进一步研究。
成骨分化过程的关键步骤包括细胞增殖、胞外基质形成以及基质矿化[15]。在骨形成中,ALP是起关键作用的标志物,并与早期细胞的成骨分化有关[16]。Chen等[17]将PRF和牙髓干细胞植入裸鼠体内,成功得到牙髓牙本质样组织,ALP的mRNA表达水平在7、14 d均有明显的升高。同样本实验中,7、14、21 d中iPRFe组ALP的mRNA表达水平均比对照组和OM组有明显地升高,提示iPRF早期就能促进hSCAPs的成骨向分化。Saeed等[18]研究表明,PRF可以促进人牙髓干细胞的成骨分化,茜素红染色矿化结节更明显。此实验中,与正常组和矿化诱导组相比,iPRFe组hSCAPs的茜素红染色显示矿化结节相对更明显,且在14 d和21 d时,OCN的mRNA表达水平均比OM组更明显,表明iPRF可促进细胞成骨分化。牙髓损伤和修复的机制包括干细胞成牙本质向分化和第三期牙本质的分泌[19]。成牙本质细胞是分泌牙本质的关键细胞,特异性地表达一些标记分子,如DSPP和DMP1[20]。Chen等[17]研究PRF在体外对牙髓干细胞分化的影响中,发现培养7 d和14 d的DSPP的表达无差异,DMP1在7、14和21 d均持续升高,但在本研究中iPRFe组DSPP的表达从14 d开始较OM组有明显升高,可能是由于细胞种类不同;而DMP1的表达趋势与本研究一致,表明iPRF能够促进hSCAPs的成牙向分化。因此,iPRF可以促进hSCAPs的成牙/成骨向分化。
综上所述,本研究证明了iPRF能促进hSCAPs的增殖、迁移和成骨/成牙向分化,为可注射型富血小板纤维蛋白应用于牙髓再生提供了一定的前期基础,但具体的机制以及应用于体内牙髓再生的效果仍需进一步探究。
