聚丙烯腈螯合纳米纤维膜对重金属离子的选择性吸附研究
2021-08-06龚宸悦武健丹张爱英冯增国
王 翔,龚宸悦,武健丹,张爱英,叶 霖,冯增国
(北京理工大学 材料学院,北京 100081)
在各类吸附材料中,螯合吸附材料由于选择性高、吸附容量高且简便高效,在水处理领域受到广泛关注[1-2]。将对金属离子具有螯合作用的基团(如偕胺肟型、氨基磷酸型、亚胺乙酸型等)键合于吸附材料表面,可有效提升吸附效果。作为一种可制备高比表面积和高孔隙率薄膜材料的新型加工方法,利用静电纺丝技术制备吸附材料方面也取得了一定的进展[3-4]。Li Yanzi等[5]将MnO2在聚多巴胺涂层的帮助下原位加载到柔性电纺聚丙烯腈(PAN)纤维上,该纤维对Pb2+具有良好的吸附能力,吸附过程遵循伪二级模型和Langmuir等温吸附模型。将静电纺纤维膜进行螯合改性并同时对多种重金属离子进行选择性吸附的研究鲜见报道。本工作制备了偕胺肟型静电纺PAN螯合(A-PAN)纳米纤维膜,研究了反应温度对 PAN 分子中腈基(—CN)转化率的影响及不同转化率的A-PAN纤维膜对Fe3+,Cu2+,Pb2+的吸附能力。
1 实验部分
1.1 主要原料
PAN,重均分子量为150 000,分析纯,西格玛奥德里奇(上海)贸易有限公司;二甲基甲酰胺(DMF),碳酸钠:均为分析纯,北京化工厂;盐酸羟胺,分析纯,阿法埃莎(天津)化学有限公司;CuCl2,Pb(NO3)2,FeCl3:均为分析纯,国药集团化学试剂有限公司。
1.2 主要仪器
SS系列静电纺丝仪,北京永康乐业科技发展有限公司;BCPCAS4800型冷场发射扫描电子显微镜,日本日立公司;IRPrestige21型傅里叶变换红外光谱仪,日本岛津公司;X-pert型X射线衍射仪,荷兰帕纳克有限公司。PHSJ-4A型pH计,上海仪电科学仪器股份有限公司;AA700型原子吸收分光光度计,美国PE公司。
1.3 纳米纤维膜的制备
称取定量PAN溶解到DMF中,室温条件下搅拌12 h,制得质量分数为10%的淡黄色PAN纺丝溶液,将PAN纺丝溶液注入20 mL注射器中,注射器前端连接内径为0.7 mm的纺丝针头,进行静电纺丝。纺丝参数为:电压16.5 kV,接收距离20.0 cm,纺丝溶液流量1.8 mL/h,环境温度25 ℃,湿度35%。纺丝结束后,于40 ℃真空干燥12 h,即为PAN纳米纤维膜,备用。
PAN纳米纤维膜的偕胺肟化改性(反应式见图1),准确称量定量PAN纳米纤维膜,加入到100 mL质量浓度为15 g/L的盐酸羟胺溶液中,并加入无水碳酸钠调节溶液pH值,在70 ℃水浴锅中反应一定时间后取出,用去离子水浸泡0.5 h,反复洗涤三次,除去钠盐和未反应的羟胺,烘干,得到A-PAN纳米纤维膜,按式(1)计算—CN转化率[6]。

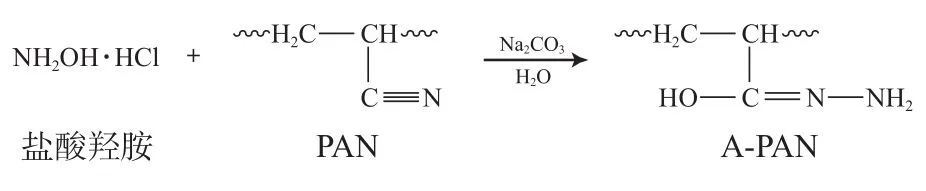
图1 PAN偕胺肟化反应式Fig.1 Amidoximation reaction of PAN
式中:CA为—CN转化率;m0,m1分别为反应前后无纺布的实际质量,g;M0为丙烯腈的相对分子质量(53);M1为羟胺的相对分子质量(33)。
1.4 吸附实验
1.4.1 重金属离子吸附实验
配制一定体积的初始质量浓度为100 mg/L的FeCl3溶液,分别取100 mL溶液置于若干个250 mL烧杯中,在烧杯中分别放入0.100 0 g左右的A-PAN纳米纤维膜。将烧杯封口,室温条件下缓慢搅拌,使溶液充分流动。于一定时间后取样,用原子吸收分光光度计测定试样中的Fe3+浓度。按式(2)计算不同时间A-PAN纳米纤维膜对Fe3+的吸附量。

式中:qt为t时刻的吸附量,下同,mg/g;C0为金属离子起始质量浓度,mg/L;Ct为t时刻溶液的质量浓度,mg/L;V为金属离子溶液体积,L;m为A-PAN纳米纤维膜的质量,g。
Cu2+,Pb2+的测试方法与Fe3+相同。
1.4.2 混合重金属离子吸附实验
配制Cu2+/Pb2+混合溶液,其中,Cu2+,Pb2+的初始浓度均为1.28 mmol/L。将0.1 g左右的A-PAN纳米纤维膜浸入100 mL的该混合溶液中,分别于不同时间取样,利用原子吸收分光光度计测定溶液中Cu2+,Pb2+的浓度,按式(2)分别计算金属离子不同时刻的吸附量。
同样配制Fe3+/Cu2+/Pb2+混合溶液,测试方法与上述相同。
1.5 测试与表征
扫描电子显微镜(SEM)观察:真空条件下将纤维试样表面喷金处理,加速电压为15.0 kV,并采用Nano Measurer软件测量纤维直径,绘制直径分布直方图。
傅里叶变换红外光谱(FTIR)分析:采用ATR衰减全反射法,波数为400~4 000 cm-1。
X射线衍射法(XRD)分析:对纤维晶体结构进行表征,衍射角(2θ)为5°~60°,扫描速率为2(°)/min。
2 结果与讨论
2.1 纤维的组成及形貌
从图2看出:2 245 cm-1处强烈尖锐的吸收峰为—CN的特征吸收峰,而经过偕胺肟化后,此处A-PAN纳米纤维的吸收峰强度明显减弱,说明偕胺肟化反应过程中部分—CN转化成了偕胺肟基(NH2—C=N—OH)。此外,A-PAN在1 580,920 cm-1附近出现了新的吸收峰,分别对应NH2—C=N—OH中的N—O及—C=N—的伸缩振动吸收峰,而在3 200~3 600 cm-1出现宽而强的吸收峰,是由于—OH的缔合作用所致。以上特征峰的出现均说明了PAN纳米纤维完成了偕胺肟化。

图2 PAN和A-PAN纳米纤维的FTIRFig.2 FTIR spectra of PAN and A-PAN nanofibers
从图3看出:PAN纳米纤维均匀且呈圆柱型,纤维的平均直径为410 nm左右;A-PAN纤维趋于卷曲并出现缠结弯曲现象,纤维的平均直径增加到580 nm左右,且A-PAN纤维膜的柔软性降低。这可能是由于偕胺肟反应的发生,一方面使—CN转化成体积更大的NH2—C=N—OH;另一方面分子间作用力增强,分子链柔顺性降低,最终导致纳米纤维直径增加,膜的柔韧性降低。

图3 偕胺肟化前后纳米纤维的SEM照片及纤维直径分布Fig.3 SEM images of nanofibers before and after amidoximation of PAN
—CN的化学改性属于吸热反应,从图4可看出:随反应温度的升高,—CN转化率迅速提高。这是反应温度的升高使PAN纳米纤维发生溶胀,更易使—CN暴露出来,且温度越高,反应物羟胺分子的扩散运动越剧烈,更容易扩散到纤维内部,与—CN的接触概率随之增加,故—CN转化率增大。
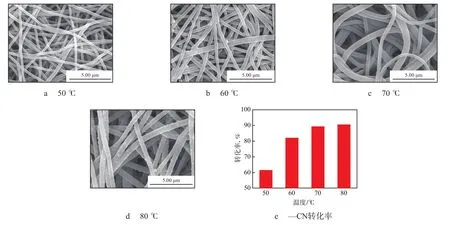
图4 不同反应温度时A-PAN纳米纤维中—CN转化率及其SEM照片Fig.4 Conversion ratio of —CN at different reaction temperatures and SEM images of A-PAN nanofibers
从图4还看出:随着反应温度的升高,A-PAN纤维卷曲程度逐渐增加;当温度为70 ℃时,A-PAN纤维呈现扭曲结构;温度为80 ℃时,A-PAN纤维表面开始有颗粒产生,且纤维之间相互粘连。
从图5可以看出:—CN转化率为0的PAN纤维在2θ为17.0°处有窄而尖锐的衍射峰,表明PAN纤维具有良好的结晶度,使其能保持一定的机械强度和较好的化学稳定性[7]。随着—CN转化率的提高,结晶峰不断减弱,当—CN转化率从35.6%增加到93.0%时,该衍射峰的强度逐渐降低,说明偕胺肟化过程一定程度上破坏了PAN纤维的晶体结构。
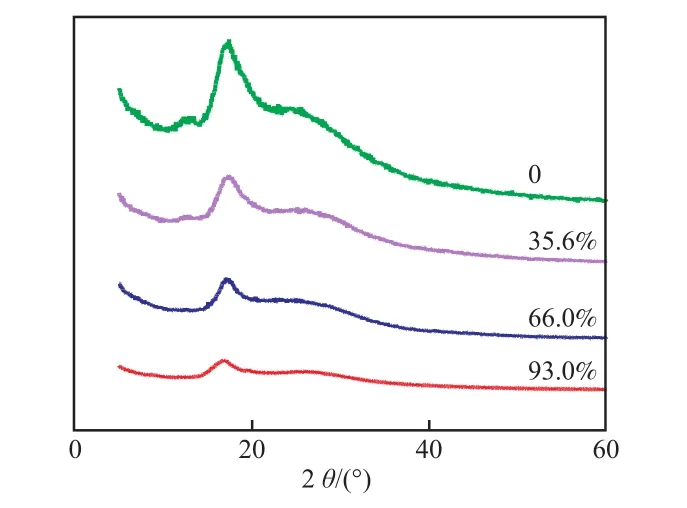
图5 不同—CN转化率的A-PAN纤维的XRD图谱Fig.5 XRD patterns of A-PAN fibers at different conversion ratios of —CN
2.2 A-PAN纤维膜对重金属离子的吸附
2.2.1 A-PAN纤维膜对重金属离子吸附能力的影响
从图6可以看出:PAN纳米纤维膜对三种离子基本不吸附;通过偕胺肟改性后,A-PAN纤维膜对金属离子的吸附能力提升较大,且随着—CN转化率的升高呈现出先增加后降低的趋势。其中,—CN转化率为80.0%左右时,纳米纤维膜具有最高的吸附能力,吸附10 h后,对Fe3+,Cu2+,Pb2+的吸附能力分别为90.0,75.2,35.8 mg/g。这表明,较高转化率的A-PAN纤维膜中,含有更多的NH2—C=N—OH,更易与重金属离子发生配位反应,因此吸附能力随着转化率的升高而明显增加。当—CN转化率高于80.0%时,结合SEM图像发现A-PAN纳米纤维缠结和粘连的程度较高,从而导致纤维膜比表面积下降,吸附能力也随之降低。另外,转化率太高的A-PAN纤维膜会变硬变脆,从而较难应用于实际。因此,比较合适的—CN转化率约为80.0%左右,可保证较高吸附能力的同时尽量保留纤维膜的力学性能。故在后续实验中均采用—CN转化率为80.0%左右的A-PAN纤维膜进行测试。
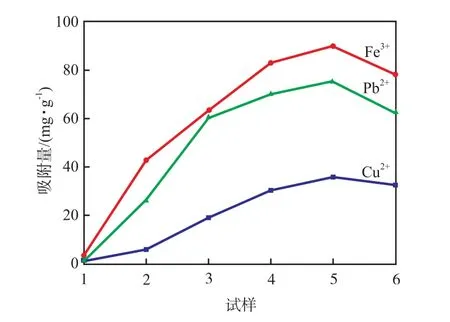
图6 不同—CN转化率的A-PAN纤维膜对Fe3+,Cu2+及Pb2+的吸附量Fig.6 Adsorption capacity of Fe(Ⅲ),Cu(Ⅱ),and Pb(Ⅱ) on A-PAN fibrous membranes at different conversion ratios
2.2.2 A-PAN纤维膜对混合重金属离子的吸附
从图7可以看出:对于Cu2+/Pb2+混合溶液,A-PAN纤维膜对Cu2+吸附量明显高于对Pb2+的吸附量,且在吸附4 h后Cu2+,Pb2+的吸附能力分别达到0.430,0.368 mmol/g,吸附量差异明显。说明A-PAN纤维对Cu2+的吸附能力略优于Pb2+,对Cu2+具有一定的选择吸附性。
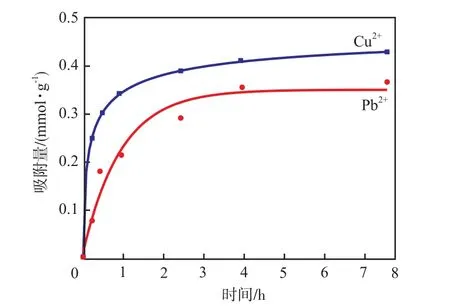
图7 A-PAN纤维膜对Cu2+/Pb2+混合离子的吸附量与吸附时间的关系曲线Fig.7 Adsorption capacity of Cu(Ⅱ)/Pb(Ⅱ) mixed ions by A-PAN fibrous membrane as a function of time
从图8可以看出:在三种金属离子浓度均为1.28 mol/L的情况下,A-PAN纤维膜对Fe3+的吸附量为1.001 mmol/g,远高于对Cu2+(0.513 mmol/g)及Pb2+(0.442 mmol/g)的吸附量,从而证明了A-PAN纤维膜对金属离子的吸附具有选择性。从金属离子的体积和电荷密度等方面定性地分析金属离子与A-PAN纤维膜的配合能力。根据Pearson软硬酸碱理论[8],将体积较小、正电荷数目多、可极化性低、不易变形的金属离子称为硬酸,其容易接受配体所提供的电子对(如碱金属、Fe3+等);将原子体积大、正电荷数目少、可极化性强的中心原子称为软酸,其不易接受配体所提供的电子对(如Cu2+,Pb2+等)。NH2—C=N—OH中含有氨基和—OH,电负性强,提供电子对的原子(N,O)极化性小,不易氧化,属于硬碱。硬酸优先于硬碱结合,且生成的配合物稳定性高,因此,A-PAN纤维膜与Fe3+的配合能力最强,与Cu2+的配合能力次之,由于Pb2+的半径比较大,配合能力最弱。故吸附能力由大到小依次为Fe3+,Cu2+,Pb2+。
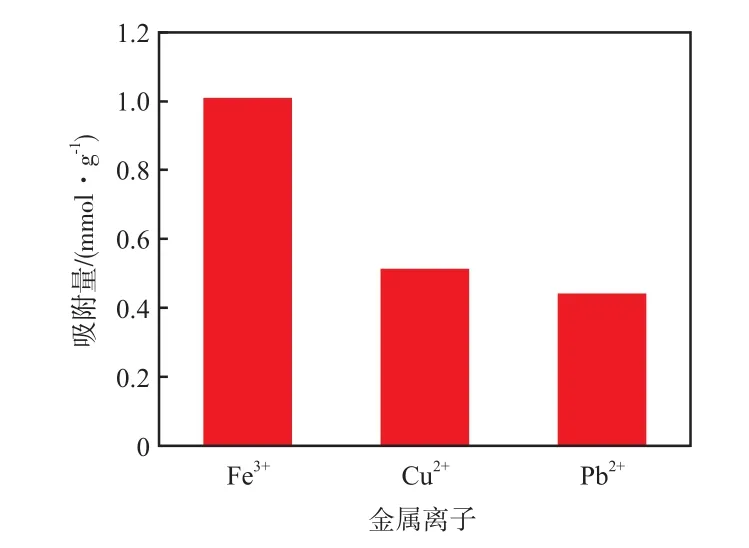
图8 A-PAN纤维膜对Fe3+/Cu2+/Pb2+混合离子的吸附能力Fig.8 Adsorption capacity of Fe(Ⅲ)/Cu(Ⅱ)/Pb(Ⅱ) mixed ions by A-PAN fibrous membrane
2.2.3 A-PAN纤维膜对重金属离子吸附机理
由于A-PAN纤维膜对Fe3+的吸附效果最好,以此为例研究了A-PAN纤维膜对重金属离子的吸附机理。从图9看出:在初始阶段,A-PAN纤维膜对Fe3+的吸附量随吸附时间的延长而急剧增加,后期增速减缓,直至达到吸附平衡状态。这是因为在配位反应初期,A-PAN纤维膜表面存在大量的配合位点,同时溶液中有大量金属离子,两者结合的机会增大,使配位反应速率增加[9];随着反应的进行,溶液中的金属离子浓度降低且A-PAN纤维膜表面配合位点减少,反应速率下降并逐渐达到平衡。从整个反应过程来看,120 min后增幅明显变缓,并在240 min后基本达到吸附平衡。
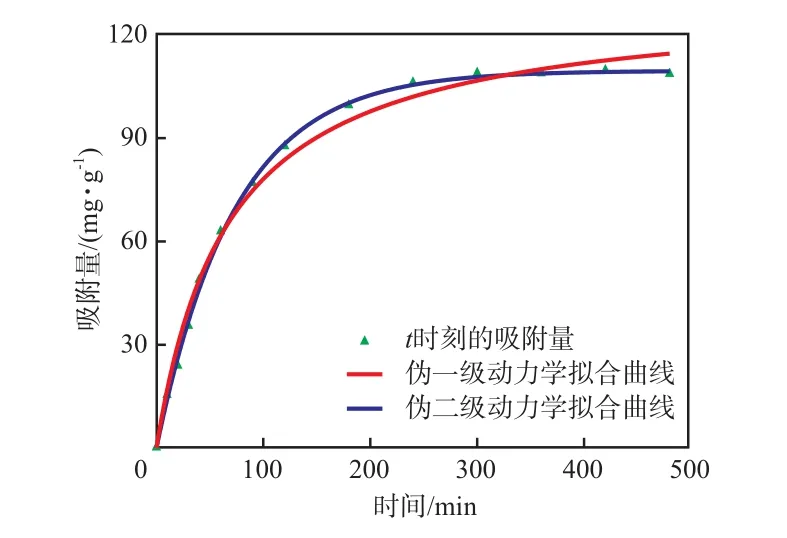
图9 A-PAN纤维膜对Fe3+的吸附动力学过程及模型拟合曲线Fig.9 Kinetic processes and model fitting curves of Fe(Ⅲ) ion adsorption on A-PAN membrane
采用伪一级动力学吸附模型[10][见式(3)]和伪二级动力学吸附模型[11][见式(4)]对实验数据进行分析。
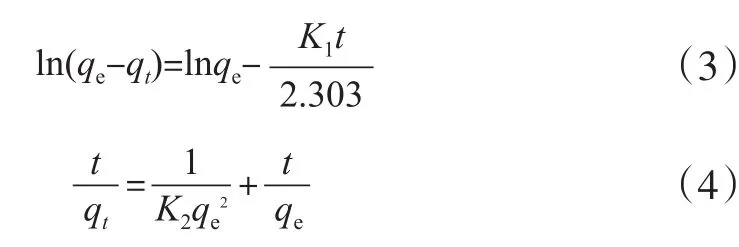
式中:qe为A-PAN纤维膜对金属离子的平衡吸附量,mg/g;K1表示伪一级吸附动力学速率常数,min-1;K2表示伪二级吸附动力学速率常数,g/(mg·min)。
通常来说,相关系数越大,表明模型对吸附过程的拟合效果越好。伪一级动力学吸附模拟方程和伪二级动力学吸附模拟方程的相关系数分别为0.990 8,0.998 9,表明伪二级动力学方程能更好地描述A-PAN纤维膜对Fe3+的吸附过程,该纤维膜对Fe3+的吸附是化学吸附。吸附过程受金属离子的扩散和NH2—C=N—OH与Fe3+的配位反应共同控制。
通过平衡等温线模型可以很好地对吸附系统进行分析和预测设计结果。通过改变Fe3+的初始浓度得到吸附等温线(见图10),并采用Langmuir等温模型[见式(5)]和Freundlich模型[见式(6)]分析实验数据。

图10 A-PAN纤维膜对Fe3+的吸附等温模型拟合曲线Fig.10 Isothermal model fitting curves for adsorption of Fe(Ⅲ) ions by A-PAN membrane
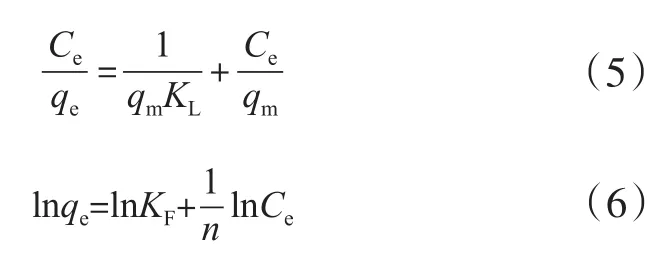
式中:qm是最大吸附容量,mg/g;KL是与吸附自由能有关的Langmuir常数,L/mg;KF是与吸附容量相关的Freundlich常数,L/mg;n-1是与吸附强度相关的溶剂参数。
通过数据拟合,Langmuir等温模型的拟合系数为0.994 2,高于Freundlich模型的拟合系数(0.988 5),说明A-PAN纤维膜对Fe3+的吸附符合Langmuir等温模型,即该吸附过程为单层吸附,吸附发生在纤维膜上特定的同质点,并且一个金属离子占据了一个反应位点,该位置就不会再有进一步的吸附。通过计算后可以得出A-PAN纤维对Fe3+的最大吸附量为117.42 mg/g。可见A-PAN纤维膜在重金属污染治理、贵金属的富集与回收等方面具有潜在的应用价值。
3 结论
a)利用静电纺丝技术结合偕胺肟改性反应成功制备了A-PAN纤维膜。反应温度的升高有助于—CN转化率的增大,进而促进对重金属离子的吸附,但同时会破环A-PAN纤维膜的晶体结构,柔韧性变差。
b)A-PAN纤维膜对单独的金属离子Fe3+,Cu2+及Pb2+均具备一定的吸附能力。吸附量呈现初期快速增长,后期逐步趋缓的行为。
c)A-PAN纤维膜对混合离子Fe3+,Cu2+及Pb2+的吸附具有选择性,吸附能力由大到小依次为Fe3+,Cu2+,Pb2+。
d)A-PAN纤维膜对Fe3+的吸附过程受离子的扩散和NH2—C=N—OH与离子的配位反应共同控制,为化学吸附。A-PAN纤维膜对Fe3+的吸附为单层吸附,最大吸附量为117.42 mg/g。
