Na2EDTA滴定法测定粗二氧化碲中铅含量
2021-08-05张园
张 园
(福建紫金矿冶测试技术有限公司 厦门分公司,福建 厦门 361101)
前言
地壳中碲的丰度很小,几乎无独立矿床,绝大部分碲元素伴生于铜、铅等重金属矿藏中。铜阳极泥是火法炼铜过程提碲的主要原料,在火法炼铜过程中,铜精矿伴生的元素碲大部分随金银进入阳极泥。铜阳极泥经卡尔多炉熔炼工艺处理回收有价元素,处理过程中产生的文丘里泥回收金、银时需要先除碲,在除碲的过程中实现资源综合利用,生产出大量碲的氧化物,称之为粗二氧化碲,其含有主元素二氧化碲及铜、铅、砷、锑、铋、硒等杂质元素,金、银等贵金属元素。
企业在铜阳极泥中综合回收有价元素,实现资源综合利用成为行业趋势,但是新工艺新技术的应用生产的产品目前没有相应的产品标准和检测标准。国内虽然有碲和二氧化碲的产品标准和检测方法,但是由于生产工艺不同,导致其中杂质元素含量不同,无法套用碲和二氧化碲方法标准。
粗二氧化碲样品中主要共存元素有碲、铅、硒、锑、铜、砷、铋,在铅的检测过程中,其他共存元素均对铅产生正干扰[1-8]。本文采用氢溴酸消除锑、砷、锡干扰,硫酸冒烟除去大部分碲、硒,硫酸铅沉淀能使铅与铜、铁等金属离子分离,再用EDTA络合滴定法,实现了粗二氧化碲中铅含量的测定。
1 实验部分
1.1 主要试剂
除非另有说明,在分析中仅使用确认为分析纯的试剂和蒸馏水或去离子水或相当纯度的水。
金属铅(ωPb≥99.99%)、盐酸、硝酸、硫酸、氢溴酸、抗坏血酸、无水乙醇、硫酸(5+95)、硫脲饱和溶液、酒石酸溶液(200 g/L)、二甲酚橙溶液(5 g/L)。
乙酸-乙酸钠缓冲溶液(pH≈5.5):称取375 g无水乙酸钠固体,溶于水中,加入50 mL冰乙酸,用水稀释至2 000 mL,混匀。
1.2 标准溶液的配制与标定
铅标准储备溶液(2 mg/mL):称取2.000 0 g金属铅(ωPb≥99.99%)于250 mL烧杯中,加30 mL硝酸(1+3),加盖表面皿,加热溶解完全,微沸驱逐氮的氧化物,取下,冷至室温,移入1 000 mL容量瓶中,以水定容至刻度,摇匀。
乙二胺四乙酸二钠标准溶液[c(Na2EDTA)≈0.010 mol/L]:称取3.72 g乙二胺四乙酸二钠于300 mL烧杯中,加水微热溶解,冷却至室温,移入1 000 mL容量瓶中,用水稀释至刻度,混匀,放置3 d 后标定。
EDTA标准溶液的标定:分取10 mL铅标准储备溶液4份,分别置于250 mL烧杯中,加入50 mL乙酸-乙酸钠缓冲溶液,搅拌,加入0.1 g抗坏血酸,加水稀释至100 mL,搅拌后,加入3~5滴二甲酚橙溶液,用EDTA标准溶液滴定至溶液由红色变成亮黄色为终点。随同试样做空白实验。
1.3 实验方法
称取0.2~0.4 g试样(精确至0.000 1 g)置于250 mL烧杯中,加水润湿后加入20 mL盐酸,加盖表面皿,于电热板上加热溶解10 min,加入5 mL硝酸加热至完全溶解,取下稍冷加入5 mL硫酸,加热至冒浓白烟,稍冷加5 mL氢溴酸,挥发砷、锑,重复挥发3次,继续冒白烟至小体积,取下冷却,加10 mL酒石酸溶液,摇匀,用水吹洗表面皿及杯壁并加至50~60 mL,于电热板上加热微沸10 min,取下,放置1 h以上。
溶液用慢速定量过滤,用硫酸(5+95)溶液洗涤烧杯及沉淀各5次,水洗涤烧杯和沉淀各1次,弃去滤液,将滤纸连同沉淀一起移入原烧杯,加入50 mL乙酸-乙酸钠缓冲溶液,加热煮沸5 min,玻棒搅拌使沉淀完全溶解,取下稍冷,加水至150 mL。加入5 mL 饱和硫脲溶液、0.1 g抗坏血酸,搅拌溶解后,滴加2滴二甲酚橙指示剂,用EDTA标准滴定溶液滴定至溶液由紫红色变为亮黄色为终点。
2 结果与讨论
实验所用粗二氧化碲样品来自国内某大型铜冶炼厂,样品中主要元素含量范围见表1。

表1 粗二氧化碲的主要成分
2.1 溶样方式选择
粗二氧化碲样品中主要共存元素有碲、硒、锑、铜、砷、铋,对铅的滴定均存在干扰。高含量锑在溶解样品的过程中易水解,影响铅量的测定;铋在硫酸冒烟过程中生成硫酸铋,在用水稀释沉淀过程中部分硫酸铋水解产生不溶于水的碱式硫酸铋,和硫酸铅共沉淀,硫酸铅铋溶解于乙酸-乙酸钠缓冲溶液后铋与EDTA标准滴定溶液络合,对铅量的测定造成正干扰。采用氢溴酸消除锑、砷、锡干扰,硫酸冒烟除去大部分碲、硒,硫酸铅沉淀能使铅与铜、铁等金属离子分离。因此,实验选择盐酸+硝酸+硫酸+氢溴酸溶解样品。
2.2 氢溴酸加入量实验
为了考察氢溴酸消除锑、砷、锡等干扰,移取10.00 mL铅标准溶液,分别加入2倍最大干扰量(按0.4 g称样量,溶液中最大干扰量:Te 320 mg,Sb 20 mg,Se 40 mg,Cu 8 mg,As 20 mg,Bi 20 mg),按实验方法进行测定,分别加入不同量的氢溴酸,实验结果见表2。
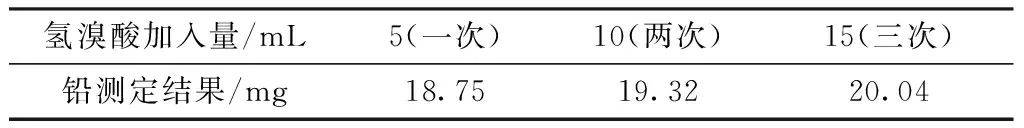
表2 氢溴酸加入量实验
实验结果表明,当分银渣样品中锑含量高时,需反复加氢溴酸3次以上才能彻底地消除锑的干扰,剩余的锑加酒石酸络合的方法消除。
2.3 酒石酸加入量实验
为了考察酒石酸对铋等干扰元素的掩蔽效果,移取10.00 mL铅标准溶液,分别加入2倍最大干扰量(按0.4 g称样量,溶液中最大干扰量:Te 320 mg,Sb 20 mg,Se 40 mg,Cu 8 mg,As 20 mg,Bi 20 mg),按实验方法进行测定,分别加入不同体积的酒石酸,实验结果见表3。

表3 酒石酸加入量实验结果
实验结果表明,加入5 mL酒石酸结果偏低,10 mL 以上测定结果差别不大,因此选择加入10 mL酒石酸作为掩蔽剂。
2.4 沉淀体积实验
分取20.00 mL铅标准溶液于250 mL烧杯中,按拟定的实验方法进行测定,分别加入不同量的蒸馏水,实验结果见表4。
由表4可知,沉淀时体积在50~60 mL时,测定结果与理论值基本一致,沉淀体积在70~80 mL时,结果较理论值偏低。因此,实验选择沉淀时体积控制在50~60 mL。

表4 沉淀体积实验
2.5 硫酸铅沉淀时间实验
分取20.00 mL铅标准溶液于250 mL烧杯中,按拟定的实验方法进行测定,沉淀后分别放置不同的时间,实验结果见表5。

表5 沉淀时间实验
由表5可知,放置1 h后沉淀基本完全,且达到稳定,实验选择沉淀放置1 h以上过滤。
2.6 干扰实验
移取5.00、25.00 mL铅标准溶液,使样品中铅量为10 mg和50 mg。分别加入2倍最大干扰量(按0.4 g称样量,溶液中最大干扰量:Te 320 mg,Sb 20 mg,Se 40 mg,Cu 8 mg,As 20 mg,Bi 20 mg),按实验方法测定铅含量,实验结果见表6。

表6 共存元素干扰实验
由表6可见,采用本方法以上干扰均可消除。
2.7 准确度实验
为了考察实验的准确度,选取了3个代表样品,按照拟定的实验方法进行加标回收实验,实验结果见表7。
由表7可见,加标回收率为97.1%~102%,可以满足粗二氧化碲中碲含量的测定。
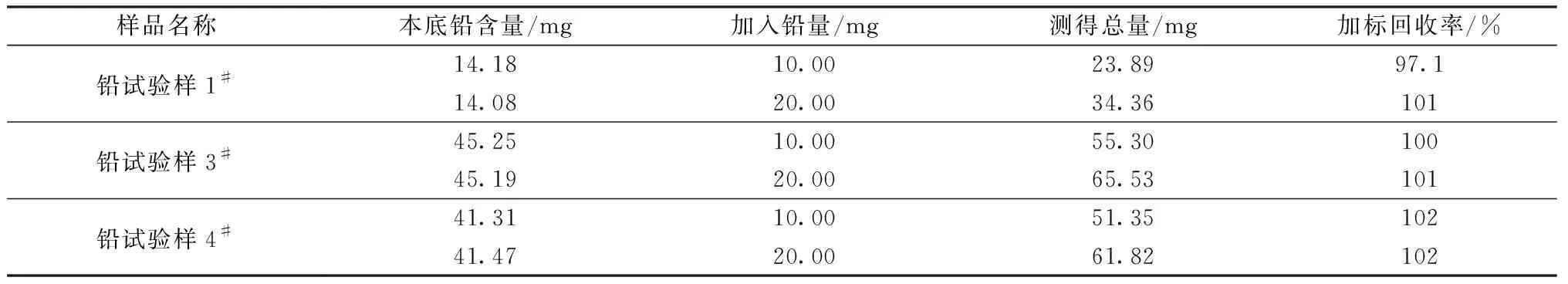
表7 加标回收实验
2.8 精密度实验
选取5个粗二氧化碲样品按照实验步骤进行精密度实验,结果见表8。
实验数据表明,该方法的精密度较好,相对标准偏差在0.10%~1.1%,满足测定要求。
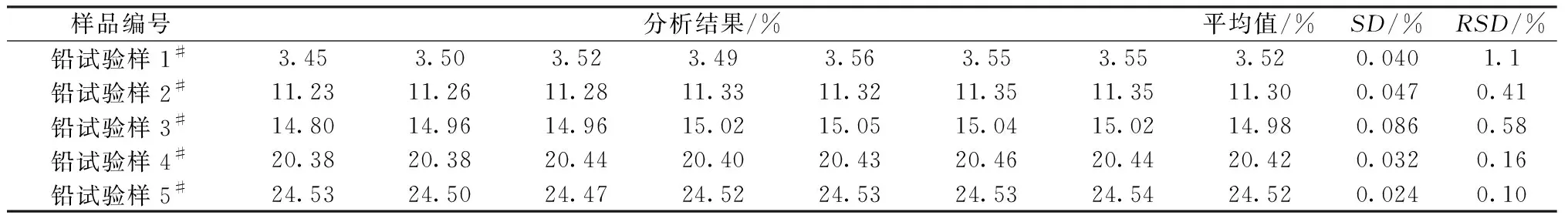
表8 精密度实验
3 结论
采用氢溴酸消除锑、砷、锡干扰,用硫酸形成硫酸铅沉淀,再用EDTA络合滴定法测定粗二氧化碲中铅量的方法。样品测定的相对标准偏差在0.10%~1.1%,样品加标回收率在97.1%~102%。本方法结果准确度高、精密度好,满足粗二氧化碲中铅量的生产控制检测要求。
