LncRNA PCAT19调控miR-137影响前列腺癌细胞增殖、细胞周期、迁移及侵袭
2021-08-05申大年咸文娟
申大年 咸文娟
1.青海省第五人民医院(青海省肿瘤医院)泌尿外科(青海西宁 810007)
2.青海省人民医院 遗传研究室(青海西宁810007)
前列腺癌是临床常见的一种恶性肿瘤,近年来,我国前列腺癌发病率逐年上升,已严重威胁人类生命安全,临床常采用手术、放化疗等方式进行治疗,但大部分患者确诊时已处于中晚期,目前前列腺癌发病机制尚未阐明,因而积极探寻新型基因对前列腺癌诊断及治疗均具有重要意义[1]。长链非编码RNA(LncRNA)在前列腺癌发生及发展过程可发挥癌基因或抑癌基因作用,并可调控细胞增殖、凋亡等生物学过程[2-4]。长链非编码RNA PCAT19(LncRNA PCAT19)在喉癌细胞中表达水平升高,并可通过调节miR-182/PDK4分子轴从而促进细胞增殖[5]。但PCAT19在前列腺癌发生及发展过程中的作用机制尚未阐明。靶基因预测显示为微小RNA-137(miR-137)与PCAT19存在结合位点,研究表明miR-137在乳腺癌细胞中表达水平降低,并可通过靶向突触细胞黏附分子(DUSP4)抑制乳腺癌发展进程[6]。但PCAT19是否可通过调控miR-137表达影响前列腺癌细胞生物学过程尚未可知。因此,本研究主要探讨PCAT19对前列腺癌细胞增殖、细胞周期、迁移及侵袭的影响,探究其对miR-137的调控作用。
材料与方法
一、材料与试剂
(一)一般资料
前列腺癌组织与癌旁组织:选取2018年3月至2019年2月本院收治的29例前列腺癌患者为研究对象,所有患者均经病理诊断为前列腺癌,年龄50~70岁,平均年龄(65.32±10.63)岁。纳入标准:临床资料完整患者。排除标准:合并其他恶性肿瘤;继发性前列腺癌患者;术前1月内接受放疗或化疗患者。术中切除前列腺癌组织与癌旁组织,置于-80℃超低温冰箱内保存。本研究经本院伦理委员会批准,所有患者知情且签署同意书。
(二)细胞与试剂
人前列腺癌细胞DU145购自上海冠导生物工程有限公司;DMEM、胰蛋白酶、胎牛血清、Lipofectamine2000、Trizol、反转录与qRT-PCR试剂均购自美国Thermo Fisher公 司;si-NC、si-PCAT19、miR-NC、miR-137 mimics、anti-miR-NC、anti-miR-137购自广州锐博生物科技有限公司;MTT试剂购自上海信帆生物科技有限公司;Transwell小室与Mgtrigel基质胶均购自美国Corning公司;兔抗人E-cadherin、N-cadherin抗体购自美国Santa Cruz公司;HRP标记的山羊抗兔IgG二抗购自武汉艾美捷科技有限公司。
二、方法
(一)实验分组
DU145细胞中加入0.25%胰蛋白酶消化,加入培养基制备细胞悬液(2.5×105个/mL)接种于6孔板(200 μL/孔),待细胞生长融合至70%时进行转染,分别将si-NC、si-PCAT19、si-PCAT19与anti-miR-NC、si-PCAT19与anti-miR-137转染至DU145细胞,分别记作si-NC组、si-PCAT19组、si-PCAT19+anti-miR-NC组、si-PCAT 19+anti-miR-137组。
(二)qRT-PCR检测PCAT19、miR-137的表达水平
采用Trizol法提取前列腺癌组织、癌旁组织及各组DU145细胞中的总RNA,参照反转录试剂盒合成cDNA。以cDNA为模板进行qRT-PCR反应,反应体系:10×PCR Buffer 2.5μL,MgSO4 2.5μL,dNTPs 2.5μL,正反向引物各0.5μL,cDNA 2μL,RNase-Free ddH2O补足体系至25μL;反应条件:95℃预变性60 s,95℃变性60 s,58℃退火30 s,72℃延伸30 s,共36次循环。PCAT19以GAPDH为内参,miR-137以U6为内参,采用2-ΔΔCt法计算PCAT19、miR-137相对表达量。
(三)MTT检测细胞增殖
取各组DU145细胞(2.5×105个/mL)接种于96孔板(100μL/孔),加入MTT溶液(20μL/孔),继续培养4 h,弃上清,加入DMSO(150μL/孔),避光振荡孵育5 min,应用酶标仪检测各孔光密度值(OD值),以OD值大小表示细胞活力大小。。
(四)检测细胞周期
取各组DU145细胞(1×106个/mL)接种于96孔板(100μL/孔),离心后(3000 r/min转速,5 min)加入预冷PBS,再次离心(3000 r/min转速,5 min),加入预冷PBS(500μL)重悬细胞,加入预冷70%乙醇(3.5 mL),充分混匀后置于4℃冰箱内孵育24 h,3000 r/min转速离心5 min,弃上清,向细胞沉淀中加入RNaseA(50μL),水浴30 min,加入PI染色液(450μL)染色30 min,应用流式细胞仪检测各组细胞周期。
(五)Transwell实验检测细胞迁移与侵袭
取各组DU145细胞加入0.25%胰蛋白酶消化,加入不含血清的DMEM培养液制备单细胞悬液(5×104个/mL),将细胞悬液加入上室(200μL/孔),下室加入培养液(600μL/孔),继续培养24 h,使用多聚甲醛固定(20 min),采用0.1%结晶紫染液染色(15 min),观察迁移细胞数。使用培养液稀释Matrigel基质胶后加入上室(40μL/孔),培养箱孵育5 h后加入DU145细胞悬液,后续步骤同细胞迁移实验,观察侵袭细胞数。
(六)双荧光素酶报告基因检测PCAT19和miR-137的靶向关系
LncBase v.2预测显示PCAT19和miR-137存在结合位点,分别构建野生型载体WT-PCAT19与突变型载体MUT-PCAT19,分别将miR-NC、miR-137 mimics与WT-PCAT19、MUT-PCAT19共转染至DU145细胞,继续培养24 h,检测各组荧光素酶活性。
(七)Western blot检测E-cadherin、N-cadherin蛋白表达
DU145细胞加入蛋白裂解液提取细胞总蛋白,采用BCA法测定蛋白浓度,取50μg变性蛋白进行SDS-PAGE,转移至PVDF膜,室温封闭2 h后分别孵育一抗稀释液(1:1000)与二抗稀释液(1:5000),室温孵育1 h,曝光,显影,应用ImageJ软件分析各条带灰度值。
(三)统计学处理
结 果
一、PCAT19和miR-137在前列腺癌组织中的表达
与癌旁组织比较,前列腺癌组织PCAT19的表达水平显著升高(P<0.05),miR-137的表达水平显著降低(P<0.05),见表1。

表1 PCAT19和miR-137的表达
二、干扰PCAT19对DU145增殖的影响
与si-NC组比较,si-PCAT19组OD值显著降低(P<0.05),G0-G1期细胞比例显著升高(P<0.05),S期细胞比例显著降低(P<0.05),G2-M期细胞比例相比差异无统计学意义(P>0.05),见图1、表2。
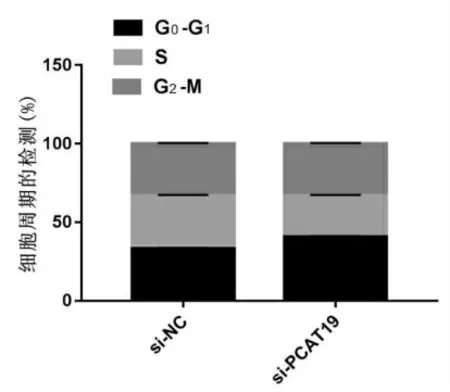
图1 干扰PCAT19对DU145周期的影响
表2 干扰PCAT19对DU145细胞活性及周期的影响(±s,n=3)

表2 干扰PCAT19对DU145细胞活性及周期的影响(±s,n=3)
注:与si-NC组相比,*P<0.05(t=27.175、37.821、18.976、15.662、18.342、0.253,P<0.05)。
分组 PCAT19 miR-137 OD值 G0-G1(%) S(%) G2-M(%)si-NC 0.94±0.05 0.99±0.05 1.10±0.05 33.13±0.51 33.70±0.54 33.17±0.41 si-PCAT19 0.14±0.01* 3.05±0.08* 0.51±0.02* 40.53±0.64* 26.39±0.43* 33.08±0.46
三、干扰PCAT19对DU145迁移侵袭的影响
与si-NC组比较,si-PCAT19组迁移及侵袭细胞数显著减少 (P<0.05),E-cadherin蛋白水平显著升高(P<0.05)见表3,N-cadherin蛋白水平显著降低(P<0.05),见图2。
表3 干扰PCAT19对DU145迁移侵袭的影响(±s,n=3)

表3 干扰PCAT19对DU145迁移侵袭的影响(±s,n=3)
注:与si-NC组相比,*P<0.05(t=31.855、30.084、21.004、18.904,P<0.05)。
分组 迁移细胞数(个)侵袭细胞数(个) E-cadherin N-cadherin si-NC 189.67±4.64 125.33±3.30 0.12±0.01 0.60±0.04 si-PCAT19 89.33±2.87*63.00±1.41*0.62±0.04* 0.15±0.01*

图2 干扰PCAT19对DU145中E-cadherin、N-cadherin蛋白表达的影响
四、PCAT19和miR-137靶向关系
LncBase v.2预测显示PCAT19与miR-137存在结合位点,见图3。miR-137过表达可明显降低野生型载体WT-PCAT19的荧光素酶活性(P<0.05),而对突变型载体MUT-PCAT19的荧光素酶活性无明显影响(P>0.05),见表4。
表4 双荧光素酶报告实验(±s,n=3)

表4 双荧光素酶报告实验(±s,n=3)
注:与miR-NC组 相 比,*P<0.05(t=28.273,P<0.05;t=0.665,P=0.542)。
分组 WT-PCAT19 MUT-PCAT19 miR-NC 0.96±0.04 0.97±0.06 miR-137 0.23±0.02* 1.00±0.05

图3 PCAT19靶向miR-137
五、干扰miR-137和PCAT19对DU145增殖、迁移、侵袭的影响
与si-PCAT19+anti-miR-NC组比较,si-PCAT19+anti-miR-137组OD值显著升高(P<0.05),G0-G1期细胞比例显著降低(P<0.05),S期细胞比例显著升高(P<0.05),G2-M期细胞比例相比差异无统计学意义(P>0.05),见图4,迁移及侵袭细胞数显著增多(P<0.05),见表6,E-cadherin蛋白水平显著降低(P<0.05),N-cadherin蛋白水平显著升高(P<0.05),见图5、表5。
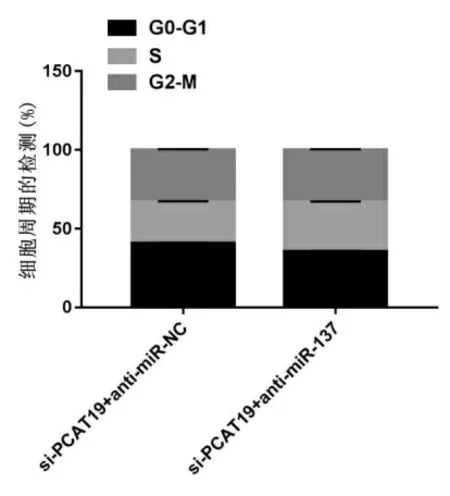
图4 干扰miR-137和PCAT19对DU145周期的影响
表5 干扰miR-137和PCAT19对DU145细胞活性及周期的影响(±s,n=3)

表5 干扰miR-137和PCAT19对DU145细胞活性及周期的影响(±s,n=3)
注:与si-PCAT19+anti-miR-NC组相比,*P<0.05(t=17.041、12.581、15.151,P<0.05;t=0.251,P=0.814)。
分组 OD值 G0-G1(%) S(%) G2-M(%)si-PCAT19+anti-miR-NC 0.52±0.02 40.66±0.52 26.38±0.38 32.96±0.40 si-PCAT19+anti-miR-137 0.96±0.04*35.47±0.49*31.49±0.41*33.04±0.38

图5 干扰miR-137和PCAT19对DU145中E-cadherin、N-cadherin蛋白表达的影响
表6 干扰miR-137和PCAT19对DU145迁移侵袭的影响(±s,n=3)
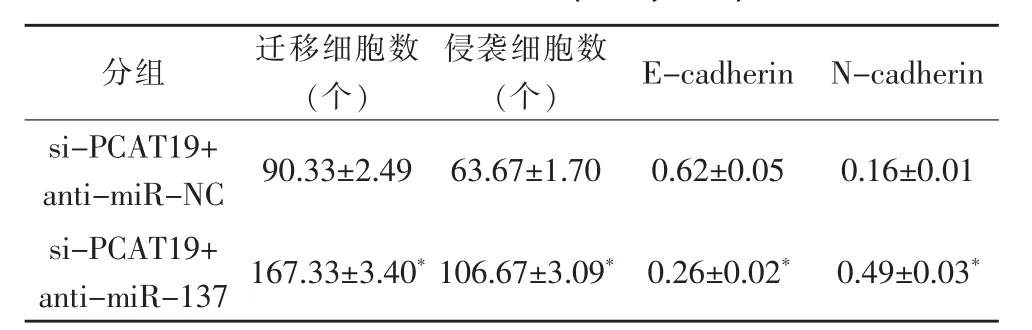
表6 干扰miR-137和PCAT19对DU145迁移侵袭的影响(±s,n=3)
注:与si-PCAT19+anti-miR-NC组 相 比,*P<0.05(t=31.647、21.118、11.579、18.075,P<0.05)。
分组 迁移细胞数(个)侵袭细胞数(个) E-cadherin N-cadherin si-PCAT19+anti-miR-NC 90.33±2.49 63.67±1.70 0.62±0.05 0.16±0.01 si-PCAT19+anti-miR-137 167.33±3.40*106.67±3.09*0.26±0.02*0.49±0.03*
讨 论
前列腺癌发病原因尚未阐明,目前尚缺乏特异性治疗靶点,因而探究前列腺癌发病机制对提高前列腺癌治疗效果及改善患者预后均具有重要意义,近年来,LncRNA可竞争性结合miRNA从而调控前列腺癌细胞增殖、凋亡等生物学过程,并可能作为前列腺癌分子治疗的潜在靶点[7-10]。
非小细胞肺癌组织中PCAT19的表达水平升高,PCAT19负调节p53而促进非小细胞肺癌细胞增殖[11]。PCAT19在前列腺癌中呈高表达,并可能参与前列腺癌发生及发展过程[12]。但PCAT19在前列腺癌发生及发展过程中的作用机制尚未阐明。本研究结果显示,前列腺癌组织PCAT19的表达水平明显升高,干扰PCAT19表达可明显降低OD值及S期细胞比例,并可提高G0-G1期细胞比例,提示干扰PCAT19表达可抑制前列腺癌细胞增殖及诱导细胞周期阻滞于G0-G1期细胞比例。E-cadherin表达上调可抑制上皮-间质转化(EMT)从而抑制细胞转移,N-cadherin表达上调可促进EMT从而促进细胞转移[13-14]。本研究结果显示,干扰PCAT19表达可明显减少迁移及侵袭细胞数,促进E-cadherin表达及抑制N-cadherin表达,提示干扰PCAT19表达可抑制前列腺癌细胞迁移及侵袭。
本研究结果证实PCAT19可靶向结合miR-137。研究表明miR-137可抑制三阴性乳腺癌细胞增殖[15]。miR-137通过靶向调控TCF4而抑制结肠癌细胞增殖、迁移及侵袭[16]。miR-137通过靶向调控SRC3而抑制人非小细胞肺癌细胞的增殖[17]。本研究结果显示前列腺癌组织中miR-137的表达水平降低,提示miR-137在前列腺癌发生及发展过程中可能发挥抑癌基因作用。本研究结果显示,共转染si-PCAT19与anti-miR-137可明显提高细胞增殖能力,降低G0-G1期细胞比例,降低S期细胞比例,并可促进细胞迁移及侵袭,还可降低E-cadherin的表达水平及提高N-cadherin的表达水平,提示干扰miR-137可明显逆转干扰PCAT19表达对前列腺癌细胞增殖、细胞周期、迁移及侵袭的作用。
综上所述,PCAT19在前列腺癌中表达水平升高,而miR-137的表达水平降低,干扰PCAT19表达可通过上调miR-137的表达从而抑制前列腺癌细胞增殖、迁移及侵袭,并可诱导细胞周期阻滞于G0-G1期,其可能作为前列腺癌分子治疗的潜在靶点。
