中空立方Cu2S匹配醚类电解液提升储锂性能*
2021-08-04郑建勇任瑞鹏吕永康
张 发,任 晶,郑建勇,任瑞鹏,吕永康
(1. 太原理工大学 煤科学与技术教育部和山西省重点实验室,太原 030024;2. 太原重工股份有限公司焦化设备分公司,太原 030024)
0 引 言
锂离子电池自1990年问世以来,由于其能量密度高、无记忆效应、长循环寿命等优点被广泛运用于生活的各个方面[1-2]。商业化的锂离子电池负极材料主要采用稳定性好的石墨,但是其固有的理论容量低(375 mAh/g)限制了全电池容量的提升[3]。过渡金属硫化物以其高的比容量、热力学和机械稳定性、且相比与所对应氧化物具有更高的电导率,被广泛研究[4-6]。但体积膨胀、离子传输动力学缓慢、以及与电解液副反应等问题,限制了其作为锂离子电池负极的应用前景。
为了克服这些问题,大量的研究者们已经在过渡金属硫化物形貌构筑和尺寸效应方面做出了巨大的努力,如中空纳米材料已得到快速发展,它们具有大的比表面积,并且可以缩短电荷转移路径并提高电子传输能力[7-10]。其中硫化亚铜(Cu2S)是一种P型窄带隙半导体材料,在催化剂,电子元件和光敏材料中具有广泛的应用。且在不同结构的硫化铜(Cu1.8S,Cu7S4等)中,Cu2S具有更好的热稳定性[7,11-12]。此外,电解液对锂离子电池性能也是重要的影响因素,合适的电解液会导致更加稳定的SEI膜并且能够缓解电极和电解液之间的副反应[13-14]。
本文通过简单的牺牲模板法合成了中空纳米Cu2S作为锂离子电池负极材料,这种独特结构的优点是,缓解体积变化引起的结构崩塌由于内腔的存在,高比表面积促进了电解质的渗透促进离子传输,同时通过优化醚类电解液和碳酯类电解液,提高电极材料的电化学可逆性。我们的研究说明了通过对电极材料的结构设计和相对应电解液优化相结合的方法有望获得高性能锂离子电池负极材料。
1 实 验
1.1 Cu2O制备
根据以前的文献制备立方体Cu2O[15]。室温下,在持续磁力搅拌下,将0.342 g CuCl2·2H2O注入200 mL去离子水中。当温度升至60℃时,将NaOH溶液(2.0 mol/L,20.0 mL)逐滴搅拌30 min,溶液从蓝色变为黑色。随后,将温度调节至55℃,逐滴加抗坏血酸溶液(0.6 mol/L,20.0 mL)。搅拌3 h后,溶液的颜色完全变成深红色。将产物用乙醇和去离子水洗涤数次,并在60℃下真空过夜干燥,得到立方Cu2O。
1.2 中空立方Cu2S的制备
在超声条件下,在40 mL乙二醇中加入0.0800 g Cu2O和3.333 g的聚乙烯吡咯烷酮,向混合物中添加0.0619 g的硫代乙酰胺。之后,将混合物转移至具有聚四氟乙烯做内衬的100 mL不锈钢高压釜中,并在240下保持24 h。将产物用乙醇和去离子水洗涤几次,置于真空干燥箱60℃过夜。将上述样品浸入氨溶液(约28%)中72 h去除多余的氧化亚铜。在此期间,氨溶液每24 h刷新一次。将产物用乙醇和去离子水洗涤数次,得到中空立方Cu2S。
1.3 材料表征
用场发射扫描电子显微镜(FE-SEM)(Nova Nano SEM 450)观察形态。通过X射线衍射(XRD,PANalytical B.V.)检查晶体结构。在FEI Tecnai G2 F20 S-TWIN上进行透射电子显微镜(TEM)观察。使用Micrometritics ASAP 2010分析仪(美国)在-196℃下测量氮吸附等温线。
1.4 电化学性能测试
电化学测试是通过纽扣半电池电池(2032)进行的,纽扣电池是在氧气和水分含量<0.1×10-6的充满Ar的手套箱中制造的。将质量比为75:15:10的Cu2S活性材料,乙炔黑和聚偏二氟乙烯(PVDF)溶解在N-甲基-2-吡咯烷酮(NMP)中,用刮刀在Cu箔上浇铸浆料,然后在真空下于120 ℃干燥12 h。使用切片机切割铜箔的直径为12 mm,活性材料的质量负载为约1.2~1.5 mg/cm2。锂片用作对电极,聚丙烯微孔膜Celgard 2400 为隔膜,1M LiPF6溶于碳酸乙烯酯和碳酸二甲酯(体积比1∶1)作为碳酯类电解液,1 mol/L LiTFSI溶于二甘醇二甲醚作为醚类电解液。循环稳定性及倍率性能是在NEWARE电池测试系统上进行的。用电化学工作站(VersaSTAT 3)进行了电化学阻抗谱(EIS)和循环伏安测试(CV)。
2 结果与讨论
2.1 样品XRD和形貌分析
如图1(a)所示,中空立方结构制备工艺过程。首先,在水浴中通过氧化还原合成立方Cu2O作为牺牲模板,然后外层合成具有立方结构的Cu2S@Cu2O。之后,通过在铵溶液中蚀刻Cu2O模板获得中空立方Cu2S。
制备的Cu2S的晶体结构通过XRD测试(图1(b))。Cu2O的所有特征峰均符合亚铜盐(PDF#78-2076))的标准卡,空间群为pn-3m,Cu2S在22.5°、27.7°、32.1°、36.1°、39.6°、46.1°、51.9°、54.6°的衍射峰与标准卡硫化铜(PDF#53-0522)的(110)、(111)、(200)、(210)、(211)、(220)、(310)、(310)晶面吻合,空间群为pm-3m。孔结构精确分析使用N2吸附/解吸等温线和相应的孔径分布图(图1c),BET模型计算的比表面积为54.211 m2/g,孔体积和平均孔径分别为0.299 cm3/g和3.818 nm。这种微孔结构不仅可以为循环过程中的体积变化提供缓冲空间,而且可以促进离子传导和电解液浸润,从而提升电化学性能。

图1 (a)样品制备过程示意图 (b)Cu2O和Cu2S的XRD图谱 (C)Cu2S的N2吸脱附等温线Fig 1 Schematic diagram of sample preparation process, XRD patterns of Cu2O and Cu2S and N2 adsorption and desorption isotherm of Cu2S
图2(a)为实验中所制备的Cu2O牺牲模板,呈现规整的立方结构,具有光滑的表面,基本没有发生团聚现象。在经过水热过程以后,在光滑的表面上均匀的生长了Cu2S且保持原本的形貌结构,在整个界面中几乎所有立方体都生长了均以稳定的Cu2S(图2(b)、(c))。破碎的立方体在一定程度上说明了中空结构Cu2S的存在(图2(d))。为进一步确定中空结构,我们对Cu2S进行了TEM测试,结果与扫描电镜相一致(图2(e))。通过高分辨率TEM(HRTEM)观察到间距为0.179 nm的晶格条纹(图2(f)),对应于Cu2S的(200)晶面与XRD结果相一致。能量色散X射线元素映射(EDX)表明整个纳米立方体中Cu、S元素的均匀分布(图2(g))。这种独特的中空立方结构不仅有利于电解液的浸润[16],暴露更多的活性位点,同时缓解电池充放电过程中的体积膨胀。

图2 (a)Cu2O的SEM图像 (b c d)Cu2S不同放大比例下的的SEM图像(e)TEM图像 (f)HRTEM 图像 (g)中空纳米立方Cu2S的EDX映射图像Fig 2 (a) Image of Cu2O SEM, (b-d) images of Cu2S images at different magnifications, (e) TEM image, (f) HRTEM image and (g) EDX mapping images of hollow Cu2S nanocubes
2.2 电化学性能
影响活性材料可逆性关键因素之一是选择合适的电解液[8,11],图3为所制备的中空Cu2S电极在不同类型电解液下的恒电流充放电曲线图。在碳酯类电解液中,尽管Cu2S电极在首圈表现出675 mAh/g的放电比容量,但首圈库伦效率低,且在随后的循环过程中,容量衰减严重。为避免深度放电下,发生的不可逆电化学反应,将放电窗口由0.01 V调整至0.5 V[10,17-19]。结果如图3(b)所示,首圈库伦效率提升,但容量逐渐衰退。这可能是由于电解液的分解和锂离子在碳酯类电解液中脱溶剂化较为困难的原因[13]。相反,在醚类电解液中,在0.5 V的放电深度下,Cu2S电极表现出较高的电化学可逆性,首圈库伦效率达到96%,且在随后的充放电过程中,容量几乎没有衰减(图3c)。综上,醚类电解液对于中空Cu2S具有好的兼容性,相比于碳酯类电解液,表现出更好的电化学可逆性。

图3 不同电解液下的充放电曲线Fig 3 Charge and discharge curves under different electrolytes
为进一步评价中空立方Cu2S的电化学性能,对其进行循环伏安扫描(CV)和长循环恒电流充放性能测试,图4(a)为所制备的Cu2S电极的循环伏安曲线,扫描速度为0.1 mV/s,电压窗口为0.5~3 V,从图中可以看出,在首圈扫描过程中,Cu2S电极在1.5 V附近展现出一个宽的还原峰对应于固体电解质膜的形成和不可逆锂离子的嵌入[20-21]。在第二圈和第三圈循环中,在2.0和1.6 V呈现出了两个可逆的还原峰,分别相对应与锂离子嵌入Cu2S活性材料中和Cu2S转化为Cu金属和Li2S的过程[22-23]。在去锂化过程中,表现为位于1.9和2.4 V的氧化峰对应于Cu金属的氧化和Li2S的转化过程。所有的氧化还原峰均与图3c的充放电曲线平台相对应。
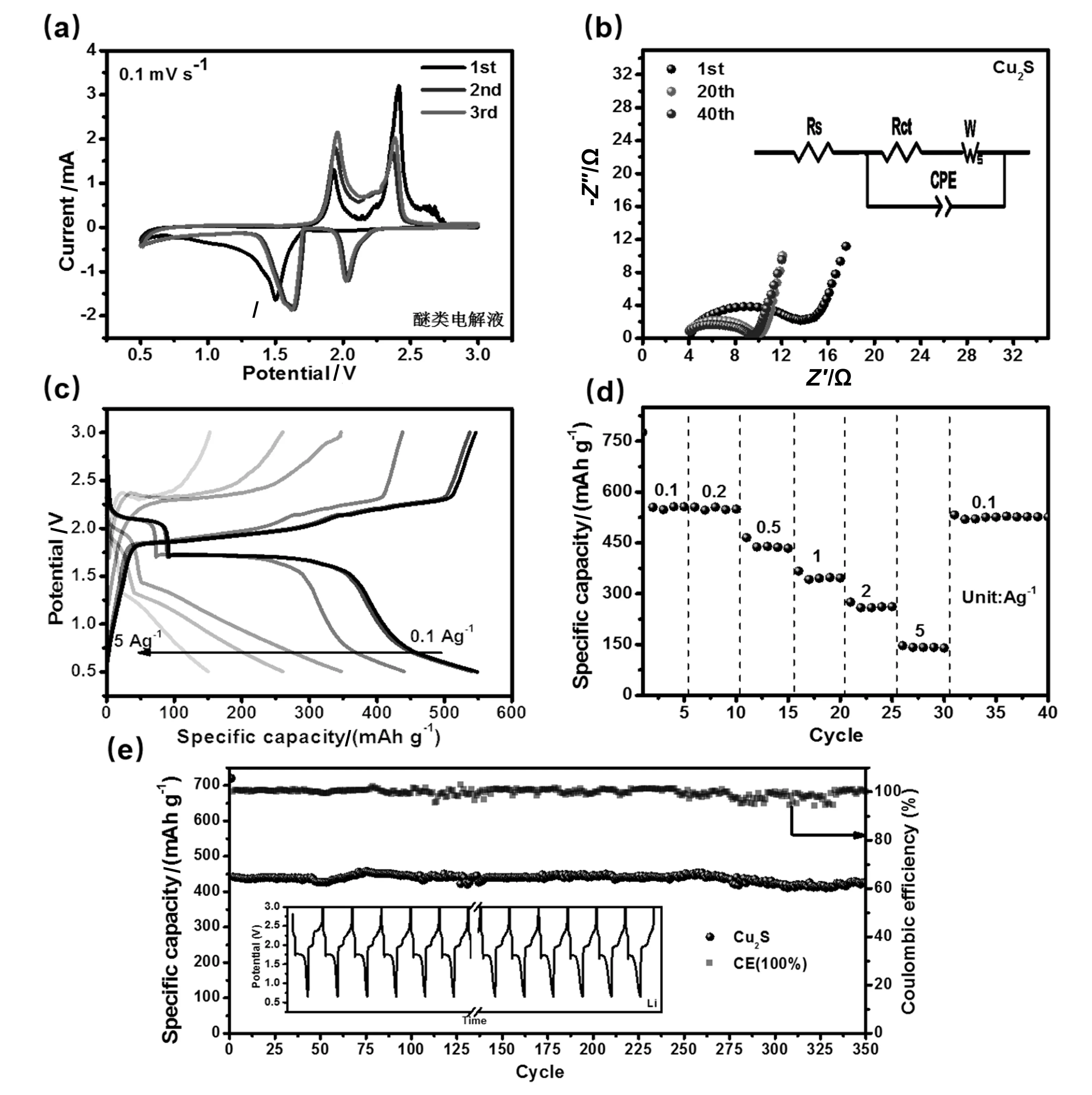
图4 (a)CV曲线在醚类电解液中(b)不同循环次数下的EIS(c)不同倍率下所对应的充放电曲线(d)倍率性能(e)在0.5 A/g的电流密度下的循环性能,插图为所对应时间电压图Fig 5 (a) CV curve in ether electrolyte, (b) EIS under different cycles, (c) the corresponding charge-discharge curve at different rates, (d) rate performance, (e) cycle performance at a current density of 0.5 A/g, the illustration shows the corresponding time-voltage curve
图4(b)为0.5 A/g电流密度下,不同循环次数的Cu2S电极的交流阻抗谱(EIS),高频区半圆直径代表电荷转移阻抗,插图为使用Z-view软件模拟的等效电路图,Rs为整个电池的欧姆阻抗、Rct为电荷转移阻抗、可以看到随着循环次数的增加,电荷转移阻抗逐渐减小,这可能是因为活性材料颗粒进一步纳米化和层间距扩大的原因[11]。图4(c、d)为Cu2S电极的倍率性能及所对应的从放电曲线,在0.1、0.2、0.5、1、2、5 A/g的电流密度下分别表现出553、548、452、353、275、148 mAh/g的可逆比容量,且当调整电流密度恢复到0.1 A/g,可逆比容量几乎没有衰减,表明中空立方Cu2S好的结构稳定性,能够适应大电流的冲击,表现良好的倍率性能。图4(e)为所制备的中空立方Cu2S电极在0.5 A/g的电流密度下的长循环性能,插图为相对应的时间电压曲线。从图中可以看出,由于电池的首圈化成过程,展现出715 mAh/g较高比容量,首圈库伦效率为62.9%,在随后的循环过程中,电极比容量保持平稳状态,经过循环350圈以后依然能够保持448 mAh/g的可逆比容量,且库伦效率几乎接近100%。相比于最近报道的过渡金属硫化物电极材料,具有一定的优势,如Cu2S/C (0.2 A/g,100圈以后110 mAh/g)[24]、Cu2S-MoS2纳米片(0.05 A/g,100圈以后320 mAh/g)[25]。如此优异的电化学性能,归因于中空立方Cu2S结构稳定性非常好,中空结构缓解了其体积膨胀,同时较大的比表面积,有利于电解液浸润,提升了离子的传输性能和电化学反应的可逆性。
3 结 论
(1)通过以Cu2O纳米立方体作为牺牲模板,经过水热反应和模板刻蚀后,成功的制备了中空立方Cu2S锂离子电池负极材料,中空纳米结构能够为体积膨胀提供缓冲空间,高比表面积能够便于电解液的浸润,缩短离子扩散路径,提升锂离子传输性能。
(2)将中空立方Cu2S作为负极材料,相比于在碳酯类电解液环境中,醚类电解液下显示了更加优异的电化学性能,拥有更高的电化学可逆性,提升了电池的库伦效率,使用醚类电解液有效的降低活性材料的分解,提升电极材料的电化学可逆性。
(3)所制备的Cu2S电极在醚类电解液中表现出高的电化学可逆性,良好的倍率性能(1 A/g电流密度下,容量为350 mAh/g),长循环稳定性(0.5 A/g电流密度下,350圈以后,保持容量为448 mAh/g)。研究结果表明通过对活性材料的结构设计以及对电解液的优化,能够实现优异的电化学性能,对制备高比容量锂离子电池负极材料具有指导意义。
