舒马普坦脂质体的处方与制备工艺优化
2021-08-03屈晓梅强永在
屈晓梅,强永在
(内蒙古医科大学附属医院药剂部,内蒙古 呼和浩特 010050)
舒马普坦,化学名为3-(2-(二甲胺基)乙基)-N-甲基-1H-吲哚-5-甲烷磺酰胺,对5-HT1D受体具有高度选择性,可收缩颅内血管,改善脑血流供应,因此常用作治疗偏头痛[1]。目前美国FDA批准的剂型有注射剂、片剂和鼻喷剂;国内上市销售的为片剂和胶囊剂,舒马普坦口服给药虽然吸收迅速,但首过效应显著,导致其生物利用度仅为14%[2];舒马普坦注射剂起效快,但注射部位反应、发热、头晕、恶心、呕吐等副作用发生率较高[3],影响其临床应用。脂质体(liposome)是由卵磷脂和胆固醇制备而成的一种新剂型,具有双分子层结构,性质类似于细胞膜,囊泡内腔可以包裹疏水性或亲水性药物,可以增加难溶性药物的水溶性、提高药物的稳定性,同时兼有良好的生物相容性、无免疫原性、增强靶向性等优点[4,5]。因此,为提高舒马普坦的治疗指数、降低不良反应发生率,本研究拟采用乙醇注入法制备舒马普坦脂质体,在单因素考察的基础上结合响应面分析法对制备工艺进行优化,并对包封率、载药量、粒径、Zeta电位等制剂学性质进行评价,为开发注射用舒马普坦脂质体提供理论依据。同时通过本研究,丰富舒马普坦临床给药手段,给患者提供更多、更便利的用药选择。
1 仪器与试药
Waters Acquity超高效液相色谱仪(美国沃特世公司),LC-500超声波清洗仪(山东济宁鲁超超声设备有限公司),2000型旋转蒸发器(郑州生化仪器有限公司),ZEN3690粒径测定及ZETA电位仪(英国马尔文公司)。
舒马普坦(广州隽沐生物科技有限公司,含量>98%,批号JM-6430);卵磷脂购自阿达玛斯(纯度>98%,批号011008202);胆固醇(艾伟拓医药科技有限公司,批号B61251);乙腈为色谱纯。
2 方法与结果
2.1 舒马普坦的UPLC测定方法
2.1.1 色谱条件[6]Waters BEH C18色谱柱(2.1 mm×50 mm,1.7μm);流动相为乙腈-水(25:75,醋酸调节pH5),流速0.3 mL/min,进样量5μL,检测波长228nm。
2.1.2 供试品溶液的制备 精密吸取舒马普坦脂质体悬浮液0.5 mL,置于10 mL量瓶中,甲醇溶解并定容,摇匀,0.22μm微孔滤膜过滤后,即得。
2.1.3 标准曲线的建立 精密称取舒马普坦对照品14.6 mg,甲醇溶解并定容至100 mL量瓶,作为对照品贮备液(浓度146μg/mL)。分别精密吸取该对照品贮备液0.1、0.5、1.0、2.0、3.0、5.0mL于10mL量瓶中,流动相定容,即得质量浓度分别为1.46、7.30、14.6、29.2、43.8、73.0μg/mL的系列对照品溶液,按“2.1.1”色谱条件进样,记录色谱峰面积,以峰面积(Y)对质量浓度(X)进行线性回归,得回归方程为:Y=983.42X+564.2(r=0.9997),结果表明,舒马普坦在质量浓度1.46-73.00μg/mL范围内,峰面积与浓度之间线性关系良好。
2.1.4 精密度试验 取质量浓度分别为7.30、29.2和73.0μg/mL的对照品溶液注入超高效液相色谱仪,分别连续进样6次,记录舒马普坦峰面积,考察日内精密度,结果RSD分别为0.35%、0.54%和0.42%;另取质量浓度分别为7.30、29.2和73.0μg/mL的舒马普坦溶液,连续测定3天,记录峰面积,考察日间精密度,结果RSD分别为0.57%、0.64%和0.49%。舒马普坦的日内和日间精密度均<1%,表明精密度良好,满足方法学验证要求。
2.1.5 稳定性试验 取同一供试品溶液,分别于0、1、2、4、6、8 h进样5μL,测定舒马普坦峰面积,计算RSD为1.17%,表明供试品溶液在8 h内稳定。
2.1.6 重复性试验 取同一批样品6份,按“2.1.2”项下方法制备供试品溶液,分别进样5μL,测定舒马普坦峰面积,计算RSD为0.65%,表明该方法重复性良好。
2.1.7 回收率试验 取同一批已知浓度的舒马普坦脂质体供试品9份,分别加入相当于样品含量80%、100%和120%的舒马普坦对照品储备液,进样测定峰面积,计算加样回收率,结果见表1。结果舒马普坦的平均回收率为98.71%,RSD为1.05%,表明方法准确度较高。

表1 舒马普坦回收率试验
2.2 舒马普坦脂质体的制备[7]
采用乙醇注入法制备舒马普坦脂质体,具体操作如下:精密称取处方量的卵磷脂和胆醇,用适量无水乙醇溶解后,边搅拌边加入溶解舒马普坦的磷酸盐缓冲液(pH 6.6),水浴超声30 min得白色混悬液;在40℃旋转蒸发仪中去除有机溶剂,即得半透明带有淡蓝色乳光的脂质体悬浮液。
2.3 脂质体包封率及载药量的测定[8]
采用超速离心法分离游离舒马普坦和舒马普坦脂质体。精密量取制备好的脂质体悬浮液1.0 mL,甲醇破乳并定容至5 mL量瓶,0.22μm微孔滤膜过滤后进样测定,带入回归方程计算得到舒马普坦浓度及药物量(W总);另取等量脂质体悬浮液,离心15 min(转速为10000 rpm)滤过,续滤液进样测定,带入回归方程计算得到游离舒马普坦浓度及游离药物量(W游离),计算包封率(%)=(W总-W游离)/W总×100%,载药量=(W总-W游离)/M总×100%,M总表示脂质体总质量。
2.4 单因素试验
2.4.1 卵磷脂/胆固醇质量比对脂质体包封率的影响 固定舒马普坦/卵磷脂质量比为1:15,磷酸盐缓冲液pH为6.6,水合时间为20 min,超声时间为30 min,旋蒸温度40℃;改变卵磷脂/胆固醇质量比(3:1、5:1、7:1、9:1、11:1)制备脂质体。测得包封率分别为46.21%、58.47%、50.18%、45.27%、41.68%。结果表明包封率随着卵磷脂/胆固醇质量比增加,呈现先增加后降低的趋势,当卵磷脂/胆固醇质量比5:1时,舒马普坦脂质体的包封率最高。
2.4.2 药物/卵磷脂质量比对脂质体包封率的影响固定卵磷脂/胆固醇质量比为5:1,其余条件同“2.4.1”,改变舒马普坦/卵磷脂质量比(1:5、1:10、1:15、1:20、1:25)制备舒马普坦脂质体,测得包封率分别为52.18%、56.39%、59.94%、57.21%、55.38%。结果表明舒马普坦/卵磷脂质量比1:15时,脂质体的包封率最高,比例过高或过低,包封率均下降。
2.4.3 超声时间对包封率的影响 固定卵磷脂/胆固醇质量比为5:1,舒马普坦/卵磷脂质量比为1:15,其余条件同“2.4.1”,超声时间分别设置为10、20、30、40、50 min制备舒马普坦脂质体。测得包封率分别为46.34%、53.66%、63.37%、59.26%、54.31%。结果表明,随着超声时间的延长,舒马普坦脂质体包封率先增大后减小,超声30 min最为适宜。
2.4.4 水合时间对包封率的影响 固定卵磷脂/胆固醇质量比为5:1,药物/卵磷脂质量比为1:15,其余条件同“2.4.1”,水合时间分别设置为20、40、60、80、100 min制备舒马普坦脂质体。测得包封率分别为62.29%、69.32%、65.17%、60.84%、58.59%。结果表明,40 min的水合时间最为适宜。
2.5 脂质体制备工艺优化
2.5.1 试验设计及结果 根据单因素试验结果,选取卵磷脂/胆固醇质量比(X1),舒马普坦/卵磷脂质量比(X2),超声时间(X3)和水合时间(X4)4个影响因素,以包封率(Y)为评价指标,采用Box-Behnken设计优化处方工艺,试验设计及安排见表2。
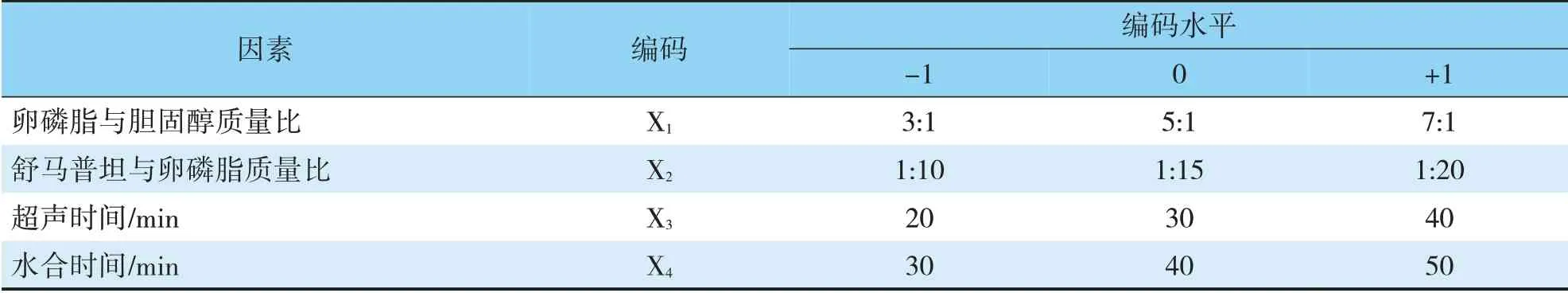
表2 试验因素及水平
2.5.2 模型拟合 实验数据用Design Expert软件处理,包括模型拟合及方差分析,得到回归方程为:Y=-437.547+22.989X1+17.731X2+7.189X3+9.653X4+0.148X1X2+0.096X1X3+0.0637X1X4-0.1195X2X3-0.0035X2X4- 0.0138X3X4- 2.951X12- 0.0848X22-0.1083X32(R2=0.9615,P<0.0001),表明拟合的模型具有显著性;而失拟项P>0.05,表明失拟项不显著,综上得出所拟合模型可准确预测实际情况。根据拟合结果,绘制3D效应面图和2D等高线图,分析影响舒马普坦脂质体包封率的因素以及因素间的相互作用,综合效应面、等高线图及方差分析结果,可以发现X1、X3、X4、X2X3、X12、X22、X32、X42的P值均小于0.05,表明其对包封率影响显著。利用Design Expert软件,以包封率最大为指标,预测超声法制备舒马普坦脂质体的最优工艺为:卵磷脂/胆固醇质量比5.4:1,舒马普坦/卵磷脂质量比1:14,超声时间31 min,水合时间42 min,预测包封率为77.01%,按此处方工艺制备3批舒马普坦脂质体,测得包封率分别为76.74%、77.19%和76.84%,平均值为76.91%,RSD为0.32%,与预测值较为接近,说明该模型准确可靠,可以用响应面法对舒马普坦脂质体的处方及制备工艺进行优化。
2.6 脂质体载药量、粒径和Zeta电位的测定
取最优工艺下制备的舒马普坦脂质体,测定计算其载药量为8.42%(w/w);另将舒马普坦脂质体悬浮液稀释一定比例,用马尔文粒度分析仪测定,结果平均粒径为(172.2±18.4)nm,多分散指数(PDI)为(0.216±0.003),Zeta电位为(-21.3±1.6)mV。
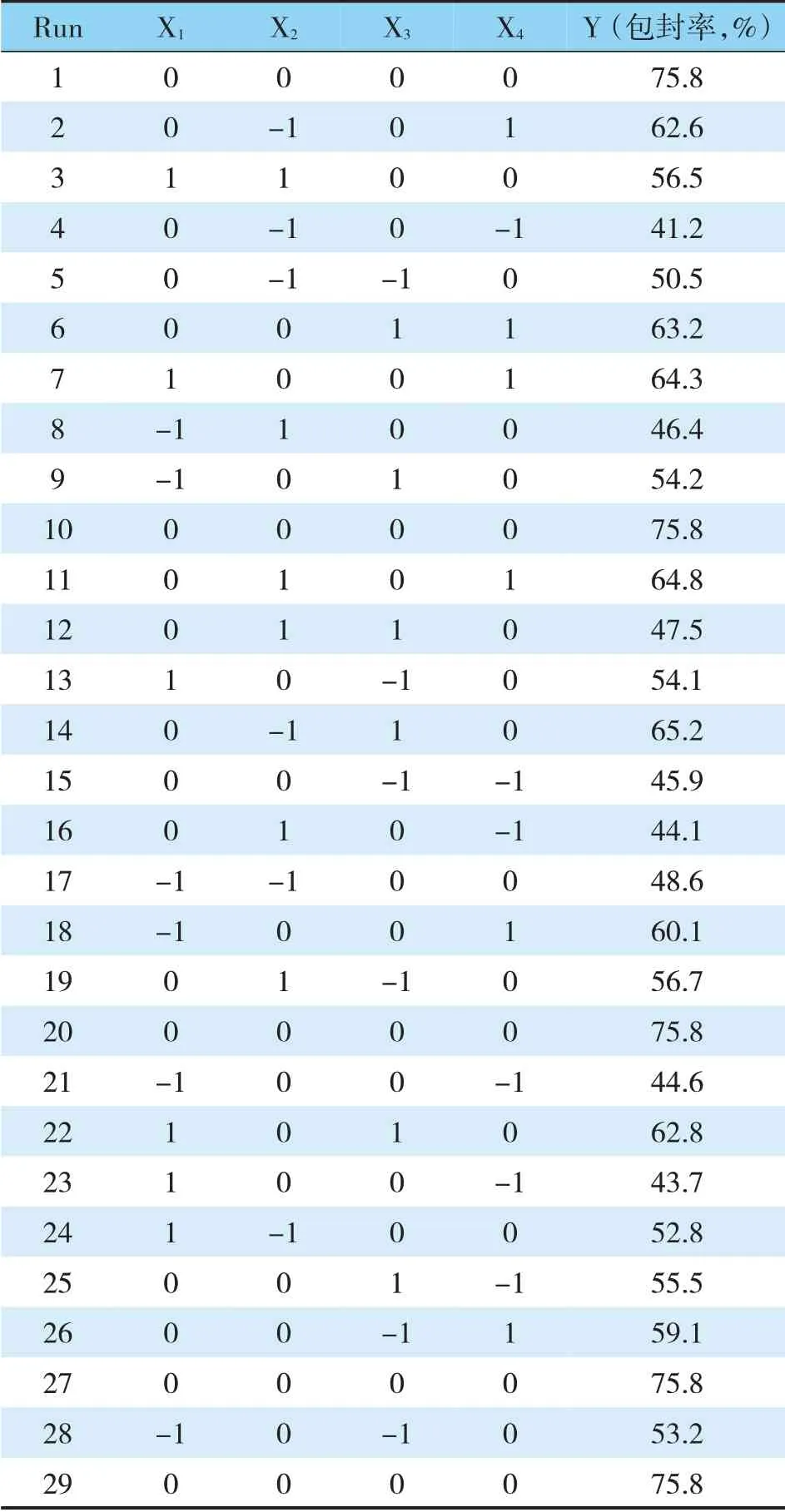
表3 试验安排及结果

图1 包封率与各因素间的3D效应面图
3 讨论
脂质体的制备方法有薄膜分散法[7,8]、乙醇注入法[9]、冷冻干燥法[10]和逆向蒸发法[11]等,预实验中分别用以上几种方法制备舒马普坦脂质体,结果以乙醇注入法包封率最高,且具有操作简便,材料环保等优点,因此确定舒马普坦脂质体制备方法为乙醇注入法。脂质体包封率的常见测定方法有透析法[12]、高速离心法和葡聚糖凝胶小柱法等[13],透析法需在透析袋内外游离舒马普坦扩散达平衡后进行测定,这一过程需要10 h,等待时间较长。本试验尝试用自制葡聚糖凝胶小柱分离脂质体,结果葡聚糖凝胶对舒马普坦保留率较低,不能将脂质体与游离药物有效分离。高速离心法操作简便,本研究发现高速离心15 min后脂质体可沉积于离心管底部,实现脂质体与游离药物的有效分离,因此本试验选择超速离心法测定包封率。
确定了脂质体的制备方法和包封率的测定方法后,选择卵磷脂/胆固醇质量比,舒马普坦/卵磷脂质量比,超声时间和水合时间4个因素进行单因素实验,初步确定了最优值的范围,在此基础上进行了4因素3水平的Box-Behnken实验设计,得到舒马普坦脂质体的最佳制备工艺,验证试验表明此条件下制备的舒马普坦脂质体包封率为(76.91±0.24)%,与预测值接近,说明预测的工艺合理可行。本方法制备的脂质体载药量略低,可能与卵磷脂用量较高有关(舒马普坦/卵磷脂为1:14),载药量与文献报道接近[14,15]。今后工作需从辅料选择及制备工艺两方面入手,通过考察选择优良的高性能辅料,再经进一步的处方优化,制备出包封率与载药量均高的脂质体。
