CuS促进Fe(III)/H2O2体系降解苯胂酸的研究
2021-08-02石云霄武汉工程大学化工与制药学院湖北武汉430205
石云霄(武汉工程大学化工与制药学院,湖北 武汉 430205)
0 引言
芬顿氧化技术通过Fe(II)分解H2O2反应生成强氧化性的羟基自由基(·OH),可实现污染物的氧化降解[1]。该技术具有成本低、操作简便等优点,因此被广泛用于降解有机污染物[2-4]。但传统芬顿反应中Fe(II)被氧化成Fe(III)后易水解沉淀并生成大量铁泥,导致芬顿反应无法持续发生,进而影响污染物降解效率[5-6]。因此,调控芬顿体系中Fe(III)/Fe(II)循环、阻止其水解沉淀,是提高芬顿体系降解污染物效率的重要途径。最近,Xing等[7]报道MoS2、WS2等金属硫化物可显著提升芬顿反应降解有机污染物的效率。但钼、钨等元素成本较高,开发成本低廉的助催化剂,提升类芬顿体系降解污染物效率至关重要。本研究采用溶剂热法合成CuS,研究其对Fe(III)/H2O2体系降解苯胂酸的促进作用,考察溶液pH值、CuS质量浓度和H2O2浓度对Fe(III)/H2O2体系降解苯胂酸的影响,分析CuS的稳定性和可重复使用性。
1 实验部分
1.1 实验试剂
一水合乙酸铜,上海凌峰化学试剂有限公司;无水乙醇、二硫化碳、九水合硝酸铁、氢氧化钠和盐酸,国药集团化学试剂有限公司;过氧化氢,武汉洪山中南化工试剂有限公司;以上试剂均为分析纯。苯胂酸,>99.0%,梯希爱(上海)化成工业发展有限公司;甲醇和三氟乙酸,HPLC级,北京百灵威科技有限公司。
1.2 CuS的制备及表征
CuS的制备参考了Li等[8]所报道的方法,具体步骤如下:将0.40g乙酸铜加至40 mL无水乙醇和20 mL去离子水的混合溶剂中,待其完全溶解后,再加2 mLCS2,继续搅拌20 min使其形成均匀的混合液。将上述混合液转移至具有容积为100 mL的聚四氟乙烯内衬的不锈钢反应釜中,在120 ℃下反应12 h。待反应釜冷却至室温后,将釜中生成的固体离心、洗涤,最后在60 ℃下真空干燥8 h,所得黑色固体粉末即为CuS。利用X射线粉末衍射仪(D8 ADVANCE,Bruker)分析所得产物的物相及晶体结构;利用扫描电子显微镜(S4800,Hitachi)表征所得产物的微观形貌。
1.3 苯胂酸降解实验及其检测方法
取50 mL苯胂酸溶液(20 mg/L)于100 mL锥形瓶中,依次加入定量的CuS、Fe(NO3)3和H2O2,使溶液中CuS、Fe(NO3)3和H2O2的浓度分别为0.2 g/L、50 μmol/L和1 mmol/L。反应开始后,每隔一段时间利用1 mL注射器取样并过0.22 μm滤膜。所得试样加入100 μL乙醇后待测。利用高效液相色谱仪(UltiMate 3000,Thermo Scientif ic)分析所取试样中苯胂酸的浓度。流动相为甲醇和0.1%的三氟乙酸溶液(V∶V=20∶80),流量为1.0 mL/min,进样量为10 μL,柱温保持在30 ℃,检测波长为262 nm。
2 结果与讨论
2.1 CuS的表征
图1 (a)为所得样品的XRD谱图,通过比对标准卡片库可知,该组衍射峰与六方相结构的CuS(PDF#06-0464)的衍射峰吻合,且未发现明显的杂质峰。由此可知,所得黑色固体粉末为六方相CuS,且通过该方法所得CuS纯度较高。图1(b)是CuS的SEM照片,从中可看出,所制备的CuS呈球状,直径约0.5 μm。

图1 制备的CuS的结构和形貌
2.2 CuS促进Fe(III)/H2O2体系降解苯胂酸
2.2.1 不同体系降解苯胂酸的效率对比
图2 为不同体系降解苯胂酸的效率对比结果。由图2可知,反应180 min后,传统类芬顿(Fe(III)/H2O2)体系降解苯胂酸效率为48.3%;加入0.2 g/L的CuS后,其降解苯胂酸的效率高达96.6%;相比之下,CuS/H2O2体系降解苯胂酸的效率仅为14.8%。上述实验结果表明,CuS催化H2O2分解的效率及其对苯胂酸降解的贡献远低于其促进Fe(III)/H2O2体系降解苯胂酸的作用。

图2 不同体系中苯胂酸的降解效率
2.2.2 反应条件对苯胂酸降解效率的影响
溶液pH值是影响类芬顿体系降解污染物效率的关键因素[9],其对苯胂酸降解效率的影响如图3(a)所示,溶液初始pH值为2.8、3.8、4.8和5.8时,体系降解苯胂酸的效率分别为99.4%、96.6%、50.3%和41.9%。可以看出,随着pH值的升高,该体系降解苯胂酸的效率逐渐降低。这是由于Fe3+的水解程度随着溶液pH值的降低而减弱,因此在低pH下,体系降解苯胂酸主要途径是CuS促进Fe(III)/H2O2体系产生·OH,进而增强苯胂酸的氧化降解。当溶液pH增加时,Fenton反应贡献降低,Fe3+絮凝贡献增大,但其去除苯胂酸效率远低于·OH氧化。
CuS的促进效果很明显,因而考察CuS的质量浓度对苯胂酸降解的影响是必要的。实验结果如图3(b)所示,CuS的投加量为0.1~0.4 g/L时,体系降解苯胂酸的效率分别为58.9%、96.6%、82.1%和72.8%。由此可知,CuS的投加量为0.2 g/L时,促进Fe(III)/H2O2体系降解苯胂酸的效果最好。CuS的投加量过多或过少均不能使体系降解苯胂酸的效率达到最佳。
H2O2的分解是体系中·OH最主要的来源,因而H2O2浓度是影响类芬顿反应的重要因素。H2O2的浓度对体系降解苯胂酸的影响结果如图3(c)所示,H2O2的浓度为0.5~2.0 mmol/L 时,体系降解苯胂酸的效率分别为93.4%、96.6%、97.1%和97.1%。H2O2浓度为1.0 mmol/L时,体系已有优良的降解苯胂酸的效率,继续加大H2O2的浓度,效率几乎没有提升,反而会增加处理成本。

图3 反应条件对苯胂酸降解效果的影响
2.2.3 CuS的重复使用性能
CuS的重复使用性能直接影响处理成本。为了探究CuS的重复使用性能,进行了5次循环降解苯胂酸的实验。结果如图4所示,在每次循环实验中,反应3 h后苯胂酸的降解率均能达到92%,表明所制备的纳米球状CuS具有良好的稳定性,能够多次重复使用,可大大降低处理成本。
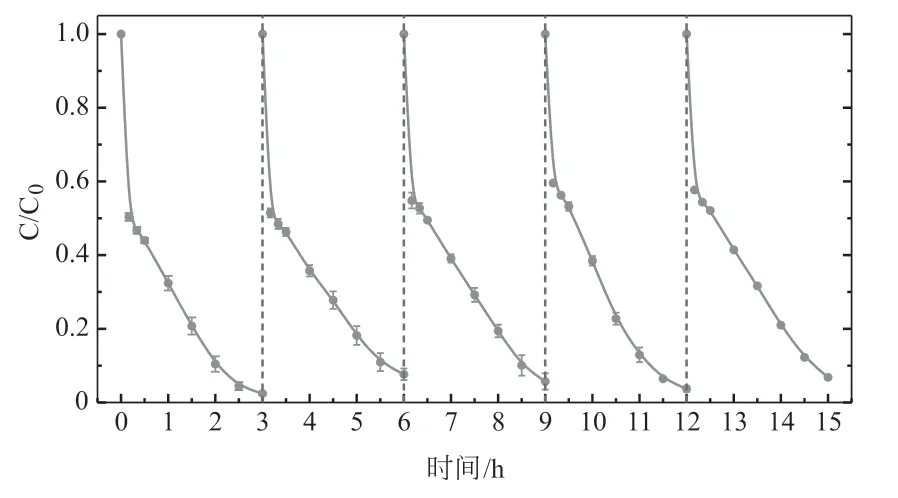
图4 CuS的可重复使用性
3 结语
采用溶剂热法成功制备的CuS能显著地促进Fe(III)/H2O2体系降解苯胂酸,反应180 min后苯胂酸的降解率即可达到96.6%,显示其具有较高的反应活性。溶液初始pH值和CuS的质量浓度对体系降解苯胂酸的影响较大,H2O2浓度对体系降解苯胂酸的影响较小。CuS在溶液初始pH值为3.8、CuS的质量浓度为0.2 g/L、H2O2浓度为1 mmol/L、Fe3+浓度为50 μmol/L的反应条件下重复使用5次,体系仍然能使苯胂酸的降解率在反应180 min后达到92%,表明所制备的CuS具有良好的可重复使用性。
