阳离子魔芋葡甘聚糖的制备与表征
2021-07-23张馨如李晓丹郭丽萍黄国清肖军霞
张馨如,李晓丹,郭丽萍,黄国清,肖军霞
(青岛农业大学食品科学与工程学院,山东青岛 266109)
魔芋葡甘聚糖(konjac glucomannan,KGM)又称魔芋葡甘露聚糖、魔芋胶、魔芋粉,是一种从魔芋(Amorphophallus rivieri)块茎中提取的中性半纤维素复合杂多糖,具有良好的持水性、增稠性、凝胶性和成膜性,同时还拥有优异的结肠靶向传输能力,因此在食品加工、生物医药和功能材料等领域具有广泛的应用[1]。多糖-蛋白质之间的相互作用及两者形成的复合物在食品、医药、化妆品、材料等领域显示出了极大的应用前景[2−4],是当前的一个研究热点。然而,天然KGM不带电荷,这限制了KGM在这一新兴领域的应用。对KGM进行离子化改性使其带上电荷后可以与多种带相反电荷的聚电解质通过静电相互作用相结合,这对于拓展KGM的应用范围具有重要意义。
目前KGM的离子化改性方法主要有阳离子化改性和阴离子化改性两种,其中阴离子化改性是最常见的方法,其技术已日趋完善,相关报道也较多。常见的阴离子改性剂有乙酸[5]、聚乙烯亚胺[6]、十六烷基三甲基氯化铵等[7]。例如,肖蕊等[8]用乙酸对KGM进行羧甲基化处理得到了不同取代度的羧甲基魔芋葡甘聚糖(carboxymethyl konjac glucomannan,CMKGM),然后选取适当取代度的CMKGM制膜并测定其机械性能,发现改性后膜的性能得到了很大改善。
相比较而言,KGM的阳离子化改性目前可见文献相对较少。已经报道的阳离子化改性方法有酯化法[9]、醚化法[10]、添加加成试剂法[11]等,其中醚化法最为常见且主要的醚化剂包括环氧丙烷[12]、阳离子瓜尔胶[13]、三聚磷酸钠[14]等。3-氯-2-羟丙基三甲基氯化铵(3-Chloro-2-hydroxypropyltrimethyl ammonium chloride,HAT)是一种重要的阳离子醚化剂,它容易与含有活泼氢的化合物发生化学反应而得到含有季铵基的衍生物,该反应副产物少、工艺简单,已被广泛用于淀粉、壳聚糖等天然多糖的阳离子化改性,在KGM改性中的应用也已有少量报导。牛春梅等[15]以HAT为醚化剂、异丙醇为分散剂对魔芋精粉进行阳离子化改性以制备阳离子KGM(cationic KGM,CKGM),研究了HAT用量、催化剂NaOH用量、反应温度和反应时间对取代度的影响,发现反应程度过高或过低都不利于CKGM取代度的提高,这为HAT在KGM改性中的应用提供了重要参考。聚电解质在静电相互作用领域的应用与其zeta电势密切相关,但是目前尚未见到KGM的HAT醚化改性条件与其衍生物zeta电势之间关系的报导,这在一定程度上限制了CKGM在聚电解质复合物、多层乳液、微囊化等领域的应用。
针对上述问题,本文拟以HAT为醚化剂对KGM进行阳离子改性以改善其理化性质,研究反应温度、反应时间及催化剂NaOH和醚化剂HAT用量对CKGM zeta电势的影响,并研究CKGM的zeta电势与其溶解度、乳化能力、微观结构和粘弹性等性质之间的关系,并对其与大豆分离蛋白(soybean protein isolate SPI)发生静电相互作用的能力进行初步研究,以期为拓展CKGM作为一种新型阳离子聚电解质在食品工业中的应用提供理论依据。
1 材料与方法
1.1 材料与仪器
魔芋精粉(食品级)湖北强森魔芋科技有限公司;大豆色拉油(食品级)润泰集团有限公司;SPI(食品级)山东高唐蓝山团;HAT(分析纯)上海麦克林生化科技公司;异丙醇、NaOH、无水乙醇分析纯,莱阳市康德化工有限公司。
BS214D分析天平 赛多利斯科学仪器有限公司;DF-101S集热式恒温磁力搅拌器 巩义市予华仪器有限公司;FE20 pH计 梅特勒-托利多仪器有限公司;DC-26MT低温恒温槽 宁波天恒仪器厂;FJ200-SH数显高速分散均质机 上海标本模型厂制造;DL-5-B低速大容量离心机 上海安亨科学仪器厂;HH-S2 数显恒温水浴锅 金坛市医疗仪器厂;SHZ-Ⅲ循环水真空泵 上海亚荣生化仪器厂;MCR102 动态剪切流变仪 奥地利安东帕有限公司;ZEN3690 马尔文动态光散射仪 英国马尔文公司;JSM-840A扫描电子显微镜 日本电子株式会社;NicoleIR200 傅里叶变换红外光谱仪 赛默飞世尔科学仪器公司;200V-1000V电子调温万用电炉中国龙口市先科仪器公司;DGX-9243 电热鼓风干燥箱 上海福玛实验设备有限公司。
1.2 实验方法
1.2.1 CKGM的制备 将5 gKGM缓慢加入到装有30 mL异丙醇的烧杯中,在磁力搅拌器搅拌下滴加NaOH,在一定温度下反应一段时间后加入HAT,继续搅拌使到达反应设定时间后,用1 mol/L HCl调节溶液pH至6.0。向反应体系中加入无水乙醇使乙醇浓度达到80%(v/v),静置30 min后收集沉淀,用80%(v/v)的乙醇水溶液冲洗数次,于50 ℃烘箱内烘干至恒重,研磨成粉即得CKGM,置于干燥器中备用[16]。
1.2.2 反应条件对CKGM zeta电势的影响
1.2.2.1 反应时间的影响 按照1.2.1 的方法,使NaOH和KGM的质量比为1:1、HAT和KGM的质量比为1:2,在40 ℃下分别反应1、1.5、2、2.5、3 h后制得CKGM,使用马尔文动态光散射仪测定其zeta电势。
1.2.2.2 反应温度的影响 按照1.2.1 的方法,使NaOH和KGM的质量比为1:1、HAT和KGM的质量比为1:2,调节反应温度分别为40、45、50、55、60 ℃,反应1 h后制得CKGM,使用马尔文动态光散射仪测定其zeta电势。
1.2.2.3 催化剂NaOH用量的影响 按照1.2.1 的制备方法,使HAT和KGM的质量比为1:2、NaOH和KGM的质量比分别为1:1、1.5:1、2:1、2.5:1 和3:1,在40 ℃下反应1 h后制得CKGM,使用马尔文动态光散射仪测定其zeta电势。
1.2.2.4 醚化剂HAT用量的影响 按照1.2.1 的制备方法,使HAT和KGM的质量比分别为1:1、1.5:1、2:1、2.5:1 和3:1,NaOH和KGM的质量比为1:1,在40 ℃下反应1 h后制得CKGM,使用马尔文动态光散射仪测定其zeta电势。
1.2.3 CKGM zeta电势的测定 将CKGM粉末溶解于去离子水中使其浓度达到0.1%(w/v),取1 mL溶液注入ZEN3690 马尔文动态光散射仪的样品池中,于室温下测定zeta电势。
1.2.4 CKGM溶解性的测定 取约0.1 gCKGM粉末(记为W)于烧杯中,倒入24.9 g的去离子水冰块,于0 ℃冰浴中保持1 h直至冰块完全融化。将该溶液于4000 r/min下离心20 min,取上清液于105 ℃干燥箱中干燥至恒重,记为m,按下式计算CKGM的溶解度:
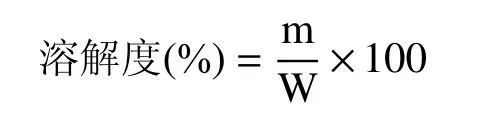
1.2.5 CKGM乳化能力及乳液稳定性的测定 取0.1 gCKGM于烧杯中,倒入24.9 g的去离子水冰块,于0 ℃下维持约1 h直至冰块完全融化。向该溶液中缓慢加入8.3 mL大豆色拉油,用FJ200-SH数显高速分散均质机于10000 r/min下分散5 min。将乳状液转移至10 mL刻度离心管中,3000 r/min离心15 min,记录乳化层高度和液体总高度,按下式计算CKGM的乳化能力(emulsification activity index,EAI)。

将所得乳液静置24 h后3000 r/min离心15 min,记录离心管中乳化层的高度和液体总高度,按下列公式计算乳液稳定性(emulsion stability index,ESI)[17]。

1.2.6 FTIR分析 将CKGM粉末与干燥的KBr按1:100 质量比混合,压片后于NicoleIR200 傅里叶变换红外光谱仪上在波数400~4000 cm−1范围内以分辨率4 cm−1进行扫描分析,每个样品扫描32 次[14]。
1.2.7 微观结构分析 在样品台上贴上一层双面胶,取适量CKGM放置于样品台上,然后喷金供SEM观察,电压为2 kV[18]。
1.2.8 流变学特性研究 将质量分数为0.01%(w/v)的CKGM水溶液置于校正好的MCR102 动态流变仪平台上,在(30±0.2)℃下,用锥板(1 º)在板间距离为0.1 mm的条件下进行频率扫描。频率扫描的范围为0~50 Hz,记录溶液储能模量(G′)和损耗模量(G′′)随扫描频率的变化。
1.2.9 CKGM与SPI的相互作用 将浓度均为1%(w/v)的CKGM溶液与SPI溶液等体积混合,调节pH至6.0,静置24 h,观察反应体系的外观并拍照。
1.3 统计分析
每个实验重复3 次,结果以平均值±标准差表示。采用SPSS统计软件(SPSS Statistics 17.0.1)进行t检验和方差分析,当P<0.05 时认为差异显著。
2 结果与分析
2.1 反应条件对CKGM zeta电势的影响
2.1.1 反应时间和反应温度对CKGM zeta电势的影响 反应时间、反应温度对CKGM zeta电势的影响见图1。可以看出,在本文所选择条件下得到的CKGM均带正电荷,表明成功发生了改性反应。当反应时间低于1.5 h时,CKGM的zeta电势随着反应时间的延长逐渐变大,当反应时间为1.5 h时达到最大值30.3 mV;此后,随着反应时间的进一步延长,CKGM的zeta电势开始下降,当反应时间为3.0 h时达到最小值6.68 mV(图1a)。反应温度对CKGM zeta电势的影响也呈现出类似的趋势,反应温度为55 ℃时CKGM的zeta电势达到最大值32.3 mV;随着反应温度的进一步升高,CKGM的zeta电势随之降低,当反应温度为60 ℃时zeta电势接近于0(图1b)。这一趋势与这两个因素对CKGM取代度的影响一致,可能是由于反应时间过长或反应温度过高时会导致多种副反应的发生[15],从而使得CKGM电荷随着反应程度的增加而增加的趋势不一致。因此在利用HAT制备CKGM时需严格控制反应的程度以获得所需的zeta电势,反应程度过高或过低均不利于CKGM zeta电势的提高。
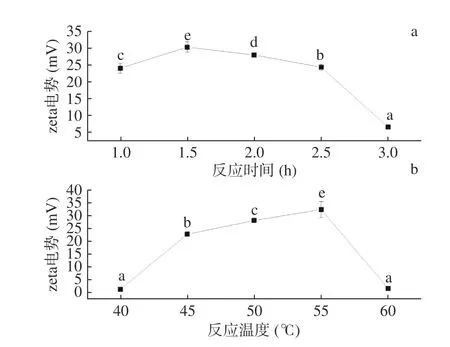
图1 反应时间(a)和反应温度(b)对CKGM zeta电势的影响Fig.1 Effect of reaction time and temperature on the zetapotential of CKGM
2.1.2 醚化剂HAT和催化剂NaOH用量对CKGM zeta电势的影响 催化剂NaOH和醚化剂HAT用量对CKGM zeta电势的影响见图2。随着NaOH(图2a)和HAT(图2b)用量的逐渐增加,CKGM的zeta电势均呈现先增加后减小的趋势,当HAT和KGM的质量比为2:1、NaOH和KGM的质量比为2:1 时,CKGM zeta电势分别达到最大值,均为36.0 mV。这可能是当体系中有少量HAT和NaOH存在时,CKGM的结合位点并未达到饱和,此时CKGM的 zeta电势随着两者用量的增加而增大;当zeta电势达到最大值后,CKGM的结合位点达到饱和,此时再继续增加HAT会导致反应体系中水含量的增加[15],不利于反应的进行,且NaOH过量不但会加速CKGM的分解,还会大量聚集在CKGM表面并中和CKGM所带的正电荷,从而导致zeta电势变小。张朝辉等[19]使用HAT醚化十二烯基琥珀酸酯化淀粉浆料时也发现,酸化淀粉的zeta电势随着醚化剂HAT的加入呈现先增加后减小的趋势。
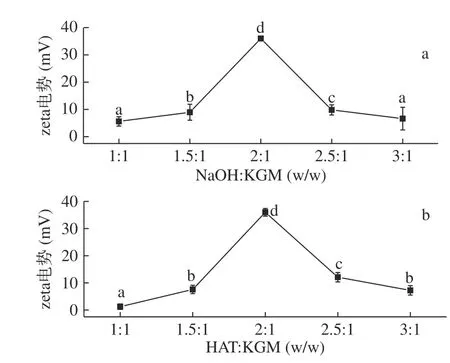
图2 催化剂NaOH(a)和醚化剂HAT(b)和用量对CKGM zeta电势的影响Fig.2 Effects of NaOH (a) and HAT(b) amount on the zetapotential of CKGM
上述研究表明,反应时间、反应温度及醚化剂和催化剂用量均可对CKGM所带电荷量产生重要影响。为了研究CKGM的zeta电势与其性质之间的关系,本文在反应温度为55 ℃、NaOH和KGM的质量比为2:1、HAT和KGM的质量比分别为1:1、1.5:1 和2:1 条件下反应1.5 h制得了zeta电势分别为4.79、23.3 和36.0 mV的CKGM对其进行后续研究,以未改性的KGM为参照。
2.2 溶解性
CKGM的zeta电势对其溶解度的影响见图3。可以看出,HAT醚化改性可以显著提高KGM的溶解性,且随着zeta电势的增加,CKGM的溶解性越大,这与CMKGM溶解性与其电荷密度之间的关系一致[20]。未改性的KGM样品的溶解度为55%,而改性后的CKGM溶解度均在65%以上,且当zeta电势为36.0 mV时达到最大值78%。造成这种现象的原因可能是由于随着醚化反应程度的增加,KGM分子链中大量羟基被阳离子所取代,导致CKGM分子之间形成氢键的能力减弱;同时随着电荷密度的增加,CKGM胶体之间的排斥作用也随之增强,这进一步阻止了它们之间的聚集,从而使得CKGM的溶解性显著提高[1,16]。
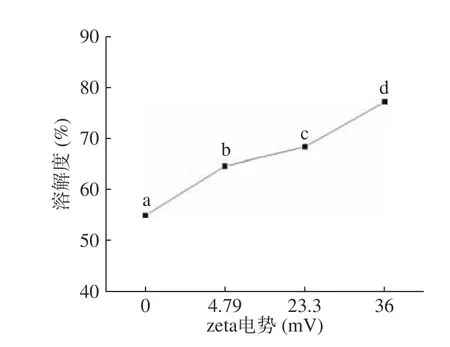
图3 zeta电势对CKGM溶解性的影响Fig.3 Effects of zetapotential on the water solubility of CKGM
2.3 乳化能力及乳液稳定性
CKGM的zeta电势对其乳化性能的影响见图4。可以看出,天然KGM并没有乳化能力,但经过HAT醚化改性后开始具备一定的乳化能力,且随着zeta电势的增加,CKGM的乳化能力和乳液稳定性均呈现先增加后降低的趋势,且均在zeta电势为23.3 mV时达到最大值分别为22.7%和21.3%(图4a~b)。这是由于HAT是一种季铵型阳离子表面活性剂,其与KGM发生醚化反应也会赋予后者一定的乳化能力,且随着醚化反应程度的增加CKGM的乳化能力随之增加;但是当醚化反应程度过高、即CKGM的zeta电势过大时,CKGM的亲水性过强、溶解性过大,导致其乳化能力和乳液稳定性反而开始降低。
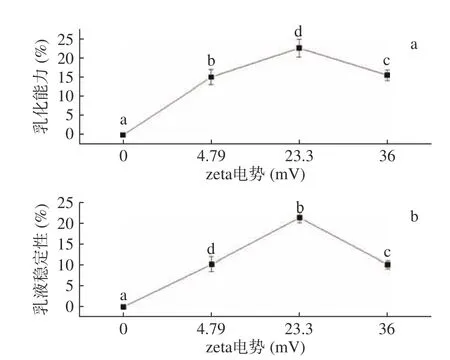
图4 zeta电势对CKGM乳化性能(a)和乳液稳定性(b)的影响Fig.4 Effect of zetapotential of on the emulsification ability (a)and emulsion stability (b) of CKGM
2.4 FTIR分析
不同zeta电势CKGM的红外光谱见图5。对于KGM,3361 和3393 cm−1为-OH的伸缩振动,1160 和1083 cm−1归属于-CH2-O-CH2的伸缩振动[21]。经过阳离子醚化改性后在3030、3027 和3029 cm−1处出现了新的振动峰,可以归属于-CN伸缩振动,且随着CKGM的zeta电势的增加,这一伸缩振动频率逐渐增强,而这类伸缩振动在KGM中并不存在,这说明KGM与HAT发生了醚化反应。
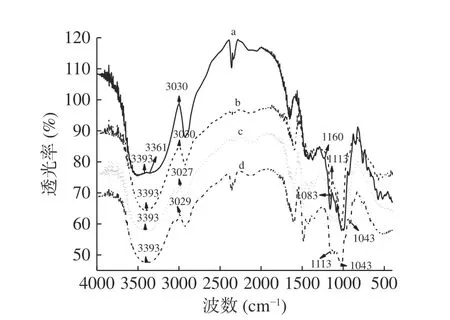
图5 KGM(a)和zeta电势为4.79 mV(b)、23.3 mV(c)和36 mV(d)时 CKGM的红外光谱图Fig.5 FTIR spectra of KGM (a)and CMKGM with zeta potential 4.79 mV (b),23.3 mV (c) and 36 mV (d)
2.5 微观结构分析
不同zeta电势CKGM的微观结构见图6。可以看出,天然KGM颗粒表面光滑有凹陷(图6a);经过醚化处理后得到的CKGM颗粒仍呈球状、表面有皱缩,且其粒径随着zeta电势的增加而降低(图6b~d),这进一步证实KGM成功发生了化学反应,HAT醚化改性破坏了KGM原有的微观结构,且醚化反应程度越大、zeta电势越高,CKGM的结构变化越明显、粒径越小[22]。

图6 KGM(a)和zeta电势为4.79 mV(b)、23.3 mV(c)和36 mV(d)时CKGM的扫描电镜图(500×)Fig.6 SEM graphs of KGM (a) and CKGM with zeta potential 4.79 mV (a),23.3 mV (b) and 36 mV (c) (500×)
2.6 流变学特性分析
CKGM的zeta电势对其流变学特性的影响见图7。KGM的储能模量G′大于损耗模量G″(图7a),说明KGM溶液形成了凝胶并表现出了固体的性质[23],而不同电势CKGM的损耗模量G″均大于储能模量G′,且G′均接近于0(图7b~d),表现出明显的液体状态。这表明,发生醚化反应后KGM的凝胶性能显著降低,这与陈国峰等[24]对KGM醚化改性产物的流变学特性的研究结果相似,同时也与本文图3 中推测的CKGM分子间氢键被削弱的推测相对应。另外,CKGM的zeta电势对其损耗模量(G′)有重要影响。当zeta电势为4.79 mV时(图6b),CKGM溶液的损耗模量最大,表明此时溶液的粘度仍然较大,CKGM分子之间的氢键相互作用仍然较为强烈;当zeta电势为23.3 mV时(图6c),由于醚化反应程度较高、分子内和分子间氢键破坏严重,CKGM溶液的损失模量随之显著降低;但是当CKGM的zeta电势进一步增加至36.0 mV(图6d)时,虽然KGM分子间原先的氢键破坏严重,但是大量氨基的引入又增强了分子间的氢键相互作用,因此其溶液的损耗模量与23.3 mV时相比又有所增加。

图7 KGM(a)和zeta电势为4.79 mV(b)、23.3m V(c)和36 mV(d)时CKGM的频率扫描曲线Fig.7 Frequency scanning curve of KGM (a) and CKGM with zeta potential 4.79 mV (b),23.3 mV (c) and 36 mV (d)
2.7 CKGM与SPI的相互作用
当两种带相反电荷的聚电解质在溶液中共存时,两者会通过静电相互作用形成复合物并发生聚集而形成沉淀[25],因此通过观察是否有沉淀产生以及沉淀量的多少便可初步判断两者是否发生了相互作用。为了验证CKGM是否可以与带相反电荷的聚电解质发生静电吸引,本文对其与SPI在pH6.0 下的相互进行了初步研究,结果如图8 所示。

图8 CKGM溶液与SPI溶液混合后(a)及静置24 h(b)后的外观Fig.8 Appearances of the mixture of the CKGM and SPI solutions before (a) and after standing for 24 h (b)
由图8a和8b可知,KGM与带负电荷的SPI溶液混合后没有产生沉淀,混合溶液较为均一,且放置24 h后无明显变化,表明两者未发生相互作用;而CKGM与SPI混合后溶液变得浑浊,且放置24 h后有明显的沉淀析出,表明CKGM与SPI之间发生了静电相互作用并形成了不溶性复合物。CKGM的zeta电势对其与SPI的相互作用有重要影响。由图8a和8b可以看出,醚化反应程度对CKGM与SPI的相互作用及所得复合物的沉淀性能有重要影响。当zeta电势为4.79 mV时,CKGM可与SPI形成可溶性复合物,但是放置24 h后会充分沉淀;当zeta电势为36.0 mV时,CKGM与SPI的相互作用明显增强,溶液的浊度明显增加,且放置24 h会出现沉淀,但是上清液仍较为混浊。这可能是由于当醚化反应程度较低时,CKGM分子间的氢键相互作用较强,以聚集体形式存在,因此与SPI发生静电吸引后形成的复合物分子较大,因此放置之后充分沉淀;而当醚化反应程度较高时,CKGM分子间的氢键相互作用破坏严重,虽然其与SPI的相互作用程度有所增加,但是所形成的复合物粒径较小,因此放置后虽然仍然能够发生沉淀,但是其沉淀的程度不如低醚化反应程度。需要说明的是当zeta电势为23.3 mV时,CKGM与SPI的反应程度远低于另外两个zeta电势,这可能是其分子间氢键被破坏与静电相互作用相比占主导的结果。
3 结论
当反应温度为55 ℃、反应时间为1.5 h、NaOH与KGM质量比为2:1、HAT与KGM质量比为2:1 时,所得CKGM的zeta电势达到最大值36 mV,醚化反应程度过高或过低均不利于zeta电势的提高。醚化改性可以显著提高CKGM的溶解性和乳化性能,且与CKGM的zeta电势密切相关。醚化反应会改变KGM的外观形态,并使其粒径变小。CKGM可与SPI通过静电相互作用形成复合物,且zeta电势对反应程度有重要影响。因而,使用HAT可以成功对KGM进行阳离子醚化改性且改性后KGM的功能性质有了明显改善,有望在食品领域获得新的应用。
