髓内钉附加钢板与单纯髓内钉固定治疗股骨转子下骨不连的临床效果对比
2021-07-23杨思宇汪国栋刘曦明
杨思宇,汤 明,汪国栋,刘曦明,罗 红
1.中部战区总医院骨科,武汉 430070;2.南方医科大学第一临床学院,广州 510515;3.华中科技大学同济医学院附属普爱医院骨科,武汉 430033;4.宜昌市第三人民医院骨科,湖北 宜昌 443000
股骨转子下骨折发生率占所有髋部骨折的10%~34%[1-2]。股骨转子下骨折是外科医师治疗的难点,不同的骨折分型对股骨转子下的定义有所不同[1]:Seinsheimer分型定义为小转子下缘平面至其以远5cm以内的区域;AO分型定义为小转子下缘平面至其以远3cm以内的区域:Russell & Taylor分型定义为小转子下缘平面至股骨峡部之间的区域。其定义目前尚未统一,外科医师初次手术时即面临挑战,发展为骨不连时更为棘手。据报道,股骨转子下骨折术后骨延迟愈合、骨不连、内固定失效等并发症总发生率7%~20%[3-4]。如何治疗股骨转子下骨不连值得广大外科医师思考。本研究回顾性分析2015年1月—2020年1月中部战区总医院骨科采用两种不同内固定治疗的35例股骨转子下骨不连患者的临床资料,旨在对比髓内钉附加钢板与单纯髓内钉固定在股骨转子下骨不连的临床疗效。
临床资料
1 一般资料
纳入标准:(1)符合股骨转子下骨折诊断标准(Russell&Taylor分型定义为小转子下缘平面至股骨峡部);(2)符合骨不连诊断标准;(3)耐受手术。排除标准:(1)合并感染;(2)重度骨质疏松;(3)合并患肢神经血管损伤;(4)初次损伤为开放伤;(5)无法耐受手术治疗;(6)失访。
本组共收治股骨转子下骨不连患者35例,其中男性23例,女性12例;年龄35~66岁,平均47.0岁;骨不连分型:肥大型4例,萎缩型11例,营养不良型20例;初次手术采用股骨近端解剖锁定板24例,采用髓内钉或髓内钉联合钢丝11例。骨不连患者均行髓内钉固定或髓内钉附加钢板固定;对于骨折断端局部稳定的患者采用更换髓内钉固定,对于骨折断端稳定性差的患者采用髓内钉附加钢板固定,并将其分为两组:髓内钉组(14例)以及钢板强化组(21例)。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。见表1。患者术前均签署手术知情同意书。本研究获医院医学伦理委员会批准。

表1 两组患者一般资料比较
2 手术方法
髓内钉组:取股骨原手术切口进入骨折部位,取出原内固定;清除骨折断端部分骨痂及填充的纤维组织,咬除断端硬化死骨并再通髓腔。视骨折断端情况取合适大小全板髂骨,并抽吸部分红骨髓,将取出髂骨剪成条状备用。逐级扩髓后完整保留扩髓留下的髓内物质,插入直径合适的髓内器械(其中3例骨折线累及小转子即高位股骨转子下骨折,为加强骨折近端固定强度选用长Gamma3髓内钉,其余均为低位股骨转子下骨折,均使用股骨重建钉固定)。将自体骨与抽吸的红骨髓以及扩髓保留髓内物质进行充分混合,植入骨折断端后采用可吸收线或钢丝行环扎固定,使用骨刀对断端中心远近各5cm内行“鱼鳞化”处理,直至红辣椒征出现。透视满意后逐层缝合。
钢板强化组:手术方法以及植骨方法同髓内钉组。对于骨折断端不稳定的患者,取尺寸大小合适的重建钢板行植骨术并加压固定骨折断端。透视满意后逐层缝合。
3 术后处理
术前30min及术后48h内常规使用头孢菌素类抗生素预防感染,术后2周内常规皮下注射低分子肝素抗凝预防下肢深静脉血栓,所有患者应用多模式镇痛:术中常规应用鸡尾酒式镇痛混合剂封闭切口周围,术后均常规放置自控式静脉镇痛泵(patients controlled intravenous analgesia,PCIA),若疼痛明显可增加非甾体抗炎药(nonsteroidal anti-inflammatory drugs,NSAIDs)药物,或者联合应用阿片类药物辅助镇痛,手术切口隔日换药。
4 术后康复
术后炎症反应减轻后即可行踝泵、股四头肌等长收缩等功能锻炼,术后3d即使用持续被动运动(CPM)逐步行膝关节、髋关节屈伸功能锻炼(2周内屈髋60°、屈膝60°,4周内屈髋90°,屈膝90°),术后2周可扶双拐下地,术后每1个月定期复查,观察内固定位置及骨折愈合情况;视复查结果早期指导患者进行部分负重练习(一般术后2个月可部分负重,术后3~6个月完全负重),全程鼓励患者进行肢体纵向叩击训练,刺激骨折断端微动。
5 观察指标
观察对比两组患者的手术时间、术中出血量、骨折愈合时间、骨折愈合率。骨愈合标准:骨折部位无压痛、叩击痛及纵向叩击痛,X线片正侧位上4个骨皮质有3个及以上有连续性骨痂生长,骨折线模糊或消失。对比两组患者术后12个月髋关节Harris评分、美国特种外科医院(hospital for special surgery,HSS)膝关节功能评分。对比两组患者术后3、6、9个月Fernandez-Esteve放射评价骨痂等级标准评分,等级分为 5 级,Ⅰ级:骨折端无放射学骨痂;Ⅱ级:骨折端出现云雾状骨痂;Ⅲ级:骨折端正侧位片出现一侧骨痂; Ⅳ级:骨折端正侧位片出现双侧骨痂;Ⅴ级:结构性骨痂形成,分值分别为 0~4 分,分值越高表示骨痂生长情况越好。
6 统计学分析
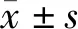
结 果
1 两组患者手术资料及骨折愈合指标比较
两组患者手术时间及术中出血量比较,差异无统计学意义(P>0.05);钢板强化组骨折愈合时间显著少于髓内钉组,差异有统计学意义(P<0.05);两组患者骨折愈合率比较差异无统计学意义(P>0.05)。见表2。

表2 两组患者手术时间、术中出血量、骨折愈合时间、骨折愈合率比较
2 两组患者术后Fernandez-Esteve骨痂评分比较
患者均门诊随访,随访时间不少于12个月;术后3个月时,两组Fernandez-Esteve骨痂评分比较差异无统计学意义(P>0.05);术后6、9个月时,钢板强化组平均Fernandez-Esteve骨痂评分显著高于髓内钉组,差异有统计学意义(P<0.05)。见表3。
3 两组患者术后髋关节及膝关节功能比较
术后12个月平均髋关节Harris评分,钢板强化组高于髓内钉组,差异有统计学意义(P<0.05);术后12个月平均膝关节HSS评分,钢板强化组高于髓内钉组,差异有统计学意义(P<0.05)。见表3。典型病例见图1、2。
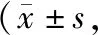
表3 两组患者术后3、6、9个月Fernandez-Esteve骨痂评分、术后12个月髋关节Harris评分以及HSS评分比较分)

图1 患者男性,53岁,高处坠落伤致左股骨转子下骨折;外院行左股骨转子下骨折切开复位内固定术,8个月后骨折未见愈合且骨折端硬化,于笔者医院就诊,考虑诊断“左股骨转子下骨不连”;完善相关检查后腰麻—硬膜外联合麻醉下行髓内钉联合自体骨移植术治疗。a.骨折线清晰,骨折端局部密度增高,骨折端硬化;b.术后2d复查,更换髓内钉固定并植骨,骨折端对位对线良好;c.术后12个月复查,骨折线消失,正侧位X线片上4个骨皮质连续,达到骨性愈合

图2 患者男性,43岁,摔伤致左股骨转子下骨折;行左股骨转子下骨折有限切开复位内固定术,13个月后骨折未见愈合且骨折端硬化,来笔者医院就诊,考虑诊断“左股骨转子下骨不连”;完善相关检查后腰麻—硬膜外联合麻醉下行髓内钉附加钢板联合自体骨移植术治疗。a.骨折线清晰,骨折端肥大硬化;b.术后2d复查,更换髓内钉附加钢板固定并植骨,骨折端对位对线良好;c.术后11个月复查,骨折线消失,骨皮质连续,局部密度均匀,达到骨性愈合
讨 论
股骨转子下区域骨折无论是在生物学还是生物力学角度上均不利于愈合,导致骨不连的发生率较高。从解剖上看,股骨转子下区域是股骨颈、大小转子向股骨干移行的部位,在这个移行过程中血供丰富的大量松质骨逐渐向血供较差的较致密的皮质骨转换,它存在“临界血供”,皮质骨的血供较松质骨差,骨质愈合能力差,愈合所需时间长,很容易发生骨不连或内固定失败[5-6]。从生物力学角度看,股骨转子下区域力学环境复杂,该区域受到多组肌肉力量的作用,髂腰肌对该区域有屈曲及外旋的力,臀中肌对其有外展的力,腘绳肌群和内收肌群对其有内收及短缩的作用力[4];其次股骨近端区域存在135°的颈干角,10°~15°的前倾角,使得股骨轴线与负重力的轴线不重合;此外转子下区域是人类骨骼中应力集中最高的区域,据估计1cm2骨骼将承受84kg的重量[7],内侧承受较高的压应力,外侧承受较高的张应力[8]。这样的力学环境使得股骨转子下区域骨折端在负重过程中受到相当大的压力,易导致骨不连[9-10]。
同时有学者提出股骨转子下骨不连的形成原因主要在于初次手术复位不良[11],故初次手术时的良好复位以及内固定物的选择对于骨折愈合起重要作用。目前对于股骨转子下骨折常用固定方式有髓内固定以及髓外固定两大类[12]:髓外固定是偏心性固定,包括股骨近端解剖锁定板、倒置微创内固定系统(less invasive stabilization system,LISS)及动力髋螺钉钢板、动力髁螺钉钢板等,钢板所承受应力力臂较髓内钉长,尤其是当合并内侧骨皮质缺损时,外侧张应力明显升高,骨折断端稳定性受到破坏,骨不连和置入物的疲劳性断裂发生率会明显增加;若对骨折端软组织进行广泛的剥离以复位内侧骨块,又会使骨折端的血供严重受损,影响骨折愈合。笔者认为初次固定最好使用髓内器械,尽管研究指出在骨不连发生率上髓内固定与髓外固定无明显差异,但是总体来说髓内固定相较于髓外固定更安全,种植失败率更低[13]。
股骨转子下骨不连一旦发生,治疗困难,在本研究中大多数患者初次骨折采用切开复位钢板内固定,因此笔者考虑其成因更倾向于血供的破坏以及钢板的应力遮挡效应,而少数肥大型骨不连患者的成因,笔者认为是因骨折断端缺乏稳定性造成。切开复位不可避免地导致了骨折端骨膜剥离过多,血供受损严重。如上文提及,股骨转子下原本就是血供条件相对较差的区域,切开复位导致血供进一步破坏,对骨折愈合无疑是雪上加霜。初次手术使用钢板属于坚强内固定,会对骨折断端产生应力遮挡,在骨折断端失去微动应力刺激的情况下,骨痂生长、塑形将会迟滞,导致骨折延迟愈合以及骨不连[14]。对于骨折断端相对稳定的患者,选择使用髓内器械更换原有的钢板,并进行逐级扩髓和自体髂骨移植术。可以对骨折断端进行新鲜化,并给愈合潜力有限的部位带来具有成骨潜能的细胞以及各类细胞因子,从而促进骨折愈合。同时笔者认为,针对高位股骨转子下骨折选择髓内器械时最好使用长Gamma钉,因其粗大的近端能加大转子下骨折近端的固定强度。Barquet等[15]采用长Gamma钉治疗26例股骨转子下骨不连患者,其在更换内固定器械的同时采用自体骨移植术,其中25例患者最终愈合,平均愈合时间为7个月,并认为股骨转子下骨不连可在取出原有内固定器械后采用长Gamma钉治疗,疗效满意。而对于骨折断端相对缺乏稳定性的患者,笔者使用髓内器械固定并进行植骨,将骨折端偏心固定转换为中心型固定,消除钢板的应力遮挡效应;并且在此基础上附加钢板进一步增强骨折断端的稳定性,为骨折愈合创造相对稳定的生物力学环境。
在本研究中,尽管骨折愈合率两组比较差异无统计学意义,但术后6、9个月的骨痂评分以及骨折愈合时间,钢板强化组均优于单纯髓内钉组。笔者认为原因在于髓内钉是中心型固定,力臂相较更短,能更好地分散应力,具有整体的生物力学优势,附加钢板给予断端局部的力学稳定却不会带来整体的应力遮挡,两者相结合促使骨折愈合更佳。初次手术后对患肢的限制时间相对较长,长时间的骨不愈合更加无法有效地锻炼患肢功能;使用髓内器械重新固定,术后对患肢的制动时间相对较短,可允许患肢早期行不负重的功能锻炼,也可早期下地部分负重,行轴向应力锻炼,刺激骨折断端骨痂生长;更换髓内钉后附加钢板,固定更加确切,相较单纯更换髓内钉,其功能锻炼时间可以更早,锻炼幅度可以更大,从而取得更好的患肢功能。本研究中术后两组髋关节及膝关节功能评分能直观地反映这一观点。也有学者与笔者观点相同,他们认为股骨转子下区骨不连与股骨峡部骨不连具有相似的特点,单纯地更换髓内钉治疗转子下骨不连可能是不够的,可能还需要在更换髓内钉的基础上附加钢板巩固[16]。
本研究也存在一定局限性,股骨转子下骨不连病例相对较少,研究样本量较小。对于股骨转子下骨不连的治疗仍需大样本量的对照比较进行进一步研究。在股骨转子下骨不连治疗方案尚无统一定论的情况下,更换髓内钉是治疗转子下骨不连的可靠方法,而附加钢板可以在不增加手术时间及术中出血量的情况下取得更好疗效,有一定临床意义。
