神经刺激仪超声引导下神经阻滞术用于下肢术后镇痛的效果观察
2021-07-21谢磊国家康复辅具研究中心附属康复医院手术麻醉科北京100176
谢磊 国家康复辅具研究中心附属康复医院手术麻醉科 (北京 100176)
内容提要: 目的:探讨下肢手术术后镇痛中神经刺激仪超声引导下神经阻滞术的应用效果。方法:将2019年2月~2020年1月行下肢手术的30例患者,随机分为两组,对照组采用静脉自控镇痛,观察组采用神经刺激仪超声引导下神经阻滞术。比较两组不同时段疼痛程度、苏醒期躁动严重程度等情况以及血清炎性因子水平变化情况。结果:观察组手术结束时、术后12h、术后24h疼痛程度评分、苏醒期躁动严重程度均低于对照组(P<0.05);观察组术后2h、术后24h的TNF-α、IL-6水平均低于对照组,IL-10水平高于对照组(P<0.05)。结论:神经刺激仪超声引导下神经阻滞术应用在下肢手术术后镇痛中,能够有效抑制术后炎症的发生,镇痛效果较为显著。
超声引导用于外周神经阻滞可提高神经阻滞成功率,减少并发症,被广大麻醉医师认可。有证据表明,超声引导可以作为神经刺激技术的一项安全的辅助方法;超声联合神经刺激仪引导对照单独使用神经刺激引导,操作时间更短,感觉神经完全阻滞的成功率更高,阻滞分布更好。股神经联合坐骨神经阻滞可用于整个下肢的手术[1]。本研究拟对实时超声结合神经刺激仪引导股神经联合坐骨神经阻滞用于下肢手术进行临床评价。
1.资料与方法
1.1 临床资料
选取2019年2月~2020年1月行Ilizarov外固定架手术的下肢肢体畸形患者30例作为研究对象,所选30例患者采用随机数表法随机分为观察组和对照组各15例。观察组中男8例,女7例,年龄14~20岁,平均(16.8±1.1)岁,其中左侧胫骨短缩10例,右侧胫骨短缩5例,最长短缩8cm,最短短缩5cm。对照组中男7例,女8例,年龄13~21岁,平均(16.9±1.0)岁,其中左侧胫骨短缩9例,右侧胫骨短缩5例,最长短缩10cm,最短短缩6cm。两组患者在年龄、性别、病情等方面无统计学差异(>0.05)。
1.2 方法
对照组采用目前常使用的PCIA技术:舒芬太尼2μg/kg+托烷司琼0.2mg/kg(100mL,2mL/h)。术后疼痛剧烈者给于盐酸地佐辛注射液5mg肌注。
观察组使用实时超声扫描引导(GE,LOGIQ 500 PRO系列),并采用神经刺激仪(德国贝朗,型号SB8X12)。HNSI2;ContiplexD连续神经丛阻滞套件,20G,0.85×1000mm)辅助。1.0%利多卡因(上海朝晖药业有限公司)、0.375%罗哌卡因(生产厂家:AstraZeneca Pty Ltd,批准文号:H20100083,商品规格:100mL:0.2g)混合液30mL(含利多卡因300mg、罗哌卡因12.5mg),分别阻滞股神经、坐骨神经(15mL股神经阻滞、15mL坐骨神经阻滞)。股神经阻滞:患者取仰卧位,探头(高频线阵探头)横向置于腹股沟处股动脉上方,辨认股动脉后,在髂筋膜下方、髂腰肌上、股动脉的外侧辨认高回声的股神经;探头外侧平面内进针,调整针尖位置至合适的注射点(针尖位置毗邻神经;神经刺激仪电流强度0.2~0.4mA时仍可引出股四头肌抽动),回抽无血后,缓慢注射局麻药。股骨、膝关节手术,在该处留置导管备用。坐骨神经阻滞:患者取健侧卧位,微屈髋屈膝,探头(低频凸阵探头)横向置于臀后方,坐骨结节与大转子之间,在臀大肌筋膜下显示高回声坐骨神经;探头外侧平面内进针,调整针尖位置至合适的注射点(针尖位置毗邻神经;神经刺激仪电流强度0.2~0.5mA时仍可引出腘绳肌、腓肠肌、足或足趾的抽动),回抽无血后,缓慢注射局麻药。胫骨、踝关节及足部手术,在该处留置导管备用。麻醉操作结束后,在所留置的硬膜外或神经阻滞导管连接镇痛泵(江苏人先医疗科技有限公司,REHN(11)无线镇痛泵,人先无线镇痛智能管理系统V1.0.0),设置模式为患者自控,并开启计时。
1.3 观察指标与判定标准
比较两组患者不同时段疼痛程度、苏醒期躁动严重程度。观察并评价两组患者手术结束时、术后12h、术后24h的疼痛程度及苏醒期躁动严重程度。采用疼痛行为(FLACC)量表及苏醒期躁动评分(PAED)量表对两组患者的疼痛程度、苏醒期躁动严重程度进行评估,疼痛评分越高、苏醒期躁动评分越高表明患者的疼痛程度、苏醒期躁动程度越严重[2]。
比较两组血清炎性因子水平变化情况。采集两组患者手术前、术后2h、术后24h静脉血3mL,测定患者的血清炎性细胞因子水平。离心取血清,对肿瘤坏死因子α(TNF-α)、白细胞介素10(IL-10)、白细胞介素6(IL-6)采用酶联免疫吸附法进行测定[3]。
1.4 统计学分析
2.结果
2.1 比较两组患者不同时段疼痛程度、苏醒期躁动严重程度
术后12h、术后24h的疼痛程度评分、苏醒期躁动严重程度均低于手术结束时(P<0.05);术后24h的疼痛程度评分、苏醒期躁动严重程度均低于术后12h(P<0.05);观察组手术结束时、术后12h、术后24h疼痛程度评分、苏醒期躁动严重程度均低于对照组(P<0.05),具体见表1。
表1. 两组患者不同时段疼痛程度、苏醒期躁动严重程度对比(n=15,±s,分)
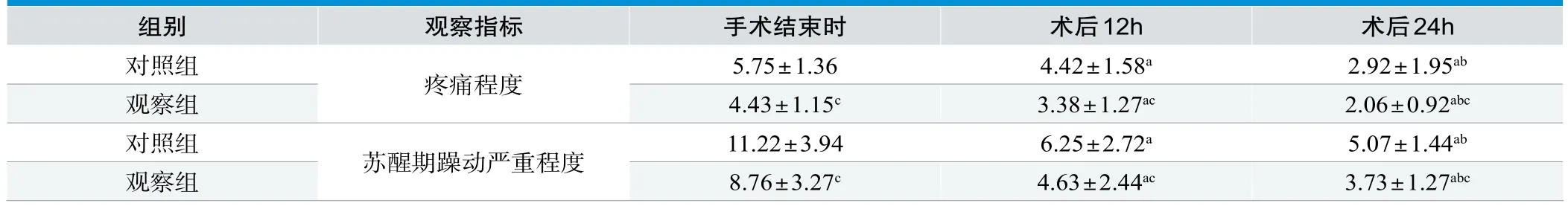
表1. 两组患者不同时段疼痛程度、苏醒期躁动严重程度对比(n=15,±s,分)
注:与手术结束时比较,aP<0.05;与术后12h比较,bP<0.05;与同时段对照组比较,cP<0.05。
组别 观察指标 手术结束时 术后12h 术后24h对照组 疼痛程度 5.75±1.36 4.42±1.58a 2.92±1.95ab观察组 4.43±1.15c 3.38±1.27ac 2.06±0.92abc对照组 苏醒期躁动严重程度 11.22±3.94 6.25±2.72a 5.07±1.44ab观察组 8.76±3.27c 4.63±2.44ac 3.73±1.27abc
2.2 比较两组血清炎性因子水平变化情况
与手术前相比,两组术后2h、术后24h的TNF-α、IL-10、IL-6水平均有明显上升,观察组术后2h、术后24h的TNF-α、IL-6水平均低于对照组,IL-10水平高于对照组(P<0.05),具体见表2。
表2. 两组血清炎性因子水平对比(n=15,±s,ng/L)

表2. 两组血清炎性因子水平对比(n=15,±s,ng/L)
注:与同组手术前对比,aP<0.05;与对照组术后2h对比,bP<0.05;与对照组术后24h对比,cP<0.05。
组别 因子 术前 术后2h 术后24h对照组 TNF-α 146.53±37.55 187.88±35.67a 207.63±47.05a观察组 144.72±35.62 163.64±39.66ab 175.72±38.82ac对照组 IL-10 20.15±5.74 23.42±5.92a 35.68±6.94a观察组 19.26±5.69 33.45±6.08ab 49.54±7.78ac对照组 IL-6 39.97±8.28 54.63±10.57a 77.52±12.42a观察组 39.73±8.05 44.68±9.13ab 59.15±9.63ac
3.讨论
随着超声技术发展,超声引导下隐神经阻滞,准确快捷方便。收肌管阻滞麻醉入路是隐神经阻滞麻醉的首选入路[4]。收肌管入路中感觉阻滞麻醉范围较广,镇痛效果明显。而收肌管阻滞重点是较少累及到患者股四头肌肌力。有研究报道,股神经阻滞会降低约48%的股四头肌肌力,收肌管阻滞麻醉会降低约8%股四头肌肌力[5]。可见收肌管阻滞不会对患者股四头肌肌力造成过多的影响,避免出现明显的运动阻滞[6]。收肌管阻滞麻醉,超声引导下有着清晰的隐神经显像;矫形手术后绷带会缠绕覆盖患者大腿远端的1/3,收肌管入路避免此区域;收肌管麻醉阻滞能确保阻滞隐神经所有分支,避免遗漏部分髌下支,麻醉效果显著[7]。疼痛是一种可被感知的具有保护性的反射,但术后痛如果不能在早期被充分控制,则可能发展为慢性术后疼痛或持续术后疼痛[8]。
在对两组苏醒期疼痛程度、躁动情绪的研究中发现,随着时间推移,两组疼痛程度评分、躁动严重程度逐渐降低,且观察组手术结束时、术后12h、术后24h疼痛程度评分、苏醒期躁动严重程度均低于对照组。患者术后疼痛程度会直接影响苏醒期躁动的发生率,疼痛程度较重,患者极易产生抗拒情绪,引发哭闹、挣扎,提升发生苏醒期躁动情绪的概率[9]。神经刺激仪超声引导下神经阻滞术具有更好的术后镇痛功效,在维持心率、血压相对稳定的情况下,可更好地减轻患者的疼痛程度,有效降低患者苏醒期躁动程度[10]。此外,观察组术后2h、术后24h的TNF-α、IL-6水平均低于对照组,IL-10水平高于对照组,表明神经刺激仪超声引导下神经阻滞术对炎性细胞因子产生了抑制的效果。
综上所述,神经刺激仪超声引导下神经阻滞术应用在下肢手术术后镇痛中,患者疼痛程度明显更低,此种镇痛方案值得应用。
