重金属快速检测技术研究进展
2021-07-14王珏王元凤徐乃丰朱照祥李芊芊伍晓斌
王珏 王元凤 徐乃丰 朱照祥 李芊芊 伍晓斌


摘 要: 由于重金属在工农业生产中的应用越来越广泛,致使环境重金属污染日益严重.为应对减轻环境重金属污染和确保人体健康的需求,新型的重金属快速检测技术成为了研究热点.针对重金属传统检测技术的仪器昂贵、需专业操作人员、不易携带、程序繁琐和耗时较长等缺陷,多种具有快速、灵敏、准确、易携带、现场实时特点的重金属快速检测技术得到了快速发展.本综述首先简析了重金属污染现状以及重金属传统检测技术的种类和特点,详细总结了各种重金属快速检测技术的原理、研究进展、实际应用及其优缺点.结合对重金属离子的长期研究,利用重金属离子敏感菌株筛选螯合剂,对如何改进重金属快速检测方法中存在的灵敏性和专一性的不足等问题提出了新颖的改进方法.
关键词: 重金属; 快速检测; 敏感菌株; 螯合剂
中图分类号: X 502; TS 07 文献标志码: A 文章编号: 1000-5137(2021)02-0186-12
Research progress on rapid detection methods of heavy metals
WANG Jue?, WANG Yuanfeng?, XU Naifeng, ZHU Zhaoxiang, LI Qianqian, WU Xiaobin*
(College of Life Sciences, Shanghai Normal University, Shanghai 200234, China)
Abstract: Heavy metals are applied more and more extensively in industry and agriculture,resulting in increasing environmental pollution of heavy metals.In response to the necessity to reduce environmental heavy metal pollution and ensure human health,new rapid detection techniques for heavy metals have become research hotspot.In view of the limitations of traditional heavy metal detection techniques such as the necessity of expensive equipment,professional operators needed,not portable,complicated procedure and long time-consuming,a variety of fast,sensitive,accurate,portable and on-site rapid heavy metal detection techniques have been developed rapidly.This paper briefly analyzed the current situations of heavy metal pollution and the types and characteristics of traditional heavy metal detection techniques, then the principle,research progress,applications,merits and demerits of various heavy metal rapid detection techniques were summarized as well.Based on our long-term research on heavy metal metabolism,we developed novel methods to improve the sensitivity and specificity of rapid detection techniques for heavy metals using heavy metal sensitive bacterial strains to screen chelators.
Key words: heavy metal; rapid detection; sensitive bacterial strain; chelator
0 引 言
重金屬是指密度大于5 g?cm-3的一类金属元素,在生物体中不可降解.按其生物功能而言,一般分为必需重金属(铜、铁等)和非必需重金属(汞、铅等).在生物体内,即使是必需重金属的含量也必需控制在极低的安全水平.随着社会经济的快速发展,重金属在工农业生产中的应用越来越广泛,而环境中的重金属污染也越来越严重[1],尤其是土壤和水体中的重金属污染,通过吸收富集作用会在食用农产品中过量积累[2],其中镉(Cd)、铜(Cu)、铅(Pb)、砷(As)、铬(Cr)、汞(Hg)的污染情况尤为严重,而这些重金属即使只在痕量水平,也会对人体健康造成严重危害[3].目前,中国50%的水源受到重金属离子的污染,全国重金属污染土地已经超过3亿亩,占总耕种土地面积的1/6以上[4],每年有1 200万吨粮食被重金属污染,经济损失达数百亿元[5].我国是农业大国,粮食、蔬菜、水果等产量皆居世界首位[6].其中,粮食和蔬菜栽培面积最广、经济地位最重要,仅上海市的“菜篮子”工程,每天消费的农产品规模达7万吨左右.快速检测食用农产品和食品中重金属含量的方法对确保国民大众健康非常重要.
最为常用的重金属离子检测方法包括:电感耦合等离子体质谱(ICP-MS)[7]、原子吸收光谱(AAS)[8]、X-射线荧光光谱(XRF)[9]、中子活化分析(NAA)以及电感耦合等离子体发射光谱(ICP-OES)[10]等传统方法,其中以ICP-MS使用最为广泛[4].这些方法的共同优点是:多元素快速分析,线性动态范围宽,检测限低;在大气压下进样,便于与其他进样技术连用;可进行同位素分析、单元素和多元素分析以及有机物中金属元素的形态分析等.然而,这些方法存在仪器昂贵、运行费用高、不易携带、程序繁琐和耗时较长等缺陷[11].因此,发展快速、便捷、低成本、简单可靠,便于现场检测的方法,是当前重金属离子检测领域的研究热点[3,12].本文介绍了生物传感器分析法、电化学、分析法、免疫分析法和纸基检测法等4种重金属快速检测方法.
1 重金属快速检测方法
1.1 生物传感分析法
生物传感分析法是用生物敏感材料作为识别元件,主要利用生物敏感元件中的活性物质与待测物发生反应,产生的化学信号经过转换放大成电信号,通过定量分析,将电信号换算为待测物浓度,最终实现特异性识别待测物的检测手段.其中最重要的元件就是作为识别元件的生物敏感材料.
1.1.1 基于电纺纳米纤维的生物传感器
电纺纳米纤维一般利用高压静电纺丝技术制得,即利用高压电流,使注射器中的聚合物溶液喷射纺丝[13].在强电场下,针头处的液滴从半球形转变成锥形,在尖端形成射流,从顶端喷射出来,固化形成超细纤维,如图1所示.静电纺丝具有良好的生物兼容性,可以实现与生物分子的自定义组合[14].通过静电纺丝技术获得纳米纤维,并进一步利用光学活性发色团,如染料、共轭聚合物、碳基纳米材料和纳米颗粒使其官能化,以产生荧光和比色,继而在传感器中使用具有光学活性的电纺纳米纤维,利用比色法和荧光法对重金属进行单一或者多重检测.
影响静电纺丝技术制备纳米纤维的因素有许多,如表1所示,深入研究这些因素能帮助提高电纺纳米纤维的稳定性.
在最近的基于荧光法的静电纺丝技术重金属检测研究中,MA等[15]将二硫缩醛改性的二酰亚胺(DTPDI)引入到聚丙烯氰(PAN)纳米纤维上,二硫缩醛在汞离子(Hg2+)作用下发生水解,从而使DTPDI与PAN脱离,形成游离的荧光染料,这种染料与Hg2+呈线性相关,能实现在2 h内对水体中的Hg2+进行检测,检出限可达1×10-9 ng·mL-1.LI等[16]开发了一种基于碳量子点包覆介孔二氧化硅/聚丙烯腈(CDs/mesoSiO2/PAN)电纺纳米纤维膜的新型无标记荧光传感器,并用于三价铁离子(Fe3+)的测定.除此以外,也有研究人员通过改变纳米纤维与其薄膜相比的表面积,进而提高静电纺丝纳米纤维的灵敏度[17].而基于比色法的静电纺丝技术重金属检测主要利用具有共轭芳香结构的有机染料与有机分子络合,沉淀重金属离子.但对该检测原理,结合纳米纤维的检测系统的研究目前尚不多见.
利用静电纺丝技术生产的荧光和比色电纺纳米纤维,因其加工简单、容易实现化学官能化、成本低、易检测等优点,非常适用于实際样品中的重金属检测.
1.1.2 微生物传感器
微生物传感器指以活的微生物为敏感材料,利用其代谢产生的光、电、热等变化,实现定量测定样品中重金属含量或评价重金属对水的毒性的方法(图2),其能直接反映各种有毒物质对生物的综合影响.
EOM等[18]在2019年利用间歇补料式的硫氧化细菌(SOB)生物反应器,实现快速检测重金属对水的毒性(图3).SOB在好氧条件下可将单质硫(作为电子供体)氧化生成硫酸盐,从而增加电导(EC)率,再通过比较电导率来检测水中的毒性.他们利用该方法监测了受重金属污染2 h后的出水处的重金属含量变化,并分析了SOB抑制率.结果表明:SOB反应器非常灵敏,适于快速检测水体中硒、汞、六价铬和砷的含量,总体检出时间缩短至2 h以内.
1.1.3 荧光生物传感器
荧光生物传感器是利用光谱和化学波导,将化学信号转化为荧光信号的传感装置(图4).当待测重金属离子的电子,受到特定激发光辐照时,会从基态跃迁到激发态,从不稳定的激发态返回基态的过程中会发射荧光,测得的荧光强度与待测物中的重金属含量呈线性相关.其主要部件包括识别结合基团、发色团和连接基团.识别结合基团选择性地和待测物通过配位键结合,导致化学环境改变,继而发色团将改变的化学环境转化成可检测的荧光或颜色信号输出(图5).连接基团连接起识别结合基团和发色团,选择合适的连接基团对输出信号至关重要.
GUO等[19]利用碳点(CDs)掺杂水凝胶波导实时荧光光谱现场选择性检测水体中的Hg2+,检出限低于4 nmol?L-1,线性范围在0~5 μmol?L-1.所测得的荧光强度会迅速减弱,5 min左右达到稳定状态,即5 min是Hg2+的最佳检测时间.史鸿燕等[20]开发了一种新型甾體不对称双缩二氨基硫脲席夫碱荧光探针,其利用3-氧代-5β-24-胆烷酸甲酯4与单缩二氨基硫脲2为原料,灵敏度较高,30 s内就能达到峰值,检测限可达0.21 μmol?L-1,可高选择性地荧光识别锌离子(Zn2+).BIAN等[21]以金纳米团簇为荧光传感器,建立了一种便携、可回收的Hg2+/Pb2+现场实时检测方法,肉眼检出限分别可达5 μmol?L-1和50 μmol?L-1.PENG等[22]研发了一种使用二氧化硅纳米粒子(也称为二氧化硅纳米粒子增强荧光(SiEF))来提高探针灵敏度和检测限的新方法.SiEF法能显著提高荧光强度和荧光团的检测限,通过紫外灯照射传感器输出信号能够直接观察到低浓度的重金属离子.HAO等[23]开发了一种基于碲化镉(CdTe)量子点和两种染料之间荧光共振能量转移的新型荧光传感器,实现了同时检测水体中的Ag+和Hg2+.
1.1.4 比色生物传感器
比色法是将重金属离子与显色剂混合,两者发生反应,生成有色分子团,产生颜色变化,再借助光度计快速检测有色分子团的方法[24](图6).
LI等[25]用一锅法制备由半胱氨酸修饰的银纳米粒子(AgNPs),借助溶液中的Hg2+实现对组氨酸的检测.在溶液中添加Hg2+有助于半胱氨酸修饰的银纳米粒子和氨基酸结合,从而使银纳米粒子聚集,颜色从原来的黄色变成粉红色.LIN等[26]利用吐温-20修饰金纳米粒子(AuNPs)实现快速检测Hg2+和Ag+,检测时间5 min.吐温-20能使由柠檬酸根修饰的AuNPs在高离子强度下保持稳定.但当待测物中含有Hg2+和Ag+时,柠檬酸盐会还原Hg2+和Ag+,并在AuNPs表面形成Hg-Au合金和Ag,吐温-20从AuNPs表面去除,AuNPs不再稳定,发生聚集,从而引起颜色变化.ZHANG等[27]也利用AuNPs,在乙二胺的条件下用硫代硫酸盐(S2O32-)作为稳定剂,检测了水体中的二价钴(Co2+),检出限为0.04 μmol?L-1(2.36×10-9ng·mL-1),线性范围为0.1~0.7 μmol?L-1.MA等[28]利用多巴胺作为稳定剂修饰银纳米粒子,实现了在10 min内对自来水中的二价铜(Cu2+)的检测,检出范围在3.20×10-9~5.12×10-9ng·mL-1.比色传感器对各种分析物都有着较高的灵敏度和选择性响应,因而被广泛应用[29].
1.2 电化学分析(EA)法
电化学分析法是以极谱法为基础,依据待测物的电化学性质检测其成分及含量的一种分析方法.电化学检测具有分析时间短、功耗低、灵敏度高、易于现场测量等特点,是目前发展最快的检测方法之一[30].但是相较于其他光学技术和光谱法,电化学分析法的灵敏度和检测限较低[31].常用的电化学分析法可分为离子选择性电极法、溶出伏安法以及电化学发光技术等.
在实际应用中,电化学分析法多与传感器配套使用.电化学传感器是基于电化学技术平台,利用待测物的电化学性质,将其化学变化转化成电信号输出,从而实现检测待测物及其组分的生物传感器[32-33](图7).纪人月[34]采用DNAzyme和MoS2-AuPt双金属纳米复合材料,研发了高灵敏电化学传感器,用于检测水中重金属Pb污染物,其检测限可达到3.8×10-15 g?mL-1,但检出时间需要5 h.GAO等[35]基于GR-5 Pb依赖性DNAzyme,以三邻菲罗啉合亚钌(1,10-phenanthroline)为探针,研制了一种电化学发光生物传感器,成功检测了Pb.通过双链DNA将电子转移到电极,产生电位阶跃激发电化学发光,检出限达9×10-12mol?L-1.这两种方法的原理均是在待测物中含有Pb的前提条件下,DNAzyme发生裂解,导致电化学发光强度降低,通过减少量来计算待测物中的铅含量.
1.2.1 离子选择性电极(ISEs)法
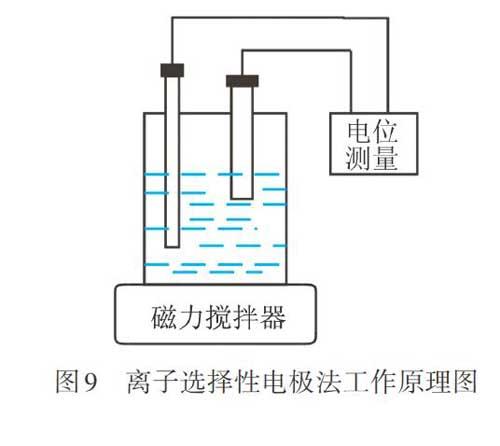
离子选择性电极法利用特定的膜材料与待测液中的离子发生特异性响应,改变原电池的电位差,改变量与待测液中离子活度的对数有关(图8,9).其原理是:将敏感膜电极和内参比电极一起插到被测溶液中,膜与液体接触时,阳离子(或阴离子)会从溶液向固液界面处迁移,而液相中存在相反电性的离子,从而形成电位差,溶液中离子浓度越大,电位差越大,通过测定电动势,能反推得到溶液中待测离子的浓度或活度.HUANG等[36]研发了一种离子选择性电极,利用导电聚硫氨基醌(PSA)纳米粒子作为敏感膜中的固体离子球来检测Pb2+,检测限为0.16 μmol?L-1,并能持续稳定21 d.这种分析方法因其成本低、准确性较高、无损、反应快的优点,而成为一种有趣的研究方向[37].GUPTA等[38]利用一种铁环胺螯合物的涂层离子选择性电极测定了自来水和矿泉水中的铁(Fe3+),检测线性范围在9.1×10-6 ~1.0×10-1mol?L-1.
1.2.2 溶出伏安法
溶出伏安法对待测物施加一定电压,待测物中的重金属离子被还原析出,附着在电极表面,再施加反向电压,让还原后的重金属离子重新氧化溶解,这个过程产生的氧化电流强度和溶液中所含重金属离子浓度呈正比,以此达到定量检测的目的[39](图10).
AGNIESZKA等[40]利用吸附溶出伏安法(AdSV)和催化吸附溶出伏安法(CAdSV)测定Co(II)-丁二酮肟(Co-DMG)络合物中的痕量Co,最低检出限为0.07 μg?L-1,检测时间在5 min以内.JOTHIMUTHU等[41]研发了一种基于阳极溶出伏安法电化学检测锰(Mn)、锌(Zn)等高电负性重金属的传感器.这种传感器由铋工作电极、银/氯化银参比电极和金辅助电极3个电极系统构成.
1.2.3 电化学发光(ECL)技术
电化学发光是指化学溶液中的自由基离子在电极表面产生均相电子移动,继而发生特异性化学发光反应的现象.ECL技术具有灵敏度高、操作便易等优点,适用于对某些溶液中特定金属离子的荧光检测[28].
ZOU等[42]在2004年研制了基于半導体量子点的ECL,并且首次实际应用.CHENG等[43]以2,3-二巯基丁二酸(DMSA)为稳定剂,制备表面未钝化的CdTe量子点(QDs),并固定在电极上,构建了一种新型ECL传感系统,用于检测低电位的金属离子,成功检测了Cu2+,检出限为3.0 nmol?L-1,线性范围在5.0~7.0 nmol?L-1.
1.3 免疫分析法
免疫分析法[44]是以抗原和抗体特异性结合为基础,采用已知抗体检测未知抗原,或者已知抗原检测未知抗体的方法.在重金属检测研究中,因为重金属本身不具有免疫原性,必须先与双功能螯合剂(如1-(4-异硫氰苄基)乙二胺四乙酸(ITCBE)、乙二胺四乙酸(EDTA)、二乙、三胺五乙酸(DTPA)等)螯合形成半抗原,具备反应原性,再与大分子蛋白偶联产生免疫原性.现有的免疫方法主要包括酶联免疫法、胶体金免疫层析法等.
1.3.1 酶联免疫(ELISA)法
酶联免疫法是将抗原抗体特异性反应和酶催化反应相结合,利用酶标仪将酶促反应结果转换成数字信号,从而实现定量检测的方法.目前研究报道已有适用于Pb,Cd,Cr,Hg,Cu等重金属检测的酶联免疫法.常用的酶联免疫法主要是间接竞争酶联免疫检测法(ic-ELISA),其检测过程是将待测溶液滴加到酶标板中,若待测物中含有重金属离子,则其会与事先包被在酶标板上的包被原一同竞争单克隆抗体.与重金属离子特异性结合的单抗会在后续的洗板中洗掉,只剩下与包被原结合的单抗,加入酶标记抗体(辣根过氧化物酶HRP)和包被原-单抗(HRP-Ab)结合显色.固相吸附的HRP-Ab含量和待测溶液的重金属离子含量成反比(图11).该方法的检测总时长一般在2 h左右.
邹淑珍[45]制备了Hg,Pb,Cd 3种有害重金属的单克隆抗体,并建立了ic-ELISA法对抗体性能进行评价.邹军辉[46]研制了一种采用间接竞争ELISA法检测样品中六价铬的试剂盒.利用纳米二氧化钛分离水样中的Cr3+和Cr6+,选择NaHSO3和 Na2S2O5作为六价铬还原剂,除去水样中原有的 Cr3+,最终制备的试剂盒检测限为0.95 ng?mL-1,灵敏度为6.2 ng?mL-1.张燚[47]制备了Hg-ITCBE抗体,鉴定后用于ic-ELISA法检测,半数抑制率(IC50)为2.95 ng?mL-1.郝代玲等[48]制备了Cu2+单克隆抗体,并确立了直接竞争ELISA方法,实现了对Cu2+的快速检测,检测灵敏度为12.89 ng?mL-1,检出限为0.88 ng?mL-1.
1.3.2 胶体金免疫层析(CGICA)法
胶体金免疫层析法是继放射性标记、荧光标记和酶联免疫法之后发展起来的固相标记免疫测定法(图12)[49].胶体金是一种疏水性金溶胶,呈红色或紫红色,用肉眼就可观察到[50],在弱碱条件下带负电荷,与蛋白质上的正电荷形成静电结合,不影响蛋白分子的性质[51].其检测过程为:将待测样品加到样品垫上后,如果待测样品中重金属超标,则其中的重金属离子会与金标垫中的金标抗体特异性结合,再沿着层析方向向前移动,到达T线,若该胶体金免疫层析的T线处是嵌有包被原的,则偶联的重金属离子(抗原)不被T线截留,在T线处不显色,而前往C线处显色;若T线处是嵌有单克隆抗体的,则偶联的重金属离子被T线截留显色,剩余的金标抗体前往C线显色.
朱旭东等[52]研发了一种基于CGICA技术的定量检测镉离子浓度的方法,采用双功能螯合剂iEDTA螯合镉离子,以匙孔血蓝蛋白(KLH)作为大分子蛋白偶联半抗原制备完全抗原,免疫小鼠制得单克隆抗体,最终该方法的检测灵敏度达50 μg?kg-1.王亚楠等[53]采用异硫氰酯法,将双功能螯合剂iEDTA先螯合Cr3+再偶联牛血清白蛋白(BSA)制备Cr-iEDTA-BSA完全抗原,利用细胞融合、体内腹水诱生技术制备Cr3+-iEDTA单克隆细胞株,建立了Cr3+胶体金免疫层析检测方法,检测水体中的Cu2+,检测限为5 ng?mL-1,检测时间为10 min. CGICA法因胶体金能与许多生物大分子非共价结合,且检测时间基本可控制在5 min左右,受到了广泛关注,并被应用于实际免疫检测中[54].
1.4 纸基检测法(PADs)
纸基检测法利用重金属离子和相关小分子的螯合反应产生颜色变化,以纸垫作为反应场所,反应颜色深浅与重金属离子含量成正相关,从而实现快速检测重金属(图13).近10年来,分析试纸条由于易携带、易于现场检测、操作简单、成本低廉和多功能分析等优点,受到越来越多的关注[55].很多研究表明:分析试纸条能够成功检测重金属离子,并应用于食品安全、健康和环境检测中[56].LOPEZ-MARZO等[57]通过纳米金与镉离子結合产生颜色反应的侧向层析(LFA)技术,检测水及饮料中的镉离子水平.RATTANARAT等[58]利用比色法和电化学法建立了一种三维微分析试纸条,能有效检测镍(Ni),Fe,Cu,Cr等重金属离子.最近,MUHAMMAD-AREE等[59]利用小分子与重金属离子结合产生颜色反应的特性制备比色试纸条,并结合智能手机拍照定量和定性分析,能够同时检测Zn,Cr,Cu,Pb,Mn等重金属离子.此方法的最大特点是易于携带和现场实时检测,但为了去除其他重金属离子的干扰,在反应的试纸条中加入了剧毒物质氰化钠,容易造成二次环境污染,且对检测人员造成危害.目前由于与重金属离子反应的小分子存在专一性低、毒性强、结合能力弱等缺陷,分析试纸条在检测敏感性、检测极限以及安全性等方面还需要做进一步改进.
为筛选出专一性高、无毒性或低毒性、结合能力强并能产生颜色反应的重金属离子螯合剂,必须找到一种灵敏直观的筛选方法.本文作者发现一些酵母突变株对某些重金属离子表现出极强的敏感性,即使在重金属含量极低的条件下,这种酵母突变株的生长也会受到抑制[60-62].螯合剂与重金属离子间的高亲和力结合则可以去除重金属离子对酵母突变株的抑制作用.以镉离子螯合剂筛选为例(图14):敲除Cd的分泌蛋白Pca1的酵母突变株失去了对细胞质内的镉离子的排除能力[63],即使少量的镉离子在细胞内的积累都会对突变体造成伤害,从而表现出对pca1Δ细胞的抑制作用(图14).Cd敏感的酵母突变株不能在过量Cd培养基上生长,如果同时加入一种小分子,能消除Cd的抑制作用,那么这种小分子有3种可能的作用:1) 可能抑制了Cd相关转运蛋白的活性,降低了细胞对镉离子的吸收;2) 小分子结合了镉离子,使得镉离子处于非自由状态,主要使处于自由状态的重金属离子对细胞产生毒害作用;3) 这种小分子可能对Cd造成的伤害有修复作用.所以,通过这种方法就有可能筛选出能和重金属离子直接结合的小分子螯合剂.
基于此原理,利用对相应重金属离子敏感的酵母突变株和高丰度小分子库,通过高通量方法筛选高效、低毒、专一的重金属离子螯合剂.并对螯合剂和重金属离子结合反应特性进行鉴定和优化,选取能产生特定颜色反应的螯合剂,制备快速检测试纸条,就能为环境和食品中的重金属检测提供一种快速有效的检测方法.
2 总结与展望
传统的重金属检测方法灵敏、准确、重复性好,仍旧是检测重金属最可靠的主流方法,但检测仪器始终存在体积大、不易携带、价格高、程序繁琐和耗时较长等限制.为确保环境、粮食、食品中重金属可即时检测,快速、便于携带、低成本、简单可靠并且便于现场检测的方法成为了重金属检测领域的重要发展方向.基于目前的技术手段,本文综述的重金属检测方法的检测极限时间都缩短到了10 min以内.这些方法借助相应的便携式传感器及重金属检测分析仪器,可以实现定量检测重金属.其中胶体金免疫层析法不需借助传感器,相对其他检测方法更为便捷,检测时间更短,但其只能用于定性分析样品中的重金属含量是否过量.所以在未来的重金属快速检测方向中,可以结合胶体金免疫层析法和纸基检测法实现定性半定量快速便携的现场重金属检测.其中,筛选出专一性高、无毒性或低毒性、结合能力强并能产生颜色反应的重金属离子螯合剂,是制备重金属离子试纸条的关键所在.
参考文献:
[1] CALLENDER E.Heavy metals in environment:historical trends [J].Treatise on Geochemistry,2003,9:67-105.
[2] GUO Z,SEOL M,GAO C,et al.Functionalized porous Si nanowires for selective and simultaneous electrochemical detection of Cd(II) and Pb(II) ions [J].Electrochimica Acta,2016,211:998-1005.
[3] BANSOD B,KUMAR T,THAKUR R,et al.A review on various electrochemical techniques for heavy metal ions detection with different sensing platforms [J].Biosensors and Bioelectronics,2017,94:443-455.
[4] 刘玮宁,张炜哲.全国3亿亩耕地遭重金属污染威胁 [J].共产党员,2011(12):27.
LIU W N,ZHANG W Z.The threat of heavy metal of 20 trillion square meters of arable land in China [J].Communist,2011(12):27.
[5] 姜妮.重金屬污染危害凸显 [J].环境经济,2011(10):10-14.
JIANG N.The obvious harm of heavy metal pollution [J].Environmental Economy,2011(10):10-14.
[6] 孙海龙.冷藏车结构特点及技术应用 [J].中国战略新兴产业(理论版),2019(7):1.
[7] GONG T,LIU J,LIU X,et al.A sensitive and selective platform based on CdTe QDs in the presence of L-cysteine for detection of silver,mercury and copper ions in water and various drinks [J].Food Chemistry,2016,213:306-312.
[8] TRINDADE N,DANTAS F,LIMA C,et al.Multivariate optimization of ultrasound-assisted extraction for determination of Cu,Fe,Ni and Zn in vegetable oils by high-resolution continuum source atomic absorption spectrometry [J].Food Chemistry,2015,185:145-150.
[9] SITKO R,JANIK P,ZAWISZA B,et al.Green approach for ultratrace determination of divalent metal ions and arsenic species using total-reflection X-ray fluorescence spectrometry and mercapto-modified graphene oxide nanosheets as a novel adsorbent [J].Analytical Chemistry,2015,87:3535-3542.
[10] LOSEV N,BUYKO V,TROFIMCHUK K,et al.Silica sequentially modified with polyhexamethylene guanidine and Arsenazo I for preconcentration and ICP-OES determination of metals in natural waters [J].Microchemical Journal,2015,123:84-89.
[11] FELDMANN J,SALAUN P,LOMBI E.Critical review perspective:elemental speciation analysis methods in environmental chemistry-moving towards methodological integration [J].Environmental Chemistry,2009,6(4):275-289.
[12] CUI L,WU J,JU H.Electrochemical sensing of heavy metal ions with inorganic,organic and bio-materials [J].Biosensors and Bioelectronics,2015,63:276-286.
[13] 帕克,刘呈坤.静电纺丝装置:设计静电纺丝工艺制备纳米纤维 [J].合成纤维,2008(2):46-49.
PARK S,LIU C K.Electrospinning device:design electrospinning process to prepare nanofibers [J].Synthetic Fiber in China,2008(2):46-49.
[14] TERRA A,MERCANTE A,ANDRE S,et al.Fluorescent and colorimetric electrospun nanofibers for heavy-metal sensing [J].Biosensors,2017,7(4):61-74.
[15] MA L,LIU K,YIN M,et al.Fluorescent nanofibrous membrane (FNFM) for the detection of mercuric ion(Ⅱ) with high sensitivity and selectivity [J].Sensors and Actuators B:Chemical,2017,238:120-127.
[16] LI Z,ZHOU H,XU B,et al.Luminescent properties and sensing performance of a carbon quantum dot encapsulated mesoporous silica/polyacrylonitrile electrospun nanofibrous membrane [J].Journal of Materials Science,2016,51(14):6801-6811.
[17] WU C,LAI J.Preparation of thermo-responsive electrospun nanofibers containing rhodamine-based fluorescent sensor for Cu2+detection [J].Journal of Polymer Research,2016,23(11):223-233.
[18] EOM H,WANG H,SEDKY A,et al.Rapid detection of heavy metal-induced toxicity in water using a fed-batch sulfur-oxidizing bacteria(SOB) bioreactor [J].Journal of Microbiological Methods,2019,161:35-42.
[19] GUO J,ZHOU J,YANG X.Fluorescent hydrogel waveguide for on-site detection of heavy metal ions [J].Scientific Reports,2017,7(1):7902-7909.
[20] 史鴻燕,石治川,赵志刚.甾体荧光探针的合成及对废水重金属离子的检测 [J].化学研究与应用,2020,32(7):1182-1187.
SHI H Y,SHI Z C,ZHAO Z G.Synthesis of steroidal fluorescent probe and evaluation of their metal ions recognition [J].Chemical Research and Application,2020,32(7):1182-1187.
[21] BIAN X,WU D,CHAI F,et al.Facile preparation of fluorescent Au nanoclusters-based test papers for recyclable detection of Hg2+and Pb2+[J].Sensors and Actuators B:Chemical,2017,241:592-600.
[22] PENG J,LI Y,XU W,et al.Silica nanoparticle-enhanced fluorescent sensor array for heavy metal ions detection in colloid solution [J].Analytical Chemistry,2018,90(3):1628-1634.
[23] HAO L,XUA G,XING R,et al.Oligonucleotide-based fluorogenic sensor for simultaneous detection of heavy metal ions [J].Biosensors and Bioelectronics,2012,36(1):174-178.
[24] 马彪奇.食品重金属污染来源危害及其检测方法分析 [J].食品安全导刊,2020(24):51.
MA B Q.Analysis of heavy metal pollution sources and its detection method in food [J].China Food Safety Magazine,2020(24):51.
[25] LI H,BIAN H.Selective colorimetric sensing of histidine in aqueous solutions using cysteine modified silver nanoparticles in the presence of Hg2+[J].Nanotechnology,2009,20(14):145502-145508.
[26] LIN Y,Y J,LIN H,et al.Colorimetric sensing of silver(Ⅰ) and mercury(Ⅱ) ions based on an assembly of Tween 20-stabilized gold nanoparticles [J].Analytical Chemistry,2010,82(16):6830-6837.
[27] ZHANG Z Y,ZHANG J,LOU T T,et al.Label-free colorimetric sensing of cobalt(Ⅱ) based on inducing aggregation of thiosulfate stabilized gold nanoparticles in the presence of ethylenediamine [J].The Analyst,2012,137(2):400-405.
[28] MA R,NIU Y,ZHANG L,et al.Colorimetric detection of copper ions in tap water during the synthesis of silver/dopamine nanoparticles [J].Chemical Communications,2011(47):12643-12645.
[29] AJAY S,PRITO J,KIRUBA D S C G,et al.Colorimetric sensors for rapid detection of various analytes [J].Materials Science and Engineering:C,2017:1231-1245.
[30] LIN C,WU J,JU X.Electrochemical sensing of heavy metal ions with inorganic,organic and bio-materials [J].Biosensors and Bioelectronics,2015,63:276-286.
[31] BABAN B,TEJINDER K,RITULA T,et al.A review on various electrochemical techniques for heavy metal ions detection with different sensing platforms [J].Biosensors and Bioelectronics,2017,94:443-455.
[32] WANG Y,PENG L,FU J,et al.Recent advances in the development of electrochemical apt sensors for detection of heavy metals in food [J].Biosensors and Bioelectronics,2020,147:111777.
[33] 杜一平.現代仪器分析方法 [M].上海:华东理工大学出版社,2015:203-205.
DU Y P.Methods of Modern Instrumental Analysis [M].Shanghai:East China University of Science and Technology Press,2015:203-205.
[34] 纪人月.基于DNAzyme和MoS2-AuPt双金属纳米复合材料的高灵敏电化学传感器用于检测水中重金属铅污染物 [D].重庆:重庆医科大学,2020.
JI R Y.Ultrasensitive Electrochemical Sensor Based on DNAzyme and MoS2-AuPt Nanocomposites for Detecting Heavy Metal Lead Pollutants in Water [D].Chongqing:Chongqing Medical University,2020.
[35] GAO A,TANG X,HE W,et al.Electrochemiluminescent lead biosensor based on GR-5 lead-dependent DNAzyme for Ru (phen)32+intercalation and lead recognition [J].The Analyst,2013,138(1):263-268.
[36] HUANG R,DING B,LI G.Combinatorial screening of potentiometric Pb(Ⅱ) sensors from polysulfoaminoanthraquinone solid ionophore [J].ACS Combinatorial Science,2014,16(3):128-138.
[37] ALEKSANDAR R,DERMOT D.Chapter 2 ion-selective electrodes in trace level analysis of heavy metals:potentiometry for the XXI century [J].Comprehensive Analytical Chemistry,2007,49:25-52.
[38] GUPTA K,SETHI B,UPADHYAY N,et al.Iron (Ⅲ) selective electrode based on S-methyl N-(methylcarbamoyloxy) thioacetimidate as a sensing material [J].International Journal of Electrochemical Science,2011,6(3):650-663.
[39] 周秀英,羅欢,韩晓燕,等.水环境重金属检测技术研究进展 [J].广东化工,2020,47(15):151-152.
ZHOU X Y,LUO H,HAN X Y,et al.Progress on detection methods of heavy metals in water environment [J].Guangdong Chemical Industry,2020,47(15):151-152.
[40] AGNIESZKA K,ANDRZEJ B,KURT K,et al.Study on catalytic adsorptive stripping voltammetry of trace cobalt at bismuth film electrodes [J].Electroanalysis,2003,15(23/24):1859-1863.
[41] JOTHIMUTHU P,WILSON R A,HERREN J.Lab-on-a-chip sensor for detection of highly electronegative heavy metals by anodic stripping voltammetry [J].Biomedical Microdevices,2011,13(4):695-703.
[42] ZOU Z,JU X.Electrogenerated chemiluminescence from a CdSe nanocrystal film and its sensing application in aqueous solution [J].Analytical Chemistry,2004,76(23):6871-6876.
[43] CHENG X,LIU X,LEI P,et al.Low-potential electrochemiluminescent sensing based on surface unpassivation of CdTe quantum dots and competition of analyte cation to stabilizer [J].Analytical Chemistry,2010,82(8):3359-3364.
[44] 丁学亮,程建,刘强.玉米中重金属与真菌毒素的检测和分析 [J].食品安全导刊,2020(21):83.
DING X L,CHENG J,LIU Q.Detection and analysis of heavy metals and mycotoxins in Maize [J].China Food Safety Magazine,2020(21):83.
[45] 邹淑珍.汞、铬、铅三种重金属免疫快速检测方法的研究 [D].无锡:江南大学,2017.
ZOU S Z.Development of rapid immunoassay for Hg Cr and Pb [D].Wuxi:Jiangnan University,2017.
[46] 邹军辉.六价铬间接竞争ELISA检测试剂盒的研制及新型一步法竞争ELISA的建立 [D].广州:暨南大学,2012.
ZOU J H.Development of indirect competitive ELISA kit and novel one step competitive ELISA for detection of hexavalent chromium [D].Guangzhou:Jinan University,2012.
[47] 张燚.Hg2+快速免疫检测技术研究 [D].长春:吉林大学,2011.
ZHANG Y.Dvelopment of Immunoassay Technique for Hg2+[D].Changchun:Jilin University,2011.
[48] 郝代玲,黄建芳,杨浩,等.重金屬铜的单抗的制备及免疫学检测方法的建立 [J].食品工业科技,2017,38(19):245-248,255.
HAO D L,HUANG J F,YANG H,et al.Preparation of monoclonal antibody against copper and establishment of immunological detection methods [J].Science and Technology of Food Industry,2017,38(19):245-248,255.
[49] 张书永.免疫胶体金快速诊断技术的临床应用与质量控制 [J].中国医学装备,2013,10(5):37-39.
ZHANG S Y.Application of immune colloidal gold technique in disease diagnosis and its quality control [J].China Medical Equipment,2013,10(5):37-39.
[50] SITHIGORNGUL P,RUKPRATANPOR S,PECHARABURANIN N,et al.A simple and rapid immuno-chromatographic test strip for detection of pathogenic isolates ofVibrio harveyi[J].Microbiol Methods,2007,71(3):256-264.
[51] 李斌.呋喃西林代谢物SEM单克隆抗体的制备及其荧光定量检测试纸条的研究 [D].广州:华南理工大学,2018.
LI B.Preparation of monoclonal antibody for nitrofurazone metabolite SEM and study on quantitative test specimen of fluorescence [D].Guangzhou:South China University of Technology,2018.
[52] 朱旭东,赵小旭.粮食中重金属镉定量快速检测方法的建立 [J].粮食科技与经济,2017,42(3):39-42,61.
ZHU X D,ZHAO X X.Preparation of a rapid method for quantitative determination of cadmium in grain [J].Grain Science and Technology and Economy,2017,42(3):39-42,61.
[53] 王亚楠,王晓斐,丁菡,等.铬离子单克隆抗体的制备及食品总铬含量检测胶体金免疫层析试纸条的研制 [J].食品工业科技,2016,37(18):63-69.
WANG Y N,WANG X F,DING H,et al.Preparation of monoclonal antibody against trivalent chromic ion and development of colloidal gold immunochromatographic assay for detecting total chromium content in food [J].Science and Technology of Food Industry,2016,37(18):63-69.
[54] 龚频,王思远,陈雪峰,等.胶体金免疫层析试纸条技术及其在食品安全检测中的应用研究进展 [J].食品工业科技,2019,40(13):358-364.
GONG P,WANG S Y,CHEN X F,et al.Research progress of colloidal gold immunochromatographic test strip technology and its application in food safety testing [J].Science and Technology of Food Industry,2019,40(13):358-364.
[55] LIN Y,GRITSENKO D,FENG S,et al.Detection of heavy metal by paper-based microfluidics [J].Biosensors and Bioelectronics,2016,83:256-266.
[56] WANG A,MOLINA G,PRIMA V,et al.Anti-LPS test strip for the detection of food contaminated withSalmonellaandE.coli[J].Journal of Microbial and Biochemical Technology,2011,3(2):26-29.
[57] LOPEZ-MARZO A M,PONS J,BLAKE D,et al.All-integrated and highly sensitive paper based device with sample treatment platform for Cd2+immunodetection in drinking/tap waters [J].Analytical Chemistry,2003,85(7):3532-3538.
[58] RATTANARAT P,DUNGCHAI W,CATE D,et al.Multilayer paper-based device for colorimetric and electrochemical quantification of metals [J].Analytical Chemistry,2014,86(7):3555-3562.
[59] MUHAMMAD-AREE S,TEEPOO S.On-site detection of heavy metals in wastewater using a single paper strip integrated with a smartphone [J].Analytical and Bioanalytical Chemistry,2020,412(6):1395-1405.
[60] WU X,SINANI D,KIM H,et al.Copper transport activity of yeast Ctr1 is down-regulated via its C terminus in response to excess copper [J].Journal of Biological Chemistry,2009,284 (7):4112-4122.
[61] WEI W,SMITH N,WU X,et al.YCF1-mediated cadmium resistance in yeast is dependent on copper metabolism and antioxidant enzymes [J].Antioxidants and Redox Signaling,2014,21(10):1475-1489.
[62] CHEN X,ZHANG R,SUN J,et al.A novel assessment system of toxicity and stability of CuO nanoparticles via copper super sensitiveSaccharomyces cerevisiaemutants [J].Toxicology in Vitro,2020,69:104969.
[63] ADLE D J,SINANI D,KIM H,et al.A cadmium-transporting P1B-type ATPase in yeastSaccharomyces cerevisiae[J].Journal of Biological Chemistry,2007,282(2):947-945.
(責任编辑:顾浩然,郁慧)
