基于网络药理学和分子对接探讨芩蒿滴鼻剂 治疗过敏性鼻炎作用机制
2021-07-09何韬毛艳顾政一
何韬,毛艳,顾政一
1.新疆医科大学药学院,新疆 乌鲁木齐 830011;2.新疆维吾尔自治区药物研究所,新疆 乌鲁木齐 830004
过敏性鼻炎(allergic rhinitis,AR)是一种常见的非特异性炎症疾病,临床以阵发性喷嚏、清水样鼻涕、鼻痒和鼻塞为主要症状。AR引起的相关并发症(如支气管哮喘、中耳炎等)可导致食欲减退、乏力、情绪失调、记忆力减退和睡眠障碍等,严重影响患者的生活质量,已成为全球性的健康问题[1]。
芩蒿滴鼻剂是维吾尔医经典验方制剂,由新疆一枝蒿、苍耳子、白芷、麻黄和黄芩5味药组成,具有抗炎、抗过敏等药理作用,功效清热解毒、通鼻窍[2]。方中君药新疆一枝蒿可清热解毒、散瘀消肿、抗过敏、抗菌,常用于治疗过敏性疾病、感冒等[3]。芩蒿滴鼻剂目前缺乏药效学研究,相关研究停留于药效物质基础和工艺优化方面,系统研究芩蒿滴鼻剂治疗AR的靶点和作用机制具有重要意义。网络药理学基于生物信息学理论,结合药动学、基因组学等多学科,通过网络模型可视化分析,阐释药物有效成分和作用机制。本研究以网络药理学方法为基础,结合分子对接技术,深入研究芩蒿滴鼻剂治疗AR的主要活性成分和核心靶点,阐述其可能的作用机制,为后续实验和临床研究奠定基础。
1 资料与方法
1.1 芩蒿滴鼻剂化学成分收集
检索中药系统药理学数据库和分析平台(TCMSP,https://tcmspw.com/tcmsp.php)及万方数据知识服务平台、中国知识资源总库,分别以“新疆一枝蒿”“苍耳子”“白芷”“麻黄”和“黄芩”为关键词,收集芩蒿滴鼻剂的化学成分。
1.2 活性成分及靶点蛋白筛选
根据药物体内ADME过程,借助TCMSP筛选新疆一枝蒿、苍耳子、白芷、麻黄、黄芩化学成分中口服生物利用度(OB)≥30%和类药性(DL)≥0.18的活性成分。将获得的活性成分导入DrugBank数据库(http://www.drugbank.ca/),获得其作用靶点,并利用Uniprot(http://www.uniprot.org/)进行靶点信息核查及整理。采用Cytoscape3.7.2软件构建药物-活性成分-靶点网络。
1.3 疾病相关靶点检索
以“allergic rhinitis”为关键词,利用DrugBank(http://www.drugbank.ca/)、DisGenet(http://www. disgenet.org/)、TTD(http://db.idrblad.org/ttd/)及PharmGKB(http://www.pharmgkb.org/)数据库进行检索,获得AR疾病相关靶点。
1.4 蛋白相互作用网络构建
将筛选到的药物和疾病靶点上传到在线韦恩图(http://bioinfogp.cnb.csic.es/tools/venny/index.html),获得交集靶点,将其输入STRING在线分析工具(http://string-db.org),选取combined_score>0.4的靶点作为核心靶点,导入Cytoscape3.7.2软件,绘制蛋白相互作用(PPI)网络。
1.5 GO和KEGG富集分析
将上述核心靶点输入DAVID6.8数据库(https:// david.ncifcrf.gov/home.jsp),设定条件为P<0.05和FDR<0.05,进行GO功能和KEGG通路富集分析。采用Omishare Tools(http://www. omicshare.com/tools/ index.php/)将分析结果可视化。
1.6 分子对接
应用AutoDock vina软件将PPI网络中度值前5位的靶点分别与度值前5位的活性成分进行分子对接验证。分别从PDB蛋白质结构数据库和ZINC数据库下载受体的晶体结构和配体的化学结构,MAPK1、IL6、TNF、PTGS2和VEGFA对应的PDB ID分别为4FV7、1ALU、5MU8、5IKR和6FMC,采用AutoDock Tools对上述蛋白受体和配体进行预处理,再用其Autogrid模块得到对接活性位点,进行分子对接。结合能<-5.0 kcal/mol的成分与靶点结合性能较好。
2 结果
2.1 药物活性成分
共检索到新疆一枝蒿、苍耳子、白芷、麻黄、黄芩化合物895个,其中查阅文献[3-4]获得新疆一枝蒿化合物58个,通过TCMSP获得化合物分别为苍耳子108个、白芷223个、麻黄363个和黄芩143个。基于OB≥30%、DL≥0.18,并去除缺少靶点预测信息的化合物,共筛选出83个活性成分,其中新疆一枝蒿12个、苍耳子11个、白芷22个、麻黄23个、黄芩31个。芩蒿滴鼻剂主要活性成分信息见表1。

表1 芩蒿滴鼻剂主要活性成分信息
2.2 药物-活性成分-靶点网络
由83个活性成分及其对应的273个靶点构建的药物-活性成分-靶点网络见图1。该网络包括361个节点、1 443条相互作用关系。

图1 芩蒿滴鼻剂药物-活性成分-靶点网络
2.3 疾病相关靶点
通过TTD、DrugBank、DisGenet、PharmGKB数据库分别检索到17、16、446、9个与AR相关靶点,删除重复靶点,得到AR相关靶点473个。
2.4 药物与疾病蛋白相互作用网络
将芩蒿滴鼻剂活性成分靶点与AR相关靶点取交集,获得51个交集靶点。构建交集靶点PPI网络,并进行节点参数拓扑分析,去除3个与其他蛋白无相互作用的蛋白质,结果见图2。其关联的化合物共63个,包括新疆一枝蒿10个、麻黄15个、白芷12个、苍耳子4个、黄芩26个。借助Cytoscape3.7.2软件对药物-活性成分-靶点网络及PPI网络进行Merge,得到其交集网络关系。运用Network Analyzer插件对化合物和靶点按度值从大到小排序,度值居前10位的化合物及靶点见表2、表3。

表2 芩蒿滴鼻剂治疗AR关键化合物(前10位)
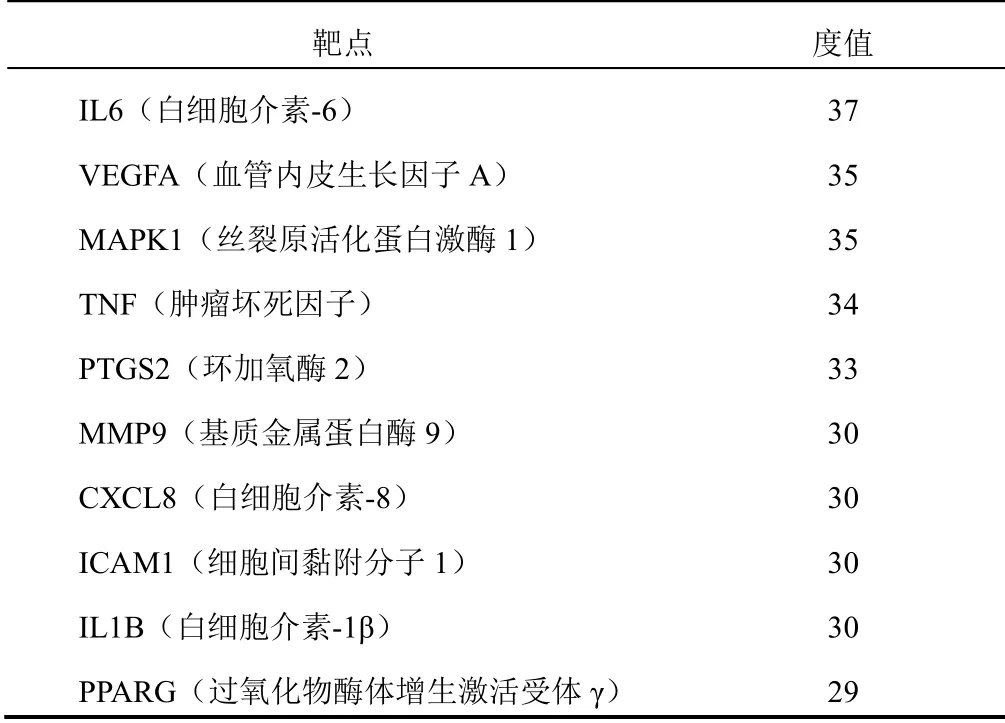
表3 芩蒿滴鼻剂治疗AR核心靶点(前10位)

图2 芩蒿滴鼻剂治疗AR关键靶点PPI网络
2.5 GO和KEGG通路富集分析
核心靶点GO分析包括生物过程(biological process)、分子功能(molecular function)和细胞组分(cellular component)三部分,结果见图3。可以看出,芩蒿滴鼻剂治疗AR的生物过程主要有刺激性应答、新陈代谢过程等,分子功能主要包括结合反应、酶催化活性等,细胞组分主要包含细胞膜、蛋白复合物等。

图3 芩蒿滴鼻剂治疗AR核心靶点GO富集分析
KEGG富集分析共得到128条通路,前20条显著富集(P<0.05)的通路见图4,涉及HIF-1信号通路、IL-17信号通路、TNF信号通路等。

图4 芩蒿滴鼻剂治疗AR核心靶点KEGG通路富集分析
2.6 芩蒿滴鼻剂主要成分与核心靶点分子对接
选取“2.4”项下度值排名前5位的靶点和化合物,分别进行分子对接验证,结果见表4。配体与受体结合的构象稳定时,能量越低其结合可能性越大。结合能<-5.0 kcal/mol表明其结合良好,结合能越小其结合性越好[5]。可以看出,这5种活性成分与靶点蛋白结合性能均较好。其中,木犀草素与MAPK1结合性最好。木犀草素与MAPK1的活性位点ASPA165等形成氢键作用力,与CYSA164形成π-烷基相互作用,见图5。

图5 木犀草素与MAPK1分子对接示意图
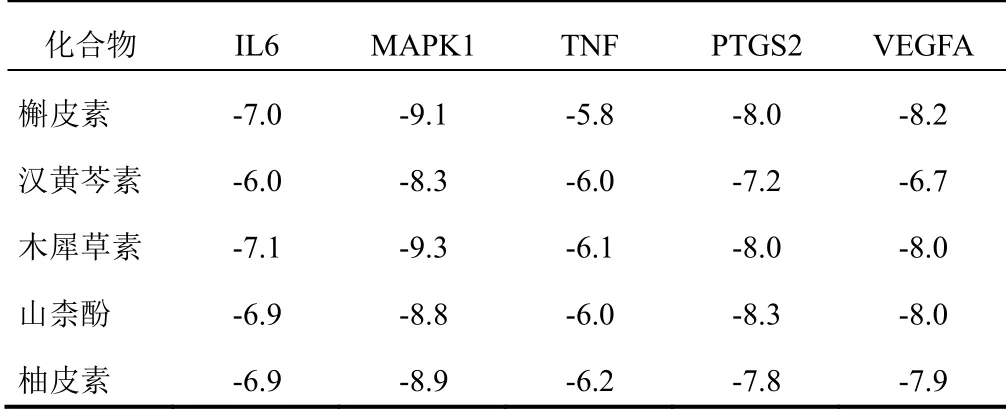
表4 芩蒿滴鼻剂关键化合物与核心靶点结合能(kcal/mol)
3 讨论
基于系统生物学理论的网络药理学,突破了单一成分作用单一靶点的局限,强调对疾病实施多靶点、多途径的调节方式[6],适用于研究由多种可用数据库和软件支持的复杂中药制剂的药效成分和作用机理[7]。本研究借助网络药理学平台,筛选出芩蒿滴鼻剂中83个活性成分,这些化合物可能是芩蒿滴鼻剂发挥药效的重要成分。槲皮素可以缓解AR相关症状,通过抑制巨噬细胞一氧化氮(NO)、肿瘤坏死因子-α(TNF-α)及白细胞介素-6(IL-6)产生,起到抗炎作用[8-9]。汉黄芩素可抑制炎症相关酶或下调促炎基因表达,减少炎症介质的产生,改善炎症相关症状[10]。木犀草素、山柰酚、豆甾醇等被证实具有抗炎活性和免疫调节作用[11-13]。本研究结果与上述文献报道一致,表明基于网络药理学筛选药物活性成分的方法具有一定的可行性。
通过活性成分与疾病靶点的PPI网络和GO富集分析,发现芩蒿滴鼻剂抗AR涉及的生物过程可能与细胞增殖、刺激性应答、趋化因子和免疫反应有关。研究表明,这些生物过程均参与了AR的发生发展[14]。通过活性成分与疾病靶点的PPI网络筛选出10个核心靶点。其中,VEGFA是一种刺激血管内皮细胞增殖的糖蛋白,通过促进血管通透性调控呼吸道炎症反应。血管内皮生长因子不仅能够调节鼻黏膜组织中趋化因子水平,还能阻止嗜酸性粒细胞和肥大细胞浸润,降低炎性细胞因子水平[15]。此外,MAPK1是调节免疫应答的重要因子。MAPK1是一种丝裂原活化蛋白激酶,通过对细胞的增殖、分化进行调控,进而发挥相应的抗炎作用[16]。
从KEGG通路富集分析结果可知,芩蒿滴鼻剂治疗AR主要通过调控HIF-1信号通路、IL-17信号通路、TNF信号通路、NF-κB信号通路和NOD样受体信号通路等,表明芩蒿滴鼻剂治疗AR主要与调节炎症因子、趋化因子介导的信号通路及免疫应答有关。HIF-1是缺氧状态下能特异性发挥活性的转录因子,在肥大细胞浸润引起低氧调节中具有重要作用[17]。IL-17是Th17细胞分泌的一种促炎症细胞因子,具有多种生物学活性。研究发现,IL-17能通过刺激靶细胞释放炎症细胞因子及调控中性粒细胞的细胞因子发挥作用,诱导IL-6、NO和前列腺素E2产生,同时上调γ-干扰素、TNF-α和CD40配体等炎症细胞因子的基因表达,促进局部炎症的发生发展[18]。NOD样受体是天然免疫系统的重要组成部分,能识别病原微生物的一些结构,如胞浆中的细菌肽聚糖片段、细菌脂多糖和病毒双链RNA等,通过驱动NF-κB、MAPK和MyD88依赖性通路的激活、细胞因子的产生,参与微生物感染引发的炎症和免疫应答[19]。本研究结果还显示,显著富集的信号通路中存在着调控其他部位的通路,如AGE-RAGE信号通路、癌症信号通路、肠道炎症信号通路等,表明芩蒿滴鼻剂可能通过多种代谢途径发挥协同治疗AR的作用。
本研究基于网络药理学和分子对接方法对芩蒿滴鼻剂的活性成分、关键靶点及其治疗AR的作用机制进行探讨,分析结果初步验证了芩蒿滴鼻剂的药效基础,主要成分及靶点均显示具有较好的结合性能,可为芩蒿滴鼻剂治疗AR提供一定依据,并为后期实验设计提供思路和方法。
