基于现行黄芪多糖生物活性检测方法的分析
2021-07-08马发顺蔡畅梁秀丽宋玉伟元雪浈
马发顺,蔡畅,梁秀丽,宋玉伟,元雪浈
(1.安阳工学院生物与食品工程学院,安阳 455000;2.河南省兽用生物制品研发与应用国际联合实验室,安阳455000;3.河南省兽药饲料监察所,郑州 450000)
黄芪多糖(APS)是由豆科植物蒙古黄芪或膜荚黄芪的干燥根经提取、浓缩、纯化而成的水溶性杂多糖[1],具有增强机体免疫功能、抗肿瘤、抗衰老、抗应激、护肝、抗病毒和较广泛的抗菌作用[2-3]。关于黄芪多糖生物活性的报道主要有注射黄芪多糖观察细胞超微结构的变化、黄芪多糖对免疫细胞的增殖作用和细胞因子分泌量的变化等[4-7]。而《中国兽药典2015版(二部)》中规定的黄芪多糖生物活性检测方法是以小白鼠为试验动物,通过观察脾指数的变化判断黄芪多糖的生物活性,陈明志等[8]、丘成桢等[9]、黄志远等[10]曾有过此方面报道,但没有对现行黄芪多糖生物活性检测方法的统计分析与评价。本研究基于我国兽药典提供的黄芪多糖生物活性检测方法,对检测结果进行统计分析,从而对现行黄芪多糖生物活性检测方法进行探讨和评价,为黄芪多糖生物活性检测方法的改进提供理论依据。
1 材料与方法
1.1材料
1.1.1 试验动物
昆明鼠(18~20 g,SPF级),购自河南省实验动物中心。使用独立送风隔离笼具饲养,设定温度20℃~26℃,湿度40%~70%,供给足量饲料,自由采食和饮水。
1.1.2 仪器和药品
电子天平(型号为ES3200),天津市德安特传感技术有限公司生产;梅特勒分析天平(型号为AB204-N),上海双旭电子有限公司生产;独立送风隔离笼具(型号为IVC-Ⅱ),上海康为医疗科技发展有限公司生产。黄芪多糖注射液(规格以C6H12O6计10 mL:0.1 g),河南省各兽药生产厂提供;生理盐水(规格为250 mL),购自河南科伦药业有限公司。
1.2 方法
1.2.1 试验设计
3种黄芪多糖样品分别独立试验设计。每种样品均设试验组和对照组各8只小鼠,3次重复试验;整个试验共用小鼠144只。购买的试验动物适应性喂养2 d后进入正试期,试验组每只小鼠腹腔注射黄芪多糖注射液0.5 mL/d,对照组每只小鼠腹腔注射等量的生理盐水;试验期为7 d。
1.2.2 黄芪多糖生物活性质量判定标准
最后1次注射黄芪多糖24 h后将小鼠颈椎脱臼处死称取体重,摘取脾脏称取脾脏重;计算每只小鼠的脾指数,脾指数=脾脏重(mg)/体重(g);再分别计算试验组和对照组的平均脾指数。3次重复中只要有1次试验组与对照组的平均脾指数差值≥2,则可判定样品合格;若平均脾指数差值<2,则判定样品不合格。
1.2.3 数据统计分析
试验组与对照组各项目间的差异显著性分析采用t检验法;3次重复间的差异显著性分析和3种样品间的差异显著性分析采用单因素方差分析法,多重比较使用SSR法。使用Excel 2010数据分析模块进行描述统计,结果以“平均值±标准差”表示;使用DPS v 7.05软件进行方差分析。
2 结果与分析
2.1各项目初步统计结果
3种样品各项目的统计结果见表1。

表1 3种样品3次重复各项目测定结果
从表1可以看出,试验组体重小于对照组,样品A和样品B的3次重复中各有1次差异极显著(P<0.01),而样品C差异不显著(P>0.05)。从脾重和脾指数2项试验组与对照组的比较来看,样品A 3次重复中有2次脾指数差异极显著(P<0.01),脾重有1次差异极显著(P<0.01);样品B有1次脾指数差异显著(P<0.05),脾重差异不显著(P>0.05);样品C脾指数差异不显著(P>0.05),但有1次脾重差异显著(P<0.05)。
从试验组与对照组脾指数的差值大小作判断,3种样品3次重复中各有1次差值大于2,所以可判定3种黄芪多糖样品均合格。
2.2试验组3次重复间的比较
试验组各项目3次重复间方差分析结果表明,样品A在体重间和脾重间差异均不显著(P>0.05),脾指数间差异显著(P<0.05);样品B在体重间和脾指数间差异均不显著(P>0.05),脾重间差异显著(P<0.05);样品C在体重间、脾重间和脾指数间均差异不显著(P>0.05)。差异显著项多重比较结果见表2。

表2 各项目3次重复间的比较
由表2可知,样品A脾指数重复A1与重复A2间差异极显著(P<0.01),重复A2与重复A3间差异显著(P<0.05),重复A1与重复A3间差异不显著(P>0.05);样品B脾重重复B1与重复B2、B3间均差异显著(P<0.05),重复B2与重复B3间差异不显著(P>0.05);其余各项目比较均差异不显著(P>0.05)。
2.3 3种样品间的比较
3种样品试验组各项目方差分析结果显示,体重间和脾指数间均差异极显著(P<0.01),脾重间差异显著(P<0.05);对照组各项目方差分析结果显示,体重间、脾重间和脾指数间均差异极显著(P<0.01);各项目的多重比较情况见表3。
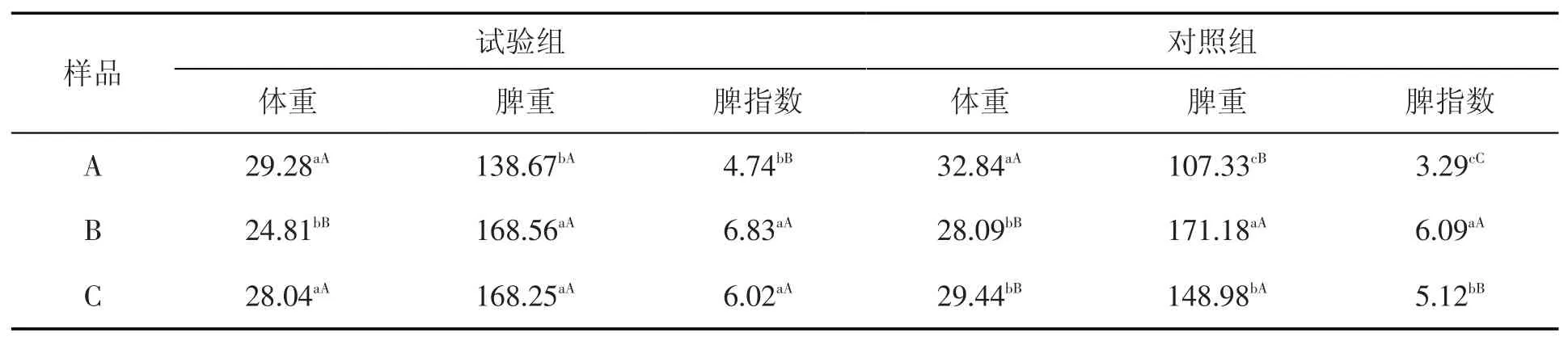
表3 各项目3种样品间的比较
从表3可见,试验组体重样品A、C与样品B间差异极显著(P<0.01),样品A与样品C间差异不显著(P>0.05);脾重样品A与样品B、C间差异显著(P<0.05),样品B与样品C间差异不显著(P>0.05);脾指数样品A与样品B、C间的差异极显著(P<0.01),样品B与样品C间差异不显著(P>0.05)。3个对照组间各项目的多重比较也存在极显著差异(P<0.01)和显著差异(P<0.05)的情况。
3 讨论与结论
3.1从试验组与对照组的比较来看,样品A和样品B脾指数均差异极显著(P<0.01),样品C脾重差异显著(P<0.05),差异显著性检验结果基本支持黄芪多糖生物活性检测结果,说明黄芪多糖具有促进小鼠脾脏生长的作用,这与元雪浈等[11]的
研究结论一致;而试验组体重均小于对照组,此表现也与元雪浈等[11]报道的结果一致。可见,本试验结果可以对现行黄芪多糖生物活性检测方法的可行性提供支持,但不能作为黄芪多糖促进动物生长的证据。试验组小鼠体重小于对照组的可能原因,一是预试期较短小鼠对注射黄芪多糖会有应激反应;二是试验期较短,黄芪多糖的促生长作用还没有充分发挥出来;三是其他因素造成随机误差的影响等。
3.2从3次重复间的比较来看,只有样品A的脾指数间存在极显著差异(P<0.01)、样品B的脾重间存在显著差异(P<0.05),其余各项均差异不显著(P>0.05)。说明试验组小鼠一方面长势均衡,试验控制良好;另一方面由于性别、年龄和初始体重等因素使小鼠对黄芪多糖的反应存在个体差异,这也是误差的重要来源。而本试验进行3次重复正可以降低试验误差,提高黄芪多糖生物活性检测的可靠性。
3.3从3种样品间各项目的比较来看,试验组体重间和脾指数间均存在极显著差异(P<0.01),脾重间存在显著差异(P<0.05),说明尽管3种样品检测结果均为合格,但是3种样品的生物学效价有所不同。这种差异可从小鼠体重、脾重及脾指数上反应出来,在3次重复间比较时,9项中只有2项差异达到显著水平,而在3种样品间比较时,试验组3个项目全部达到显著水平。3种样品间存在较大差异性的原因可能是3种样品来自不同的兽药生产厂家,其生产原料、生产条件和生产工艺等不同所造成。3个对照组各项目的差异性可能与购买小鼠批次不同、试验时间不同有关,除了试验误差之外不排除有系统误差的影响。
3.4现行黄芪多糖生物活性检测是按照《中国兽药典2015版(二部)》载明的方法进行的,但药典上提供的方法只是原则性描述,并没有具体的试验设计及误差控制办法。在实际检测中为了控制试验误差,陈明志等[8]对试验动物的初始体重和性别进行分层处理后再进行随机分组,丘成桢等[9]通过延长预试期和用滤纸吸附脾脏表面血污后称重,黄志远等[18]从小鼠饲养管理方面排除误差干扰,这些都是有益的探索。丘成桢等[9]认为若适应性喂养时间过短小鼠处于应激状态,会影响机体对黄芪多糖的反应,但适应性喂养时间过长可能导致小鼠对黄芪多糖的敏感性下降。关于试验误差控制问题有待进一步研究。
