中空碳纳米球的制备及VOCs吸附性能
2021-06-29王红宁宋夫交黄维秋陈若愚
王红宁,黄 丽,宋夫交,朱 婷,黄维秋,钟 璟,陈若愚
(1.常州大学江苏省精细石油化工重点实验室,常州 213164;2.常州大学江苏省油气储运技术重点实验室,常州 213016;3.盐城工学院江苏省新型环保重点实验室,盐城 224051)
挥发性有机化合物(VOCs)被释放到大气中已经成为日益受到关注的全球问题[1].目前已报道了许多旨在减少大气中VOCs的技术,包括吸附[2]、催化燃烧[3]、光催化转化[4]、生物降解[5]及等离子分解[6]等.其中,吸附技术因具有高效、便捷、低能耗和运行成本廉价的优点而成为首选[7].常用的商业用吸附剂有活性炭(AC)、硅胶(SG)、沸石和金属有机骨架材料(MOFs),但这些材料具有孔隙堵塞再生性差[8]、热稳定性差、易吸附水分子[9]、存储容量不足以及成本高等缺点[10].多孔碳材料具有良好的热稳定性[11]和化学稳定性[12]、良好的导热和导电特性[13,14]、足够的机械强度和弹性[15,16],密度小,且具有非常高的比表面积和大的孔容[17,18],还对水分以及H2S和SO2等腐蚀性气体表现出更好的稳定性[19,20],因此已被广泛用作VOCs的吸附剂[21].研究较多的新型碳材料主要有介孔碳、微孔碳以及碳纳米管等.其中微孔碳材料的吸附性能会因为水蒸气分子与VOCs的竞争吸附堵塞微孔而降低[22];碳纳米管的聚集会限制其商业应用[23]且生产成本比较高[24];而介孔材料具有优于微孔碳材料的良好的VOCs 传质能力,所以成为优先选择的吸附材料.当前,碳材料作为VOCs吸附剂仍存在吸附能力有待提高、合成过程过于复杂等问题.开发一种可以简单制备、且具有优异VOCs 吸附能力的空心碳纳米球(HCNSs)是目前研究面临的挑战.
制备HCNSs 的常用方法通常可分硬模板方法[25,26]和软模板方法[27~29].此前,Dai 等[30]提出了一种“硅助长”自组装策略来制备HCNSs,其中涉及在阳离子表面活性剂存在下聚合间苯二酚-甲醛(RF)树脂和正硅酸四乙酯(TEOS).采用Stöber小球法时使用TEOS对于形成空腔是必不可少的;然而,表面活性剂模板的尺寸决定了壳中的孔径限于4.7 nm.目前,制备具有可调节和大孔径的单分散HCNSs仍然是一个挑战,特别是使用简单的一步法和无表面活性剂的方法来进行制备.
本文在碱性水-醇混合溶液中,通过将间苯二酚甲醛树脂(RF)与快速生成的氧化硅球表面羟基共缩合形成酚醛树脂-氧化硅复合材料并碳化刻蚀来获得HCNSs.该方法简单、不使用表面活性剂,且通过改变硅源摩尔比可合成空腔均一、内径可控、高比表面积和孔容的HCNSs.本文还对HCNSs的静态和动态VOCs吸附性能进行了研究.
1 实验部分
1.1 试剂与仪器
无水乙醇、氨水、正硅酸四乙酯(TEOS)、正硅酸四丙酯(TPOS)、氢氟酸、正己烷和甲苯(国药集团化学试剂有限公司);甲醛(上海凌峰化学试剂有限公司);间苯二酚(Aladdin 化学试剂有限公司).所用试剂均为分析纯.92#汽油(中国石油化工股份有限公司).
JEM-1200EX型透射电子显微镜(TEM,日本电子株式会社);Nicolet-460型傅里叶变换红外光谱仪(FTIR,美国赛默飞世尔公司);Trstar II 3020型全自动比表面积和孔隙分析仪(美国麦克仪器公司);使用GC-950型气相色谱仪[SE-54毛细管(30 m×0.25 mm×0.33 μm)、氢火焰检测器和N2000色谱离线工作站,柱温100 ℃,气化温度150 ℃,检测温度150 ℃;氮气、氢气和空气的流速分别为30、30 和180 mL/min]检测吸附柱流出气体的浓度.
1.2 实验方法
1.2.1 HCNSs 的制备(1)二氧化硅球的合成与涂覆:在室温、搅拌条件下将硅源加入到含有乙醇(70 mL)、H2O(10 mL)和NH3·H2O(3 mL,质量分数25%)的溶液中,搅拌20 min后,向溶液中加入间苯二酚(0.400 g)和甲醛(0.560 mL,质量分数37%),搅拌24 h.以6000 r/min的速率离心分离沉淀物,用水和乙醇洗涤,并在50 ℃下干燥约12 h,得到RF@SiO2复合材料.以不同摩尔比的TEOS/TPOS(总硅量固定为12 mmol)作为硅源制备系列RF@SiO2复合材料,其它条件保持不变.
(2)碳化:将干燥的RF@SiO2复合材料在氮气气氛下的管式炉中从室温以2 ℃/min 的升温速率升温至700 ℃,煅烧5 h后冷却至室温.得到的样品命名为SiO2&C.
(3)二氧化硅刻蚀:将碳化产物分散在质量分数10%的氢氟酸溶液中,搅拌24 h进行刻蚀,以除去二氧化硅.通过离心回收产物,用水和乙醇洗涤至中性,并在50 ℃下真空干燥12 h,即得到HCNS,命名为HCNS-x(x为TEOS/TPOS摩尔比).
1.2.2 二氧化硅球的制备 在室温、搅拌条件下将硅源加入到含有乙醇(70 mL)、H2O(10 mL)和NH3·H2O(3 mL,质量分数25%)的溶液中,并搅拌24 h.以6000 r/min 的速率离心分离沉淀物,用水和乙醇洗涤,并在50 ℃下干燥约12 h.得到的样品命名为SiO2.
1.2.3 氧化除碳后的氧化硅球的制备 将HCNSs 制备过程中的碳化产物SiO2&C 置于马弗炉中,在700 ℃空气中氧化5 h.得到的样品命名为SiO2&C-C.
1.2.4 静/动态吸附实验 静态吸附实验中,将粉末样品装载在无盖的称量瓶(50 mm×30 mm)中.在0.90 mbar(90 Pa)的高真空下,将样品加热到100 ℃预处理2 h,以除去水分和吸附的小分子化合物等杂质.将装有适量吸附质(蒸馏水、正己烷、甲苯、92#汽油)的干燥器置于恒温水浴槽中,向称量瓶中加入一定质量的吸附剂,并将称量瓶在25 ℃下与VOCs或水蒸气充分接触24 h.吸附达到饱和后,测量吸附后的质量.通过在真空环境中将样品加热到100 ℃并保持75 min(样品的质量不再改变)来执行解吸程序.分别通过公式(1)和(2)计算吸附剂的静态吸附容量和解吸效率.所有静态吸附实验均进行5次(包括5个吸附-解吸循环),以确保数据的可重复性.

式中:X(g/g)和Y(%)分别为样品的吸附容量和解吸效率;m1(g)和m2(g)分别为吸附前后的样品质量;m3(g)和m4(g)分别为脱附前后样品的质量.
动态吸附实验中,将约0.480 g的样品装入固定床反应器中.在进行吸附测试之前,将样品在真空条件下于100 ℃预处理约12 h,以除去物理吸附的水分子和少量有机杂质.以空气作为载气,并进行调节,以保持总流量为0.130 L/min(正己烷和甲苯浓度分别为0.290和0.381 g/L).通过使用配备有火焰离子检测器的GC测量吸附前后的浓度变化来确定吸附容量.吸附剂的平衡动态吸附容量(qe,g/g)由穿透曲线根据公式(3)计算得出:

式中:cA(g/L)和c0(g/L)分别是通过固定床塔的吸附质气体的出口和入口浓度;FA(L/min)为正己烷和空气的混合气体流量;t(min)为吸附时间;m(g)为吸附床中吸附剂的质量.
为了研究水蒸气对HCNS-0/4的正己烷、甲苯的动态吸附性能的影响,使用水饱和载气(在相对湿度为95%时)进行了对照实验.同时,在相同条件下完成了动态吸附循环性能测试.根据式(3)由穿透曲线计算出正己烷、甲苯的平衡动态吸附容量qe,n-hexane和qe,toluene.利用式(1)根据样品在动态吸附前后的质量变化计算总平衡动态吸附容量(qe).样品解吸效率的计算与静态吸附过程一致.水蒸气平衡动态吸附容量(qwater)通过qe-qe,n-hexane和qe-qe,toluene计算.还进行了双组分的动态吸附(竞争性吸附,相同体积的正己烷和甲苯)测试,根据式(3)以及各自的标准曲线计算出相应的吸附容量.
2 结果与讨论
2.1 HCNSs样品的表征
图1为加入不同TEOS/TPOS摩尔比的硅源制备的HCNSs样品的TEM照片.当只以TEOS为硅源时(HCNS-4/0)[图1(A)],空心碳球的粒径和壳厚度分别约为280和15 nm,颗粒具有高度均匀性和良好的分散性,碳球边缘清晰,壳壁致密.随着硅源中TPOS比例的增大,所制备的HCNSs样品粒径分别增加至290,310,354 和426 nm,同时壁厚分别增加至24,32,44 和63 nm,碳球壳壁逐渐变得疏松[图1(B)~(D)].所制备的HCNSs 样品的粒径和壳厚度随着TPOS 比例的增大而增加,表明选择TPOS作为单一硅源是获得具有较大孔径的HCNS 的关键,这归因于丙氧基比乙氧基具有更大的空间效应,导致TPOS的聚合速率比TEOS慢[30,31],所以SiO2球的形成过程更加可控[32].在反应体系中,TPOS水解和缩合的速度比TEOS慢,SiO2粒子不断被缓慢释放出来,并均匀成核自组装形成SiO2核心粒子,该核心粒子接下来被用作空腔的模板.当RF开始聚合并在SiO2核心粒子表面成核时,仍然有大量的SiO2粒子可以与SiO2核心粒子共存.SiO2粒子及其聚集体通过弱氢键与RF低聚物相互作用,共同凝聚到SiO2核心粒子上,形成了SiO2@SiO2/RF核壳结构.在有限的聚合时间内,更低的TEOS/TPOS摩尔比可以减小水解缩合生成的二氧化硅Stöber 球的密度,为间苯二酚与甲醛的共缩合反应提供更大的球形模版,而用于形成SiO2/RF的SiO2粒子的增加导致了更大的SiO2聚集体,因此也增大了壁厚和粒径[31].

Fig.1 TEM images of HCNS-4/0(A),HCNS-3/1(B),HCNS-2/2(C),HCNS-1/3(D)and HCNS-0/4(E)
HCNSs样品的FTIR谱图如图2所示.图中3420 cm-1处的宽吸收峰是O—H键的伸缩振动引起的,随着TEOS/TPOS 混合物中TPOS 比例的增加,羟基峰的强度升高,这说明引入更多的TPOS 会增加硅烷醇基的强度和O—H 键的弯曲振动,从而吸附的水分子的量也增加了,其中HCNS-0/4的O—H峰强度最强.2916,2851 和1384 cm-1处的特征峰为甲基的C—H 伸缩振动特征峰,1621 cm-1处是苯环的振动峰.而1204和1167 cm-1处为C—H的面内变形振动吸收峰.图S1(见本文支持信息)中在1100 cm-1出现了很强的吸收峰,它是由Si—O—Si 键反对称伸缩振动所致,在800 cm-1附近的吸收峰是Si—O—Si键的对称伸缩振动吸收峰,表明SiO2的存在.而在HCNSs的红外谱图中没有发现Si—O—Si键的吸收峰,表明SiO2已被完全除去.综上所述,以间苯二酚和甲醛为原料在经过碳化和刻蚀除去SiO2后得到了空心碳球.
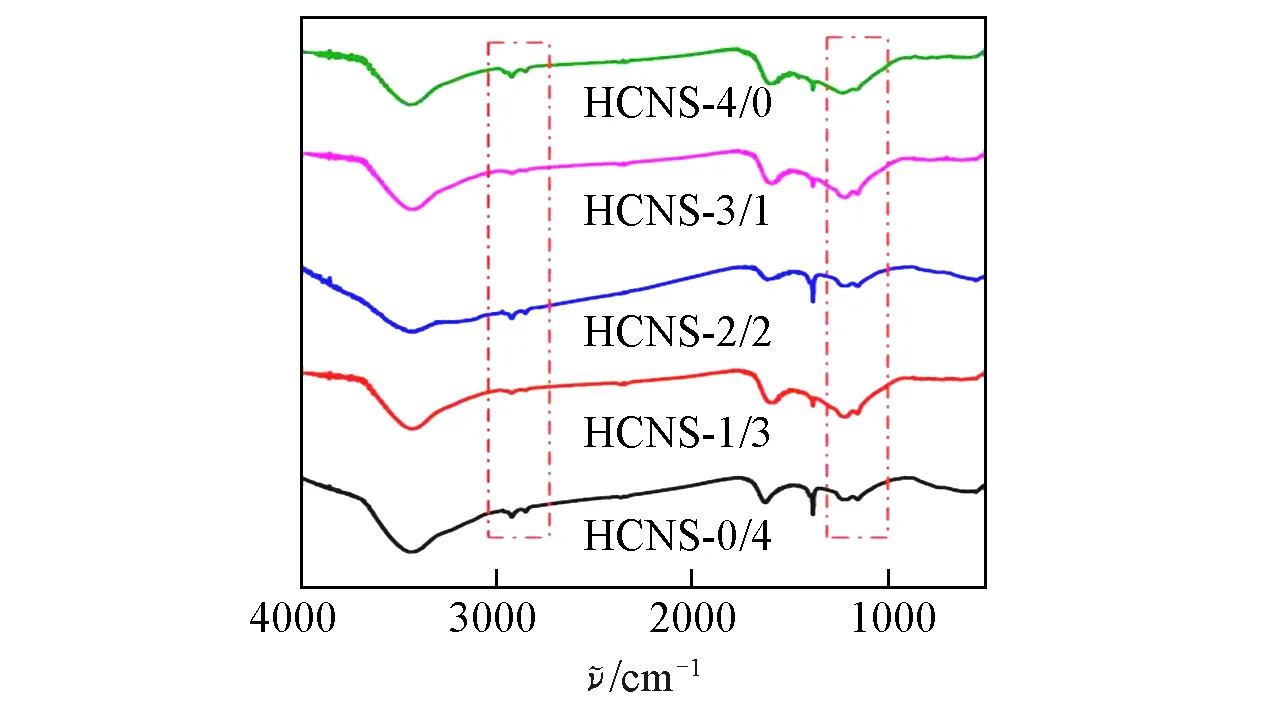
Fig.2 FTIR spectra of HCNSs
图3(A)和(B)分别为HCNSs和AC的氮气吸附-脱附曲线和孔径分布曲线(根据BJH模型通过氮气吸附等温线的吸附分支计算得到).各样品的比表面积(SBET)、孔容(V0)和平均孔径列于表1 中.所有HCNSs样品均呈现出Ⅳ型等温线并伴有H4型滞后环,表明HCNSs是典型的介孔材料.其由于具有较大的孔径和较小的吸附阻力,可以加速VOCs 吸附的动力学过程[33];其较大的比表面积和孔容可为吸附质分子提供有效的吸附位点[23],从而增加吸附量.而AC为I型等温线,是典型的微孔材料,虽然其比表面积较高,但由于富含的大量微孔结构在吸附过程中会阻碍VOCs分子特别是尺寸比较大的VOCs分子向孔中传输,且由于AC的亲水性,水蒸气会和VOCs分子竞争吸附从而堵塞微孔,因此会大大降低吸附性能[34].由图3(B)可以看出,所有样品均只有1个较尖锐的峰,说明所制备的HCNS-x的孔径分布都比较均一,其中HCNS-0/4孔径最大,为5.4 nm.

Fig.3 N2 adsorption-desorption isotherms(A) and pore size distribution curves(from adsorption branches)(B)of HCNS-x and AC
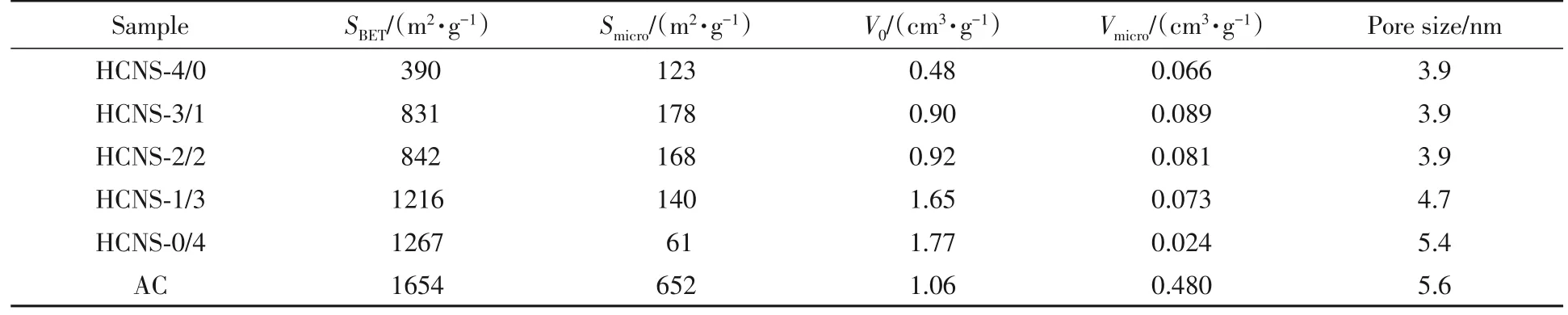
Table 1 Pore structure parameters of HCNS-x and AC
由表1可以看出,HCNS-4/0具有最小的SBET(390 m2/g)和V0(0.48 cm3/g).随着TEOS/TPOS混合物中TPOS比例的增加,所制得的HCNSs的SBET和V0逐渐增大,平均孔径也逐渐增大.这是因为在碱性条件下,除了可由TEOS 和TPOS 水解生成小尺寸SiO2胶体外,还可以促进现有SiO2颗粒的二次成核,使得生成的SiO2颗粒具有较大的尺寸,形成孔径较大的材料[35].且TPOS比TEOS的反应性低[36],水解和缩合速度比TEOS慢,会不断缓慢释放SiO2粒子,在SiO2-RF低聚物自组装过程中,更多的TPOS则会导致更多的SiO2粒子附着在一起形成更大的聚集体,从而增大了孔径、SBET和V0,所以越高的TPOS 比例可以获得越大孔径和越高SBET及V0的吸附材料.HCNS-0/4的SBET为1267 m2/g,是HCNS-4/0的3.25倍,V0为1.77 cm3/g,是HCNS-4/0 的3.73 倍.综上所述,通过改变TEOS/TPOS 的比例可以有效地调控合成HCNSs的尺寸、SBET,V0和平均孔径.
图S2(A)(见本文支持信息)显示了SiO2和SiO2&C,SiO2&C-C样品的氮吸附-脱附曲线.SiO2&C-C的等温线为具有H4 型滞后环的IV 型等温线,表明其为典型的介孔材料.图S2(B)为SiO2,SiO2&C,SiO2&C-C的孔径分布曲线.可以看到,SiO2&C-C只有1个较尖锐的峰,表明SiO2&C-C在4.7 nm处具有相对较窄的孔径分布.表S1(见本文支持信息)列出了SiO2,SiO2&C,SiO2&C-C的SBET,V0和平均孔径.SiO2&C-C的SBET为169 m2/g,远大于SiO2及SiO2&C,但又远小于HCNS-0/4.
2.2 HCNSs样品的静态吸附-脱附性能
HCNSs 样品与商品化AC 的正己烷、甲苯和油气的静态吸附容量与解吸效率如图4 所示.由图4(A)可见,在静态吸附实验中,HCNS-4/0的正己烷静态吸附容量在HCNS系列样品中最低,为1.06 g/g.随着硅源中TPOS 比例的增加,所制备的HCNS 样品对正己烷的吸附量逐渐增加,并在TEOS 与TPOS摩尔比为0/4时(HCNS-0/4)达到最大(2.02 g/g),是HCNS-4/0的1.91倍.甲苯作为溶剂和提高汽油辛烷值的芳香族添加剂也会经常出现在日常环境中.图4(B)为HCNSs 样品的甲苯静态吸附容量图.与正己烷的吸附相似,HCNSs样品的甲苯吸附容量也随着TPOS比例的升高而增大.其中HCNS-4/0 具有最低的甲苯吸附容量(0.435 g/g),而HCNS-0/4 的甲苯静态吸附容量最高,可达1.42 g/g,是HCNS-4/0的3.26倍.

Fig.4 Static n-hexane,toluene and oil vapor adsorption capacities(A—C) and desorption efficiencies(D—F)of HCNS-x and commercial AC after fire adsorption-desorption cycles
图4(C)为HCNSs 样品的油气静态吸附容量图,与正己烷和甲苯的静态吸附容量变化趋势一致,HCNSs样品的油气吸附容量随着TPOS比例的升高而增大.在所有HCNSs系列样品中,HCNS-4/0具有最低的油气吸附容量(0.236 g/g),HCNS-0/4的油气静态吸附容量最高,达到了0.927 g/g,是HCNS-4/0的3.93倍.此外,在多次的脱附解吸实验中[图4(D—F)],经过5次吸附-脱附循环,HCNSs系列样品对正己烷、甲苯、油气的解吸效率保持稳定,且均保持在98.0%以上,表明HCNSs系列样品具有优异的脱附再利用能力.而商品化AC 第一次的正己烷、甲苯和汽油的吸附容量分别为0.666,0.653 和0.658 g/g,是HCNS-0/4的正己烷、甲苯和汽油吸附容量的0.330,0.460和0.710倍.且商品化AC第二次的正己烷、甲苯和汽油吸附容量均有下降,分别为0.455,0.391和0.422 g/g,分别比第一次下降了31.7%,40.1%,35.9%.直到第三次吸附时正己烷、甲苯和汽油的吸附容量才趋于稳定,分别为0.455,0.390 和0.421 g/g.HCNS-0/4 的正己烷、甲苯和汽油吸附容量分别是AC 稳定后吸附容量的4.44,3.64,2.20倍.商品化AC的解吸效率仅能达到93.0%左右,且第一次解吸效率为72.6%,说明正己烷/甲苯/油气分子不能完全脱附出来,这影响了其在VOCs吸附领域的应用.
在实际应用中,水蒸气的存在会影响VOCs的吸附性能,因此考察了HCNSs样品的静态吸附水能力.HCNSs 样品对水蒸气的静态吸附容量及解吸效率如图5 所示.从图5(A)中可以看出,与吸附VOCs气体分子一样,随着硅源中TPOS比列的增加,HCNSs对水蒸气的静态吸附容量也逐渐提高.其中HCNS-4/0的水静态吸附容量最小,为0.278 g/g,HCNS-0/4有最大的水静态吸附容量(0.885 g/g).从图5(B)中可以看出,经过5次吸附-脱附循环,HCNSs系列样品对水的解吸效率保持稳定,且均保持在98.0%以上.商品化AC第一次水静态吸附容量为0.673 g/g,第二次水吸附容量为0.450 g/g,比第一次减少了33.1%,到第三次吸附时其水吸附容量为0.437 g/g,水吸附容量才逐渐趋于稳定.同样从图5(B)可看出,商品化AC的水解吸效率不高,约为75.6%,表明水分子难以脱附出来,这会影响吸附剂的吸附稳定性和重复利用性能.

Fig.5 Water static adsorption capacity(A) and desorption efficiency(B) of HCNS-x and commercial AC after five adsorption-desorption cycles
图S3(见本文支持信息)为SiO2,SiO2&C和SiO2&C-C样品的静态吸附-脱附实验结果.可以发现在预处理之后,SiO2和SiO2&C的静态VOCs吸附性能较低,而SiO2&C-C的静态正己烷、甲苯、汽油和水的吸附容量相对较高,分别为0.118,0.128,0.138和0.242 g/g.静态解吸结果表明它们具有良好的脱附效率.然而从静态吸附实验结果可以发现,上述样品的VOCs 吸附性能均较低.可能是由于它们的非空心结构产生的高密度和低比表面积导致了其低的吸附量.
HCNSs样品的正己烷和甲苯的静态吸附容量与孔结构参数之间的关系如图6所示.图6(A)和(B)示出了HCNSs 样品的正己烷静态吸附容量与孔结构参数之间的联系.当SBET和V0较低时,吸附量较低,仅为1.06 g/g;随着SBET和V0逐渐增加,吸附量曲线上升;当SBET和V0达到1200 cm2/g和0.508 cm3/g时,吸附量达到最大值(2.01 g/g).可以发现,正己烷的静态吸附容量随着比表面积SBET[图6(A),三角形&黑线]和总孔容V0[图6(B),三角形&黑线]的增加而逐渐增大.同样,HCNSs系列样品中HCNS-4/0样品的Smicro和Vmicro最低,其正己烷吸附量也最低.但正己烷的静态吸附容量与微孔比表面积Smicro[图6(A),正方形&蓝线]和微孔孔容Vmicro[图6(B),正方形&蓝线]的变化之间没有显著的关系.对比HCNS-4/0与HCNS-0/4的吸附结果可以发现,2个样品具有相近的Smicro和Vmicro,但是HCNS-0/4的正己烷吸附量是HCNS-4/0的1.90倍,这是因为HCNS-0/4的SBET和V0分别是HCNS-4/0的3.25倍和2.94倍,说明HCNSs的正己烷吸附能力与其SBET和V0大小有关.
图6(C)和(D)为HCNSs样品的甲苯静态吸附容量与孔结构参数之间的联系.同样可以发现,随着SBET和V0的提高,HCNSs的甲苯吸附量增加,由HCNS-4/0的0.435 g/g增加到1.42 g/g;而HCNSs的甲苯吸附量与Smicro和Vmicro之间未表现出明显相关性.因此可以判断,HCNSs的甲苯吸附能力与材料的SBET和V0有关.综上所述,高SBET值和高V0值的HCNSs样品具有高吸附性能,而高Smicro值和高Vmicro值的HCNSs样品则不一定有高吸附性能.
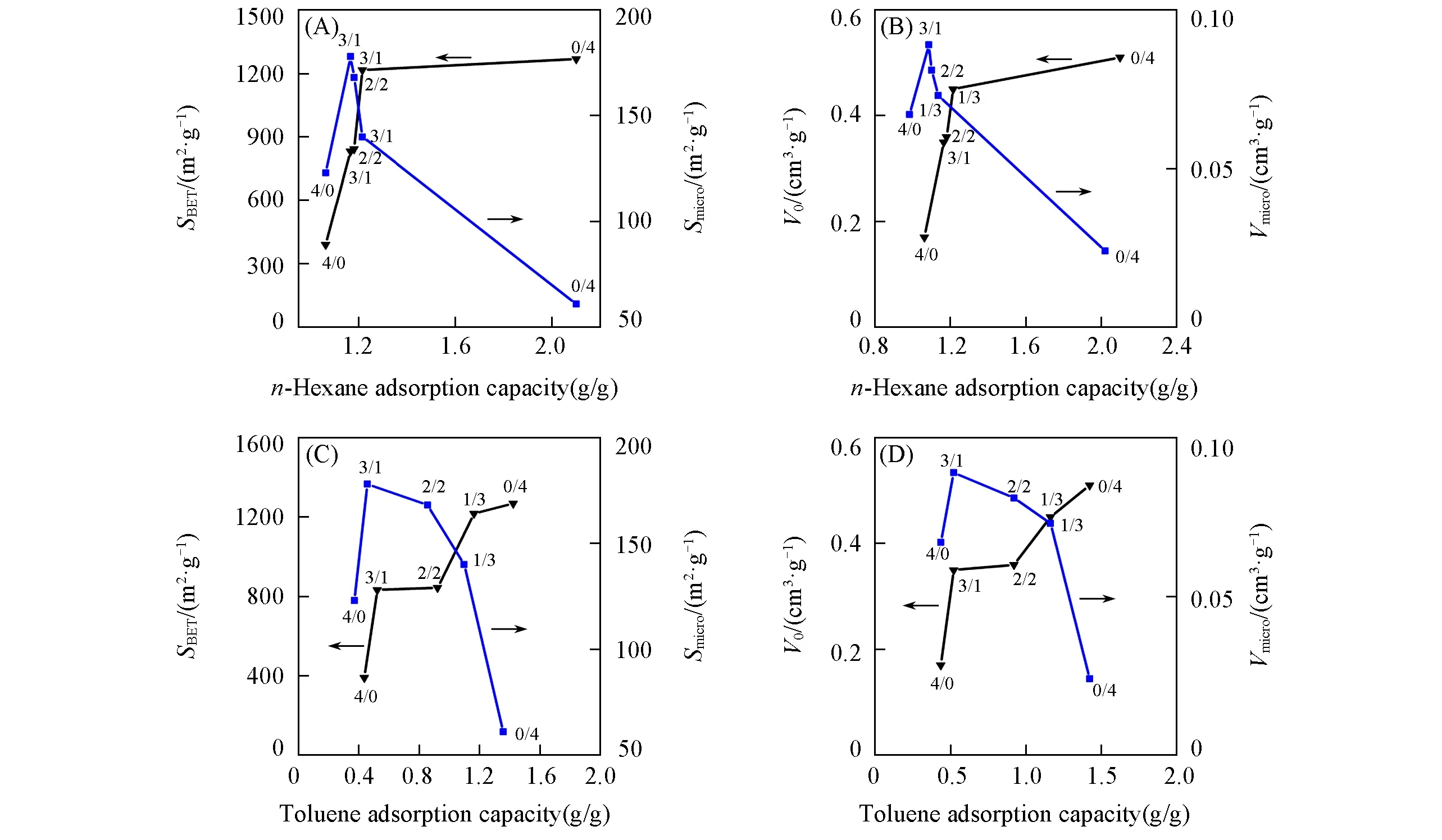
Fig.6 Relationship between static n-hexane and toluene adsorption capacities of HCNSs and pore structure parameters SBET&Smicro(A,C)and V0&Vmicro(B,D)
2.3 HCNS-0/4对单组分VOCs的动态吸附-脱附性能
HCNS-0/4 样品具有较高的VOCs 吸附容量和稳定性,故考察其动态吸附,并以商品化AC 作为参考.动态正己烷吸附穿透曲线、动态吸附容量和解吸效率如图7 所示.HCNS-0/4 与商品化AC 的动态正己烷吸附实验数据总结如表2所示.其中图7(A)为第一次动态吸附穿透曲线,图7(B)为第五次动态吸附穿透曲线.将正己烷-空气混合气体通过动态吸附装置,用流量计控制气体流速保持稳定.当浓度达到入口处的10%时,即为穿透.图7(A)和(B)的吸附曲线符合吸附带随着时间平移的动态过程.如图7(A)和表2 所示,商品化AC 第一次动态正己烷吸附对应的穿透时间与平衡时间分别为36 和74 min,HCNS-0/4 样品对应的正己烷穿透时间与平衡时间分别为44 和82 min.第五次动态吸附实验中,商品化AC对应的正己烷穿透时间与平衡时间分别为28和58 min,HCNS-0/4对应的正己烷穿透时间与平衡时间分别为42和80 min.可以发现吸附剂的第一次正己烷吸附穿透时间和平衡时间均大于第五次,表明在多次吸附-解吸实验之后,吸附剂的吸附性能出现了下降.需要指出的是,不同吸附剂的动态吸附容量与其穿透时间呈现正相关的关系,即吸附穿透时间越长,其动态平衡吸附容量越大[37].而HCNS-0/4样品的正己烷吸附穿透时间和平衡时间均大于商品化AC,表明HCNS-0/4具有更好的正己烷动态吸附能力,因此HCNS-0/4的动态正己烷吸附平衡容量大于商品化AC.图7(C)和(D)为5次动态正己烷吸附容量以及解吸效率图.可以看出空心多孔碳球HCNS-0/4具有相对稳定的吸附容量,保持在2.01 g/g 左右,第三次动态吸附容量为1.95 g/g,比第一次下降了3.08%,然后逐渐趋于稳定,其解吸率也基本保持在98.0%左右.而商品化AC样品由于在吸附过程中发生劣化,导致其第二次动态吸附容量(0.480 g/g)相比第一次下降了20.0%,而且第一次解吸率仅为73.7%,出现了解吸不彻底的问题,使得其重复利用性受到了限制.

Fig.7 Breakthrough curves for n-hexane of HCNS-0/4 and AC(A,B)and the comparison of the equilibrium adsorption capacities(C)and desorption efficiencies of five times(D)

Table 2 Summary of experimental data of dynamic adsorption between HCNS-0/4 and commercial AC
HCNS-0/4的甲苯动态穿透曲线如图8所示,相应的穿透时间、平衡时间和甲苯吸附容量列于表3.可见,甲苯在HCNS-0/4 样品上第一次吸附的穿透时间和平衡时间分别为38 min和68 min,均比正己烷短.甲苯在HCNS-0/4 上的第一次动态平衡吸附容量为1.37 g/g,小于正己烷的动态吸附结果.HCNS-0/4 的正己烷和甲苯吸附容量大可归因于其高表面积和大孔容改善了正己烷和甲苯的质量传递.在第五次甲苯动态吸附实验中,HCNS-0/4的穿透时间和平衡时间分别为36 min和64 min,动态吸附容量为1.34 g/g.可以看出,HCNS-0/4 的第一次甲苯动态吸附穿透时间和平衡时间均大于第五次的结果,经过5 次吸附-解吸实验后,吸附剂的吸附性能下降了约2.19%.从表3 可以看出,HCNS-0/4具有相对稳定的甲苯吸附能力,5次吸附-解决实验中的吸附容量保持在1.34~1.37 g/g区间,解吸率也保持在99.2%以上.
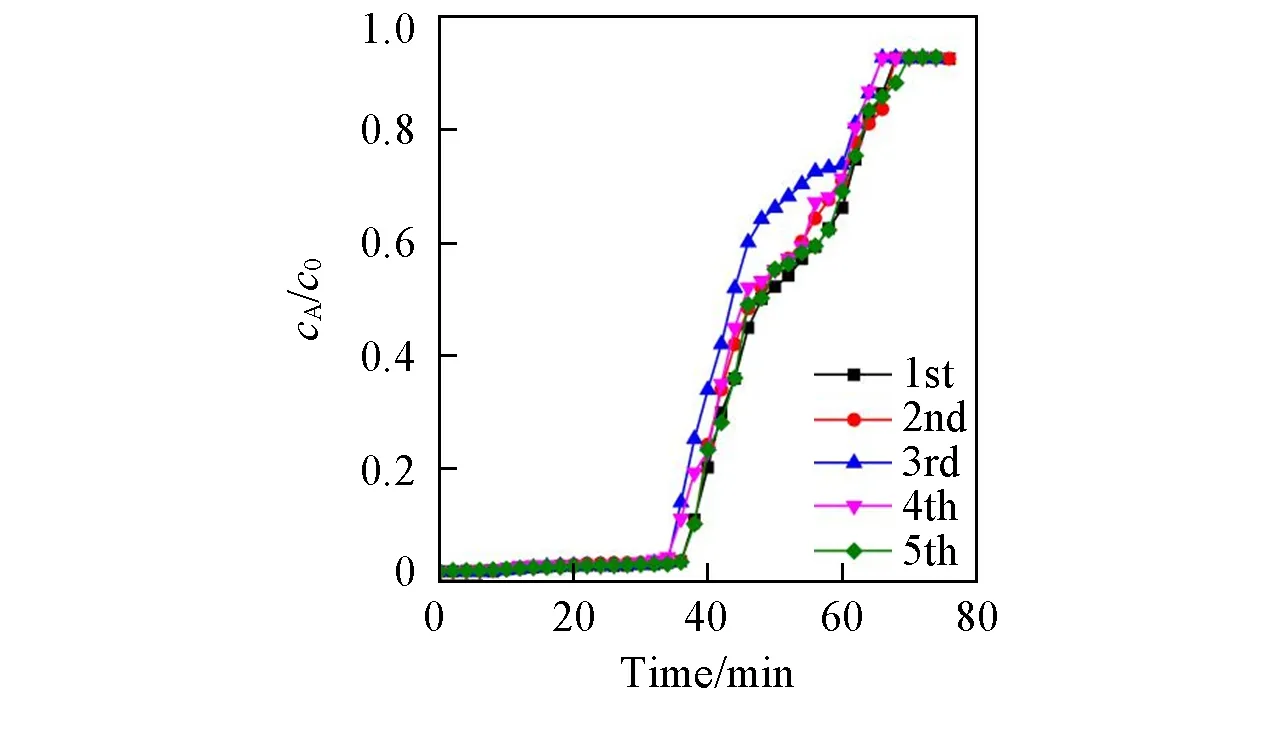
Fig.8 Breakthrough curves for toluene of HCNS-0/4

Table 3 Dynamic adsorption parameters of toluene on HCNS-0/4
图S4(A)(见本文支持信息)为HCNS-0/4对正己烷和甲苯5次动态吸附前后以及AC对正己烷5次动态吸附前后的氮气吸附-脱附等温线.HCNS-0/4对正己烷和甲苯动态吸附后的等温线表现出具有H4型滞后环的Ⅳ型等温线,而AC对正己烷5次动态吸附后的等温线依旧是Ⅰ型等温线,表明经过5次动态吸附之后没有改变HCNS-0/4和AC的孔结构.图S4(B)为HCNS-0/4对正己烷和甲苯5次动态吸附前后以及AC对正己烷5次动态吸附前后的孔径分布曲线(由等温吸附曲线的吸附分支根据BJH模型计算得出).可以清楚地看到,HCNS-0/4对正己烷和甲苯动态吸附后只有1个尖峰,表明动态吸附后的HCNS-0/4的孔径分布相对较窄,在5~7 nm的窄区间之内;AC对正己烷动态吸附后也只有1个尖峰,表明动态吸附后的AC的孔径分布相对较窄,在5.5 nm左右.表S2(见本文支持信息)列出了HCNS-0/4对正己烷和甲苯动态吸附后以及AC对正己烷动态吸附前后的比表面积、孔容和平均孔径.从表S2中可以看出,HCNS-0/4对正己烷动态吸附后的SBET和V0分别比吸附前降低了10.6%和1.29%;而对甲苯动态吸附后的SBET和V0比吸附前降低了7.81%和4.06%.HCNS-0/4 动态吸附正己烷和甲苯后SBET和V0的下降导致了动态吸附容量的降低.而AC 对正己烷动态吸附后的SBET和V0分别比吸附前降低了20.8%和17.0%.经过5次动态吸附之后,AC的SBET和V0比HCNS-0/4减小得更多.
在使用水饱和载气(95%RH)进行的实验中,正己烷在HCNS-0/4上的动态吸附显示出相似的结果(图9).水饱和载气在HCNS-0/4上的首次穿透时间为42 min,比没有水蒸气的穿透时间(44 min)短,且观察到较低的qe,n-hexane(1.91 g/g),其qe,n-hexane/qwater约为19.1(表4).为了测试吸附剂在水饱和载气的正己烷动态平衡吸附过程中的可重复使用性,通过在100 ℃的真空中热处理75 min,至样品质量不变来再生HCNS-0/4.吸附测试结果表明,HCNS-0/4 具有稳定的穿透时间和动态平衡解吸能力,平均解吸率为99.4%,弱吸附在外表面或HCNS-0/4 的开放中孔的正己烷分子在解吸条件下容易被水饱和载气解吸.以上结果进一步证实,与水蒸气相比,HCNS-0/4对VOC的亲和力更高.

Fig.9 Breakthrough curves for n-hexane under 95%RH of HCNS-0/4

Table 4 Ddynamic n-hexaneadsorption parameters under 95%RH of HCNS-0/4
在使用水饱和载气(95%RH)进行的实验中,甲苯在HCNS-0/4 上的动态吸附显示出相似的结果(图10).水饱和载气在HCNS-0/4 上的首次穿透时间为36 min,比没有水蒸气时的穿透时间(38 min)短,且观察到较低的qe,toluene(1.35 g/g),其qe,toluene/qwater约为67.5(表5).HCNS-0/4具有稳定的穿透时间和动态甲苯平衡解吸能力,平均解吸率为99.4%,弱吸附在外表面或HCNS-0/4 的开放中孔的甲苯分子在解吸条件下容易被水饱和载气解吸.此实验结果进一步证实,与水蒸气相比,HCNS-0/4对VOC的亲和力更高.

Fig.10 Breakthrough curves for toluene under 95%RH of HCNS-0/4

Table 5 Competitive dynamic adsorption parameters of toluene and water on HCNS-0/4
2.4 HCNS-0/4对双组分VOCs的动态吸附-脱附性能
为了进一步研究VOCs分子与吸附剂表面烃基之间的亲和力,研究了正己烷和甲苯在HCNS-0/4上的竞争吸附.图11显示了正己烷和甲苯混合物在干燥条件下在HCNS-0/4的上的穿透曲线,表6列出了相应的动态吸附参数.正己烷和甲苯混合物的吸附曲线表明选择性是动力学驱动的,即基于分子在孔中扩散速率的差异.通常,对于具有不同动力学直径但接近材料孔径的分子可观察到这种选择性.因此,与较小尺寸的分子相比,较大尺寸的分子更倾向于小的深度扩散,从而导致更短的穿透时间.因此,对比在相同条件下单组分VOC 的相应吸附结果,在双组分竞争吸附下,正己烷的首次穿透时间和平衡时间(分别为32 和64 min)以及甲苯的首次穿透时间和平衡时间(分别为24 和56 min)均变短,而相应的平衡吸附容量(分别为1.18 和0.810 g/g)则变得更小.由于正己烷的穿透时间比甲苯长,因此正己烷的吸附容量也相应地比甲苯高.这是由于正己烷和甲苯的极性不同,正己烷的极性弱于甲苯,而组成与有机硅源相似,所以正己烷分子优先吸附在HCNS-0/4 的表面上,而芳烃(甲苯)与HCNS-0/4 的相互作用较弱,导致穿透时间短且动态吸附容量低,说明HCNS-0/4 对正己烷比对甲苯更有亲和力.
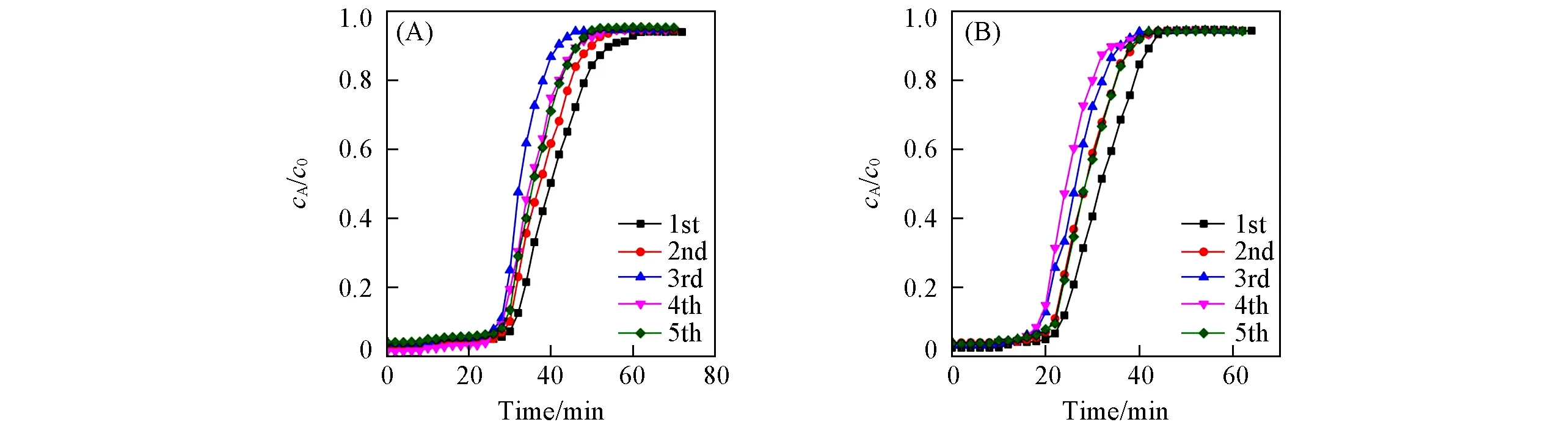
Fig.11 Breakthrough curves for n-hexane and toluene competitive adsorption of HCNS-0/4

Table 6 Dynamic competitive adsorption parameters of n-hexane and toluene on HCNS-0/4
3 结 论
采用一步、无表面活性剂的方法,以间苯二酚甲醛树脂为碳源,TEOS/TPOS 为硅源,经碳化酸蚀后合成了大粒径、单分散性良好的HCNSs.TEM、红外光谱和氮气吸附-脱附等温线等测试结果表明,所制备的HCNSs 为空心介孔碳材料,且通过改变TEOS/TPOS 的摩尔比,合成的HCNSs 的粒径与壁厚分别在280~430 nm 和15~63 nm 区间内可调.随着硅源中TPOS 比例的提高,HCNSs 的粒径和壁厚增大,比表面积、孔容和平均孔径都有提升.其中HCNS-0/4具有最大的粒径(426 nm)和壁厚(63 nm)、最高的比表面积(1216 m2/g)和孔容(1.77 cm3/g).静态和动态VOCs吸附实验结果表明,在多次的吸附-脱附实验中,HCNSs均具有较高的吸附容量、良好的吸附稳定性和高解吸效率.其中HCNS-0/4样品具有高的静态正己烷(2.02 g/g)、甲苯(1.42 g/g)和油气(0.926 g/g)吸附容量,吸附能力远强于商品化AC.在动态吸附正己烷的实验中,HCNS-0/4也表现出远高于商品化AC的动态平衡吸附容量和动态吸附稳定性,证明了其优于商品化AC的动态吸附性能.HCNSs尤其是HCNS-0/4的静/动态吸附实验结果表明其在VOCs气体吸附领域有应用潜力.
支持信息见http://www.cjcu.jlu.edu.cn/CN/10.7503/cjcu20200864.
