全腹腔镜下NOSES手术在直肠癌中的应用及近期疗效分析
2021-06-28孙礼山赵豹董磊王学东
孙礼山, 赵豹, 董磊, 王学东
直肠癌为胃肠道最常见的恶性肿瘤之一,发病率和致死率均较高。腹腔镜直肠癌根治术以创伤小、解剖清晰、恢复快等优点逐渐代替传统的开腹手术,成为直肠癌根治手术的首选方式[1]。为了达到最大化微创的目的,最新提出的经自然腔道取标本手术(natural orifice specimen extraction surgery,NOSES)被应用于直肠癌的手术治疗中,该术式通过腹腔镜下切除吻合、标本经自然腔道取出和无需腹部辅助切口等方式体现出更好的微创效果[2]。研究认为,腹腔镜技术、NOSES等技术的成熟应用使得直肠癌患者的保肛概率明显增加,且应用NOSES手术可明显减少传统腔镜手术带来的疼痛及术后切口疝、切口感染、肠梗阻等并发症的发生率[3-4]。然而,NOSES手术具有严格的手术适应证,并非对全部直肠癌患者都适用。本研究通过比较腹腔镜下结肠吻合技术在直肠癌NOSES手术与传统腹腔镜手术中的应用效果,以探讨腹腔镜下结肠吻合并NOSES手术治疗直肠癌的可行性、安全性及近期疗效。
1 资料与方法
1.1 一般资料
选取皖北煤电集团总医院2017年4月至2019年4月收治的80例直肠癌患者。纳入标准:①经病理诊断确诊,符合2010年WHO制定的直肠癌相关诊断标准[5];②肿瘤环周直径≤5 cm,Dukes分期A~B期;③符合手术相关指征,无手术相关禁忌证;④术前检查无肿瘤种植、侵犯相邻器官或远处转移。排除标准:①同时合并其他部位原发性癌;②合并肝肾等重要脏器功能障碍、免疫异常、急慢性感染、血液系统疾病及精神疾病;③无法配合完成研究;④术前行放化疗及其他治疗;⑤合并影响本研究结果的其他因素。依据治疗方法的不同将本组80例患者分为对照组(35例)和研究组(45例)。对照组中男20例,女15例;年龄25~77(51.6±3.9)岁;Dukes分期:A期16例,B期19例;低分化腺癌18例,中分化腺癌17例。研究组中男29例,女16例;年龄22~76(50.9±3.7)岁;Dukes分期:A期24例,B期21例;低分化腺癌25例,中分化腺癌20例。两组患者性别(χ2=0.442)、年龄(t=0.820)、Dukes分期(χ2=0.457)、分化类型(χ2=0.135)比较差异无统计学意义(P>0.05),具有可比性。本研究获得医院医学伦理委员会批准通过,患者均自愿参与本研究并签署知情同意书。
1.2 方法
1.2.1 对照组 行传统腹腔镜手术治疗。于患者脐上10 mm开孔进行观察,并于左右下腹各开2个操作孔辅助处理,于下腹正中行8 cm辅助切口,取出标本并完成吻合。
1.2.2 研究组 行腹腔镜下结肠吻合并NOSES手术治疗。患者取截石位,并依照直肠全系膜切除术(total mesorectal excision,TME)原则行腹腔镜5孔法探查腹腔,于左右下腹各建立2个操作孔,于盆腔和乙状结肠系膜交界处打开腹膜,探查并游离肠系膜下血管,血管夹置于肠系膜下血管,并尽量保留左结肠血管,切断结扎血管并彻底清扫周围淋巴结。
对低位患者行经肛门全直肠系膜切除术(transanal total mesorectal excision,TaTME),将肛门及肛周消毒后置入lonestar肛门盘状拉钩,肉眼直视下于肿瘤下缘1.5 cm及肿瘤距齿状线2 cm处缝合荷包,荷包边缘下缘0.5 cm处切开并置入starport操作平台,肿瘤距齿状线2 cm以上则先置入starport操作平台然后缝合荷包。于荷包下缘0.5 cm处切开直肠壁黏膜、黏膜下层及纵行肌至括约肌间隙,进入TME间隙与腹腔组汇合完成游离。经肛拖出肿瘤及近端肠管,肛门外游离直肠标本,置入吻合器抵钉座推至腹腔。荷包缝合直肠肛管远断端,腹腔镜监视下完成结肠与直肠肛管端-端吻合。通过抗菌可吸收缝合线加固吻合口,置入肛管。
对中高位(肿瘤距肛门>7 cm)患者采用切除拖出式,腹腔完成游离后于肿瘤下方行闭锁式尼龙扎带扎闭肠管,经肛反复冲洗肿瘤下方2 cm处超声刀离断肠管,放置标本保护套,经标本保护套放入吻合器抵钉座,经标本保护套伸入卵圆钳取出标本,腹腔镜下用0.1%双氯苯双胍己烷(洗必泰)冲洗,3/0可吸收缝合线连续缝合近端肠管包埋抵钉座,再荷包缝合远端肠管。采用16号红尿管保护吻合器头经肛深入后打结固定,取走红尿管并对合吻合器击发完成吻合。冲洗并置入肛管引流管。
1.3 观测指标
①手术指标:手术时间、术中出血量及预防性造口数量;②术后病理学指标:淋巴结清扫数量、标本完整度、肿瘤最大横径、环周切缘阳性率;③术后康复指标:肠功能恢复时间、住院时间、术后24 h及术后48 h的VAS评分、术后6个月及1年的复发情况;④免疫功能及炎性指标:于术前1 d、术后1 d、3 d、5 d抽取患者静脉血3 ml,采用流式细胞术检测淋巴细胞亚群CD3+、CD4+、CD8+细胞数量,并计算CD4+/CD8+;采用酶联免疫吸附试验(ELISA)检测血清C反应蛋白(CRP)水平;⑤生活质量评分:于术后30 d采用简明健康状况调查表(SF-36)调查患者的生活质量,综合评估其生理功能、生理职能、一般健康状况、躯体疼痛、活力、社会功能、情感职能、精神综合评分及躯体综合评分。
1.4 统计学方法
2 结果
2.1 两组手术及术后病理指标比较
研究组与对照组术中出血量、淋巴结清扫数量、标本完整度、预防性造口数量、肿瘤最大横径、环周切缘阳性率、术前及术后24、48 h VAS评分、腹腔感染及吻合口漏并发症发生率比较差异无统计学意义(P>0.05);研究组的手术时间长于对照组,肠功能恢复时间、住院时间短于对照组,差异有统计学意义(P<0.05),见表1。
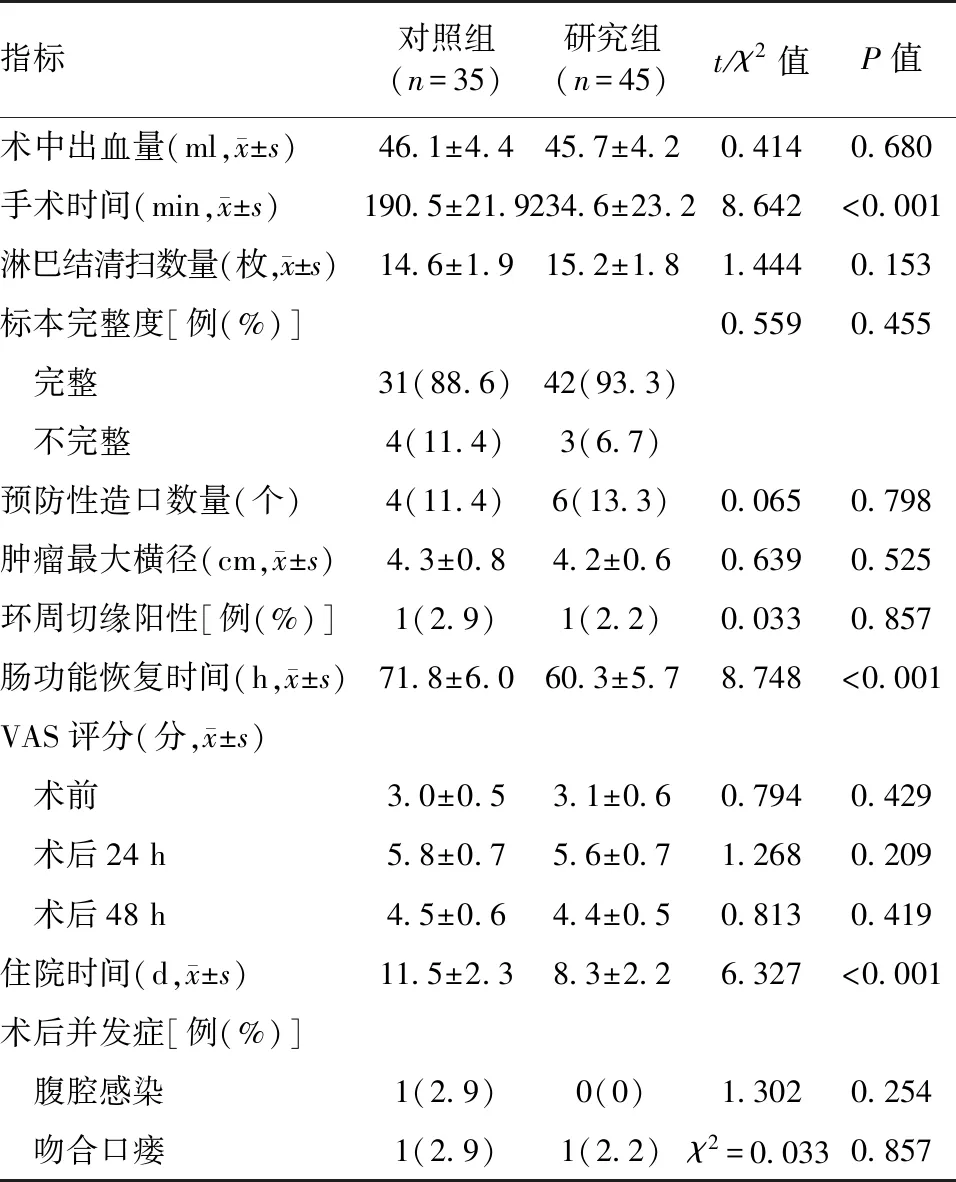
表1 两组手术及术后病理学指标比较
2.2 两组手术前后免疫及炎症指标比较
术前1 d、术后1、3、5 d,两组的免疫功能指标CD3+、CD4+、CD8+、CD4+/CD8+差异无统计学意义(P>0.05);术前1 d,两组CRP水平差异无统计学意义(P>0.05);术后1、3、5 d,两组CRP水平均高于术前1 d,且研究组高于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组手术前后免疫及炎症指标比较
2.3 两组术后复发情况比较
术后6个月,两组复发率比较差异无统计学意义(P>0.05);术后1年,研究组的复发率低于对照组,差异有统计学意义(P<0.05),见表3。其中对照组中5例复发患者肿瘤位置距离肛门<3 cm 1例,3~6 cm 3例,>6 cm 1例;研究组复发1例肿瘤位置距离肛门3~6 cm。
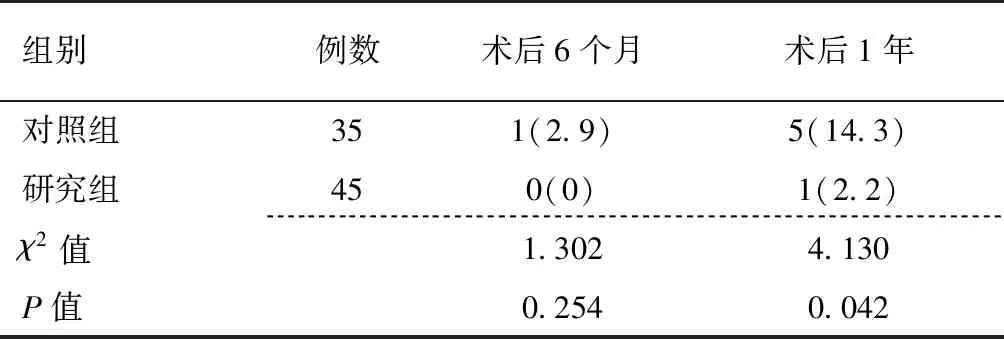
表3 两组术后复发情况比较 [例(%)]
2.4 两组术后近期生活质量评分比较
研究组术后躯体疼痛评分低于对照组,其余各项评分均高于对照组,差异有统计学意义(P<0.05),见表4。

表4 两组术后近期生活质量评分比较
3 讨论
过去开腹手术是治疗结直肠癌的主要术式,但却存在出血多、切口大、恢复慢等问题,随着微创技术的发展和应用,腹腔镜手术越来越受到外科医生的青睐。腹腔镜手术相比于开腹手术具有明显优势,其切口小、患者术后疼痛明显减轻、恢复更快,且在远期疗效上与开腹手术相当[6]。普通的腹腔镜手术需要在腹壁行辅助切口,容易造成瘢痕和腹壁功能障碍。NOSES术式由王锡山等[7-8]根据经自然腔道内镜手术(NOTES)术式研究提出,其通过经肛门手术内镜、腹腔镜器械、软质内镜等设备进行腹腔内手术操作,并经阴道、直肠或口腔等自然腔道取出标本的腹壁无辅助切口手术,不仅可以更微创、更美观,也更完美地展示了腹腔镜手术的优势。腹盆腔中胃、直肠、小肠、泌尿、肝胆、妇科肿瘤等都可以开展NOSES手术,且在特定结直肠癌患者手术治疗中取得了显著进展[9-10]。
本研究通过比较采用全腹腔镜下NOSES手术及采用传统腹腔镜手术的直肠癌患者,结果显示研究组的手术时间虽然长于对照组,但是肠功能恢复时间、住院时间明显短于对照组,提示全腹腔镜下吻合小切口切除经NOSES手术治疗直肠癌比传统腹腔镜手术患者术后恢复快。传统的腹腔镜下直肠癌手术需要于腹壁行4~8 cm辅助切口以取出肿瘤标本和放置吻合器抵钉座,这个腹壁切口的存在一定程度上抵消了部分微创手术的效果,使得患者术后并发症风险明显提高。这一切口也是导致患者术后疼痛的主要原因。腹壁切口瘢痕的存在不仅存在美容学的缺憾,也给患者造成长期的负面心理暗示。NOSES手术与传统腔镜手术最大的区别在于无腹壁取标本辅助切口,标本经自然腔道取出,术后仅存在几处微小Trocar瘢痕。多项研究发现NOSES术式适用于各个部位的结直肠肿瘤,对结直肠肿瘤手术的根治效果已经得到广泛认同[11-12]。
全腹腔镜下吻合技术和腹腔镜管状吻合器吻合技术为两种不同的结直肠癌根治术消化道重建方式[13],其中全腹腔镜下吻合技术采用直线吻合器进行食管空肠侧吻合术,对于患者术后胃肠道功能恢复影响较小,且NOSES手术方案减少了患者的腹部损伤刺激,手术安全性得到提升。CRP为临床常用的炎性因子,其在机体感或损伤时明显升高,对于直肠癌患者术后伤口恢复及炎性并发症具有一定提示作用。机体免疫功能对于抵抗肿瘤发展、抑制炎性因子数量增加及促进直肠癌患者术后功能恢复具有重要意义。本研究中,研究组术后1、3、5 d的CRP水平明显低于对照组,两组免疫功能指标比较则无明显差异。分析患者复发情况,发现复发部位以距离肛门3~6 cm的患者居多,原因是此处为盆腔及会阴部交界处,位置较深,术中容易损伤肠壁导致肿瘤细胞脱落种植,或存在清扫不彻底导致肿瘤残余,导致术后复发。对于患者近期生活质量的评估显示,研究组的整体生活质量评分相对更优,对照组患者受术后疼痛反应、切口并发症、炎症刺激、腹部切口美观性等方面的影响,容易给患者生理、心理带来一定的负面影响,导致患者近期生活质量降低。而NOSES手术肠系膜游离层面、血管离断、淋巴结清扫、肠管离断等手术操作及原则基本与传统腹腔镜手术一致,但其取标本途径及消化道重建方式不同。NOSES手术不存在腹部切口,减少了患者腹部损伤刺激,患者术后疼痛明显减轻,可较早下床活动,有利于肠道功能的早期恢复,更有助于患者术后恢复,从而使患者的短期预后效果更佳。
然而,NOSES术式具有较为严格的适应证,对于肥胖、肿瘤直径较大等患者不适用,此类患者可经全腹腔镜下切除肿瘤并于下腹部做外横内纵切口取出标本,这样的术式也称作类NOSES手术。同时,无瘤和无菌是直肠癌乃至所有肿瘤外科手术所坚持的基本原则,对于NOSES手术的无瘤和无菌原则把控具有一定挑战性,如何有效防止吻合器抵钉座经肛置入腹腔或在腹腔内开放肠腔进行包埋时严格遵守无菌操作规范,如何确保肿瘤组织在经自然腔道拖出时不会因挤压造成肿瘤细胞入血或脱落引发医源性扩散值得临床注意[14-15]。只要严格遵循手术操作规范,并对患者适应证掌握得当,结直肠癌行全腹腔镜下NOSES手术是安全可行的。
综上所述,全腹腔镜下NOSES手术治疗直肠癌近期效果显著,患者肠道功能恢复快、复发率低,术后近期生活质量得到明显提升。
