血液分析仪日常室内质量控制中新鲜血比对方案的建立
2021-06-26郑翠玲
郑翠玲,王 力,程 焱,崔 巍
(国家癌症中心 国家肿瘤临床医学研究中心 中国医学科学院北京协和医学院肿瘤医院检验科,北京 100021)
目前,临床实验室血常规检测工作需要同时使用数台血液分析仪才能够完成,由于不同仪器检测原理、内部构造及其他因素的影响,同一临床标本在不同仪器上的检测结果可能存在一定的差异。因此,保证不同仪器间检测结果的准确性和一致性,不仅是检验工作的重点,也是国际标准化组织(the International Organization for Standardization,ISO)15189标准对检验结果可比性的要求[1]。为了有效保证检验结果的准确性、一致性和可比性,进行高效的室内质量控制(internal quality control,IQC)是必要措施,临床实验室一般使用仪器配套质控品来进行IQC,但配套质控品成本高、有效期短、多次重复混匀后会导致部分检测数据出现漂移。为解决这一问题,本研究建立了一套利用新鲜全血标本进行日常IQC的方案,截至目前,运行良好。
1 材料和方法
1.1 标本来源
实验室每天在完成IQC后,按照美国临床实验室标准化协会(the Clinical and Laboratory Standards Institute,CLSI)EP9-A2[2]文件的要求,从测定当天的乙二胺四乙酸二钾抗凝标本中选择新鲜血比对标本,该标本各项指标均在参考区间内,无异常警示,标本量约2 mL。新鲜血比对标本尽可能在6 h内完成[3-4]比对。
1.2 仪器与试剂
日本Sysmex公司XN-9000血液分析仪(包含5个模块)和XS-800i血液分析仪(2台),共7台仪器。以性能良好、规范化操作、定期参加我国国家卫生健康委临床检验中心室间质量评价,且结果为优秀的血液分析仪作为靶机,以其他血液分析仪作为比对仪器。所有仪器均使用配套质控品和试剂。
1.3 评价项目
评价项目包括白细胞(white blood cell,WBC)计数、红细胞(red blood cell,RBC)计数、血红蛋白(hemoglobin,Hb)、血细胞比容(hematocrit,HCT)、血小板(platelet,PLT)计数。
1.4 方法
1.4.1 新鲜血比对 根据北京协和医学院肿瘤医院血常规检测标本量分布情况,实验室每日完成IQC后,在尽可能短的时间内挑选新鲜血标本,在靶机上进行检测,将测定结果(5001)传输至实验室信息系统(laboratory information system,LIS),作为后续比对的基准值;约9:00时将新鲜血标本在XN-9000血液分析仪的5个模块上进行检测,将第1次比对仪器测定结果(5011、5021、5031、5051)和靶机测定结果(5041)传输至LIS;约10:30将新鲜血标本在所有血液分析仪上进行检测,将第2次比对仪器测定结果(5012、5022、5032、5052、5072、5082)和靶机测定结果(5042)传输至LIS;若标本量无法满足后续检测或检测时间超过6 h,在第2次新鲜血比对后,重新挑选1份新鲜血标本,在靶机上进行测定,并将结果(5003)传输至LIS,作为关机前比对的基准值;约15:30时,将新鲜血标本在所有血液分析仪上进行关机前比对,将关机前比对结果(5013、5023、5033、5053、5073、5083)和靶机测定结果(5043)传输至LIS。在LIS中自动按照公式计算相对偏差,并判断是否超出相对偏差标准,如果超出标准,用红色(比对仪器测定结果高于基准值)或蓝色(比对仪器测定结果低于基准值)显示。仪器间相对偏差的计算公式为:相对比对偏差(%)=(第1次比对结果-5041)/5041×100%;靶机运行过程中相对偏差的计算公式为:相对比对偏差(%)=(5041-5001)/5001×100%;比对仪器运行过程中相对偏差的计算公式为:相对偏差(%)=(第2次比对结果-第1次比对结果)/ 第1次比对结果×100% 。
1.4.2 判断标准 参照1988年美国临床实验室改进法案(the Clinical Laboratory Improvement Amendments of 1988,CLIA'88)允许误差(WBC计数为±15%、RBC计数为±6.0%、Hb为±7.0%、HCT为±6.0%、PLT计数为±25.0%),以1/2 CLIA'88允许误差的作为仪器间相对偏差标准,以1/3 CLIA'88允许误差的作为同一仪器运行过程中的相对偏差标准。以相对偏差(%)≤相应的比对标准为合格,否则为不合格。
2 结果
2.1 仪器间新鲜血标本比对结果
在确定仪器IQC在控后,选取1份新鲜全血标本,用所建立的方法比较比对仪器与靶机的测定结果,LIS自动采集、计算比对数据,并自动提示异常情况,针对不同原因引起的异常情况采取相应措施,确保仪器运行正常,以便有效监控仪器稳定性。仪器间比对的原始数据见表1。
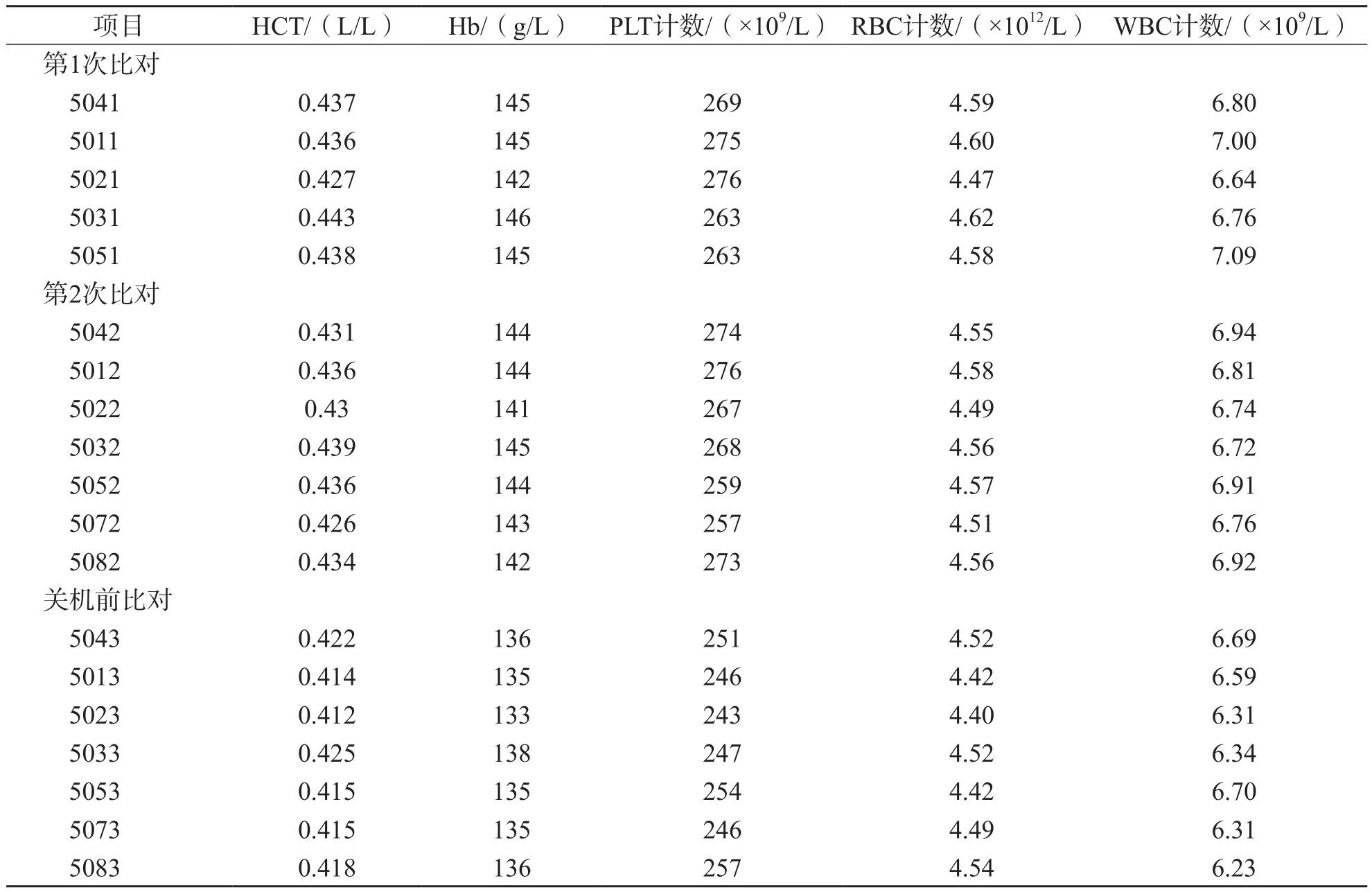
表1 仪器间新鲜血标本比对原始数据
2.2 仪器间新鲜血标本比对相对偏差
比较相对偏差与1/2 CLIA'88允许误差(WBC计数为≤±7.50%、RBC计数为≤±3.00%,Hb为≤±3.50%、HCT为≤±3.00%、PLT计数为≤±12.50%),以超过80%的标本的相对偏差在1/2 CLIA'88允许误差范围内为比对合格,仪器间检测结果具有可比性,一致性良好。仪器间新鲜血标本比对数据相对偏差见表2。
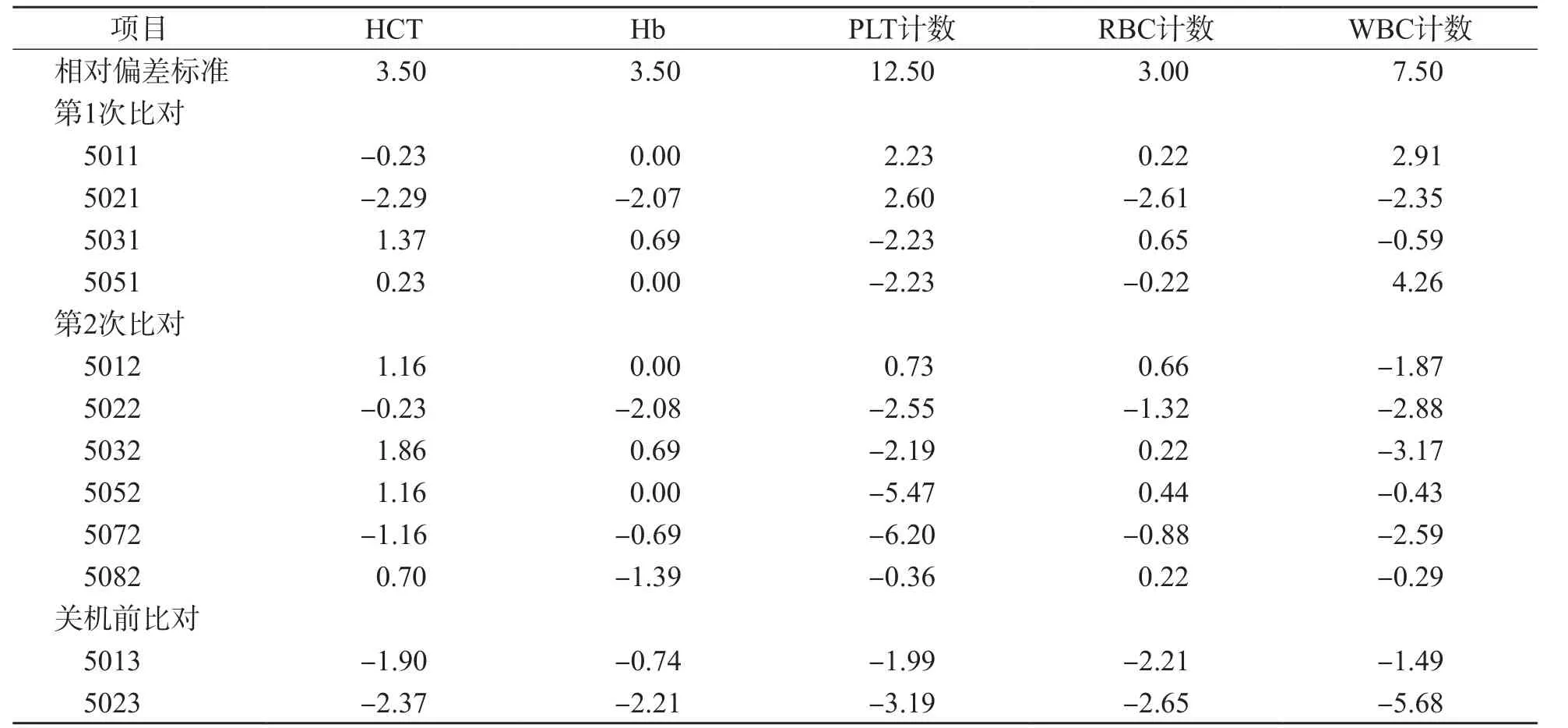
表2 仪器间新鲜血标本比对相对偏差 %
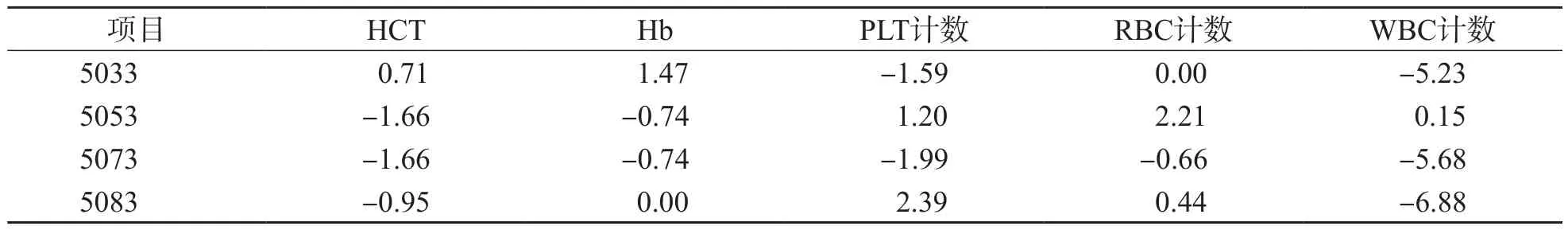
续表2 %
2.3 仪器运行过程中新鲜血标本比对结果
在仪器日常运行过程中的不同时间点检测所选取的比对标本,及时评估仪器运行过程中的性能。应用所建立的方法对所有血液分析仪日常运行过程的比对结果进行评估,结果显示,仪器运行稳定时,新鲜血标本比对结果具有可比性。仪器运行过程中比对的原始数据见表3。
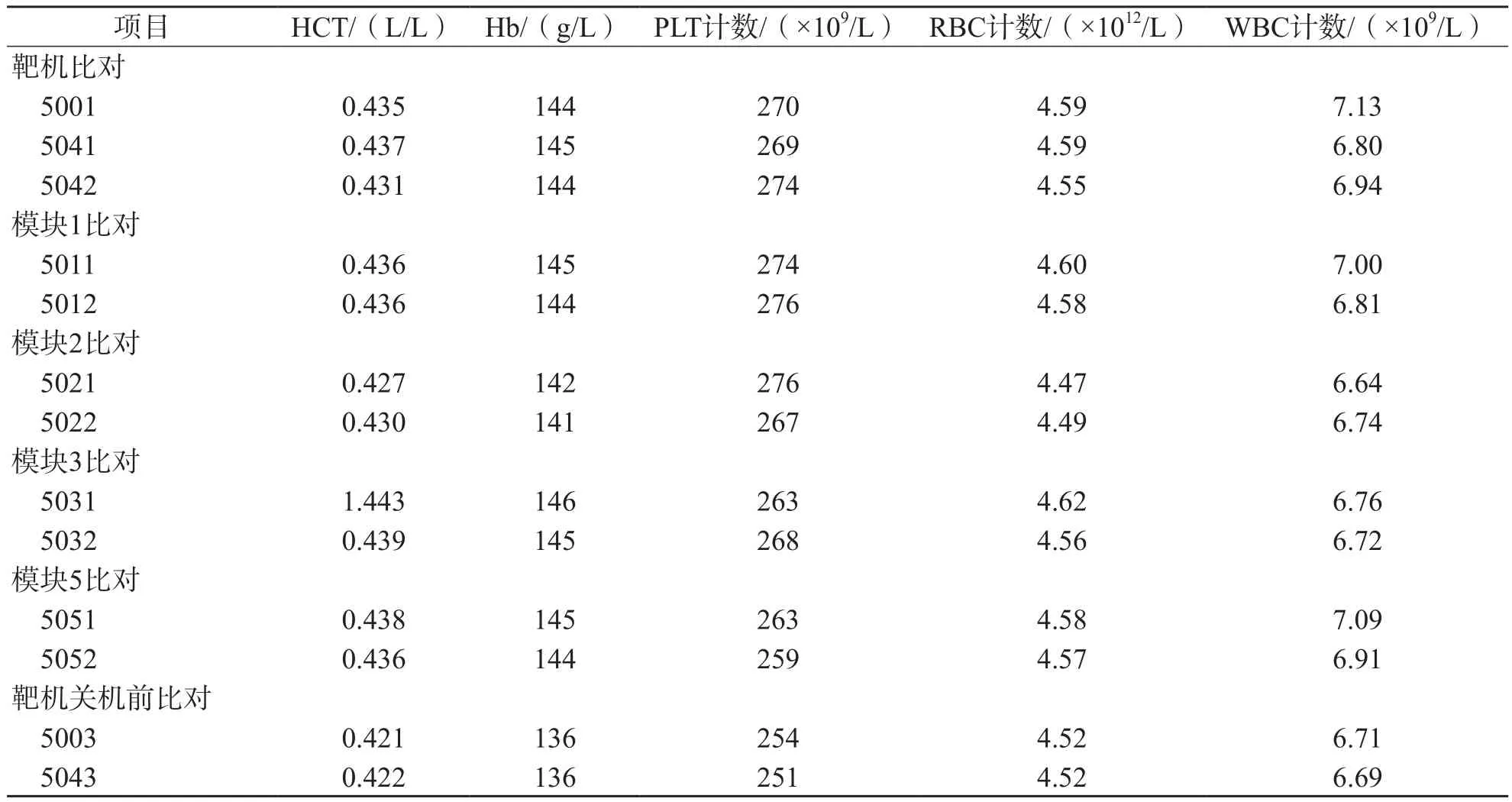
表3 仪器运行过程中新鲜血标本比对结果
2.4 仪器运行过程中新鲜血标本比对相对偏差
将比对数据的相对偏差与1/3 CLIA'88允许误差(WBC计数为≤±5.00%、RBC计数为≤±2.00%、Hb为≤±2.30%、HCT为≤±2.00%、PLT计数为≤±8.30%)进行比较,有超过80%的比对数据的相对偏差满足1/3 CLIA'88允许误差的标准,仪器运行稳定。仪器运行过程中新鲜血标本比对相对偏差见表4。
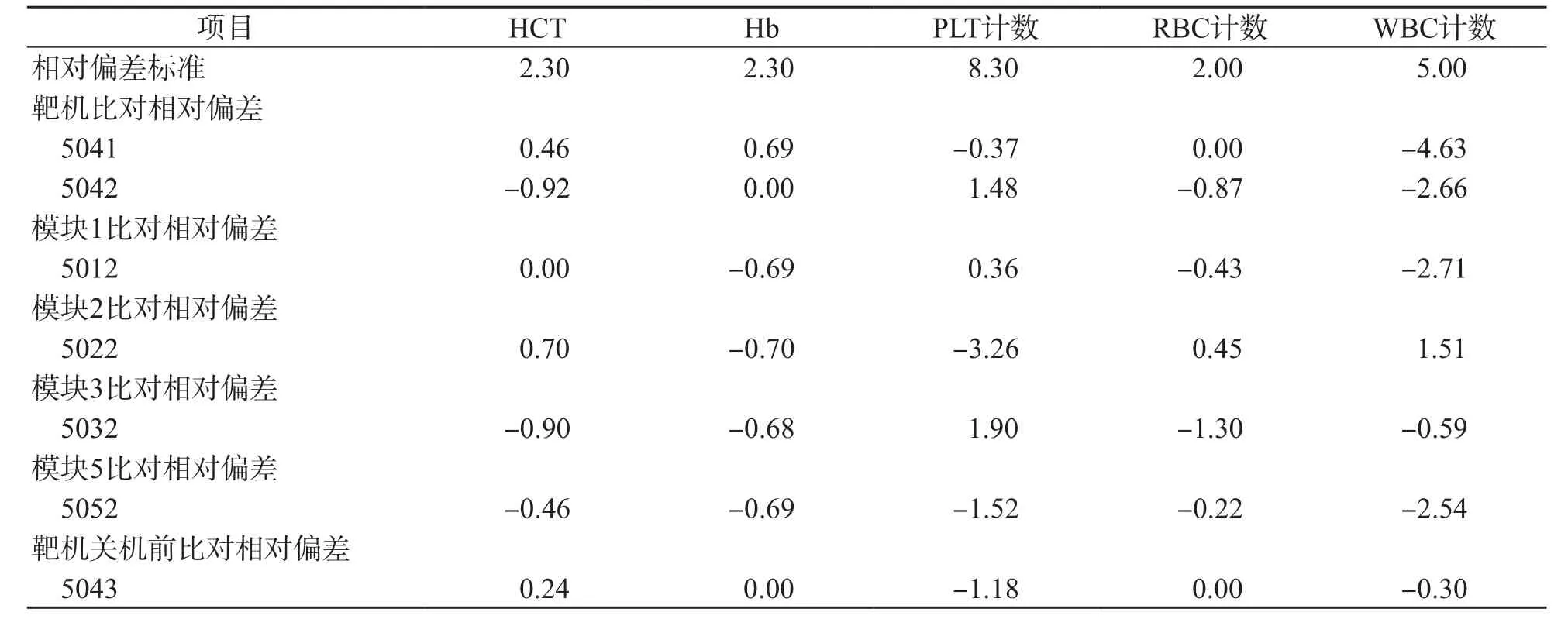
表4 仪器运行过程中新鲜血标本比对相对偏差 %
3 讨论
随着血常规项目检测量的逐渐增大,很多医院都拥有多台血液分析仪,为了减少检验差异,提高检测结果的一致性和准确性,IQC是保证血液分析质量的必要措施,而使用仪器配套质控品是IQC最重要的条件之一。然而配套质控品成本高、有效期短,在一定程度上增加了血液分析仪IQC的难度,为确保不同血液分析仪血常规检测结果的一致性,建立一个经济、便捷、有效的IQC方案非常必要。本研究建立的血液分析仪日常IQC中的新鲜血比对方案已经应用了26个月,通过不断地对方案进行改进,现已趋于成熟。在方案运行过程中,我们发现应重点关注以下几点:(1)靶机的选择,应选择性能良好、规范化操作、使用配套试剂的血液分析仪,其室间质量评价、校准和IQC满足要求,从而保证检测结果的准确性和稳定性;(2)新鲜血标本比对的选择,应选择无PLT聚集、大PLT、有核RBC、RBC碎片、脂浊等异常提示,检测结果处于正常参考区间的患者新鲜血常规标本,不建议选择低值标本,因为低值标本测定结果可导致相对偏差偏大,从而影响对仪器比对结果的正确判断(临床可接受);(3)比对频次的确定,应考虑科室标本量和新鲜血稳定性这2个因素,标本量大的时段应增加比对次数,因此,我们在标本量集中的上午安排了2次比对;此外,根据文献报道[2-4],在室温(20 ℃~25 ℃)条件下6 h内完成标本的检测可以保证新鲜血标本的稳定性,因此,我们最先建立了用关机前比对代替关机前质控的方法,这不仅保证了全天检测结果的准确性,而且节约了成本;(4)比对相对偏差标准的建立,建立实验室自身的IQC新鲜血比对标准较直接采用某个标准更能反映实验室仪器的质量,我们在方案建立之初仅将1/2 CLIA'88允许误差作为仪器间比对的相对偏差标准,但是ISO 15189评审专家建议增加仪器运行过程中的比对,于是我们首次建立了将仪器运行过程中比对用于日常IQC的方法,其相对偏差标准为1/3 CLIA'88允许误差;(5)比对实验标本量,应尽量选择血量足够(约2 mL)的标本,如果比对的仪器数量多,可以选择同血型检测结果在参考区间内的数个标本配置成新鲜血比对标本[5];(6)比对结果观察方式的选用,本研究在LIS中建立了每日新鲜血比对完成IQC的功能,自动完成比对数据采集、计算和超过相对偏差标准的提示,克服了人工记录数据和计算的不便,可实时监控新鲜血比对标本的检测偏差,实时观察、打印,从而便利地实施新鲜血比对的IQC。
本研究所建立的方案并不是一成不变的,它可以随着实际条件的改变,不断地进行完善,如当参加比对的血液分析仪多于10台时,建议采用多台仪器的平均值作为靶值,而不是选择靶机检测值作为靶值,这样更能反映日常工作的真实水平,使仪器间相对偏差处于可接受范围。
总之,新鲜血比对标本无基质效应,将其应用于血液分析仪IQC,不仅降低了IQC的成本,更保证了实验室内不同仪器间检测结果的一致性和可比性,还可有效监测仪器运行过程中的稳定性,为实验室认证奠定了基础,值得在临床实验室推广应用。
