基于熵权法和灰色关联分析法评价安徽省不同产地黄精药材质量
2021-06-24冯治国宋大伟范欣荣叶赛金鲍康德姜程曦
冯治国,赵 祺,#,朱 强,宋大伟,范欣荣,叶赛金,鲍康德,*,姜程曦,,4*
1.温州医科大学药学院,浙江 温州 325035
2.池州市九华山黄精研究所,安徽 池州 247100
3.安徽济人药业有限公司,安徽 亳州 236800
4.安徽省九华山佛教医药研究所,安徽 池州 247100
黄精为“十大皖药”之一,因集药用、食用、观赏于一身,市场需求量近年来迅速增加,价格不断提高,应用领域不断扩大[1]。安徽省药用黄精主要来源于多花黄精Polygonatum cyrtonemaHua,适宜生长于表层水分充足且富含腐殖质的砂质土壤及荫蔽之地[2]。但由于野生黄精类药材组成成分因土壤、气候和光照等生境的不同而异[3],不同产地黄精的质量和临床效果有很大差别。目前关于黄精药材质量评价的方法,多集中在生药学鉴定方面[4],或基于1 种或2 种指标性成分[5-6]和基于指纹图谱研究的单一评价模式[7-8]等,综合评价报道较少。
灰色关联度分析法(grey relational analysis)是灰色系统分析方法的一种,是根据因素之间发展趋势的相似或相异程度,作为衡量因素间关联程度的一种方法[9]。由于灰色关联度分析蕴含的“灰色思维”与中医药理论特点相吻合,已应用于石韦PyrrosiaeFolium[10]、黄柏Phellodendri ChinensisCortex[11]、龙胆GentianaeRadixetRhizoma[12]、牡丹皮MoutanCortex[13]等中药材的质量评价。熵权法(entropy weight method)是一种客观赋权法,用来判断某个指标的离散程度,熵作为不确定性的一种度量。信息量越大,不确定性就越小,熵也就越小[14]。本研究采用熵权法和灰色关联度法相结合的质量研究模型[15],以20 个产地野生多花黄精为研究对象,在《中国药典》2020年版规定的指标基础上,增加总皂苷、薯蓣皂苷元含量测定,构建安徽省不同产地黄精药材质量评价的灰色关联度模型,进行安徽省黄精药材质量的综合评价研究,为安徽省多花黄精优质种源的筛选提供了参考依据。
1 仪器与试药
1.1 仪器
SX2-2.5-10Z 箱式电阻炉(上海博迅实业有限公司医疗设备厂);电子分析天平(d=0.1mg,赛多利斯科学仪器有限公司);真空干燥箱(上海森信实验仪器有限公司);RE-52AA 型旋转蒸发仪(上海亚荣生化仪器厂);JP-100S 型超声波清洗机(深圳市洁盟清洗设备有限公司);SP-754P 型紫外分光光度计(上海光谱仪器有限公司);LC-20A 型液相色谱仪(日本岛津公司)。
1.2 试剂
高氯酸、正丁醇、香草醛、蒽酮、浓硫酸、冰醋酸、无水葡萄糖均为分析纯;人参皂苷Rb1(上海安谱实验科技股份有限公司,批号42520050,质量分数≥98%),薯蓣皂苷元(上海源叶生物科技有限公司,批号B20177,质量分数≥98%)。
1.3 样品
2018年9月26日~10月7日,先后于青阳县西华乡、石台县、祁门县等地方采挖野生多花黄精整株植物,经温州医科大学药学院中药学教研室鲍康德副教授鉴定所有样品均来源于百合科黄精属多花黄精P.cyrtonemaHua,来源见表1。然后将采集的20 批次野生多花黄精去泥土,洗净,去须根,初加工蒸制15 min 至透心,切厚片,干燥,成为饮片。
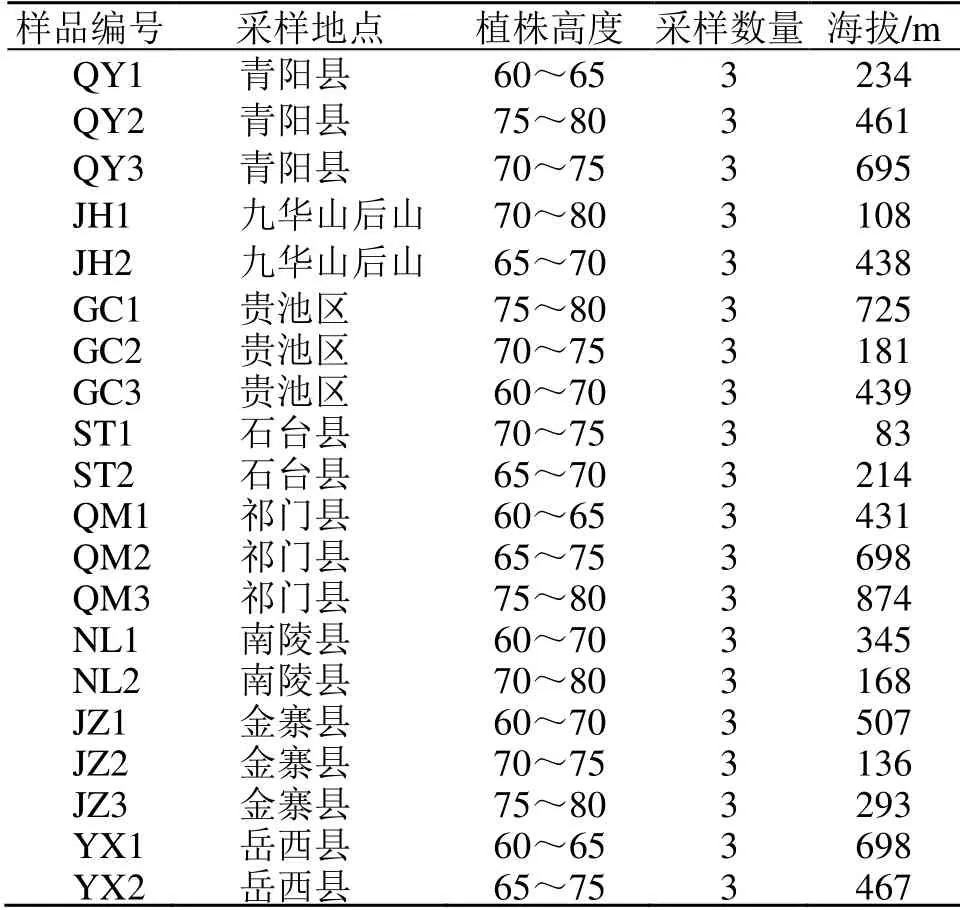
表1 安徽省不同产地野生多花黄精样品来源Table 1 Sources of wild P.cyrtonema from different populations in Anhui Province
2 方法与结果
2.1 基本指标测定
参照《中国药典》2020年版黄精项下测定20批次黄精药材的水分、总灰分、酸不容灰分、浸出物和无水葡萄糖含量[16]。每批样品重复测3 次,结果见表2。
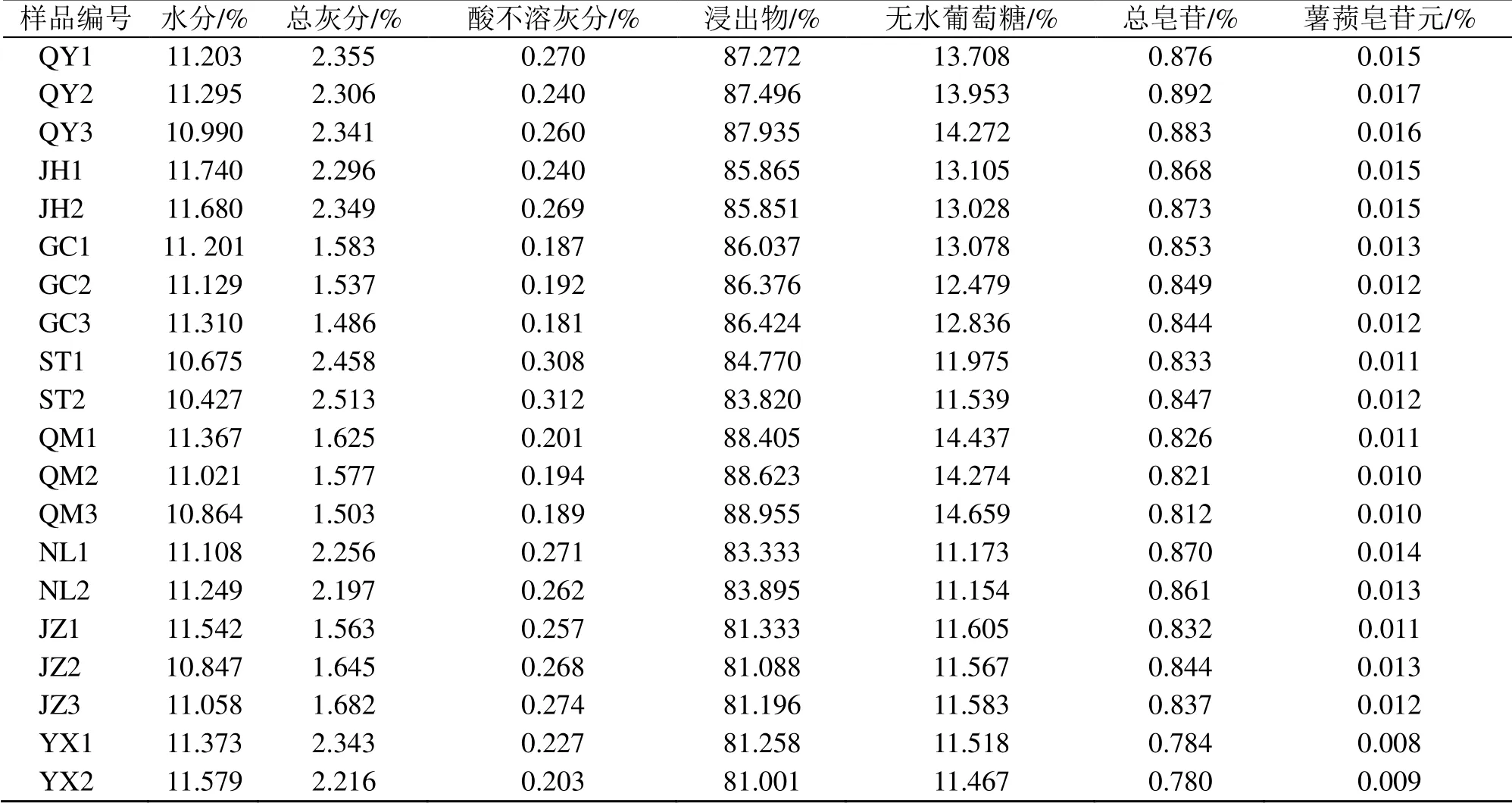
表2 不同产地黄精样品测定结果Table 2 Determination results of Polygonati Rhizoma from different populations
总灰分含量=(灰化后总质量-空坩埚质量)/样品质量
酸不溶灰分含量=(酸化后总质量-空坩埚质量)/样品质量
无水葡萄糖含量=C×Vs×N/M
C为根据标准曲线测的样品浓度;Vs 试管中溶液体积;N提取液为稀释倍数;M为样品质量。
2.2 总皂苷含量的测定
2.2.1 空白溶液制备 加0.2 mL 5%香草醛-冰醋酸溶液(新鲜配制),冰浴时加0.8 mL 高氯酸,混匀,60 ℃水浴加热15 min,再冰浴2 min,加5 mL冰醋酸,混匀,静置5 min,即得[17-19]。
2.2.2 对照品溶液的制备 取人参皂苷Rbl对照品11.3 mg,精密称定,加甲醇溶解,定容至10 mL,摇匀即得。
2.2.3 供试品溶液制备 将黄精饮片于60 ℃干燥6 h 后,用粉碎机粉碎过四号筛。取黄精样品粉末1.00 g,精密称定,加14 倍量水饱和正丁醇,40 ℃超声提取50 min,滤过,滤渣再提取1 次,合并2次滤液,置25 mL 量瓶中,加水饱和正丁醇至刻度,摇匀,即得供试品溶液。
2.2.4 标准曲线的绘制 取人参皂苷Rbl对照品溶液40、80、120、160、200 µL,置10 mL 具塞试管中,挥尽溶剂,之后步骤同空白溶液制备方法,以相应试剂为空白,照紫外一可见分光光度法(通则0401),在550 nm 处测定吸光度(A)。以A值为纵坐标(Y),人参皂苷Rbl质量为横坐标(X),绘制标准曲线,得回归方程Y=0.004X-0.0748,R2=0.999,表明人参皂苷Rbl质量在45.2~226.0 µg 线性良好。
2.2.5 总皂苷的测定 精密量取上述溶液100 µL,挥尽溶剂,之后步骤同空白溶液制备,以相应试剂为空白,按照紫外-可见分光光度法(通则0401),在550 nm 处测定A值。计算结果见表2。
皂苷含量=M1×250/M2
M1为根据标准曲线测的样品质量,M2为样品质量
2.3 薯蓣皂苷元含量测定
2.3.1 对照品溶液的制备 精密称取薯蓣皂苷元5 mg 倒入5 mL 量瓶中,加入甲醇至刻度,充分摇匀,制成含1 mg/mL 薯蓣皂苷元对照品溶液。采用0.22 μm 的滤膜滤过,低温保存,备用。
2.3.2 供试品溶液的制备 精密称取黄精样品粉末2 g 置烧瓶内,加入100 mL 的80%乙醇,充分摇匀,称定质量,加热回流3 h,待冷却后再称量,减少的质量用乙醇补足,充分摇匀,抽滤,取滤液备用。准确量取40 mL 的滤液,旋干乙醇后加3 mol/L 盐酸溶液100 mL 溶解,加热回流3 h,待冷却后,再移到分液漏斗内,加入20 mL 正丁醇萃取,重复2 次,保留正丁醇层,再次旋干,残渣加甲醇10 mL 定容至刻度,再加10 mg/mL 壳聚糖冰醋酸溶液0.001 mL,过夜,采用0.22 μm 的滤膜滤过,低温保存[20]。
2.3.3 色谱条件 Hypersil ODS2(200 mm×4.6 mm,5 μm)色谱柱,以乙腈(A)-水(B)为流动相,梯度洗脱:0~2 min,5%~10% A;2~10 min,10%~35% A;10~15 min,35%~60% A;15~20 min,60%~80% A;20~25 min,80%~100% A。体积流量0.2 mL/min,柱温30 ℃,检测波长203 nm,进样量10 μL。
2.3.4 方法学考察 根据文献方法[20]测定稳定性、重复性、精密度及加样回收率。样品溶液在4 ℃条件下放置24 h,稳定性试验RSD 为0.70%,精密度试验RSD 为0.42%,重复性试验RSD 为1.4%,平均加样回收率为100.3%,RSD 为0.65%,均符合要求。
2.3.5 样品的测定 取供试品溶液进样,按照“2.3.3”项下色谱条件,“2.3.2”项下制备方法,色谱图见图1,结果见表2。
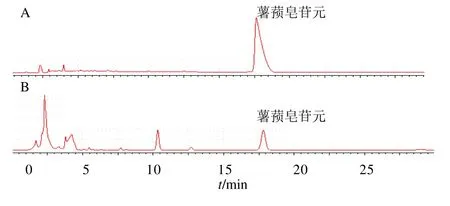
图1 薯蓣皂苷元(A)和黄精药材(B)HPLC 色谱图Fig.1 HPLC chromatogram of iosgenin reference substance(A)and Polygonati Rhizoma (B)
通过以上结果,表明黄精药材符合《中国药典》2020年版规定,含水量在10.427%~11.740%,ST2水分最少,GC3 水分最多;总灰分在1.486%~2.513%,酸不溶灰分在0.181%~0.312%,GC3 总灰分最少,ST2 总灰分和酸不溶灰分最多;浸出物在81.001%~88.955%,YX2 浸出物含量最少,QM3含量最多;无水葡萄糖含量在11.154%~14.659%,NL2 含量最少,QM3 含量最多;总皂苷含量在0.714%~0.898%,YX2 含量最少,QY2 含量最多;薯蓣皂苷元含量在0.008%~0.017%,YX1 含量最少,QY2 含量最多。
2.4 熵权法
2.4.1 数据标准化处理:假设给定了k个指标,n个样本(n=20,k=7),对原始数据进行标准化处理,标准化处理公式:
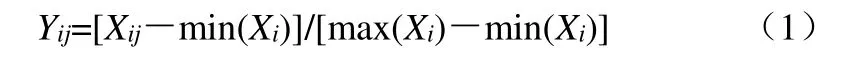
Xij为原始数据,Xi为样品第i个指标的均值。
2.4.2 求各指标的信息熵 根据信息论中信息熵的定义,一组数据的信息熵(Ej):

pij=Yij/∑Yij,若pij=0,则定义lnpij=0。
确定各指标权重各个指标的信息熵后,计算各指标的权重(Wi),计算结果见表3。

表3 熵权法计算所得信息熵及权重Table 3 Information entropy and weight calculated by entropy weight method

Ei为样品第i个指标的信息熵。
2.5 灰色关联度法
2.5.1 原始数据标准化处理 为了更好的实现数据的计算和管理,需对原始数据进行规格化处理[21-22],规格化处理公式:

Xik为原始数据,Xk为样品第k个指标的均值。
2.5.2 关联系数的计算 设其中最优参考序列记为{Ysk},最差参考序列记为{Ytk},相对于最优参考序列和最差参考序列的关联系数分别按公式(5)、(6)计算:

ρ为分辨系数,本实验ρ取值为熵权法“2.4.2”项下计算所得各指标关联系数,计算结果见表4。
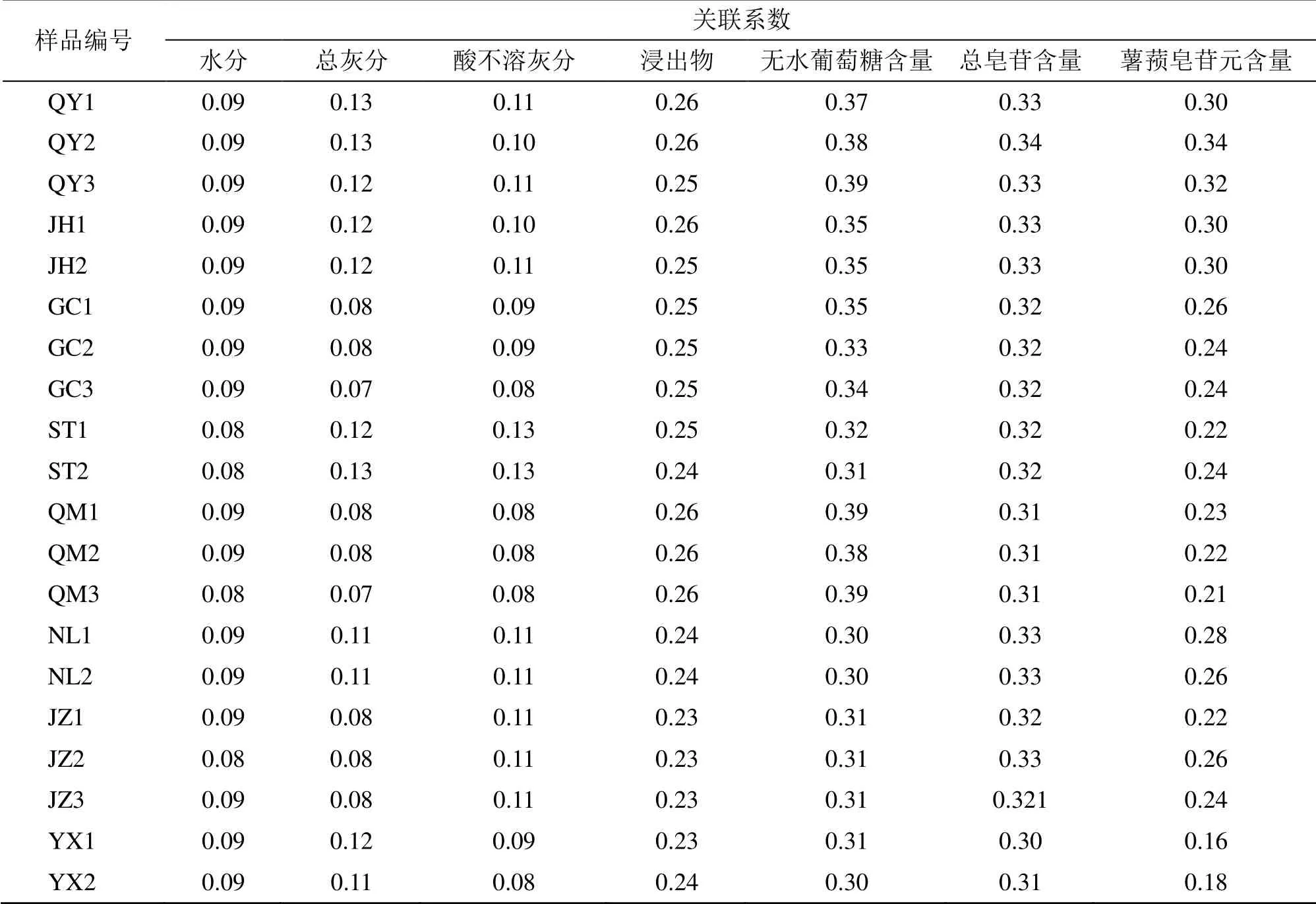
表4 各评价单元相对于最优参考序列的关联系数Table 4 Correlation coefficients of each evaluation unit with respect to optimal reference sequences
2.5.3 关联度的计算:最优参考序列关联度ri(s)和最差参考序列关联度ri(t)分别按公式(7)和公式(8)计算:

2.5.4 相对关联度的计算 相对关联度ri与最优参考序列关联度ri(s)和最差参考序列关联度ri(t)密切相关,计算方法如下:

计算结果见表5,根据相对关联度的大小对评价单元序列进行排序,最终得到优劣评价结果。
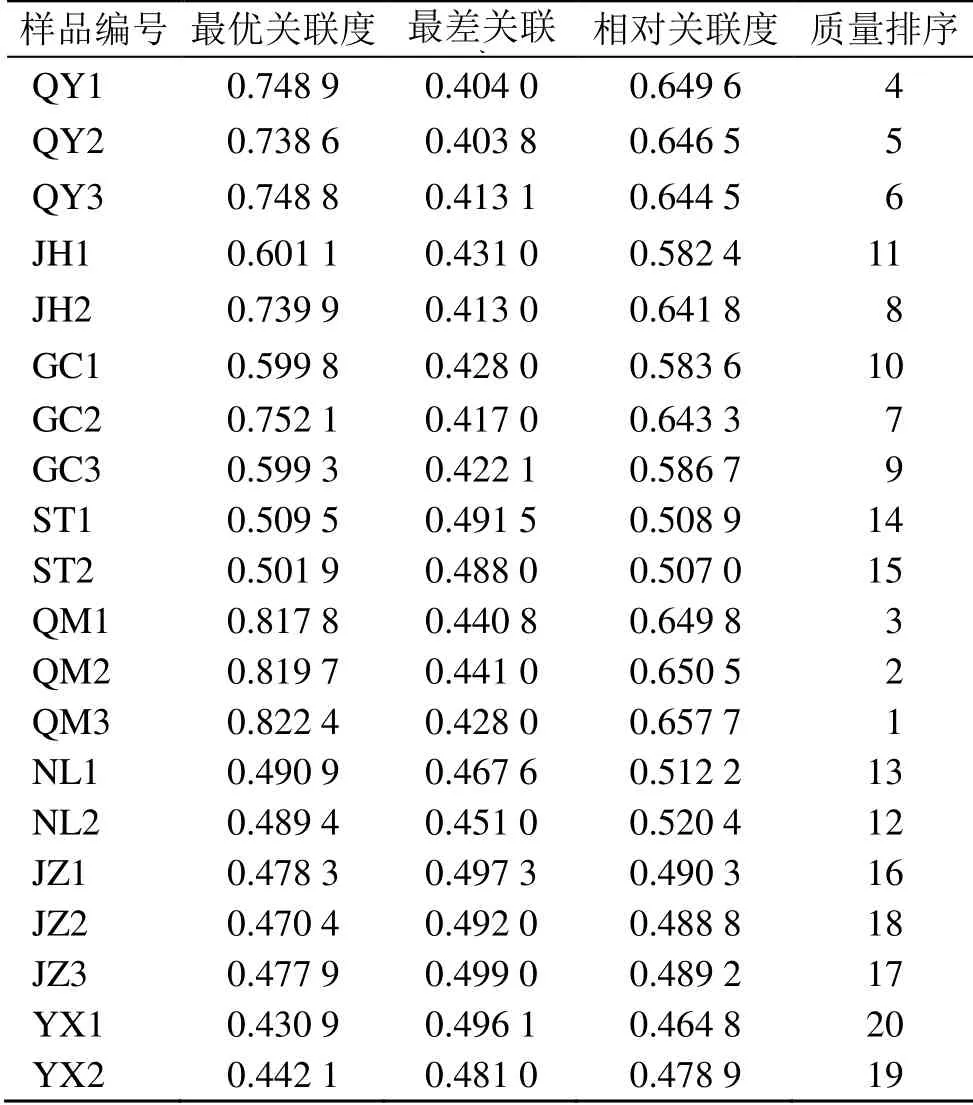
表5 不同产地黄精样品相对关联度及质量排序Table 5 Relative correlation degrees and quality ranking orders of Polygonati Rhizoma from different populations
从质量研究角度分析,浸出物、有效成分含量越高质量越好[23-24]。本研究通过以浸出物、总皂苷、薯蓣皂苷元含量等7 种指标,通过灰色关联模型和熵权模型,对安徽省野生多花黄精进行质量评价,发现黄精药材相对关联度介于0.464 8~0.657 7,说明安徽省内各产地黄精的质量存在一定差异;依据不同产地黄精的相对关联度大小,相对关联度>0.55 的样品有11 批,相同县内不同海拔的黄精药材相对关联度略有差异,总体上祁门县的黄精质量评价度最高,这与吴其国等[25]、钱枫等[26]的研究结果基本一致。此外,祁门县、贵池区、青阳县的样品排名靠前,品质较优,可在以上产地区域建立高品质栽培基地,规范加工方法,能总体提高黄精药材质量。相对关联度<0.55 的样本集中在石台、岳西、金寨、南陵等地,样品的排名相对靠后,品质较差,其中岳西县的黄精质量评价度最低,可能与药材的土壤特性、生长环境和地理位置有关。
3 讨论
黄精属于多基原药材,一般来说,多花黄精以安徽、湖南、贵州所产质量较优[27]。近年来随着人们日益增长的健康需求,黄精产业发展逐步迈入快车道,安徽各地区广泛种植黄精。但由于气候、水肥等生境的不同,导致黄精药材各化学成分含量存在差异[28]。本研究通过综合评价黄精药材质量,发现祁门县、贵池区、青阳县品质较优,说明可在以上产地区域建立黄精规范化种植基地,基于多指标成分构建的熵权和灰色关联度模型评价安徽省不同产地黄精药材质量,方法简单客观,为黄精优质种源的筛选提供了参考依据。
质量是中药产业的生命线,中药质量诸多问题是阻碍中药现代化、国际化的瓶颈之一[29]。中药成分复杂,各成分间通过多维度、多层次非线性协同作用发挥药效[30],因此评价中药质量仅以单一化学成分为指标具有一定局限性,应该进行多指标综合评价。且由于灰色关联度计算中各计算指标ρ 没有一个量化的方法,多数沿用文献中的方法取ρ=0.5(指标数量≥4)[31-32],分析结果不够真实客观,而将各评价指标根据熵权法赋值进行区分后,再用灰色关联度质量评价模型进行分析,可以区分不同指标对整体的影响。本实验围绕中药成分有效性、可测性、特有性的属性,建立中药多成分体系宏观质量表征的灰色关联模型和熵权模型,选择了基础指标水分、灰分,加上浸出物、无水葡萄糖含量、总皂苷等有效成分,共7 个指标,能较客观地反映其内在质量。但由于黄精多糖结构复杂,结构鉴定、次生代谢研究还不够深入,从现有的成分指标难以全面评价,且尚未发现黄精特有成分,因此,未来还需从黄精原植物体内中药化学代谢途径、节点代谢或代谢网络研究,多角度、全方位地研究黄精有效成分,从而实现黄精药材质量评价体系从点到面的转变。
利益冲突所有作者均声明不存在利益冲突
