氢同位素色谱分析研究进展
2021-06-24王伟伟夏立东李海容张伟光周晓松龙兴贵彭述明
王伟伟,夏立东,李海容,张伟光,周晓松,龙兴贵,彭述明
中国工程物理研究院 核物理与化学研究所,四川 绵阳 621900
为了从根本上解决能源和可持续发展问题,可控核聚变是一条重要的途径。最典型的核聚变反应是氘(D)氚(T)反应,聚合后生成氦原子,并释放17.6 MeV的中子:
D+T=He+n+17.6 MeV
氕(1H,H)、氘(2H,D)、氚(3H,T)是天然存在的三种氢同位素。氕是稳定同位素,该原子核由一个质子组成,天然丰度大于99.98%。氘也是稳定同位素,该原子核由一个质子和一个中子组成,天然水中氘丰度约为0.015 6%。氚原子核由一个质子和两个中子组成,是一种不稳定的同位素,根据美国国家标准与技术研究院(National Institute of Standards and Technology, NIST)数据显示,氚的半衰期为(4 500±8) d,即(12.32±0.02) a。
氢的稳定化学形态,以同核分子态(H2、D2、T2)或异核分子态(HD、DT、HT)形式存在。同核分子态中存在两种不同的自旋方式:正态(ortho-)、仲态(para-),不同温度下正-仲态比例不同,如常温下H2的正、仲态比例为3∶1。同核态与异核态之间存在如下交换平衡:



在催化剂的存在下,可以加速实现上述交换反应的平衡[1-2]。氚衰变释放β粒子也可以起到催化的效果[3]。
为了在地球上实现可控核聚变,全球最大的激光核聚变装置,被称为“人造太阳”的美国国家点火装置(NIF)已在2010年完成了首次综合点火实验。由33个国家参与合作建设的国际热核聚变实验堆(ITER)已在法国卡达拉舍开始建造。一旦ITER成功,有望实现聚变能源的商业利用。在2011年,我国提出并启动了中国聚变工程实验堆(CFETR)[4],目前已完成顶层设计[5]。为了实现稳态运行,需要通过增殖氚来平衡各种氚消耗,实现氚自持是CFETR的一个重大科学目标[6]。
氚增殖包层用于氚增殖、回收、纯化与再循环[5]等,是未来聚变电站核心技术之一。ITER氚增殖实验包层(ITER-TBM)系统完成包层模块中氚的实时提取和氦冷却气的除氚/净化任务,氚分析系统不仅要实时测定TBM模块的产氚速率,而且要对提取、净化系统中氚和杂质气体的成分准确监测,以确定氚提取或净化效率[7-8]。这其中需突破氢同位素(H、D、T)的在线、快速分析技术。
1 氢同位素色谱分析
用于测定气体组成的分析方法有多种,如质谱法、激光拉曼法、气相色谱法等。气相色谱法是其中最可靠的一种方式[1,9-10]。该方法依靠了氢同位素与材料吸附-扩散协同作用实现了氢同位素的分离。
1.1 氢吸附作用
一般地,固体表面吸附量与气体压力密切相关,压力越大,吸附量越多。固相吸附量Ws与气相含量Wg的比例,可以定义为保留因子k:
k=Ws/Wg
(1)
相同体积、压力条件下,Wg保持不变,吸附能力越强,Ws越大,k越大。Chu等[11]认为,固体材料表面的化学组分对物理吸附几乎没有影响,而与多孔材料的比表面积、孔径分布密切相关。氢同位素吸附量与比表面积成线性关系,微孔吸附斜率明显大于介孔吸附斜率,这与微孔内吸附势强化有关[12-13]。
1.2 氢同位素效应
在热力学平衡状态下,一般用分离因子来描述氢同位素在两相(气、固相)分布中存在的同位素效应:
α12=k2/k1
(2)
式中:α12表示两种氢同位素组分1、2间的分离因子;k1、k2分别指的是组分1、2的保留因子。在77 K下多孔材料物理吸附氢同位素,存在微弱的正同位素效应。在H2-D2体系中,α12=1.1~1.2[11,14],即氘吸附量略多于氕吸附量。
1.3 吸附-扩散协同作用
色谱分离过程是一个吸附、扩散协同过程,一般用分离度(resolution,Rs)来衡量。Rs12可用以下关系式表示[15]:
(3)
式中,N1为组分1的理论塔板数,与色谱柱长以及柱效有关。柱效通过理论塔板高度(height equivalent to one theoretical plate,H)来描述:
H=L/N
(4)


(5)
2 色谱柱用多孔材料
气相色谱法利用经过改性的多孔材料在低温下实现氢同位素的分离[17-18]。因此,为了提升色谱分析性能,有必要了解氢同位素与多孔材料、氢同位素与改性物、改性物与多孔材料之间的作用关系,以及三者的协同作用。
2.1 多孔材料的种类
目前研究较多的多孔材料有炭材料、金属氧化物、分子筛、有序介孔材料、金属有机框架材料等。炭材料可细分为富勒烯[19]、炭纳米管[20-21]、碳分子筛[22-23]、碳气凝胶[21]、有序介孔碳[24-26]等材料。金属氧化物研究较多的是硅胶[27-28]、氧化铝[29-30]。有序介孔材料(ordered mesopore materials, OMMs)主要包括M41S家族[31-35]和SBA家族[36-41]。金属有机框架材料可以分为几类:ZIFs[42]、COFs[43]、MOPs[44]等。
按照孔径大小,多孔材料可以分为微孔材料(小于2 nm)、介孔材料(2~50 nm)以及大孔材料(大于50 nm)。微孔又可细分为超细微孔(ultramicropores,小于1 nm)、大微孔(supermicropores,1~2 nm)。孔径大小不同,表现出特征氮吸附等温线。
活性氧化铝最早于1958年被发现可以分离氢同位素同核分子自旋异构体[45]。这种活性氧化铝经过氧化铁[46-49]或氯化锰[1,17,50-53]改性后,正-仲态发生合并,形成单一的色谱峰。然而,以微孔为主的沸石分子筛并未能很好地分离氢同位素[54]。
2.2 多孔材料的改性
沸石分子筛(zeolite)由硅铝框架(AlO2)x-(SiO2)y构成,由于该框架带有负电荷,需要有金属阳离子对其进行改性实现电荷平衡。阳离子的种类变化会引起分子筛的孔径发生变化。当Na+改性A型分子筛时,孔径由0.42 nm缩小至0.38 nm;K+半径更大,改性后孔径小于0.3 nm。当Ca2+或Mg2+等二价离子改性分子筛时,由于离子数量减少,分子筛孔径及孔容均有所提高。
为了提高多孔材料的催化活性,可以通过镶嵌其它金属氧化物来改变介孔硅表面的酸性。Zukal等[55]利用不同含量氧化铝对SBA-15材料进行改性。利用引入阳离子的方法来补偿SBA-16涂敷氧化铝的酸性表面[56]。通过共沉淀的方式将不同TiO2引入SBA-16中[57]。除了金属氧化物改性以外,OMMs还可以作为纳米金属粒子(活性位点)的载体材料。相比微孔分子筛,气体分子能更容易接近这些活性位点。将纳米银粒子负载到介孔氧化硅上,增强了对CO2的吸附作用[58]。SBA-16表面经过三乙基二胺(TEDA)改性后[59],可以增加CO2的吸附量。
基于Kelvin宏观分析模型BJH(Barrette-Joynene-Halenda)分析表明,MnCl2改性前后活性氧化铝中微、介孔同时存在[17,50]。密度泛函理论(density function theory, DFT)模型也验证了这一结果[60],MnCl2改性前多孔氧化铝既含有少量小于1 nm(0.7 nm)的超细微孔,又含有少量小于2 nm大于1 nm的大微孔(1.5 nm),改性后超细微孔消失,大微孔略有减少,介孔孔容随着改性负载量的增加逐渐减少。相比BJH模型,DFT模型在描述微、介孔共存时的孔径分布准确性更好[61]。
2.3 氢同位素与改性物的相互作用
2.3.1阴离子 Matta等[62]研究了H-与H2的相互作用,可形成H-(H2)n(n=1~6)复合物,阴离子H-处于中心位置,与周围呈对称分布的中性分子产生弱吸附作用。类似地,当卤素阴离子与氢分子作用[63]时,也会出现多个氢分子的对称分布现象,Cl-与F-最多可以吸附6个氢分子,Br-最多可以吸附7个氢分子。


图1 阳离子复合物M+-H2以及阴离子复合物A--H2的平衡结构
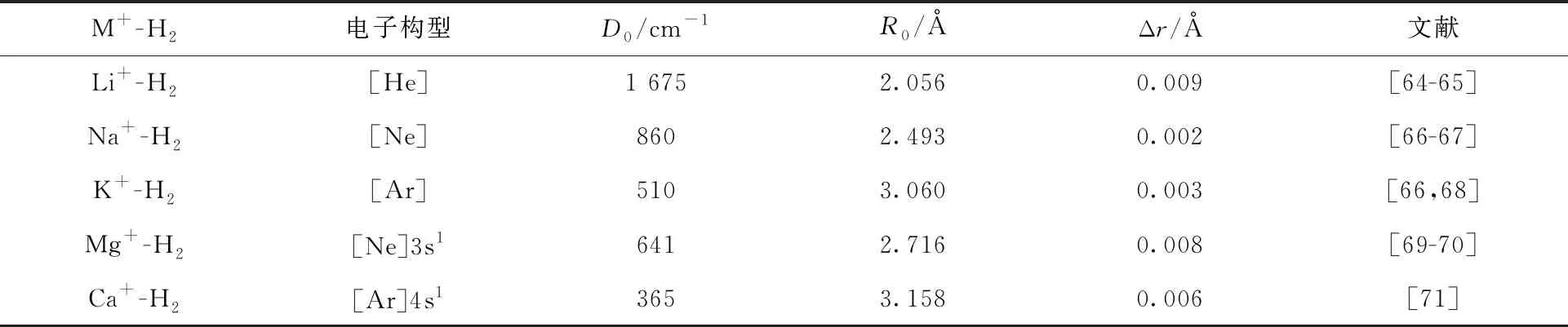
表1 M+-H2复合物的物性参数(M包括碱金属、碱土金属)
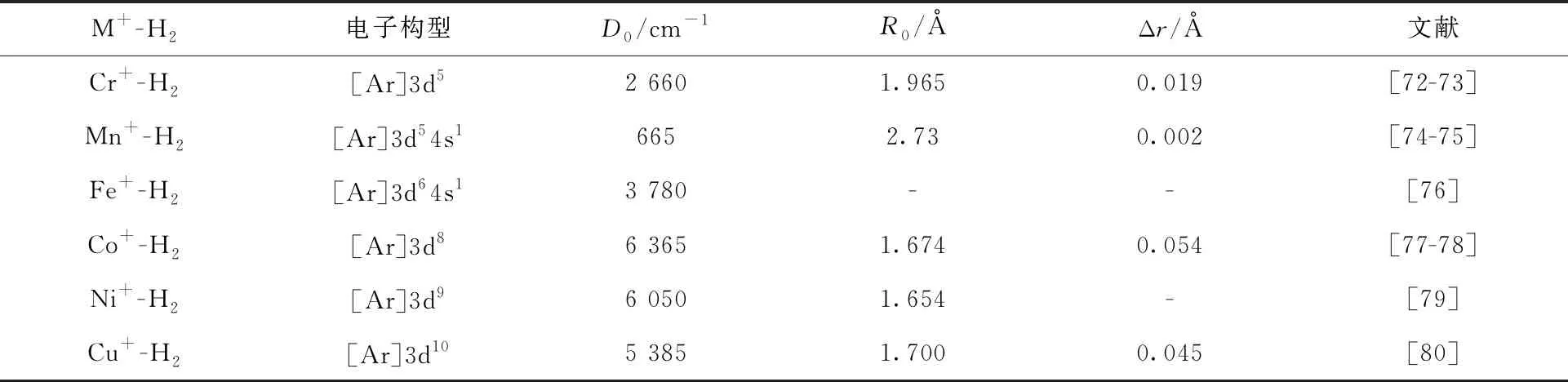
表2 M+-H2复合物的物性参数(M包括过渡金属)
2.3.3阴、阳离子共同作用(化合态) M+…H2复合物不稳定,通常情况下H2与多孔固体中金属阳离子发生作用。低温(77 K)下氢分子与不同分子筛发生吸附作用后,H-H振动频率会发生不同变化[81-88]。频率位移ΔνHH与吸附焓ΔH⊖,并没有与M+-H2复合物那样符合简单的对应关系。如Li+偏离了这一关系,因为Li+与分子筛骨架内O原子配位紧密,导致氢分子与O的距离过近,削弱了H2分子的吸附稳定性。其次,Na-ZSM-5(ΔνHH=-63 cm-1)的ΔH⊖高达-11 kJ/mol,其原因是Na+在两个10元环通道连接处的低配位造成的。可以看出,同种金属阳离子受到不同负电荷环境的影响,与H2的吸附能略有不同。随着M+…H2吸附作用的增强,H—H键被逐渐削弱,最终发生断键现象,形成金属氢化物。中间还有若干个过渡形态[89],如图2所示。初始H—H键长为0.74 Å, M+…H2复合物形成时键长为0.8~0.9 Å,加长M+…H2复合物的键长为1.0~1.2 Å,当键长大于1.6 Å时,H—H键已经发生断裂。
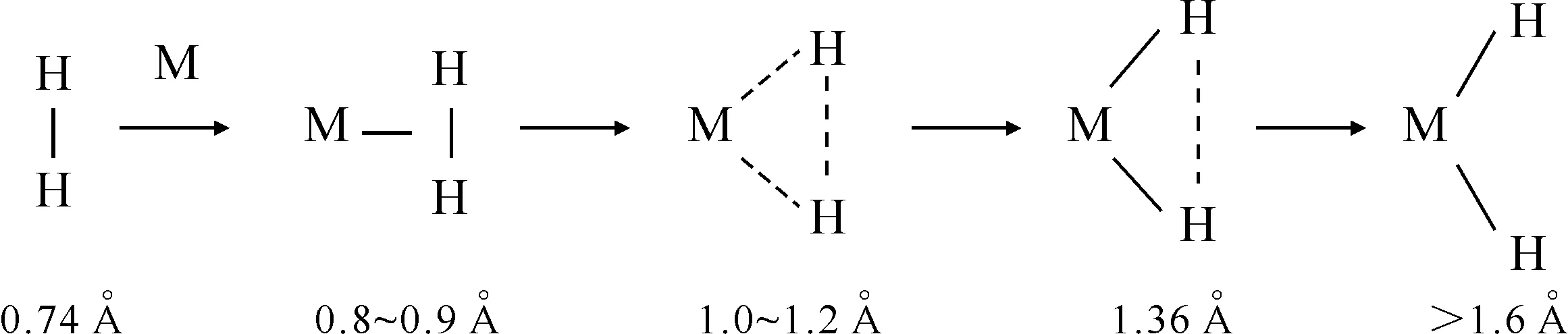
图2 M+…H2吸附作用的几种形态
2.4 氢同位素与改性多孔材料的相互作用
2.4.1负载量 MnCl2改性前、后活性氧化铝与氢同位素相互作用,分离性能发生明显改变(图3)[60]。如图3所示,负载前活性氧化铝(Mn00)保留时间较长,分离度较差。MnCl2改性后(Mn01),H2-HD分离度达到了1.5,保留时间缩短至10 min以内。结合孔径分布分析,MnCl2负载后,多孔氧化铝中超细微孔消失,氢同位素分离度有了显著提高,说明超细微孔对氢同位素的吸附作用过强,导致了氢同位素色谱峰拖尾。随着负载量的增加(Mn02、Mn03),多孔氧化铝的孔容逐渐变小,色谱峰保留时间逐渐变小,分离度先增加后减少。
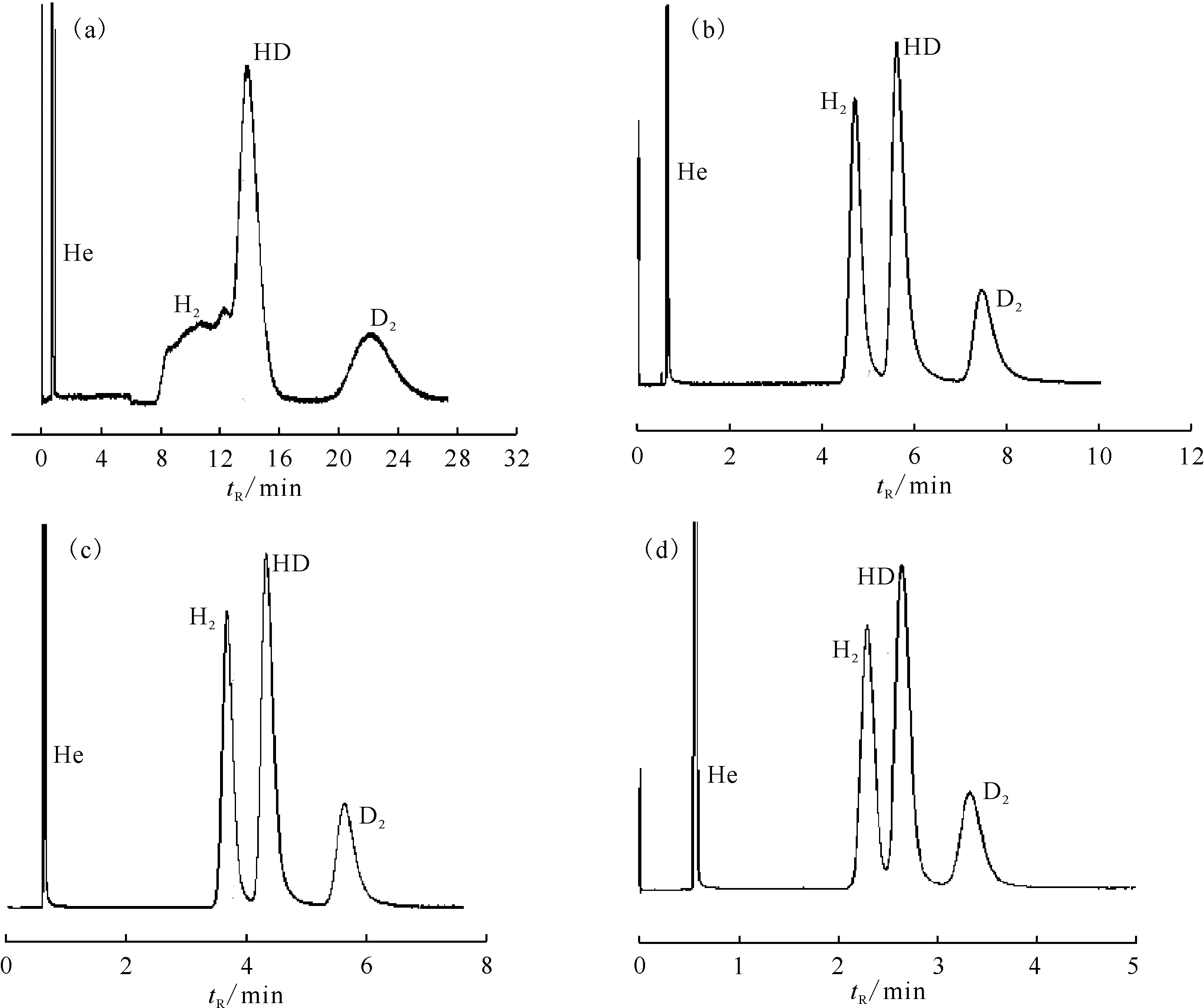
柱尺寸3 m×φ1.2 mm(内径),10 mL/min,78 K(液氮),50 μL(50 kPa)
2.4.2阳离子 除了MnCl2改性外,其它阳离子氯化物改性后,活性氧化铝的氢同位素分离效果有所不同[90]。图4为不同金属阳离子氯化物负载后多孔氧化铝的DFT孔径分布。如图4所示,除了氯化铁修饰多孔氧化铝 (Fe@A)以外,其它样品的孔径分布基本一致,表现在分离效果上,Fe@A的氦组分保留时间大于其它样品的氦保留时间,这与氧化铝被水解产生的盐酸所腐蚀有关,颗粒间填充更加紧实,气阻变大,He在柱内流动性变差。氯化镍修饰多孔氧化铝 (Ni@A)的保留因子最大,但比表面积并不是最大的,这说明阳离子与氢分子的吸附在其中起到了关键作用,即Ni(Ⅱ)通过Kubas作用[89]增强了氢分子的键长,引起了分子直径变大,减少了与孔壁的距离,进而增强了吸附作用。通常情况下,H—H的σ成键电子云会进入到Ni(Ⅱ)的d电子空轨道。不同之处,Ni(Ⅱ)d电子对电子云又反馈给了H—H的反键空轨道σ*内,引起H—H键长的增加。氯化钠修饰多孔氧化铝 (Na@A)、氯化钾修饰多孔氧化铝 (K@A)出现了明显的氢同位素同核分子(H2、D2)正-仲态分离现象,这与NaCl、KCl本身不具有磁性有关。

■——Un@A(未修饰多孔氧化铝),○——Mn@A(氯化锰修饰多孔氧化铝),△——Fe@A(氯化铁修饰多孔氧化铝),▽——Co@A(氯化钴修饰多孔氧化铝),◆——Ni@A(氯化镍修饰多孔氧化铝),(氯化铜修饰多孔氧化铝),☆——K@A(氯化钾修饰多孔氧化铝),——Na@A(氯化钠修饰多孔氧化铝)V为单位质量的孔体积,w为孔径


■——Un@A,○——MnS@A(硫酸锰修饰多孔氧化铝),△——FeS@A(硫酸铁修饰多孔氧化铝),▼——CoS@A(硫酸钴修饰多孔氧化铝),◆——NiS@A(硫酸镍修饰多孔氧化铝),(硫酸铜修饰多孔氧化铝),☆——KS@A(硫酸钾修饰多孔氧化铝),——NaS@A(硫酸钠修饰多孔氧化铝)
3 氢同位素色谱分析柱研究进展
多孔材料的孔径分布、改性物性质对分离效果产生显著影响。除此之外,改性多孔材料的颗粒大小、填装工艺也会影响分离效果。涡流扩散因子A满足以下关系式:
A=2λdp
(6)
式中:λ为填充因子,即紧实程度;dp指的是填充颗粒的直径大小。为了降低理论塔板高度H,有必要降低λ及dp。降低λ的途径是提高填充的紧实程度;减少dp的途径是缩小粒径。涡流扩散情况只出现在填充柱内,毛细管柱(如PLOT柱,porous layer open tubular)不存在该现象,即A=0,这是PLOT柱高柱效的一个重要原因。
此外传质因子C与柱径有关,减少柱径可降低传质因子C,进而降低理论塔板高度H。一定范围内,增加柱长可显著提升分离性能。
3.1 填充柱
表3中列出了多种色谱填充柱的填充参数[1,17,45-50,60,90-98]。由表3可以看出,文献中色谱柱装填颗粒大小差别较大(粒径0.075~0.5 mm),建议粒径为0.075~0.1 mm[99]。随着填充工艺的改进,柱径由最初0.8 cm逐步缩小到0.16 cm。填充柱柱长一般在0.5~3 m之间。5 m填充柱(内径0.1 cm)在10 min内可实现含氚氢同位素六组分的基线分离(分离度大于1.5),如图6所示。

表3 固定相种类及柱尺寸参数

5 m填充柱,内径0.1 cm
3.2 PLOT柱
为了提高分析速度并提高柱效,日本Kawamura等[10]首次完成了氯化锰改性氧化铝石英PLOT柱的H-D混合气的分离性能测试,分离时间为1 min,H2-HD的分离度为1.12。由于该柱为石英管材质容易折断,不适合于含氚放射性实验操作,后续未见含氚气体的测试报道。受此启发,国内进行了金属PLOT柱(MnCl2改性氧化铝,20 m长,内径0.53 mm)的研制,并开展了含氚气体的分析测试,测试结果示于图7[90]。

柱长20 m,内径0.53 mm
如图7所示,氢同位素六组分的总测试时间为3.5 min,与填充柱相比,分析时间缩短至1/10[100-108],检测下限为20×10-6~50×10-6(体积分数),比填充柱检测下限(200×10-6~500×10-6)低了一个量级[106]。
由于PLOT柱的柱效较高,适合于氢同位素正-仲态比例的测定。利用15 m硫酸钠改性氧化铝PLOT柱可在1 min内实现H2的正-仲态基线分离[109]。60 m硫酸钠改性氧化铝PLOT柱可以实现正态H2(o-H2)和HD的基线分离,o-H2和HD分离度达到了2.0[109]。
4 研究展望
4.1 多孔材料的孔径分布
如图4、5所示,多孔氧化铝以介孔结构为主,说明液氮温度下,氢同位素与多孔材料相互作用的主要孔径范围为2~50 nm。为了验证该论断,有必要选择纯介孔材料进行分离测试。对OMMs的进一步深入研究,将有助于进一步提升多孔材料的氢同位素分离性能,加深孔径分布对分离性能的理解。
4.2 固相表面的吸附能测试
目前研究局限于77 K下氧化铝中氢同位素的分离效果,其它温度下的氢同位素效应,由于实验条件(液氮)的原因未能开展。今后可开展基于低温氦制冷机的测试设备研制,获得稳定一致的低温温度场,通过制冷机对氦气降温,获得稳定、可控的样品测试温度。
4.3 氢同位素的常温分离
要实现氢同位素色谱分离,目前需要低温环境(如液氮),限制了气相色谱法的应用推广。由于存在d电子反馈作用,实现了常温下对氢分子的吸附,这将为常温分离氢同位素提供一条新思路。MOFs是金属阳离子与阴离子载体的另一种组合方式。过渡金属有机化合物已经实现了氢在常温下以分子状态吸附。如果以MOFs多孔骨架为基底或分散相,稳定结合并均匀分布Ni、Cu等过渡金属,同时利用骨架阴离子调控过渡金属离子的Kubas作用强度,有望实现氢同位素分子在常温下的分离。
4.4 色谱仪在线功能的增强
氢同位素色谱分析方法,目前主要作为一种静态定量分析手段,而对动态、在线的分析应用,存在一些局限性。PLOT柱分析时间短,替代填充柱后将大大提升气相色谱法在线测试能力,但目前PLOT柱制备成功率较低,且使用寿命较短,需要进一步优化制备工艺。ITER的ANS系统中将色谱仪整机放在手套箱内,离取样点较远,且不支持在线分析。在线色谱仪研制需要进一步的深入。
