2D TiO2/Ag3PO4异质结复合催化剂的制备及其光催化性能研究
2021-06-23陈庆涛石向东张文杰梁娓娓杨茂森姜利英陈凤华
陈庆涛 石向东 张文杰 梁娓娓 杨茂森 姜利英 陈凤华*
(郑州轻工业大学 1. 材料与化学工程学院; 2. 电气信息工程学院, 郑州 450002)
引 言
近年来,随着工业化进程的加快,由工业废水中芳香有机化合物所导致的环境污染问题越来越受到人们的重视[1]。半导体光催化降解技术可以直接利用太阳能,在室温下通过氧化还原反应将水中的有机污染物分解成二氧化碳和水,具有清洁、高效、彻底和无二次污染的优点,成为当前治理有机污染物的有效途径[2-3]。
在众多光催化剂中,经典的半导体TiO2因具有光催化活性高、化学稳定性好、价格低廉以及环境友好的特点而受到广泛关注。但是TiO2的禁带宽度大,对太阳光中的可见光利用率较低,光生电子- 空穴复合率高,限制了其在环境领域中的应用[4-5]。研究表明,利用贵金属元素(Au、Ag等)[6-7]、稀土元素[8-9]或非金属元素(以C、N、P等为代表)[10-12]对TiO2进行掺杂,或者将具有代表性的Bi基[13-14]、Ag基[15-17]等可见光型的光催化剂与TiO2进行复合形成异质结,均可以不同程度地提高TiO2的光催化效率,拓宽其可见光吸收范围。除了调控光催化剂的结构外,形貌的可控合成也是提高TiO2光生电子和空穴分离效率、改善吸附性能、提高光催化活性的行之有效的方法[18-19]。二维金属氧化物因其独特的层状结构,具有高比表面积、大比例的暴露活性位点以及特有的光电性能等优势[20-21],引起了人们的广泛关注。但是当前对TiO2的研究以零维、一维和三维居多,而二维TiO2(2D TiO2)的研究相对较少。
本文利用溶剂热法制备了2D TiO2纳米片,以硝酸银为银源、磷酸氢二钠为磷酸源,在所获得的2D TiO2表面沉积Ag3PO4纳米颗粒,制备了2D TiO2/Ag3PO4复合光催化材料,并以罗丹明B(RhB)为污染物模型,研究其在氙灯模拟日光灯下的光催化降解活性,考察2D TiO2与Ag3PO4的物质的量比以及H2O2的加入对催化性能的影响,以期获得高催化活性的TiO2基可见光催化剂。
1 实验部分
1.1 实验原料
聚环氧乙烷- 聚环氧丙烷- 聚环氧乙烷三嵌段共聚物(P123)(相对分子质量为5 800)、钛酸四丁酯(Ti(C4H9O)4)(纯度99%)、硝酸银(AgNO3)(分析纯),Sigma- Aldrich公司;乙二醇、磷酸氢二钠(Na2HPO4)、无水乙醇、浓盐酸、异丙醇、30%(质量分数)H2O2,分析纯,国药集团化学试剂有限公司;硫酸钠(Na2SO4)、铁氰化钾(K3[Fe(CN)6])、亚铁氰化钾(K4[Fe(CN)6]·3H2O)、EDTA- 2Na,化学纯,天津市风船化学试剂科技有限公司;氯化钾(KCl),化学纯,天津市科密欧化学试剂有限公司;罗丹明B、对苯醌,化学纯,麦克林公司。
1.2 催化剂的制备
2D TiO2纳米片 采用溶剂热法制备2D TiO2纳米片。将1.26 g Ti(C4H9O)4与0.74 g浓盐酸混合搅拌均匀,加入到含有0.2 g P123的3 mL乙醇中,磁力搅拌30 min,然后取2.5 mL该混合溶液加入到装有20 mL乙二醇的50 mL高压反应釜内,于150 ℃反应20 h。反应结束后,冷却至室温,离心分离,得到白色2D TiO2纳米片,依次用乙醇和水清洗3次后于80 ℃下烘干待用。
2D TiO2/Ag3PO4复合光催化剂 取50 mg制备的2D TiO2纳米片粉末,超声分散于10 mL去离子水中,与10 mL AgNO3溶液(3.4 mg/mL)混合并避光搅拌12 h后,逐滴滴加10 mL Na2HPO4溶液(2.39 mg/mL),滴加完毕后,继续避光搅拌反应5 h。反应结束后,离心分离产物,依次用乙醇和水清洗3次,冷冻干燥,得到2D TiO2/Ag3PO4。改变AgNO3和Na2HPO4的浓度,可以得到2D TiO2和Ag3PO4的物质的量比分别为10∶1、10∶3和10∶5的2D TiO2/Ag3PO4复合光催化剂,分别标记为2D TiO2/Ag3PO4(10∶1)、2D TiO2/Ag3PO4(10∶3)和2D TiO2/Ag3PO4(10∶5)。若没有2D TiO2纳米片粉末的存在,则得到Ag3PO4纳米颗粒。
1.3 催化剂的表征
采用日本JEOL公司的JEM- 2100型透射电子显微镜(TEM)和JSM- 6490LV型扫描电子显微镜(SEM)观察样品的微观形貌。采用日本RIGAKU公司的D/max 2500型X射线衍射仪(XRD)测试样品的晶型结构,测试电压为40 kV,电流为20 mA,扫描速率为2(°)/min,采用Cu靶Kα1辐射线(λ=0.154 05 nm)。采用美国Thermo公司的ESCALAB 250Xi 型X射线光电子能谱仪(XPS)进行元素组成分析,单色Al Kα (1 486.6 eV),功率150 W,500 μm束斑,以C 1s的结合能284.8 eV校准。采用日本Hitachi公司的U- 3900H型紫外可见光谱仪和F- 4600型荧光光谱仪进行紫外- 可见光谱(UV- Vis)和荧光光谱测试。采用日本麦奇克拜尔有限公司的BELSORP- Mini II型比表面积和孔隙度分析仪测试比表面积和孔体积。以上仪器表征的复合光催化剂均是2D TiO2/Ag3PO4(10∶5)。
1.4 光催化性能测试
取20 mg光催化剂加入20 mL RhB溶液(20 mg/L)中,在暗处磁力搅拌30 min 使体系达到吸附平衡,然后置于300 W氙灯下进行光降解反应,光源距离液面约15 cm,每隔一定时间取样,通过紫外可见光谱仪(Thermo Evolution 201型,美国Thermo公司)在554 nm处测定RhB浓度,从而获得光催化降解的进程。按照下式计算RhB的降解去除率D。
式中,C0为初始的RhB浓度,Ct为t时刻的RhB浓度。
1.5 电化学性能测试
使用传统的三电极电池系统和CHI 660D电化学工作站(上海辰华仪器有限公司)进行电化学性能测试。2D TiO2、2D TiO2/Ag3PO4和Ag3PO4依次为工作电极,同时,铂电极和饱和Ag/AgCl电极作为对电极和参比电极。工作中从高压氙气短弧灯(Phillips公司的300 W氙灯)照射工作电极。相对于饱和甘汞电极(SCE),在0.1 moL/L的Na2SO4电解质中测量光电流。电化学阻抗谱(EIS)在0.1 mol/L KCl、5 mmol/L铁氰化钾和5 mmol/L亚铁氰化钾组成的电解质溶液中测定,所用的频率范围为1 Hz~100 kHz。
2 结果与讨论
2.1 催化剂的表征结果
2.1.1微观形貌
图1为所制备的2D TiO2纳米片、2D TiO2/Ag3PO4复合光催化剂和纯Ag3PO4颗粒的SEM图。从图中可以看出,所制备的2D TiO2呈现明显的片状二维结构(图1(a)和1(b)),在2D TiO2/Ag3PO4复合材料中Ag3PO4纳米颗粒均匀分散在二维TiO2片层的表面(图1(c)和1(d)),与纯Ag3PO4颗粒(图1(e))相比,复合材料中Ag3PO4纳米颗粒的尺寸相对比较均匀,粒径为100 nm左右,可以推断二维片层结构的TiO2在一定程度上阻碍了Ag3PO4颗粒的晶体生长和团聚,这与文献[22]报道的结果相一致。

图1 所制备的2D TiO2纳米片、2D TiO2/Ag3PO4复合光催化剂和纯Ag3PO4颗粒的SEM图Fig.1 SEM images of the prepared 2D TiO2 nanosheets, 2D TiO2/Ag3PO4 catalyst and bare Ag3PO4 particles
图2为所制备的2D TiO2纳米片的TEM图以及2D TiO2/Ag3PO4复合光催化剂的TEM和高分辨TEM(HRTEM)图。由图2(a)可以看出TiO2呈现较大的片层结构,有明显的褶皱。由图2(b)可以很明显地看到Ag3PO4与2D TiO2纳米片结合后,大量的Ag3PO4纳米颗粒分布在TiO2表面,平均颗粒尺寸约为100 nm,与相应的SEM结果相吻合。从图2(c)可以看出,Ag3PO4和2D TiO2的晶格条纹间距分别为0.269 nm和0.481 nm,分别与Ag3PO4和TiO2的(210)和(001)晶面相对应,并且可以清晰地看到接触紧密的2D TiO2/Ag3PO4异质结界面的存在。

图2 所制备的2D TiO2纳米片的TEM图以及2D TiO2/Ag3PO4复合光催化剂的TEM和HRTEM图Fig.2 TEM images of the prepared 2D TiO2 nanosheets, TEM and HRTEM images of 2D TiO2/Ag3PO4 catalyst
2.1.2晶型结构
2D TiO2纳米片和2D TiO2/Ag3PO4复合光催化剂的XRD图谱如图3所示。图3(a)中,24.8°和48.3°处出现的衍射峰分别对应于锐钛矿TiO2(JCPDS:73- 1764)的(101)和(200)晶面。此外,图3(a)中还出现了金红石TiO2位于27.5°处(110)晶面的衍射峰,说明所制备的2D TiO2纳米片是由金红石相和锐钛矿相组成的混晶相,这种结构可以很好地抑制光生电子空穴对的复合,使TiO2的光催化效率增加,光催化效率高于单晶相[23]。但是由于所制备的TiO2为片层较薄的二维结构,其XRD图谱中衍射峰强度整体较弱,样品的结晶度不高,所以当2D TiO2与Ag3PO4纳米颗粒复合后,图3(b)中只出现了Ag3PO4位于20.8°、29.6°、33.2°、36.5°、42.5°、47.8°、52.7°、55.0°和57.3°的衍射峰,分别对应于(110)、(200)、(210)、(211)、(220)、(310)、(222)、(320)和(321)晶面(JCPDS:06- 0505),而TiO2的衍射峰被覆盖。
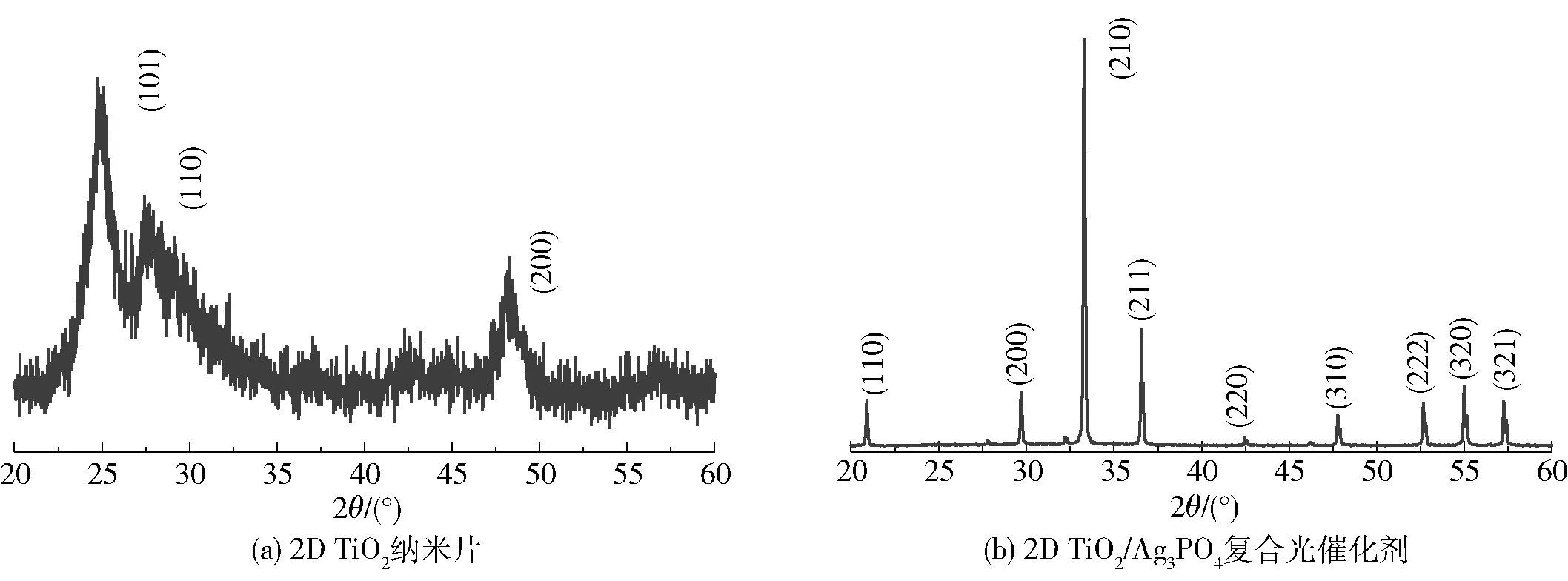
图3 所制备的2D TiO2纳米片和2D TiO2/Ag3PO4复合光催化剂的XRD图谱Fig.3 XRD patterns of the prepared 2D TiO2 nanosheets and 2D TiO2/Ag3PO4 catalyst
2.1.3元素组成分析
图4是所制备的2D TiO2/Ag3PO4复合光催化剂的XPS图谱。从图4(a)中可以看出,所制备的2D TiO2/Ag3PO4复合材料的表面元素主要为P、C、Ag、Ti和O这5种元素。从图4(b)中可以看出,Ti 2p的XPS高分辨图谱含有3个结合能(EB)分别位于457.6 eV(Ti 2p3/2)、458.5 eV(Ti 2p3/2)和463.4 eV(Ti 2p1/2)的特征峰,前2个分别属于锐钛矿相和金红石相化学环境下的Ti 2p3/2峰[24-25],这与XRD结果相吻合。从图4(c)中可以看出,373.2 eV (Ag 3d3/2)和367.6 eV(Ag 3d5/2)的峰是Ag3PO4中的Ag+特征峰,而位于372.8 eV(Ag 3d3/2)和366.8 eV(Ag 3d5/2)的峰是Ag0特征峰, 说明在Ag3PO4的生成过程中部分被光还原分解为Ag纳米颗粒[26]。根据图4(d)所示的O 1s高分辨图谱可知复合材料中O的化学环境有3种,电子结合能分别位于529.4、530.3、530.9 eV,分别对应于Ti—O、Ti—O—Ag和P—O的特征峰[27]。Ti—O—Ag化学键的存在表明2D TiO2和Ag3PO4之间存在强的化学键作用,有异质结的存在。为了进一步证明这一点,我们利用XPS表征了2D TiO2和Ag3PO4复合前后Ti和Ag的电子状态,结果如图5所示。从图5中可以看出,未复合前,Ti元素的2p1/2和2p3/2的结合能分别处于约463.3 eV和457.6 eV,Ag元素的3d3/2和3d5/2的结合能分别处于约374.5 eV 和368.5 eV,两种材料复合之后,Ti元素的2p1/2和2p3/2的结合能均增加了1.1 eV,Ag元素的3d3/2和3d5/2结合能均降低了0.6 eV,结合能的偏移说明Ti和Ag之间有电子传递,也证明了异质结的形成,从而有利于电子- 空穴的分离和电子转移,提高光催化活性。
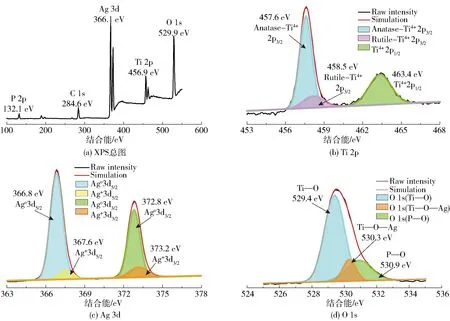
图4 所制备的2D TiO2/Ag3PO4复合光催化剂的XPS总图以及Ti 2p、Ag 3d、O 1s的XPS高分辨图谱Fig.4 XPS spectrum of 2D TiO2/Ag3PO4 catalyst, and high resolution XPS spectra of Ti 2p, Ag 3d and O 1s
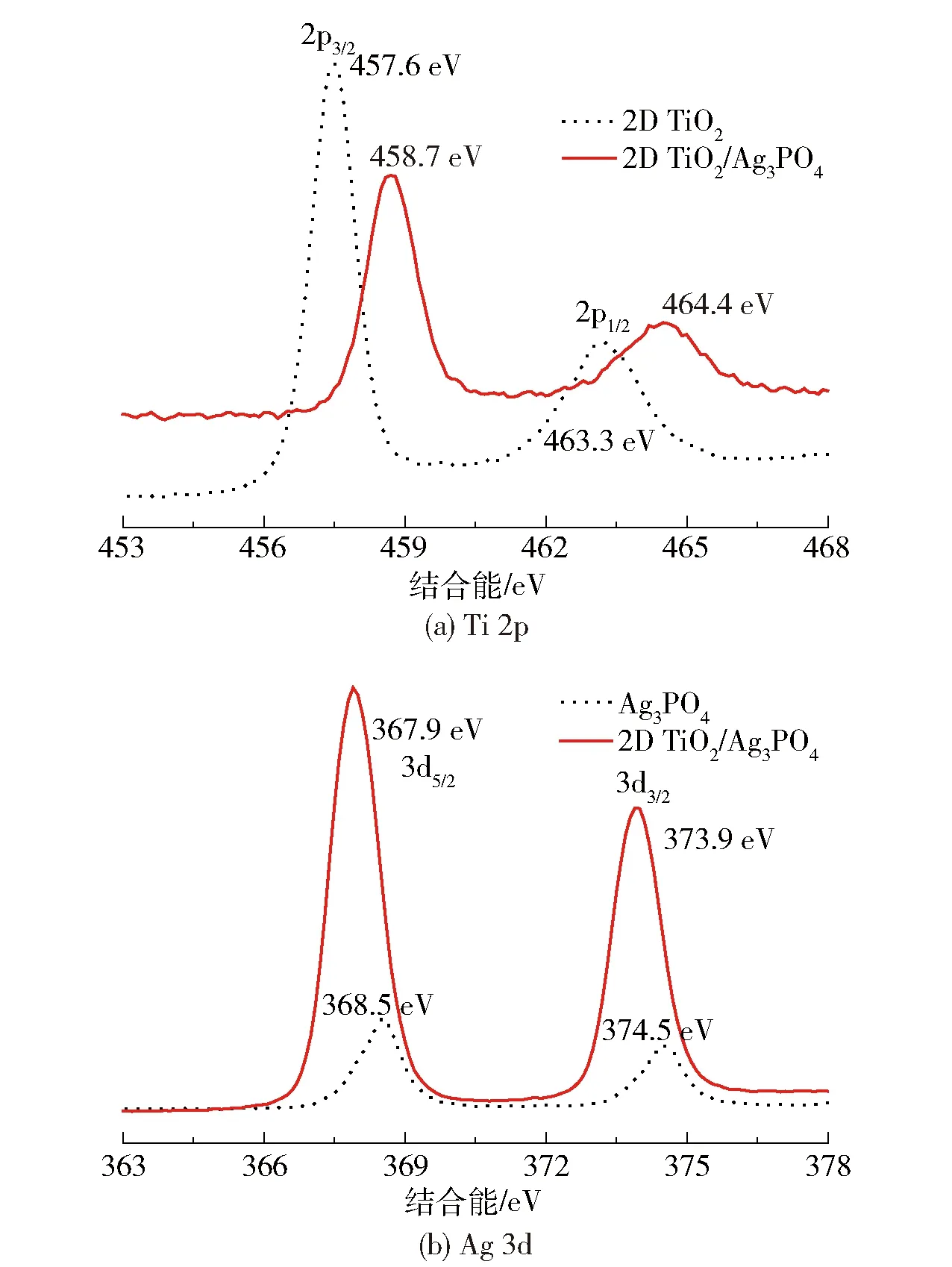
图5 2D TiO2和Ag3PO4复合前后Ti 2p和Ag 3d的XPS高分辨能谱Fig.5 High resolution XPS spectra of Ti 2p and Ag 3d before and after combining of 2D TiO2 and Ag3PO4
2.1.4紫外-可见光谱
图6为2D TiO2、纯Ag3PO4和2D TiO2/Ag3PO4光催化剂的固体紫外- 可见光吸收光谱。从图中可以看出2D TiO2在紫外区域有良好的吸收强度,而纯Ag3PO4与2D TiO2/Ag3PO4光催化剂在波长小于530 nm的范围内均有较强的紫外- 可见光吸收,与纯Ag3PO4相比,2D TiO2/Ag3PO4在紫外- 可见光区域的吸收强度更强,从而更加有利于复合材料对污染物进行光催化降解。
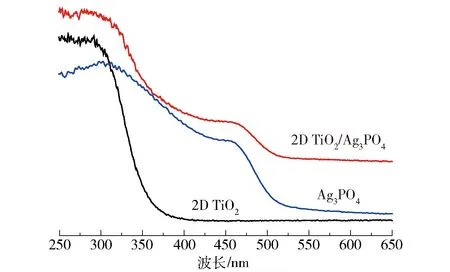
图6 2D TiO2、纯Ag3PO4和2D TiO2/Ag3PO4的紫外- 可见光吸收光谱Fig.6 UV- Vis spectra of the prepared 2D TiO2, bare Ag3PO4 and 2D TiO2/Ag3PO4
2.1.5荧光光谱
光生电子和空穴的结合可以以荧光的形式释放,故光致发光(PL)光谱是研究光生载流子复合效率的有效方法,PL光谱发光强度反映了电子- 空穴对的复合重组效率。一般来说,PL光谱发射峰强度越低,光生电子与空穴的重组率越低,进而预示着光催化剂的光催化活性越高[28]。图7是2D TiO2、Ag3PO4和2D TiO2/Ag3PO4光催化剂的PL光谱(激发波长λex=357 nm),从图中可以明显看出3个样品在420~500 nm内出现了发光峰,但是2D TiO2/Ag3PO4复合催化剂的发射峰强度比2D TiO2和Ag3PO4的强度弱很多,由此可以确定2D TiO2与Ag3PO4的复合可以加快光生载流子迁移率,减缓光生电子- 空穴的重组复合,进而提高催化剂的光催化活性。
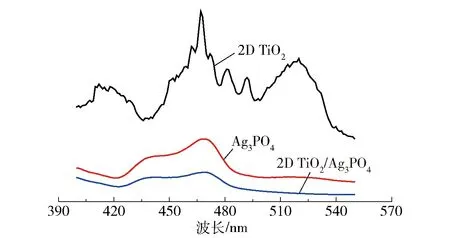
图7 2D TiO2、纯Ag3PO4和2D TiO2/Ag3PO4的荧光光谱Fig.7 Photoluminescence (PL) spectra of the prepared 2D TiO2, bare Ag3PO4 and 2D TiO2/Ag3PO4
2.1.6比表面积和孔体积
图8为所制备的2D TiO2/Ag3PO4光催化剂的N2吸附- 脱附曲线。结果表明2D TiO2/Ag3PO4的等温吸附曲线呈典型的Ⅳ型,其比表面积和孔体积分别为78.211 m2/g和0.114 cm3/g,而商业化的TiO2纳米粒子(P25)的比表面积为50 m2/g[29],说明所制备的2D TiO2/Ag3PO4具有较高的比表面积,在吸附- 光催化降解污染物的反应过程中能够提供较多的活性吸附位点和反应位点,有利于吸附- 光催化活性的提高。
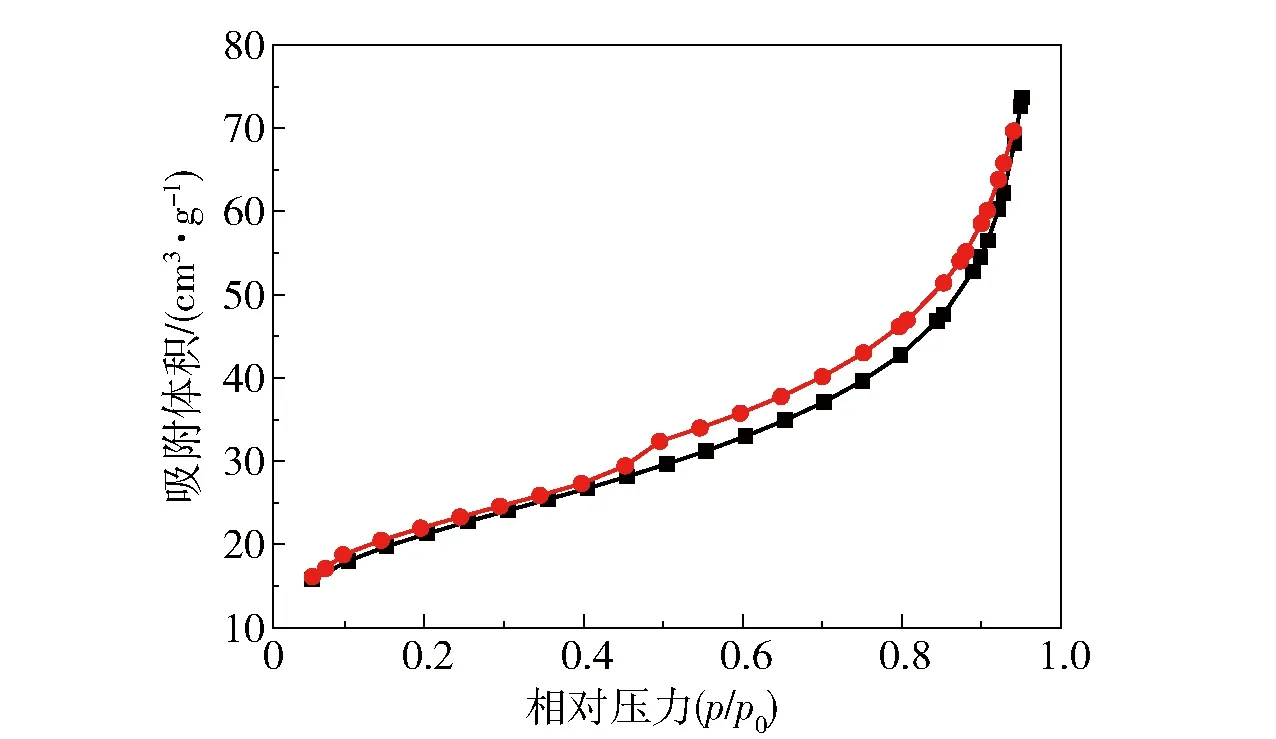
图8 所制备的2D TiO2/Ag3PO4复合光催化剂的N2吸附- 脱附曲线Fig.8 N2 adsorption-desorption isotherms of the prepared 2D TiO2/Ag3PO4 catalyst
2.2 催化性能
2.2.1复合材料的吸附-光催化降解性能
分别以2D TiO2、Ag3PO4和不同物质的量比的2D TiO2/Ag3PO4为催化剂,考察其在可见光催化降解RhB的过程中RhB浓度和时间的关系,结果如图9所示。
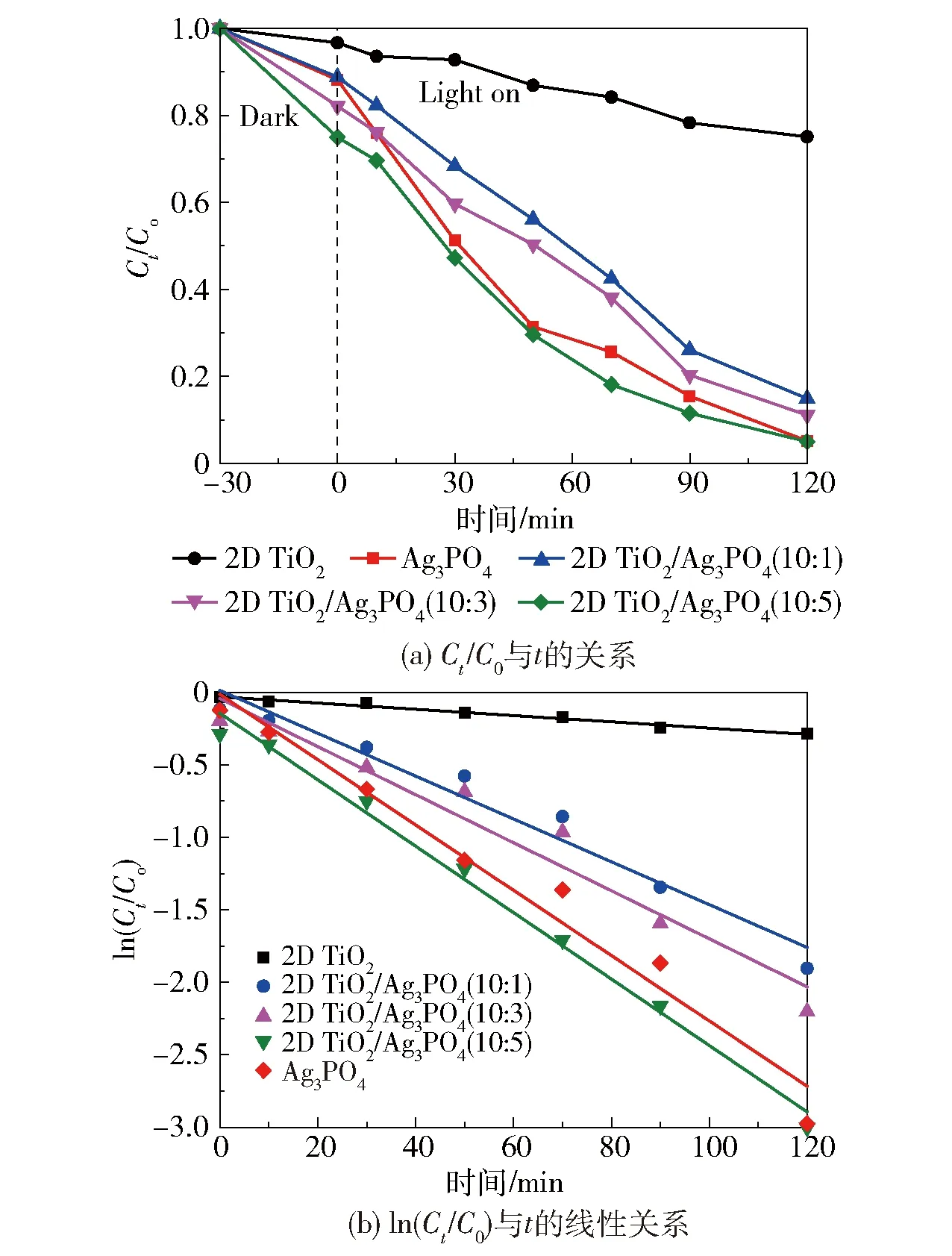
图9 不同催化剂在降解RhB的过程中RhB浓度和时间的关系Fig.9 The relationship between RhB concentration and time during the degradation of RhB using different catalysts
从图9(a)中可以看出,黑暗条件下搅拌30 min达到吸附平衡时RhB的吸附量,以及相同时间内光催化剂在可见光照射下对RhB的降解去除率均随着Ag3PO4含量的增加而升高。黑暗条件下搅拌30 min时,物质的量比为10∶1、10∶3和10∶5的2D TiO2/Ag3PO4分别可以吸附约11.2%、17.9%和25.1%的RhB分子,而未复合的2D TiO2对RhB的吸附率仅为3.3%。可见光照射120 min后,2D TiO2/Ag3PO4(10∶1)、2D TiO2/Ag3PO4(10∶3)和2D TiO2/Ag3PO4(10∶5)对RhB的降解去除率分别为85.2%、89%和95.1%,均显著高于未复合Ag3PO4的2D TiO2的降解去除率(24.9%),2D TiO2的降解作用实际源于其吸附和RhB染料分子的自降解以及长时间光源照射产生的热促自降解之间的相互促进。紫外光谱中RhB的吸收峰强度与其浓度成正比,由此我们通过拟合反应物浓度与时间的函数关系,得出反应速率常数k,结果如图9(b)和表1所示。结果表明,2D TiO2和不同物质的量比的2D TiO2/Ag3PO4光催化降解RhB的反应均为一级动力学反应。将2D TiO2与Ag3PO4复合,其吸附- 可见光催化降解性能随着Ag3PO4含量的增加而提高,并且2D TiO2/Ag3PO4(10∶5)复合材料的可见光催化降解性能优于Ag3PO4(k为0.022 5 min-1)。

表1 不同催化剂的反应速率常数k和线性相关系数R2Table 1 Reaction rate constants and linear correlationcoefficients for different catalysts
根据文献报道及本课题组前期的研究工作[26,30-31],随着光催化降解反应的进行,Ag3PO4中的银离子会发生光腐蚀而被还原成银单质,从而会造成光催化活性的降低,因此本文还考察了H2O2的加入对复合材料光催化性能的影响,结果如图10所示。从图中可以看出,在相同的光催化降解试验条件下,加入少量H2O2(0.25 mL)可以使得2D TiO2/Ag3PO4(10∶1)在可见光照射50 min 时对RhB的降解去除率达到88.3%,远高于未加H2O2的2D TiO2/Ag3PO4对RhB的降解去除率(43.9%),而单独的H2O2对RhB的降解去除率仅为6.4%,由此可以说明少量H2O2的加入可以极大地提高2D TiO2/Ag3PO4的光催化降解活性。
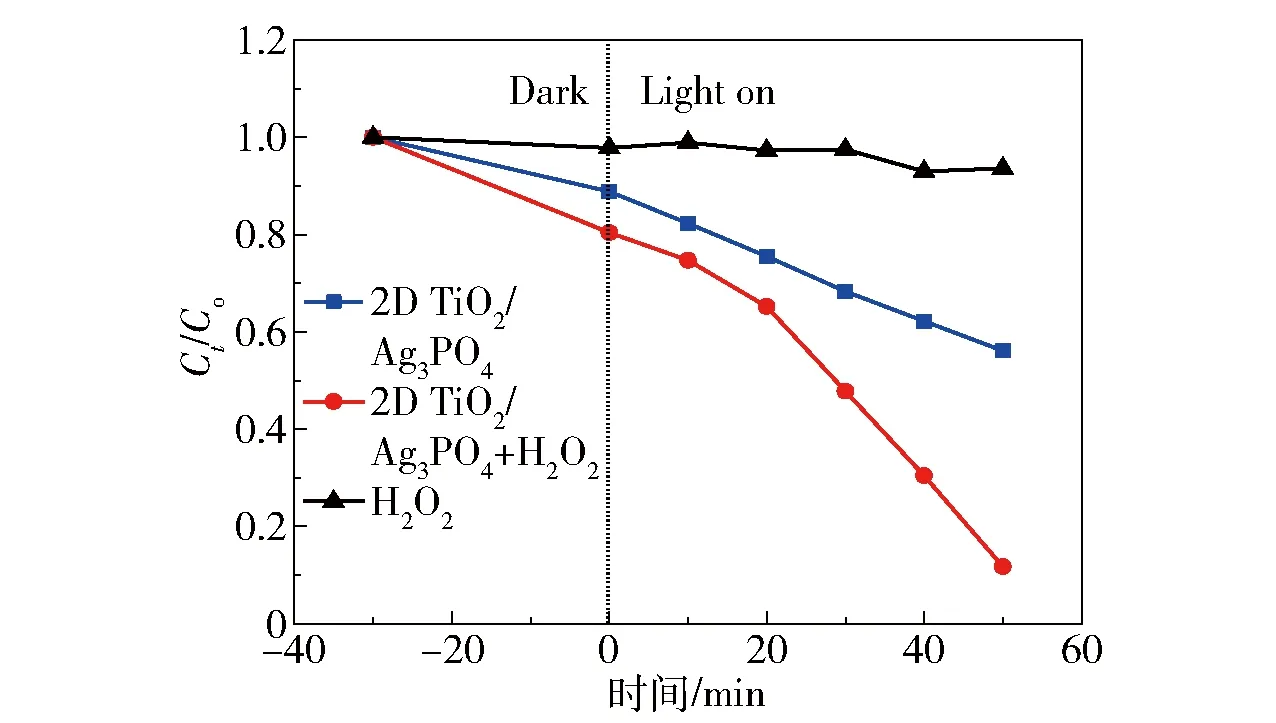
图10 添加H2O2对2D TiO2/Ag3PO4可见光催化降解RhB性能的影响Fig.10 Effect of H2O2 on photocatalytic degradation of RhB by 2D TiO2/Ag3PO4 under visible light irradiation
2.2.2复合材料的电化学性能
电化学阻抗和光电流可以用于进一步评估光催化剂产生和转移光生载流子的能力。图11(a)为2D TiO2、Ag3PO4和2D TiO2/Ag3PO4(10∶5)光催化剂的瞬态光电流响应曲线,从图中可以看出,2D TiO2/Ag3PO4(10∶5)的光电流密度明显高于Ag3PO4和2D TiO2,表现出更有效的电子空穴分离和更快的电荷转移,从而更有利于光催化降解反应[32]。图11(b)是2D TiO2、Ag3PO4和2D TiO2/Ag3PO4(10∶5)在光照下的EIS曲线。通常来说,EIS曲线圆弧半径越小,电荷的转移电阻越小,电荷转移速率越快[33]。由图11(b)可以看出,与单独的2D TiO2和Ag3PO4相比,2D TiO2与Ag3PO4复合后的圆弧半径明显较小,表明光生载流子在2D TiO2/Ag3PO4复合材料中的电荷转移电阻较小,该复合材料能够提高光生载流子的转移速率和传输效率,有助于增强光催化活性。
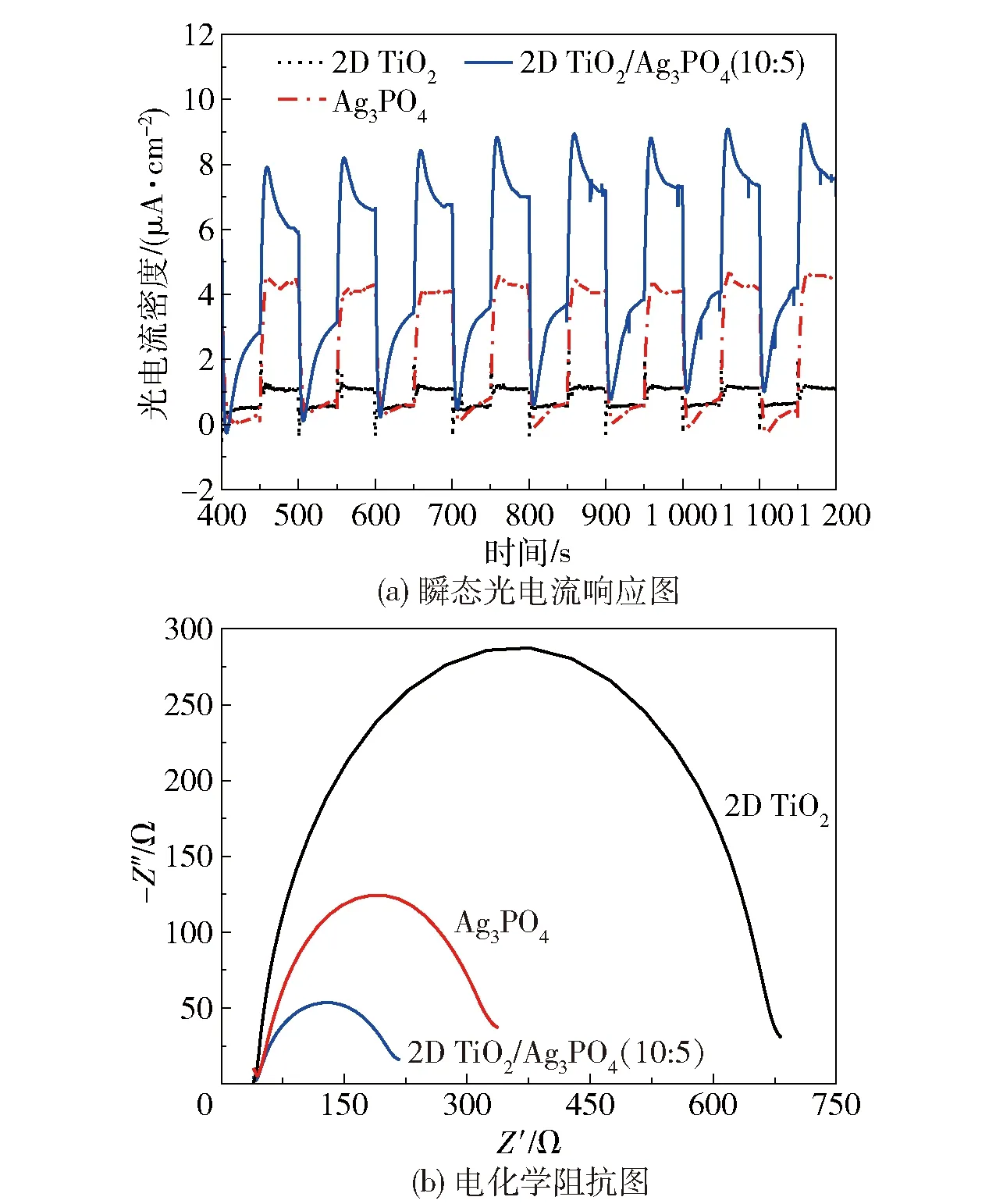
图11 不同催化剂的瞬态光电流响应图和电化学阻抗图Fig.11 Transient photocurrent response and EIS diagrams for different catalysts
2.3 光催化降解反应过程中活性物质的确定及机理分析
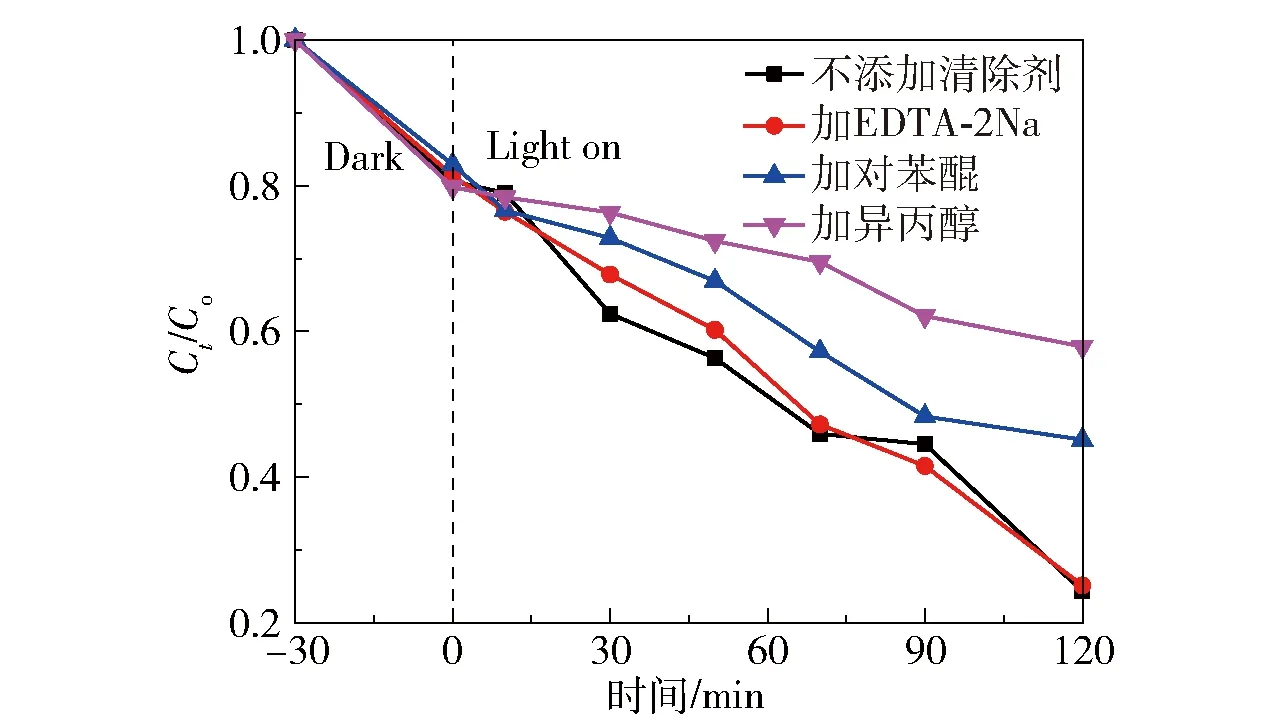
图12 添加不同清除剂时2D TiO2/Ag3PO4(10∶5)复合材料对RhB的光降解性能Fig.12 Photodegradation of RhB by 2D TiO2/Ag3PO4(10∶5) composites in the presence of different scavengers
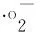
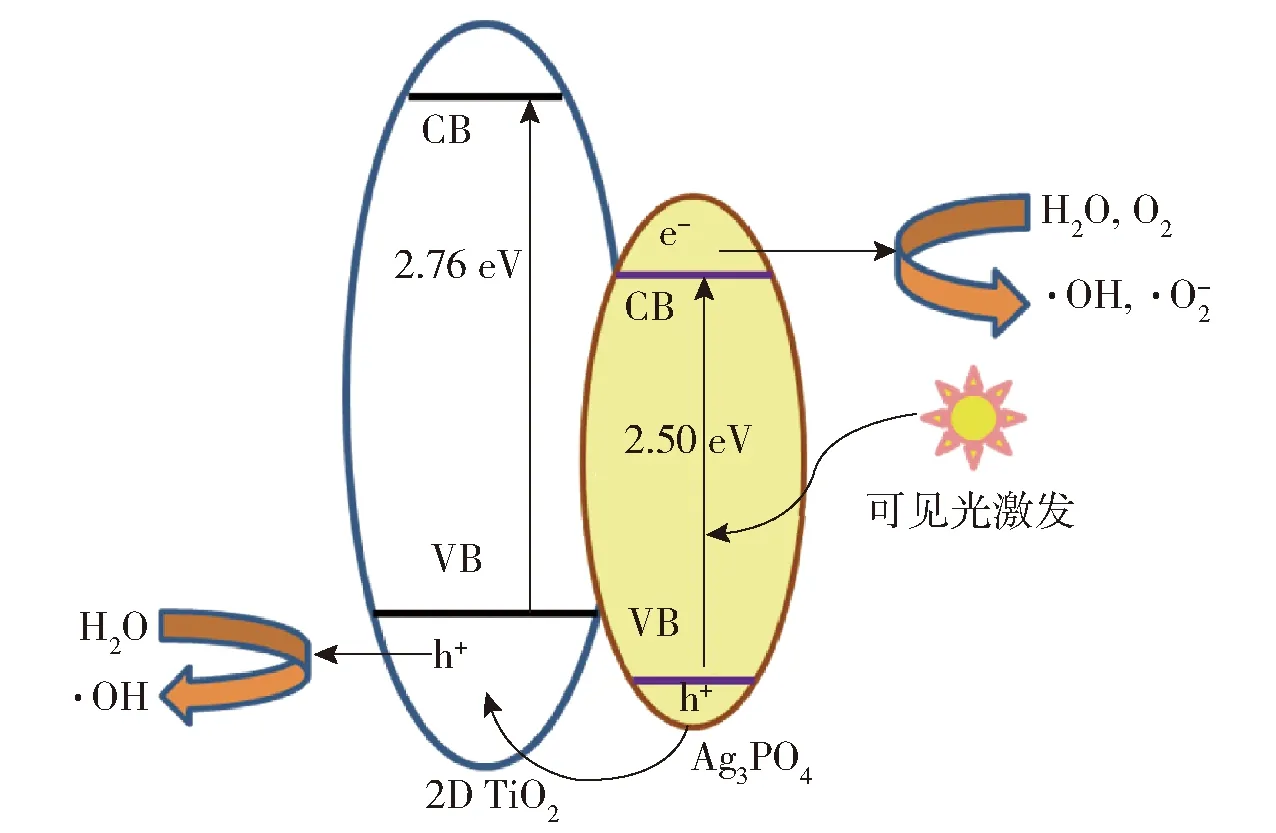
图13 2D TiO2/Ag3PO4光催化体系中光生电子和空穴的迁移示意图Fig.13 Migration of photo-generated e- and h+ in the 2D TiO2/Ag3PO4 photocatalytic system
具体反应机理如下所示。
2D TiO2/Ag3PO4+hν→2D TiO2/Ag3PO4(e-+h+)
2D TiO2/Ag3PO4(e-+h+)→2D TiO2(h+)/Ag3PO4(e-)
h++H2O→·OH+H+
2e-+O2+2H+→H2O2
h++OH-→·OH
·OH+RhB→CO2+H2O
3 结论