原花青素调控抑癌基因 p53/AMP 活化蛋白激酶通路抑制多囊卵巢综合征大鼠颗粒细胞自噬的实验研究
2021-06-17王漫丽
王漫丽
作者单位:洛阳市妇幼保健院产科一区,河南 洛阳 471000
多囊卵巢综合征(PCOS)是妇科临床常见的内分泌功能紊乱疾病,也是育龄期女性继发不孕症的常见病因。据统计,我国育龄期女性中 PCOS 的发病率约为 5%~10%,且随着女性生活压力的剧增呈增长趋势,可并发不孕症、糖尿病、高血压、甚至是子宫内膜癌等 ,危害甚重 。 目前临床上常用的PCOS 疗法有药物调节内分泌、改善胰岛素抵抗等,对有强烈生育愿望者给予来曲唑或克罗米芬等促排卵,有一定作用,但临床效果有限。既往报道显示,卵巢颗粒细胞自噬可维持卵巢生殖功能,正常情况下卵巢细胞增殖和自噬、凋 亡处于平衡状态,而卵巢颗粒细胞自噬异常激活可能是 PCOS 发生的重要机制。而抑癌基因 p53(p53)∕AMP 活化蛋白激酶(AMPK)信号转导通路可参与调控卵巢颗粒细胞自噬 ,可作为 PCOS 治疗药物开发的新靶点。原花青素是一种生物类黄酮混合物,具有特殊的分子结构,可从蓝莓叶、葡萄籽等中提取,属于一种强效抗氧化剂。有研究发现,原花青素可调控恶性肿瘤细胞的自噬,还可减轻 PCOS 并动脉粥样硬化模型大鼠的病理改变。但原花青素是否可通过调控 p53∕AMPK 通路抑制 PCOS 大鼠卵巢颗粒细胞自噬仍需深入研究,而探讨该课题可为此类病人新药的研究与开发提供方向,故于 2018年 4月至 2019年 6月开展如下动物实验。
1 材料与方法
1.1 材料
1.1.1 实验动物 60 只雌性 SD 大鼠,无特定病原体(SPF)级,7~9周龄,体质量范围为 200~260 g,购自郑州大学医学院实验动物中心[SCXK(豫)-20180001],卫生检疫合格,本研究符合一般动物实验伦理学原则。
1.1.2 主要试剂及仪器 原花青素(沈阳中科药业有限责任公司 ,国食健字 G20041220,批 次180415A,提纯后纯度≥98%);来曲唑(浙江海正药业股份有限公司,批号 H20084597,批次 1805116);羧甲基纤维素(CMC)(南京道斯夫生物科技有限公司);枸橼酸氯米芬(广州康和制药有限公司,批号H44021970,批次 201804102);睾酮检测试剂盒、促黄体生成素(FSH)检测试剂盒、雌二醇检测试剂盒(均购自南京建成生物研究所);苏木精-伊红(HE)染色试剂盒 、单丹磺酰尸胺(MDC)染色试剂盒 、Trizol 试剂盒、蛋白提取试剂盒(均购自法国生物梅里埃公司);二氨基联苯胺(DAB)显色液(购自深圳晶美生物科技有限公司);兔抗鼠 p53、微管相关蛋白 1 轻链 3Ⅱ(LC3Ⅱ)、AMPK、p-AMPK 单克隆抗体、酶标记的山羊抗兔 p53、LC3 Ⅱ、AMPK、p-AMPK 多克隆抗体(均购自美国 Santa Cruz 公司)。
RT-6000 型酶标仪(购自美国 Rayto 公司);DSZ-70PHC 型光学显微镜(购自日本 Carton 公司);5084R 型台式离心机(购自德国 Eppendorf 公司);Cytomics ™ FC 500 型流式细胞仪(购自美国 Beckman Coulter 公司);2720 型聚合酶链扩增反应仪(购自美国 ABI 公司);PowerPac Basic 型电泳仪(购自美国 Bio-Rad 公司);EPS300 型蛋白质电泳仪(购自美国 Thermo 公司);Trans-Blot SD 型转膜仪(购自美国Bio-Rad 公司)。
1.2 方法
1.2.1 分组、建模及干预 60 只成年雌性 SD 大鼠按照 1~60 自然数进行编号,以计算机生成随机数字表,按照随机、均等原则分为 N 组、M 组、P 组、LD 组、MD 组 和 HD组 ,每组各10只 。 除N组外均建立PCOS 模型。建模方法:来曲唑灌服,剂量为 1 mg∕kg,溶于 1% CMC 中,连续 21 d;N 组同时灌服等容积、等浓度的基质羧甲基纤维素,共 21 d。参照文献方法验证模型。然后 P 组给予枸橼酸氯米芬溶液5.21 mg∕kg 灌服,LD 组、MD 组和 HD 组分别给予 25、50、100 mg∕kg 原花青素灌服,N 组和 M 组均给予等量生理盐水灌服,均每天 1 次,连续 24 d。
1.2.2 血清性激素水平检测 包括睾酮、FSH、雌二醇。分别于治疗前后抽取尾静脉血 5 mL,3 500 r∕min 离心 15 min 取血清,采用化学发光法(睾酮)、酶联免疫吸附测定(FSH、雌二醇)检测,需按照对应试剂盒说明书操作。
1.2.3 卵 巢组 织 病理 观察 取 0.4% 戊巴比妥 0.1 mL∕kg 腹腔注射,大鼠昏迷后取 75% 乙醇对腹部皮肤常规消毒,将腹腔打开并取出新鲜的卵巢组织。中性福尔马林浸泡固定,梯度浓度乙醇溶液脱水,包埋并切片,HE 染色试剂盒处理,封片并以光学显微镜放大观察。
1.2.4 卵巢颗粒细胞自噬率检测 将卵巢组织取出后以生理盐水冲洗,5 min×3 遍。将脂肪组织剔除,刺破卵泡,磷酸盐缓冲液冲洗,200 目筛过滤。离心处理,参数:800 r∕min,5 min。取沉渣,调整细胞浓度 ,至 1×10个∕毫 升 。 MDC 染色 ,浓度 0.05 mmol∕L,37 ℃温育 60 min 并以磷酸盐缓冲液清洗。以流式细胞仪术检测卵巢颗粒细胞自噬率。
1.2.5 卵巢组织 p53、AMPK mRNA 表达检测 取卵巢组织,匀浆研磨,以试剂盒提取总核糖核酸,反转录。配置反应体系,其中 p53 正向引物:5’-ACTGCTAGATTAGAGCTAGATCGA-3’,反向引物 :5’-CTGCTAGATCGATATTAGCTATAGCGAT-3’;AMPK 正向引物:5’-CTCGATAGGATCGATAGATCGAAC-3’,反向引物 :5’-CTCGATATGATCTAGTATAGATCAGA-3’;β 肌动蛋白(β -actin):正向引物 :5’-CTGCTCGATAGATCGATAGCTAGC-3’,反向引物:5’-CTGCTGATAGCTAGCTAGGGATTC-3’。 以 PCR 仪反应,条件:95 ℃、10 min,40 个循环:95 ℃、10 s→60 ℃、20 s→72 ℃、20 s,60 ℃、5 min。取产物电泳,分析并计算目的基因的表达量,即 2。
1.2.6 卵巢组织 p53、LC3 Ⅱ、AMPK 蛋白表达及 p-AMPK 检测 采用蛋白质印迹法,取卵巢组织匀浆研磨,灭活并以磷酸盐缓冲液冲洗。提取总蛋白,定量后上样电泳,脱脂奶粉封闭,室温下孵育 1 h。滴加一抗,4 ℃下孵育过夜;磷酸盐缓冲液冲洗,滴加二抗,37 ℃下孵育 2 h,再次以磷酸盐缓冲液冲洗。以 DAB 显色,以蒸馏水终止显色反应,暗室曝光、显影和定影。拍照扫描,计算蛋白相对表达量,即目的蛋白与内参(β-actin)的比值。
2 结果
2.1 治疗前后血清性激素水平对比
N 组、M 组、P组、LD 组、MD 组和 HD 组分别有 1 只、3 只、2 只、1只、1 只和 1 只大鼠非正常原因死亡,均剔除。各组治疗前后血清睾酮、雌二醇和 FSH 对比差异有统计学意义(P
<0.001),治疗后 N 组血清性激素水平与治疗前差异无统计学意义(P
>0.05),M 组血清睾酮、FSH 水平均升高,雌二醇水平下降(P
<0.05);治疗前后 M 组、P 组、LD 组、MD 组和 HD 组血清睾酮、FSH水平均高于 N 组,雌二醇水平均低于 N 组(P
<0.05);治疗后 P 组、LD 组、MD 组和 HD 组血清睾酮、FSH 水平均低于 M 组,雌二醇水平均高于 M 组(P
<0.05);治疗后 LD 组血清睾酮、FSH 水平均高于 P组,雌二醇水平低于 P 组(P
<0.05);MD 组血清性激素水平与P 组差异无统计学意义(P
>0.05);HD 组血清睾酮、FSH 水平均低于P组 ,雌二醇水平高于P组(P
<0.05);LD 组、MD 组和 HD 组血清性激素水平均呈剂量依赖性,每两组间差异有统计学意义(P
<0.05)。见表1。2.2 卵巢组织病理学变化观察
N 组卵泡排列整齐,大小均匀,结构清晰,颗粒细胞规整,可达 8~9层,大多均可见卵丘;M 组卵泡排列严重紊乱,大小明显不一,结构极度混乱,颗粒细胞紊乱且排列稀疏,细胞层仅 1~2 层,仅有极少量黄体组织;P 组卵泡排列稍显紊乱,大小不均,结构轻微混乱,颗粒细胞排列紊乱且轻微稀疏,颗粒细胞 5~6 层,有黄体组织;LD 组卵泡排列紊乱,大小不均,结构混乱,颗粒细胞排列明显紊乱且排列稀疏,颗粒细胞仅 3~4 层,有少量黄体组织;MD 组与 P 组相近;HD 组卵泡排列稍显紊乱,基本均匀,少部分结构不清,颗粒细胞大多相对规整,可达 7~8 层,可见卵丘。
表1 各组大鼠治疗前后血清性激素水平对比
2.3 卵巢颗粒细胞自噬率对比
N 组、M 组、P 组、LD 组、MD 组、HD组卵巢颗粒细胞自噬率分别为(7.12±0.56)% 、(18.93±3.12)% 、(11.20±1.82)% 、(13.45±2.10)% 、(11.08±1.79)% 、(9.86±1.05)%(F
=41.368,P
<0.001)。与 N 组比较其余五组均升高,与M 组比较,P 组、LD 组、MD 组和 HD 组均下降,与 P 组卵巢颗粒细胞自噬率比较,LD 组升高、LD 组下降,与 LD 组比较,MD 组、HD 组卵巢颗粒细胞自噬率均下降,且 HD 组低于 MD 组(P
<0.05)。2.4 卵巢组织 p53、AMPK mRNA 表达对比
各组卵巢组织 p53 mRNA 表达对比,差异有统计学意义(P
<0.001);各组卵巢组织 AMPK mRNA 表达差异无统计学意义(P
>0.05)。见表2。2.5 卵巢组织 p53、LC3 Ⅱ、AMPK 蛋白表达及 p-AMPK 对比
各组卵巢组织 p53、LC3 Ⅱ蛋白表达及 p-AMPK 对比差异有统计学意义(P
<0.001);各组卵巢组织 AMPK 蛋白表 达差异 无 统计学 意义(P
>0.05)。见表3、图1。3 讨论
PCOS 常见的病因有下丘脑-垂体-卵巢轴功能异常、代谢紊乱、肾上腺功能失常及遗传等,可引起被膜纤维化增厚,导致卵巢囊性增大、影响正常排卵。目前人们对该病的具体机制认识尚浅,且临床治疗方案多缺乏特异性,而新药研究也缺乏治疗靶点,因此采用新的药物通过已知的途径发挥治疗作用是目前重要课题。卵巢颗粒细胞自噬与卵细胞的发育、排出等生理过程均有密切关联,细胞自噬与细胞生物学改变有密切关系。而抑制卵巢颗粒细胞自噬是当前针对 PCOS 新药研究的热点。
表2 各组大鼠卵巢组织 p53、AMPK mRNA 表达对比
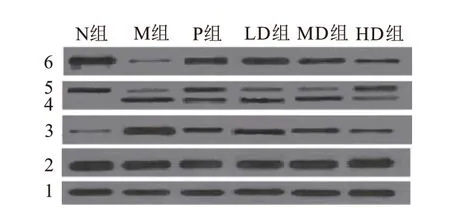
图1 蛋白质印迹法检测各组大鼠卵巢组织 p53、LC3 Ⅱ、AMPK蛋白表达及 p-AMPK

表3 各组大鼠卵巢组织 p53、LC3 Ⅱ、AMPK 蛋白表达及 p-AMPK 对比
本研究中,P 组、LD 组、MD 组和 HD 组治疗后血清性激素水平均显著改善,M 组治疗后血清性激素水平均显著恶化,N 组均无明显变化,且治疗后 HD组血清性激素水平改善最理想,可知原花青素和枸橼酸氯米芬均有助于改善 PCOS 大鼠血清性激素水平。睾酮主要由卵巢、腺外组织、肾上腺皮质转化,在 PCOS 发病过程中,睾酮显著升高,主要原因是卵泡雄激素浓度过高,可促进黄体细胞内雄激素转化为双氢睾酮,抑制卵巢的正常发育;雌二醇主要来源是卵巢,在 PCOS 发生过程中可导致雌激素不足,抑制黄体细胞内雄激素向雌激素的转化,因而其水平较低;FSH 主要由垂体前叶促性腺激素细胞分泌,可刺激颗粒细胞增生和卵泡生长发育,在PCOS 中 FSH 的水平显著升高,且对 PCOS 病情有评估作用。因此在 PCOS 治疗中应积极调控血清性激素水平。原花青素是目前公认的高效自由基清除剂和天然抗氧化剂,常用于抗氧 化应激损伤治疗,在 PCOS 中的作用报道尚少。结合上述分析和本研究结果,推测原花青素可调控 PCOS 大鼠血清性激素水平,且高浓度的原花青素对其调控作用明显优于枸橼酸氯米芬,显示出良好的挖掘价值。在本研究 HE 病理学变化观察中显示,M 组卵巢组织有严重的病理改变,P 组、LD 组、MD 组和 HD 组均有所减轻,且 HD 组与 N 组最为接近,提示原花青素可减轻 PCOS 大鼠卵巢组织的病理学改变,且呈剂量依赖性。因此原花青素不仅可调控 PCOS 大鼠血清性激素水平,还可减轻卵巢组织病理改变。
此外,本研究关于卵巢颗粒细胞自噬率的对比结果中显示,N 组<HD 组<MD 组∕P 组<LD 组<M 组,表明原花青素可抑制 PCOS 大 鼠卵巢颗粒细胞自噬,且其作用呈剂量依赖性。在基因及蛋白表达检测结果中显示,原花青素可上调 p53 基因及蛋白表达,抑制 AMPK的磷酸化 ,控 制 LC3 I 向 LC3 Ⅱ 转化,推 测该药物很可能是通过上述 途径实现抑制PCOS 大鼠卵巢颗粒细胞自噬的。成熟卵泡的颗粒细胞是卵泡最重要的单元,颗粒细胞增殖、分化在卵泡发育过程中均有参与,且可促进卵母细胞的发育与成熟。颗粒细胞是否凋亡可直接影响卵母细胞的发育潜能,而自噬与凋亡关系密切,有研究表明自噬是凋亡的引导机制,而 LC3 I 向 LC3 Ⅱ转化是卵巢颗粒细胞发生自噬的重要表现。 p53∕AMPK 信号通路在自噬过程中也有调控作用,其中p53 基因与蛋白可负性调节细胞自噬,还可通过转录依赖性途径增加 AMPK 蛋白的磷酸化水平进而促进细胞自噬。研究显示,卵巢颗粒细胞自噬过程中,p53∕AMPK 通路不仅可参与直接调控,还可调控 LC3 I 向 LC3 Ⅱ的转化间接影响细胞自噬。根据本研究结果和上述分析,推测原花青素可通过调控 p53∕AMPK 通路,上调 p53.基因及蛋白表达,抑制AMPK 的磷酸化,控制 LC3 I 向 LC3 Ⅱ转化进而抑制卵巢颗粒颗粒细胞自噬的。
综上所述,在 PCOS 大鼠中给予原花青素灌服可改善血清性激素水平,减轻卵巢病理改变,抑制卵巢颗粒细胞自噬,且呈剂量依赖性,中剂量原花青素的效果与枸橼酸氯米芬均相近,而高剂量原花青素的效果均最佳,推测很可能与调控 p53∕AMPK通路,上调 p53 基因及蛋白表达,抑制 AMPK 的磷酸化,控制 LC3 I 向 LC3 Ⅱ转化有关。但其具体作用机制及在临床治疗中应用的可行性仍需要进一步探讨,可作为进一步的研究方向。
