石杉碱甲在中国老年受试者中药动学和安全性研究*
2021-06-15钱泓洁张梦琪邹扬刘淑云王伟陈倩刘罡一刘昀余琛贾晶莹
钱泓洁,张梦琪,邹扬,刘淑云,王伟,陈倩,刘罡一,刘昀,余琛,贾晶莹
(1.上海市徐汇区中心医院中心实验室,上海药物I期临床暨药物一致性评价工程技术研究中心 上海 200031;2.上海市徐汇区中心医院急诊科,上海 200031)
阿尔茨海默病(Alzheimer's disease,AD)是最常见的神经退行性疾病,我国65岁以上老年人中AD患病率为3.21%[1],严重影响患者生活质量,并造成巨大的社会负担。基于AD的胆碱能假说,已有多种胆碱酯酶抑制剂(cholinesterase inhibitors,ChEI)被批准用于AD的治疗[2]。石杉碱甲是从石杉科植物千层塔(蛇足石杉)中提取的一种可逆性ChEI,本研究旨在考察石杉碱甲在中国老年受试者体内的药动学(pharmacokinetics,PK)特点和安全性,对老年群体用药提供一定的参考。
1 资料与方法
1.1研究对象 本研究纳入60~80岁无重要脏器功能障碍的男性和女性老年受试者。入选标准包括:心、肝、肾功能基本正常;血清天冬氨酸氨基转移酶(AST)和丙氨酸氨基转移酶(ALT)≤1.5倍正常值上限;内生肌酐清除率不低于参考值的80%。主要排除标准为给予研究药物前3个月内出现以下情况者:心肌梗死、严重/不稳定型心绞痛、冠状动脉/外周动脉旁路移植、充血性心力衰竭、脑血管意外,包括短暂性脑缺血发作,癫、肾功能不全、机械性肠梗阻、心动过缓、支气管哮喘等疾病,以及严重糖尿病患者。允许对基础疾病使用合并用药,并记录使用的药物和用法用量。本研究经本院伦理委员会批准,研究过程符合赫尔辛基宣言,严格遵守CFDA-GCP进行。所有受试者均自愿签署知情同意书。
1.2试验设计 所有入组受试者单次服用石杉碱甲片(上海医科大学红旗制药厂,批号:110303,规格:每片0.05 mg)0.1 mg。分别于给药前、给药后0.25,0.5,0.75,1,1.25,1.5,2,3,4,6,8,12,24,36,48 h采集血样1.5 mL,分离血浆后在-20 ℃储存直到分析。在给药前和给药后0~2、2~4、4~8、8~12、12~24、24~36、36~48 h收集PK尿样,记录体积,取5 mL样本在-20 ℃储存直至分析。在整个研究过程中监测受试者生命体征和记录不良事件,在筛选时和给药后第3天接受体格检查、12导联心电图和实验室检查(血常规、尿常规、肝肾功能、血糖)。
1.3生物分析 采用经验证的液相色谱-串联质谱(LC-MS/MS)法测定血浆和尿液中石杉碱甲浓度,符合《中华人民共和国药典》中生物样品定量分析方法验证指导原则的规定。
仪器:QTRAP®5500串联质谱仪(美国AB Sciex公司);液相系统(日本岛津公司)。在血浆中加入内标石杉碱乙,用乙腈直接沉淀蛋白法处理样品。采用SeQuant ZIC-HILIC(100 mm×2.1 mm,3.5 μm)色谱柱进行分离,柱温35 ℃;流动相为含5 mmol·L-1甲酸铵0.1%甲酸溶液-乙腈;流速0.3 mL·min-1;柱温35 ℃;梯度洗脱;进样体积5 μL;正离子多反应检测(MRM),离子通道分别为m/z243.2 →210.2(石杉碱甲),m/z257.2→198.6(石杉碱乙)。结果显示石杉碱甲线性范围0.05~10 μg·L-1(r>0.999),定量下限0.05 μg·L-1,提取回收率81.0%~95.4%,批内、批间精密度RSD均<8%,内标的基质效应因子在2.11~2.28[3]。
1.4统计学方法 使用WinNonlin 6.4版软件(美国Pharsight公司)采用非房室模型进行PK参数分析,包括峰浓度(Cmax)、峰时间(tmax)、血浆浓度-时间曲线下面积(AUC(0-72 h))、AUC(0-∞)、半衰期(t1/2)等。并计算给药后48 h内尿液排泄率。采用SPSS 22.0版软件进行统计学分析,采用独立样本t检验对男女受试者PK参数进行比较,以P<0.05为差异有统计学意义。
2 结果
2.1患者基线资料 14例老年受试者(男、女各7例),年龄63~79岁,平均(69.4±5.2)岁,均按计划完成研究。平均身高为(158.6±9.0) cm,平均体质量为(65.7±9.9) kg。其中10例伴有基础疾病,包括高血压、糖尿病、高脂血症和前列腺增生,在研究期间未停用相应的合并用药。
2.2PK分析 老年受试者单次口服石杉碱甲0.1 mg,平均血浆药物浓度-时间曲线见图1。主要的PK参数:Cmax为(0.92±0.28) ng·mL-1,tmax为(2.61±1.67) h,AUC(0-72h)为(15.12±4.73) ng·h·mL-1,AUC(0-∞)为(16.99±4.92) ng·h·mL-1,t1/2为(14.38±3.87) h;同时对既往石杉碱甲PK和生物等效性研究文献进行检索,见表1。老年受试者单次服用石杉碱甲0.1 mg后48 h累计尿液药物排泄率为34.77%,见表2。
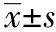
表1 既往研究和本研究中的主要PK参数
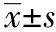
表2 石杉碱甲尿液排泄

图1 单次口服石杉碱甲0.1 mg后中国老年受试者体内的药物浓度-时间曲线
在所有分析的PK参数中,男性受试者t1/2(17.20±3.05 )h 显著长于女性受试者(11.56±2.15)h,P=0.002,其他参数比较差异无统计学意义,见表3。

表3 不同性别受试者的主要PK参数
2.3安全性 试验期间未发生严重不良事件。1例(7.1%)受试者在给药当天出现发热、腹泻、腹痛和低钾血症,并接受了静脉补液、抗菌药物和补钾治疗。研究医生判断上述不良事件与研究药物可能无关。
3 讨论
既往石杉碱甲动物实验结果显示,在大鼠肝微粒体中,石杉碱甲的代谢主要由细胞色素P450(CYP)1A2介导,CYP 3A1/2可能起次要作用[8],同时,在药理学剂量下,石杉碱甲对肝CYP同工酶的活性和表达没有影响,这表明石杉碱甲与其他伴随药物发生药物相互作用的概率较小[9]。在大鼠、小鼠和犬体内的实验表明,石杉碱甲具有很高的生物利用度,口服后几乎完全吸收[10-11]。
国内外在健康受试者中,曾开展过多项石杉碱甲临床研究。在6例平均年龄为27岁健康志愿者中进行单次口服石杉碱甲0.99 mg的PK研究[4],平均血浆Cmax为8.4 ng·mL-1,tmax为79.6 min,终末消除半衰期(t1/2)为288.5 min。在另一项PK研究中,12例20~25岁健康志愿者口服单剂量石杉碱甲0.4 mg,平均血浆Cmax为2.59 ng·mL-1,tmax为58.33 min,AUC(0-∞)为2 450.34 mg·min·mL-1[5]。在中国健康受试者中单次给药剂量高达0.99 mg[4],以及在美国轻中度AD患者中为期24周石杉碱甲给药剂量0.4 mg,bid临床研究中,均获得良好的安全性数据[12]。但上述研究的剂量均大于临床常用剂量,且在特殊人群尤其是神经退行性疾病(包括AD和其他类型的痴呆)的目标人群老年人,目前尚未建立完整的PK数据。
本研究中,笔者选择临床推荐剂量(0.1 mg)在无认知功能障碍的中国老年人进行单次给药的PK试验,耐受性良好。本研究的受试者人群大部分伴有基础疾病,包括高血压、糖尿病、高脂血症和前列腺增生,在研究期间使用相应的合并用药,这可能会对石杉碱甲的PK特性产生影响,然而,高血压、糖尿病和血脂异常均是老年人群常见的疾病,也是AD和血管性痴呆的危险因素,本研究对象在一定程度上代表适用石杉碱甲的实际老年人群,且石杉碱甲与本研究中的药物无已知的药物相互作用,因此考虑研究中合并用药的情况对本研究的结论无显著影响。
由于不同研究的给药剂量不同,根据现有数据无法对PK参数直接进行比较,笔者对既往石杉碱甲PK和生物等效性研究的文献进行检索并汇总[4-7]。与文献报道石杉碱甲临床研究不同,本研究选择的研究对象为老年受试者,更符合石杉碱甲临床应用的患者人群。在本研究中,Cmax为(0.92±0.28) ng·mL-1,与既往PK和生物等效性研究进行比较,Cmax与给药剂量基本成正比例关系;AUC(0-72h),AUC(0-∞)均接近于既往非老年人群研究中0.2 mg剂量组AUC数据;尽管本研究给药剂量小于其他研究,但tmax和t1/2较其他研究更长。上述结果提示,老年人群对石杉碱甲的吸收和消除均较年轻人更为缓慢,这可能与老年人群胃肠道功能及肝肾功能减退有关,从而导致体内药物总的暴露量更高。
石杉碱甲在AD患者中通常是每天服用,因此消除减缓可能会导致体内药物蓄积,王月娥等[11]在小鼠实验中发现石杉碱甲可经尿液快速清除,认为其体内蓄积风险较小,但本研究中尿液PK数据显示服药后48 h内仅约35%从尿液中清除,提示石杉碱甲在老年人体内仍有蓄积的风险,应在临床用药中予以关注。然而,由于没有直接的对照研究设计,不能排除这些差异受到不同研究在制剂、试验设计和分析方法等方面不一致的影响。除此之外,男性老年受试者t1/2较女性显著延长,此类性别差异在以往的研究中没有报道,具体机制有待进一步探究。
综上所述,石杉碱甲在中国老年受试者中安全性、耐受性良好。药动学数据显示,与健康非老年受试者相比,老年受试者的AUC更高、tmax和t1/2更长,说明老年人服用石杉碱甲后的暴露程度更高,吸收和消除过程更缓慢,临床应用中需要引起注意。
