立体定向放疗联合XELOX方案治疗结直肠癌肝转移的临床效果
2021-06-11李宏雨
李宏雨
(鄢陵县中医院 肿瘤内科,河南 许昌 461200)
结直肠癌肝转移(colorectal liver metastasis,CLM)是结直肠癌发展到晚期的不良事件之一,其病死率较高,由于病灶大多无法根治切除,因而临床治疗时多进行放疗、化疗[1]。其中卡培他滨联合奥沙利铂(XELOX)方案是临床治疗结直肠癌、胃癌等较常用的辅助性方式;立体定向放疗(stereotactic body radiation therapy,SBRT)可精确定位病灶治疗靶区,提高局部病灶放射效果[2]。两种治疗方案均可一定程度上延长患者的生存时间,但两者联合治疗CLM的研究相对较少。本研究选取2018年6月至2020年6月鄢陵县中医院收治的100例CLM患者作为研究对象,探讨SBRT联合XELOX方案治疗CLM的临床效果,以期为临床治疗方案的制定提供参考。
1 资料与方法
1.1 一般资料选取2018年6月至2020年6月鄢陵县中医院收治的100例CLM患者作为研究对象,根据治疗方式分为对照组(XELOX方案治疗)和观察组(SBRT联合XELOX方案治疗),各50例。对照组:男29例,女21例;年龄43~71岁,平均(58.12±2.41)岁;结肠癌28例,直肠癌22例。观察组:男30例,女20例;年龄40~73岁,平均(58.11±2.38)岁;结肠癌31例,直肠癌19例。两组性别、年龄、疾病类型比较,差异无统计学意义(P>0.05)。本研究经鄢陵县中医院医学伦理委员会审批。
1.2 选取标准(1)纳入标准:①符合CLM相关诊断标准[3]且病理活检、CT或MRI检查证实为CLM;②美国东部肿瘤协作组评分[4]≤2分;③病理类型为腺癌且预计生存时间>6个月。(2)排除标准:①骨髓造血功能异常;②合并严重基础疾病;③治疗时更改治疗方案;④临床资料缺失。
1.3 治疗方法
1.3.1对照组 接受XELOX化疗方案。入院后,常规进行肝肾功能、血常规等检查。第1~14天口服卡培他滨(齐鲁制药有限公司,国药准字H20143365),服用剂量为1 000 mg·m-2,每日2次,然后停用7 d;第1天,以130 mg·m-2的剂量静滴奥沙利铂(Sanofi-Aventis France,国药准字H20171065)2 h。以21 d为1个周期,治疗2个周期。
1.3.2观察组 接受SBRT联合XELOX化疗。XELOX化疗方案与对照组一致,于化疗当天,接受SBRT治疗,具体方法如下。患者取仰卧位,运用CT扫描患者腹部,层厚5 mm,间距1 mm,确定肿瘤体积、位置。根据CT所采集的数据构建三维图像,根据软件勾画的靶区确定靶体积、临床靶体积、计划靶体积,设立4~6个非共面野,根据直线加速器上已定剂量进行放疗,肿瘤中心剂量为52~68 Gy,同时根据仪器显示情况确保90%的等剂量曲线覆盖了计划靶区,每周3~5次。以21 d为1个周期,连续治疗2个周期。
1.4 观察指标(1)近期疗效。治疗2个周期后,参照RECIST 1.1标准[5]评估近期疗效。完全缓解(complete remission,CR):病灶全部消失且维持>4周。部分缓解(partial remission,PR):与治疗前比较,病灶缩小>30%且维持>4周。疾病进展(progression disease,PD):与治疗前比较,病灶增大≥20%或出现新病灶。疾病稳定(stable disease,SD):介于PR与PD之间。总缓解率(overall response rate,ORR)等于CR例数与PR例数之和除以总例数。(2)血清相关指标:治疗前、治疗2个周期后,清晨取患者肘静脉血3 mL,以3 000 r·min-1转速离心5 min,离心半径为8 cm,取上清液,以酶联免疫吸附法检测血清网膜素-1(omentin-1)、血管生成素-2(angiopoietin-2,Ang-2)水平,试剂盒选自泉州市睿信生物科技有限公司。(3)药物毒副作用:治疗期间,按照WHO规定的抗癌药物的毒副反应相关标准[6]评估(如肝功能损伤、消化道不良反应、骨髓抑制、周围神经毒性等),分为Ⅰ~Ⅳ级。
2 结果
2.1 近期疗效观察组ORR高于对照组(P<0.05)。见表1。
2.2 血清相关指标治疗前,两组omentin-1、Ang-2水平比较,差异无统计学意义(P>0.05);治疗2个周期后,两组omentin-1、Ang-2水平均降低,且观察组omentin-1、Ang-2水平均低于对照组(P<0.05)。见表2。
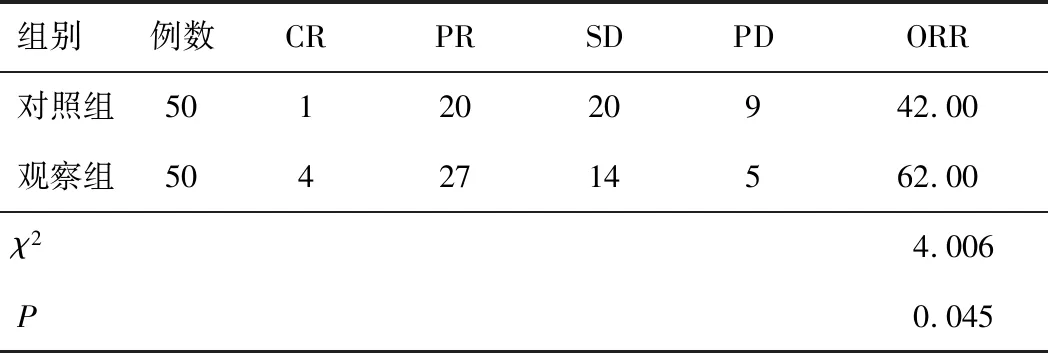
表1 两组近期疗效比较(n,%)
表2 两组治疗前后血清相关指标比较
2.3 药物毒副作用两组肝功能损伤、消化道不良反应、骨髓抑制、周围神经毒性发生率比较,差异无统计学意义(P>0.05)。见表3。
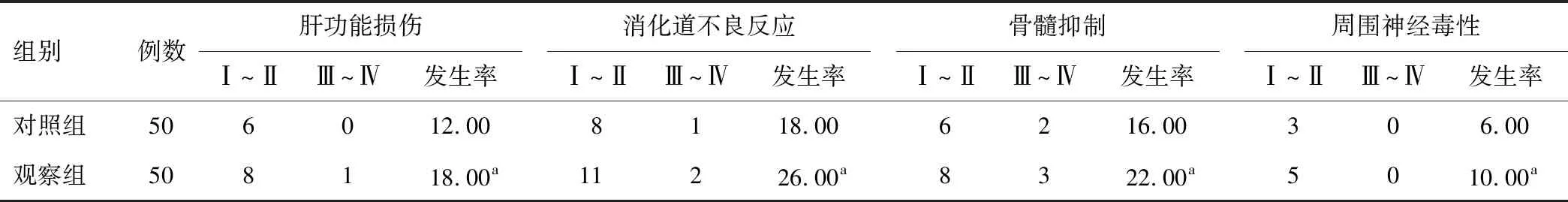
表3 两组药物毒副作用比较(n,%)
3 讨论
虽然CLM病灶大多无法进行外科切除,但由于病灶在一段时间内仅局限于肝脏内,因而积极治疗肝转移病灶对延长患者生存期具有积极作用。XELOX方案虽然是临床推荐治疗CLM的方案之一,但由于化疗药物的作用及机体耐受力等原因,毒副作用较多,因而寻找更为安全有效的治疗方案具有必要性。
相关研究发现,SBRT可通过对病灶高剂量照射来消灭肿瘤细胞,对提高临床治疗效果具有一定的作用[7]。本研究发现,观察组ORR高于对照组,提示了对CLM患者采用SBRT联合XELOX方案可提高近期疗效。分析其原因可能是:XELOX方案中卡培他滨在胸腺磷酸化酶作用下转化为5-氟尿嘧啶,杀伤肿瘤细胞,奥沙利铂可抑制恶性肿瘤DNA的合成,促使癌细胞凋亡,且两者具有协同作用[8]。SBRT可使最高剂量聚焦于肿瘤中心,同时依据肿瘤的深度调整剂量点位置,消灭恶性肿瘤的同时最大限度降低对正常组织的损伤,因而与XELOX方案联合运用后可进一步提高临床疗效[9]。
omentin-1是一种脂肪因子,与恶性肿瘤的发生发展关系密切,可促进结肠癌细胞的增殖,抑制其凋亡;Ang-2可调节肿瘤血管的生成,而肿瘤侵袭转移过程伴随血管的生成,因而观察两指标的变化可评估治疗效果[10]。本研究结果显示,治疗2个周期后,观察组omentin-1、Ang-2水平均低于对照组,表明SBRT联合XELOX方案治疗CLM可降低血清omentin-1、Ang-2水平。分析其原因可能是,omentin-1、Ang-2水平参与肿瘤增殖、转移的进程,而SBRT联合XELOX方案可抑制肿瘤细胞的增殖,因而导致其水平降低。此外,本研究结果显示,两组肝功能损伤、消化道不良反应、骨髓抑制、周围神经毒性发生率比较无明显差异,可见SBRT联合XELOX方案治疗CLM未增加不良反应,可能与SBRT尽量减少对周围组织的放射有关。
综上所述,对CLM患者采用SBRT联合XELOX方案可提高近期疗效,降低血清omentin-1、Ang-2水平,且不增加药物毒副作用,是较为有效的治疗方案。
