Ru Cs/Mo2C纳米棒制备及电催化析氢的研究
2021-06-09秦伟艳
秦伟艳
(西安航空职业技术学院航空维修工程学院,西安 710089)
0 引 言
电催化析氢反应(HER)是实现间歇可再生能源(如太阳能和风能)的高效存储和转换的关键。众所周知,铂(Pt)是目前最高效的电解水析氢催化剂,具有优异的产氢性能[1-2]。然而,稀缺和高昂的价格限制了其大规模应用。近年来,HER在酸碱性电解液下获得较大的研究进展,但仍存在一系列问题,如离子交换膜昂贵、酸碱雾会污染氢气和电解液的强腐蚀性等。中性电解液具有反应条件温和、催化剂兼容性广泛和安全性高等优点[3-4]。寻找在中性电解液中具有优异的HER催化性能和稳定性的催化剂已成为目前的研究热点。近几年,过渡金属碳化物,例如WC(碳化钨)[5]、W2C(碳化二钨)[6]、Mo2C(碳化钼)[7-8]、MXenes(二维过渡金属碳化物、氮化物或碳氮化物)[9]等,具有与Pt高度相似的d带电子结构,且在各种电解液中具有强稳定性,表现出优异的电催化性能[10-11]。然而过渡金属催化剂在电催化产氢中存在过电压过高、效率较低的问题。
相比于Pt,钌(Ru)成本低,仅为Pt成本的1/25,具有类Pt-H键结合的强度和高的稳定性,被认为是潜在的Pt催化剂替代品[12]。若能将Ru以原子或簇的形式高度分散在合适的基底上,不仅可以减少Ru用量,同时暴露更多的活性位点,达到类Pt催化剂的HER性能[13]。因此,开发出一种简单和低成本的方法合成单原子或簇电解水析氢催化剂仍具有重要的研究意义[14]。本文采用简单的溶剂热法将钌纳米簇(Ru Cs)高度分散过渡金属碳化钼(Mo2C)上得到纳米棒复合材料(Ru Cs/Mo2C)。复合催化剂材料能有效降低贵金属使用量,实现中性电解液下高效的电催化析氢和稳定性,为昂贵的商业化Pt催化剂提供了一种较好的代替品。
1 实 验
1.1 化学试剂及试验仪器
钼酸铵((NH4)6Mo7O24·4H2O,分析纯)采购于天津市化学试剂第四厂凯达化工厂;四氯合铂酸钾(K2PtCl4,质量分数99.99%),氢氧化钾(KOH,分析纯),乙二胺(C2H8N2,分析纯)和聚乙烯吡咯烷酮((PVP)(C6H9NO)n,分析纯)均采购于国药集团化学试剂有限公司;浓硫酸(H2SO4(质量分数98%)),乙二醇((EG)(CH2OH)2,分析纯)采购于广州光华试剂有限公司;无水乙醇(CH3CH2OH,分析纯)采购于天津富宇精细化工有限公司;萘酚(5%Nafion,Sigma试剂);蒸馏水(H2O),实验室自制;氩氢气体(Ar/H2(V(H2) ∶V(Ar)=9 ∶1)),采购于西安快特气体公司。X射线衍射仪(XRD)(Bruker AXS-D8,Cu Kα辐射,λ=0.154 18 nm,测试范围2θ角为30°~80°)。场发射扫描电子显微镜(FESEM,型号Hitachi SU-8010,3 kV),透射电子显微镜(TEM,型号FEI TALOS F200X,200 kV)和X射线光电子能谱(XPS,型号PHI 5000 VersaProbe II XPS)。
1.2 7.79%Ru Cs/Mo2C催化剂的制备
1.2.1 Mo2C载体的合成
将1.24 g(NH4)6Mo7O24·4H2O、890 μL C2H8N2溶于30 mL水中,然后在搅拌下滴加1 mol/L HCl溶液调至pH值约为4~5。所得溶液放入反应釜120 ℃水热反应6 h,随后用乙醇抽滤冲洗,得到的白色前驱体90 ℃干燥,即Mo3O10(C6H8N)2·2H2O。将100 mg Mo3O10(C6H8N)2·2H2O放入管式炉中在体积比V(H2) ∶V(Ar)=1 ∶9气氛下以5 ℃/min的升温速率升至650 ℃维持2 h,自然冷却至室温,得到Mo2C纳米棒。
1.2.2 7.79%Ru Cs/Mo2C催化剂的合成
首先,将10 mg RuCl3溶于2 mL乙二醇(EG)中得到溶液A,将PVP溶于2 mL EG中得到溶液B,将50 mg Mo2C分散在15 mL EG中得到分散液C。然后,将溶液C在120 ℃油浴下剧烈搅拌1 h。随后将溶液A和溶液B同时逐滴加入到溶液C中,接着在120 ℃下搅拌17 h后将沉淀物离心并用无水乙醇洗涤数次,90 ℃下干燥12 h,记为Ru Cs/Mo2C。通过电感耦合等离子体(ICP) 测量Ru Cs/Mo2C样品中Ru的精确质量分数为7.79%,记为7.79%Ru Cs/Mo2C。
1.2.3 3.68%Ru Cs/Mo2C和13.8%Ru Cs/Mo2C催化剂的合成
与7.79%Ru Cs/Mo2C催化剂的合成方法类似,不同之处在于原料RuCl3的加入量不同,合成3.68%Ru Cs/Mo2C催化剂时需加入5 mg RuCl3,合成13.8%Ru Cs/Mo2C催化剂时需加入20 mg RuCl3,其他条件不变,通过电感耦合等离子体测量得到实际负载量。
1.3 电化学性能测试
所有电化学测量在CHI 700E电化学工作站(CH Instruments Inc.)进行,使用标准三电极体系进行测量,涂有样品的玻碳电极,饱和Ag/AgCl电极和碳棒电极分别作为工作电极,参比电极以及对电极。本研究中所有电位均参考可逆氢电极(RHE),根据E(RHE)=E(Ag/AgCl)+0.197+0.059×pH进行换算。工作电极的制备:将5 mg催化剂和100 μL 5%Nafion溶液分散在900 μL乙醇中并超声处理30 min以形成均匀的墨汁,然后取5 μL墨汁滴加到直径为3 mm的玻碳电极上, 负载量为0.35 mg·cm-2。电化学性能测试在磷酸缓冲液(PBS,1 mol/L,pH=7)中进行。通过计时电压法和连续CV循环测试催化剂的稳定性。
2 结果与讨论
2.1 结构表征
首先,研究7.79%Ru Cs/Mo2C催化剂微观结构。图1为Mo2C的SEM和HRTEM照片,从图1可以看出,Mo2C为均匀的纳米棒,且TEM照片晶格明显。图2(a)、(b)和(c)为Ru Cs/Mo2C催化剂的SEM和TEM照片,表明在负载Ru后形貌并没有发生变化。且和图2(d)的高倍数透射电子显微镜(HRTEM)结果相比较,7.79%Ru Cs/Mo2C的HRTEM照片上多出了Ru的晶格条纹,证实了Ru是以簇的形式存在。层间距为0.238 nm对应于Mo2C的(111)晶面,层间距为0.206 nm对应于Ru的(101)晶面,见图2(e)。图2(f)为Ru Cs/Mo2C的元素分析,纳米棒上均匀的分散Ru、Mo和C元素,综合以上结果证实了Ru以簇的形式高度均匀地分散在Mo2C基底上,成功制备出了7.79%Ru Cs/Mo2C催化剂。另外,7.79%Ru Cs/Mo2C的表面积(36.8 m2/g)相较于纯Mo2C(42.7 m2/g)变小了,纯Mo2C和7.79%Ru Cs/Mo2C的比表面积和孔径分布如图3所示,进一步说明Ru簇成功负载在了Mo2C多孔纳米棒上,Ru进入小孔,降低了纯Mo2C的表面积,进一步说明Ru以簇形式存在。

图1 Mo2C的SEM照片和HRTEM照片Fig.1 SEM image and HRTEM image of Mo2C

图2 7.79%Ru Cs/Mo2C催化剂的结构、形貌和成分分析:(a,b)SEM照片;(c)TEM照片;(d,e)HRTEM照片;(f)Ru、Mo和C元素的EDX映射Fig.2 Structure, morphology and composition analysis of 7.79%Ru Cs/Mo2C catalyst:(a, b) SEM images; (c) TEM image; (d, e) HRTEM images; (f) EDX mapping of Ru, Mo and C elements
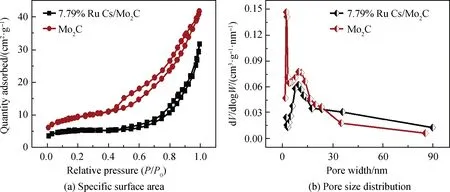
图3 纯Mo2C和7.79%Ru Cs/Mo2C的比表面积和孔径分布Fig.3 Specific surface area and pore size distribution of Mo2C and 7.79%Ru Cs/Mo2C
图4为通过X-射线粉末衍射对材料进行物相表征的XRD和XPS谱。如图4(a)所示,所合成的Mo2C与PDF#15-0457相对应。负载Ru样品后,XRD的衍射峰并没有发生变化。为了证实Ru的存在,对催化剂材料进行了X射线光电子能谱(XPS)的测试,结果如图4(b)和4(c)所示。图4(b)表明,结合能为234.2 eV、232.0 eV、231.1 eV和228.6 eV的峰归属于Mo2C,此外,位于235.3 eV的峰归属于MoO3,这是由于Mo2C表面通过空气接触部分氧化所致[15],进一步证实了该基底材料为Mo2C。图4(c)表明,位于461.5 eV和483.9 eV的结合能的峰归属于金属零价Ru0,证实了在Mo2C上Ru的存在[16]。综合以上的表征分析,初步证实了7.79%Ru Cs/Mo2C催化剂的成功制备。
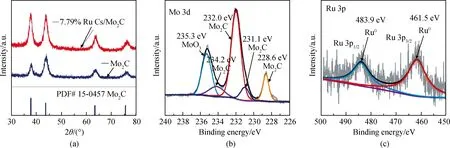
图4 (a)Mo2C和7.79%Ru Cs/Mo2C催化剂的XRD谱以及7.79%Ru Cs/Mo2C催化剂的XPS能谱图:(b)Mo 3d;(c)Ru 3pFig.4 (a) XRD patterns of Mo2C and 7.79%Ru Cs/Mo2C catalyst and XPS spectra of 7.79%Ru Cs/Mo2C catalyst: (b) Mo 3d; (c) Ru 3p
2.2 电催化性能评价
通过三电极系统评估了7.79%Ru Cs/Mo2C在1 mol/L 磷酸缓冲液中的HER性能,并与纯Mo2C和商业化20%(质量分数)Pt/C进行了比较(细节见试验部分),如图5所示。从图5(a)的极化曲线可以看出,合成的3.68%Ru Cs/Mo2C,7.79%Ru Cs/Mo2C和13.8%Ru Cs/Mo2C催化剂的起始电位基本上和20%Pt/C催化剂的起始电位一致,都接近于零。另外,从图5(a)可知,随着Ru负载量的增大,其电流密度也随之增大,然而在增大到一定程度时,其催化性能基本保持不变。另外在-10 mA·cm-2电流密度下7.79%Ru Cs/Mo2C的过电势为104 mV,远远低于纯Mo2C的过电势(244 mV),同时其过电势与20%Pt/C的过电势(105 mV)基本相等。值得一提的是,当电流密度为-100 mA·cm-2时,7.79%Ru Cs/Mo2C的过电势为327 mV,远远小于20% Pt/C催化剂的过电势(428 mV)和纯Mo2C的过电势(454 mV),如图5(b)所示。另外,Tafel斜率值被用来证实电催化HER反应动力学的快慢,其值越小表明动力学速率越快[7]。从图5(c)结果可以看出,7.79%Ru Cs/Mo2C催化剂的Tafel斜率为96.30 mV·dec-1,其值小于纯Mo2C的Tafel斜率值(108.59 mV·dec-1),进一步证实了7.79%Ru Cs/Mo2C催化剂优异的催化动力学。为了进一步了解7.79%Ru Cs/Mo2C催化剂的电子转移能力,对其进行了电化学阻抗测试。从图5(d)的结果表明,与纯Mo2C和20%Pt/C催化剂相比,7.79%Ru Cs/Mo2C催化剂的电荷转移阻抗比Mo2C和20%Pt/C催化剂都要小,表明催化剂界面与电解液之间的电阻降低,电子转移速度加快。为了表征催化剂的催化活性,测试了7.79%Ru Cs/Mo2C催化剂双电层电容(Cdl),其值与电化学活性面积成正比[8]。图5(e)和图5(f)均为不同扫速下的循环伏安(CV)法曲线,从图5(e)和图5(f)中的曲线通过计算0.273 V(versus RHE)下的氧化还原电流差值的绝对值(Δj=ja-jc,ja表示氧化还原电流密度正值,jc表示氧化还原电流密度负值)来得到7.79%Ru Cs/Mo2C和Mo2C的双电层电容(见图5(g))分别为81.88 mF·cm-2和47.80 mF·cm-2,说明7.79%Ru Cs/Mo2C催化剂具有较大的活性面积。催化剂的稳定性也是评价催化剂性能的另一项指标。
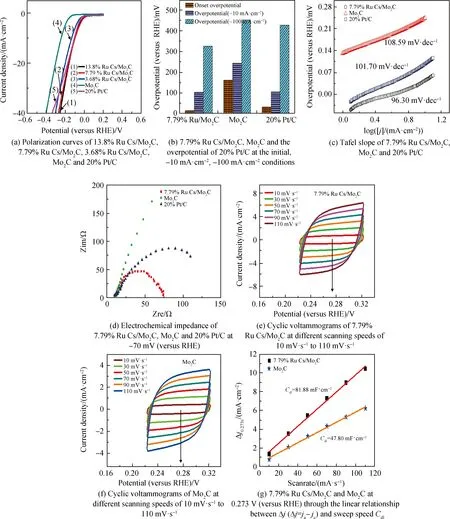
图5 Ru Cs/Mo2C、Mo2C和20%Pt/C样品在1 mol/L PBS中性电解液中的析氢性能对比Fig.5 Comparison of hydrogen evolution performance of Ru Cs/Mo2C, Mo2C and 20%Pt/C samplesin 1 mol/L PBS neutral electrolyte
以100 mV·s-1的扫描速率,在0.4 V和-0.5 V之间通过循环伏安法在中性电解液中进行测试,结果如图6所示。1 000圈前后的极化曲线几乎没有变化,见图6(a)。同时,在-10 mA·cm-2的恒电流密度下,对于Ru Cs/Mo2C催化剂进行时间-电压的测试。图6(b)的结果进一步表明催化剂在中性电解液中优异的稳定性。综上所述,所合成的7.79%Ru Cs/Mo2C催化剂,在中性电解液中表现出优异的电催化活性和极高的稳定性,大大降低了催化剂的生产成本,在未来的清洁能源应用中具有巨大潜力。
3 结 论
通过简单的溶剂热还原方法制备不同负载量的Ru Cs/Mo2C纳米棒催化剂。研究表明钌纳米簇(Ru Cs)高度分散在具有类铂属性的过渡金属碳化钼(Mo2C)上。7.79%Ru Cs/Mo2C催化剂在中性电解液中表现出了优异的电催化性能和稳定性。Ru Cs/Mo2C催化剂降低了贵金属电催化剂的成本,解决了中性电解液中商业化Pt催化剂电催化析氢性能差的问题,为昂贵的商业化Pt催化剂提供了一种较好的代替品。
