FeS与TiO2共存对水泥熟料中Ti的固化与迁移及矿物组成的影响
2021-06-09冯庆革梁思亮柏秀奎王东波赵政术黄丽霖
冯庆革,梁思亮,杨 义,柏秀奎,王东波,赵政术,黄丽霖
(1.广西大学资源环境与材料学院,南宁 530004;2.广西鱼峰集团有限公司,柳州 545000)
0 引 言
利用水泥窑协同处置尾矿时,常常引入S和Ti等元素,不仅会增加水泥窑尾气中SO2的排放,同时也会影响水泥熟料矿物的含量和性质,进而改变熟料质量。TiO2作为水泥熟料中的微量组分,质量分数在0.02%~1.00%之间[1],作为低挥发性元素[2],少量的TiO2在水泥熟料形成过程中起矿化剂作用,可降低液相粘度并稳定β-C2S,张巨松等[3]也认为TiO2对β-C2S具有稳定作用,但Bucchi[4]认为TiO2没有稳定β-C2S的作用。Volkonskii等[5]研究报道,Ti4+能够取代Si4+形成相应的固溶体,导致C3S和C2S的晶体发生畸变,进而促进水泥的水化。据Shang等[6]报道,Ti4+不仅能够替代熟料中的Fe3+,还可以替代Al3+形成固溶体。
众多学者常关注无机硫酸盐对水泥熟料矿物组成[7-11]和微量元素固化迁移的影响[12-15]。然而,水泥原料中亦存在无机硫化物,其会对水泥熟料的矿物形成产生影响。FeS作为无机硫化物的主要来源之一,其对水泥熟料煅烧及质量的影响越来越受到人们重视,FeS反应温度较低,通常在400~700 ℃之间,反应过程中不仅产生SO2,同时由于S2-的存在,使得分解炉内产生氧化还原反应,影响水泥煅烧工艺过程。
实际生产中发现,在水泥协同处置尾矿时,FeS和TiO2同时存在会直接影响水泥熟料强度,产生这种现象的原因未见相关报道。针对这一问题,本文通过掺入不同含量FeS和1.00%(质量分数)TiO2研究FeS和TiO2共存时对水泥熟料中Ti的固化与迁移及矿物组成的影响。
1 实 验
1.1 熟料制备
为避免带入其他元素,采用分析纯试剂制备水泥熟料,设计率值为:石灰饱和系数KH为0.90±0.01,硅率SM为2.5±0.1,铝率IM为1.6±0.1。根据3个率值计算生料中各组成配比和熟料理论矿物组成,见表1,其中S以FeS的形式掺入。按表1制备好生料后,分别称取20.0 g生料加入适量蒸馏水搅拌均匀,压片,置于105 ℃干燥箱内烘干。将压制后的样品放入马弗炉内,以10 ℃/min的速率升温至950 ℃,保温30 min,再以5 ℃/min的速率升温至1 450 ℃,保温60 min后取出,室温冷却,制得水泥熟料。当熟料煅烧温度大于650 ℃时,FeS与O2发生反应(见式(1))会提供Fe2O3[16],为保证煅烧前计算的熟料率值不变,需减少相应Fe2O3的添加量。
4FeS+7O2→2Fe2O3+4SO2
(1)
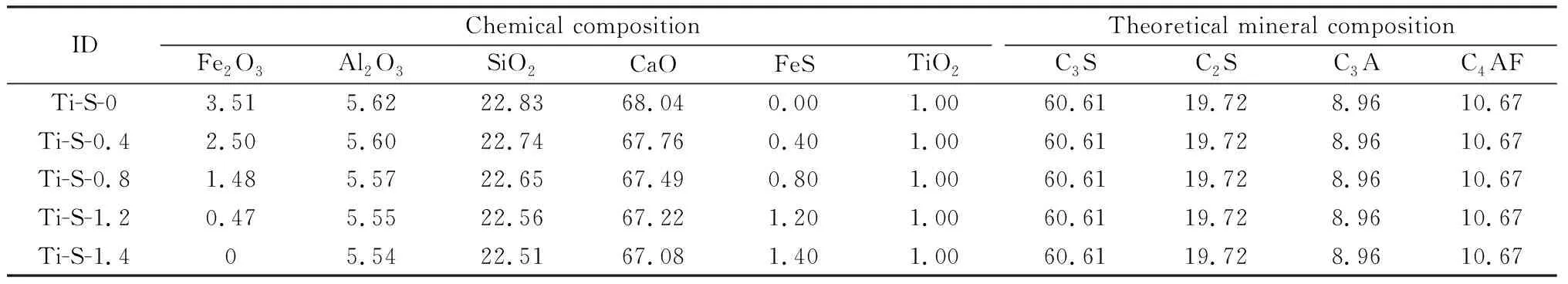
表1 水泥生料的主要化学组成和熟料的理论矿物组成(质量分数)Table 1 Main chemical composition of raw materials and theoreticalmineral composition of clinker (mass fraction) /%
1.2 矿物提取
硅酸盐相:将2.000 g的熟料粉末加入200 mL蔗糖-氢氧化钾溶液中(100 g蔗糖,100 g 氢氧化钾,1 000 g水),在常温下磁力水浴锅中加热至95 ℃并搅拌25 min,用布氏漏斗进行抽滤,残渣先用热水洗涤1次,再用甲醇洗涤5次,在105 ℃烘干至恒重。
中间相:将6.000 g熟料加入200 mL水杨酸-甲醇溶液中(水杨酸与甲醇质量比为1 ∶5),常温下,用磁力搅拌75 min,用布氏漏斗和慢速滤纸过滤,残渣用甲醇溶液洗涤5次,在105 ℃烘干至恒重。
1.3 性能表征
1.3.1 Ti含量测量
样品经过HCl-HNO3-HF-HClO混合液消解之后,采用 NEXION 350X型电感耦合等离子体发射光谱仪(ICP-OES)测量熟料、硅酸盐相和中间相中的Ti含量,并计算Ti固化率R,如式(2)所示。
(2)
式中:K为单位质量水泥熟料中Ti的含量,mg/g;C为单位质量水泥生料中Ti的含量,mg/g;L为煅烧过程中生料的烧失量,%。
1.3.2 EDS测试
将块状熟料进行打磨、抛光和喷金之后,用HORIBA EX-350型能量色散光谱仪(EDS)进行检测得到水泥熟料中元素分布图,加速电压为20 kV。
1.3.3 XRD测试
用Rigaku D/MAX 2500V型X射线衍射仪(XRD)进行物相表征,并结合Rietevld全谱拟合法对熟料矿物组成进行定量分析,测试条件:Cu Kα(λ=0.150 46 nm),管电压40 kV,管电流100 mA,角度2θ=10°~70°,步长0.02°,速度5(°)/min。
1.3.4 XPS测试
用Thermo Scientific ESCALAB 250XI型X射线光电子能谱仪(XPS)对熟料中的表面元素进行定性/定量分析,测试条件:Al Kα(hv=1 486.6 eV),功率150 W,500 μm束斑,C1s(284.8 eV)校准。
2 结果与讨论
2.1 FeS对Ti固化及迁移分布的影响
不同FeS掺量下Ti在水泥熟料中的固化率如图1所示。由图1可见,Ti的固化率并未随FeS掺量增加发生明显变化,说明FeS掺入对水泥熟料固化Ti的能力影响不大,这与Kolovos等[17]报道的结果一致。但是,FeS的掺入使得Ti由中间相向硅酸盐相迁移,结合图2不同FeS掺量下Ti在硅酸盐相和中间相中的含量可知,随着FeS掺量增加,Ti在硅酸盐相中含量增加,而在中间相中含量减少。
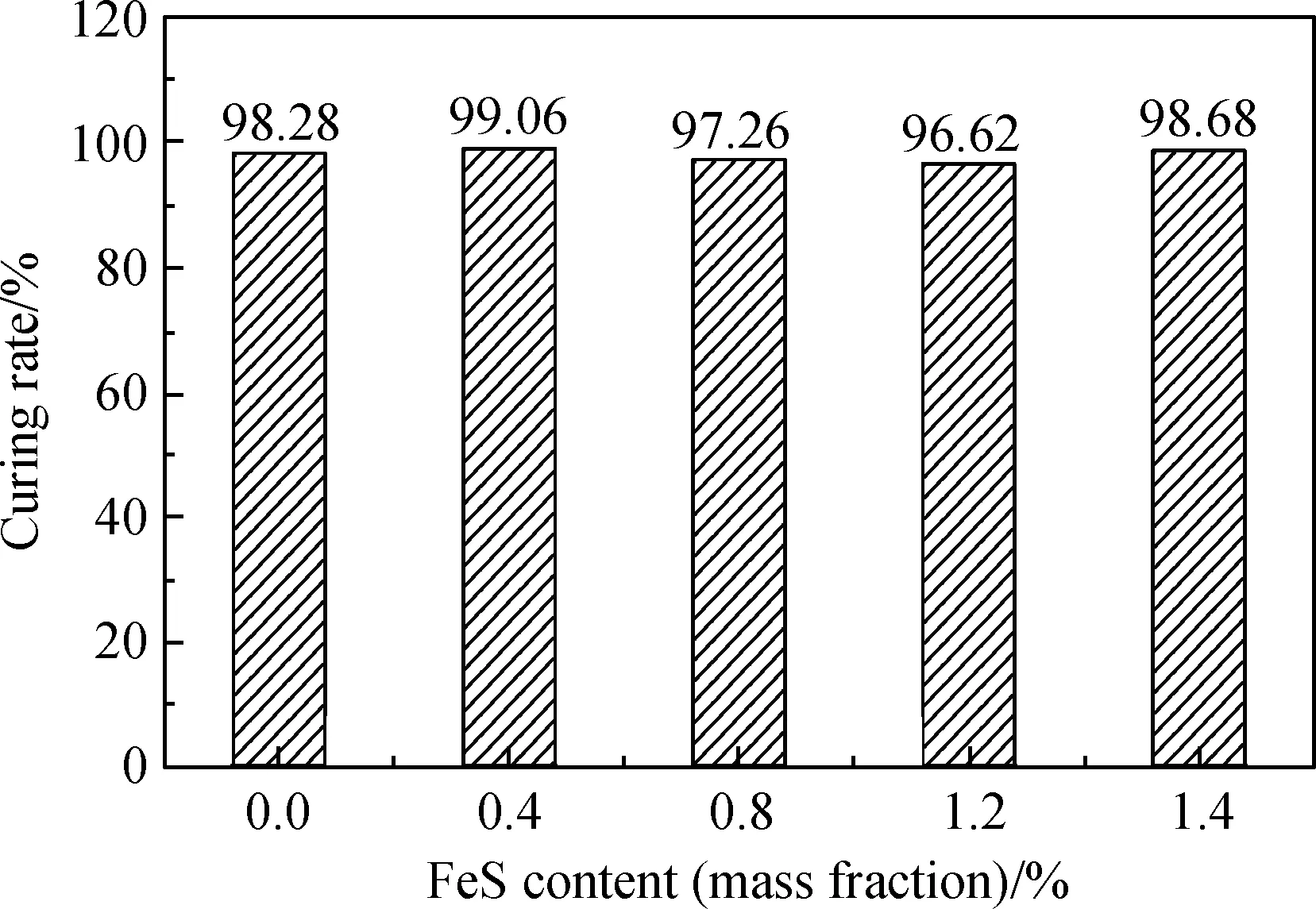
图1 不同FeS掺量下Ti在水泥熟料中的固化率Fig.1 Curing rate of Ti in cement clinkerwith different FeS content

图2 不同FeS掺量下Ti在硅酸盐相和中间相中的含量Fig.2 Ti content in silicate phase and intermediatephase with different FeS content
为进一步分析FeS的掺入对水泥熟料中Ti迁移与分布的影响,对Ti-S-0、Ti-S-0.8和Ti-S-1.4熟料进行EDS点扫描,通过EDS点扫描得到的化学组成计算所测点的摩尔比,以便确认该点对应的矿物相。每种矿物相随机选取5个扫描点,取平均值作为矿物相中Ti含量,结果如图3所示。由图3可知,随着FeS掺量的增加,Ti在中间相C3A和C4AF中的含量逐渐减少,在硅酸盐相C3S和C2S中的含量逐渐增加。相对于Ti-S-0样品,Ti-S-1.4样品中Ti在C3S、C2S中的含量分别增加了26.1%、46.9%,而在C3A、C4AF中Ti含量则分别减少了13.0%、6.2%。
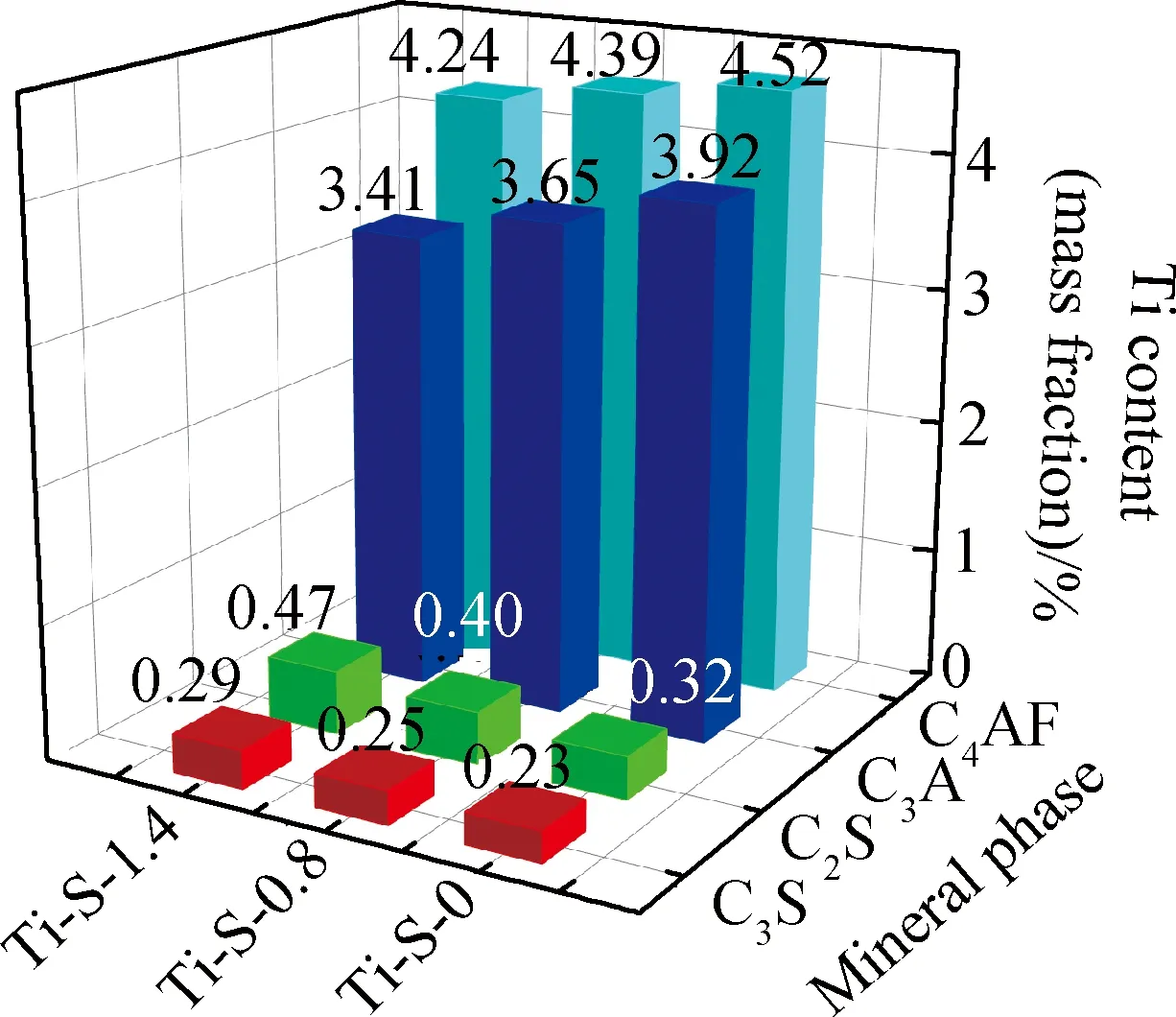
图3 Ti在熟料各矿物相中的含量图3 Ti content in each mineral phase of clinker
2.2 FeS和TiO2共存下熟料中离子的化学价态变化
FeS在熟料煅烧过程中发生氧化还原反应,对熟料中离子化学价态产生影响,为此对Ti-S-0、Ti-S-0.8和Ti-S-1.4三个样品进行XPS测定,结果如图4~图6所示。其中Si2p的高斯拟合峰对应的是[SiO4]4-四面体中的Si-O键,硅离子为+4价;Ca2p的一对高斯拟合峰Ca2p3/2和Ca2p1/2对应的是Ca-O键,钙离子为+2价;Al2p的高斯拟合峰对应[AlO4]4-四面体中的Al-O键,铝离子为+3价;Ti的一对高斯拟合峰Ti2p3/2和Ti2p1/2对应Ti-O键,钛离子为+4价;S的高斯拟合峰S2p对应硫酸盐中的S-O键,硫离子为+6价。FeS的掺入使Fe价态发生了显著变化,未掺入FeS时,如图4(e)所示,Fe仅存在一对高斯拟合峰Fe2p3/2和Fe2p1/2;掺入FeS后,如图5(f)和图6(f)所示,Fe同时存在两对Fe2p的高斯拟合峰,其中处于较低能级的一对高斯拟合峰Fe2p2/3和Fe2p1/2对应FeO中的Fe-O键,而处于较高能级的一对高斯拟合峰Fe2p2/3和Fe2p1/2对应Fe2O3中的Fe-O键,说明FeS的掺入使铁离子以+2价和+3价形式存在熟料中。
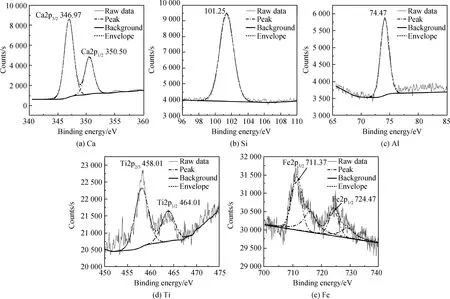
图4 Ti-S-0熟料中Ca、Si、Al、Ti、Fe的XPS谱Fig.4 XPS spectra of Ca, Si, Al, Ti and Fe in Ti-S-0 clinker
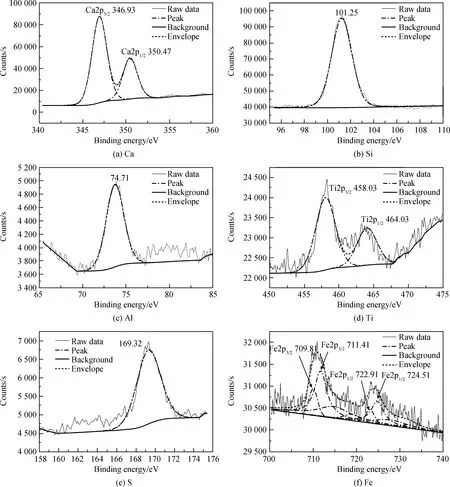
图5 Ti-S-0.8熟料中Ca、Si、Al、Ti、S、Fe的XPS谱Fig.5 XPS spectra of Ca, Si, Al, Ti, S and Fe in Ti-S-0.8 clinker
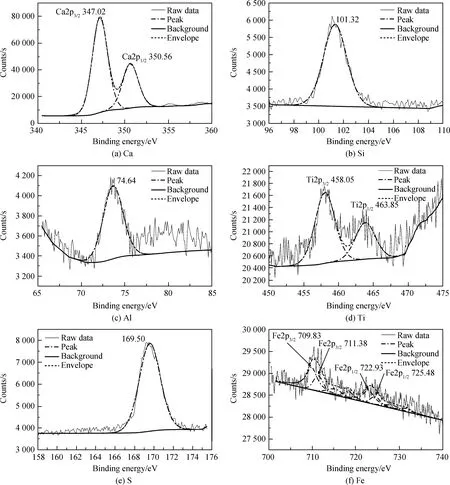
图6 Ti-S-1.4熟料中Ca、Si、Al、Ti、S、Fe的XPS谱Fig.6 XPS spectra of Ca, Si, Al, Ti, S and Fe in Ti-S-1.4 clinker
根据结晶学理论[18],外来离子取代熟料中离子的能力与离子半径、电价、电负性等化学结构参数有关,表2为熟料中各离子的基本参数。按照外来离子进入晶体结构位置的不同,可将固溶体分为置换型固溶体和间隙型固溶体。由于熟料中晶体结构的间隙空间有限,只能容纳一些半径较小的离子(如H、C和N等离子),而熟料中的离子半径相对较大,很难进入晶体结构的间隙中[19]。因此,为分析不同离子价态间的取代固溶,引入结构性差异因子D[20-21]与Hume-Rothery 经验公式Δr[21],其中,Δr表示在置换固溶体中,原子或离子的大小对形成连续或有限置换固溶体的影响能力,即相互替代的原子或离子尺寸愈接近,则固溶体愈稳定。
(3)
式中:R为不同离子半径,pm;Rm为相应离子半径,pm;Δx为不同离子与相应离子的电负性之差;Z为不同离子的电价。
(4)
式中:r1为半径大的溶剂(基质晶体)的离子或原子半径;r2为半径小的溶质(杂质)离子或原子半径。当Δr小于15%时,溶质与溶剂之间可以形成连续固溶体;当Δr在15%~30%时,溶质与溶剂之间可以形成有限型固溶体;当Δr大于30%时,溶质与溶剂之间很难形成或不能形成固溶体,更倾向于形成中间相或化合物[21]。
图7为Fe2+、Fe3+分别与Ca2+、Si4+的D值和Δr值,图8为Ti4+分别与Fe2+、Fe3+、Ca2+、Si4+的D值和Δr值。从图7(a)中可看出,Fe2+与Ca2+的D值和Δr值分别为0.402和24.24%,均低于Fe3+和Ca2+,说明Fe2+较Fe3+更容易取代Ca2+而进入熟料矿物中,因而FeS掺入带来的Fe2+增加,使硅酸盐相中的Fe2+相应增加。从图7(b)可知,Fe2+、Fe3+与Si4+的D值分别为0.116和0.097,而Δr值均大于30%,表明Fe2+、Fe3+不易取代Si4+。由图8可知,Ti4+与Fe2+的D值和Δr分别为0.108和9.33%,均低于Ti4+与Fe3+,说明Ti4+更容易取代熟料中的Fe2+,其次是Fe3+。此外,Ti4+分别与Ca2+、Si4+的D值和Δr值远高于Ti4+与Fe2+、Fe3+,故Ti4+取代熟料中离子的可能性大小为Fe2+>Fe3+>Ca2+>Si4+。综合以上分析和图3可知,FeS引起Ti迁移的原因可能是Fe2+取代C2S中Ca2+后再被Ti4+取代,从而使Ti在硅酸盐相中含量增加,在中间相中含量减少。

表2 熟料中各离子的基本参数[22]Table 2 Basic parameters of each ion in clinker[22]

图7 Fe2+、Fe3+分别与Ca2+、Si4+的D值和Δr值Fig.7 D value and Δr value of Fe2+ and Fe3+ with Ca2+ and Si4+ respectively

图8 Ti4+分别与Fe2+、Fe3+、Ca2+、Si4+的D值和Δr值Fig.8 D value and Δr value of Ti4+ with Fe2+, Fe3+, Ca2+ and Si4+ respectively
2.3 FeS和TiO2共存对熟料矿物组成的影响
图9为不同熟料样品的XRD谱。从图9(a)中可看出,随着FeS掺量增加,C3S特征峰(2θ=51.6°)和C4AF特征峰(2θ=12.2°)强度逐渐减弱,C2S特征峰(2θ=31.0°)和C3A特征峰(2θ=33.3°)强度逐渐增强。单掺Ti时,在晶面间距d=2.711 5 nm(2θ=33.0°)处出现α-C2S衍射峰,随着FeS掺量的增加,α-C2S衍射峰强度逐渐增强,表明Ti的掺入能够使C2S以高温型α-C2S存在,而FeS的掺入促进α-C2S的形成。从图9(b)可看出,随着FeS掺量的增加,α-C2S的晶面间距d值逐渐增大(2.711 5 nm→2.712 5 nm→2.713 4 nm→2.714 9 nm→2.716 8 nm),表明FeS的掺入促进Ti4+进入α-C2S晶体中,且Ti4+的半径(68 pm)大于Si4+的半径(41 pm),使得硅氧四面体晶格膨胀变形,晶胞变大,晶面间距d值随之增大。
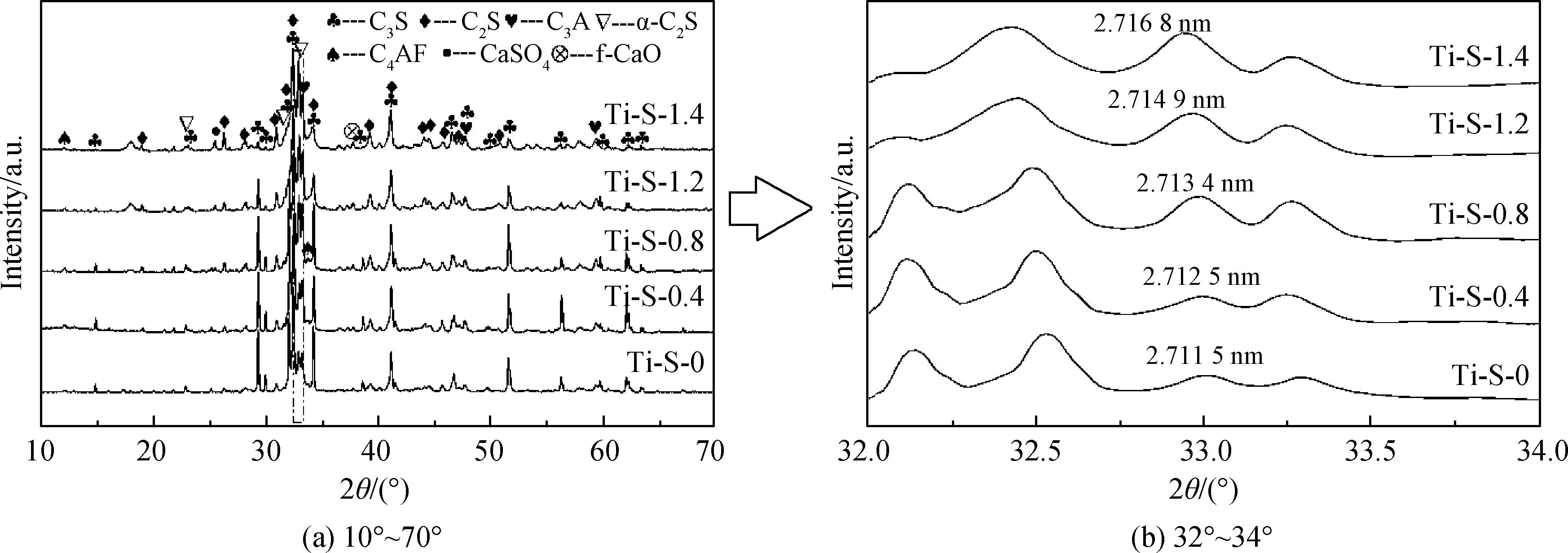
图9 不同FeS掺量下熟料的XRD谱Fig.9 XRD patterns of clinker with different FeS content
表3为Rietveld全谱拟合法计算的不同FeS掺量下熟料矿物的含量。从表3中可看出,随着FeS掺量的增加,C2S、C3A含量分别增加了18.12%~69.39%、4.43%~35.35%,C3S、C4AF含量分别减少了16.66%~67.50%、2.73%~23.30%。朱晓燕等[23]研究表明,熟料中Fe2+的存在易引起阿利特分解,形成二次贝利特和f-CaO。当熟料中Fe2+含量增加时,C2S含量逐渐增加,甚至可达71%[24]。通过对Ti-S-0、Ti-S-0.8、Ti-S-1.4熟料样品进行Fe元素的XPS分析得出,未掺FeS时,如图4(e)所示,仅有Fe3+的高斯拟合峰。当FeS掺入后,如图5(f)和图6(f)所示,出现Fe2+的高斯拟合峰。随着FeS掺量的增加,Fe2+/Fe3+摩尔比从0增加至1.88,即熟料中Fe2+含量逐渐增加,导致C2S含量显著增加。由于熟料中Fe2+的存在,C3A无法吸收足够Fe3+形成C4AF,导致C4AF含量减少,C3A含量增加。此外,熟料中CaSO4含量的增加,消耗熟料体系中的CaO,导致C2S无法吸收足够的CaO形成C3S,进而阻碍C3S的形成,但由于Fe2+的存在易使得熟料中CaO的含量增加。因此,熟料中Fe2+和CaSO4含量的增加,均不利于C3S的形成,C2S含量随之增加。

表3 Rietveld全谱拟合计算不同FeS掺量下熟料矿物的含量Table 3 Mineral content of clinker with different FeS content calculated by Rietveld full spectrum fitting
通过计算Fe2+与Al3+的D值(0.220)和Δr值(50%>30%)可知,Fe2+难以取代C3A中的Al3+形成C4AF。因此,熟料中的C3A含量增加,C4AF含量减少。
3 结 论
(1)FeS的掺入对熟料固化Ti的能力影响较小,但随着FeS掺量增加,Ti由C3A向C2S迁移,使C2S中Ti的含量增加,其原因可能是FeS掺入引起Fe2+取代C2S中Ca2+后,再被Ti4+所取代。
(2)Ti4+能够稳定高温型α-C2S,而FeS的掺入能够促进Ti4+进入C2S晶格中,使得α-C2S的晶面间距增大,进而增强硅酸盐相对Ti固化的能力。
(3)随着FeS掺量增加,熟料中Fe2+/Fe3+摩尔比从0增至1.88,导致C3S和C4AF含量逐渐降低,C2S和C3A含量逐渐增加。此外,生成CaSO4亦不利于C3S的形成。
