原子荧光法测定绞股蓝茶中硒含量的方法及不确定度的评定
2021-06-09景文祥
景文祥,喻 莉,刘 欢,余 英
1. 宜宾林竹产业研究院,四川 宜宾 644000;2. 西南科技大学 材料科学与工程学院,四川 绵阳 621000;3. 四川中电福溪电力开发有限公司,四川 宜宾 645100;4. 四川威尔检测技术股份有限公司,四川 成都 610041
绞股蓝(Gynostemma pentaphyllum (Thunb.) Makino),草本攀援类植物,又名“五叶参”、“七叶胆”,含有多种与人参皂苷相同的成分[1-3],具有益气健脾、化痰止咳、清热解毒的功效[4-5]。绞股蓝茶采用绞股蓝叶腋部位的嫩芽和龙须制备,茶汤碧绿,味清香、微苦,入喉回甘。绞股蓝茶中含有丰富的皂苷及微量元素[6],具有降“三高”、延缓衰老、调节脂肪代谢、抗癌[7]等作用,因此深受大众喜爱[8-10]。
硒(Se)在自然界中以无机硒和有机硒两种状态存在[11],在人体内具有调节机体免疫、血糖、血脂、抗氧化、心血管、视力等生理活性。当人体内含有较高的血硒水平和较低的血硒水平均会导致一些疾病。硒在人体内安全范围较窄,仅差1 ~ 2个数量级[12-13]。故对于食品中硒含量的准确、高效、简便分析方法及不确定度的评定在生产和食品安全上具有很高的价值。目前,茶叶中硒含量的测定标准采用GB/T 5009.93—2017,采用湿法或微波进行消解结合ICP-MS法[14]、荧光分光光度法[15]、原子荧 光法[16-17]进行定量分析,但由于消解及赶酸温度、时间等条件凭经验判断,具有不确定性,导致结果不能精确控制。本试验以绞股蓝茶为研究对象,采用微波消解——原子荧光法测定其中硒的含量,优化了仪器分析条件并进行了不确定度的评定,可为绞股蓝茶企业及相关检测机构提供技术支持。
1 材料与方法
1.1 材料与试剂
绞股蓝茶购自平利县百草堂生物科技有限公司。硒标准溶液,GSB G62029—90(3401),购自国家钢铁材料测试中心钢铁研究总院。生物质成分分析标准物质芹菜,GBW10048(GSB-26),购自地球物理地球化学勘察研究所。
盐酸(GR),重庆川东化工(集团)有限公司;硝酸(GR)、铁氰化钾(AR)、氢氧化钾(GR)、硼氰化钾(GR)、铁氰化钾(AR),均购自成都市科隆化工试剂厂;实验用水为实验室自制超纯水,电阻率≥18.25 MΩ·cm。
1.2 仪器与设备
PF6-1型原子荧光分光光度计,北京普析通用仪器有限公司;AR124CN型电子分析天平,奥豪斯仪器(上海)有限公司;WX-8000型微波消解仪,上海屹尧仪器科技发展有限公司;G-160型智能控温电加热器,上海屹尧仪器科技发展有限公司;实验室常用玻璃量器均为A级且检定合格,使用前经1∶5(V/V)的硝酸-水溶液浸泡12 h以上。
1.3 实验方法与不确定度评定
1.3.1 样品消解
称取一定质量的样品(精确至0.0001 g)于消解管中,加入5 mL硝酸,加盖过夜,然后进行微波消解。待样品消解完全、冷却、排气后,将消解管置于智能控温电加热器中,一定温度下加热至近干,再加 5 mL 的 6 mol/L HCl-H2O溶液,继续加热至溶液呈现清亮无色或略微泛黄,放置冷却,用水多次洗涤消解管,合并洗涤液至 25 mL 容量瓶中,加入 6.25 mL 的 10 g/L K3[Fe(CN)6]-H2O溶液,用水定容,摇匀,备用。同时按上述方法制备空白试剂3份[18-20]。
1.3.2 仪器检测条件
按一定的负高压、灯电流(主灯电流、辅灯电流设定值相同,下同)、载液浓度、还原剂(硼氰化钾碱液)浓度、载气流速、屏蔽气流速下进行测定,读数时间12 s,延迟时间3 s,原子化器温度200℃,炉高8 mm,载液第一次进样量1.5 mL,载液第二次进样量1.5 mL,样品进样量1.0 mL,采用自动进样方式,测定波长为196.0 nm,计算方式为峰面积,平行测定3次取平均值,记录数据。
1.3.3 硒元素标准曲线的绘制
100 μg/mL硒的标准溶液:精确吸取1.00 mL 的 1000 μg/mL 硒的标准溶液于 10 mL 容量瓶中,5 %(V/V)的盐酸-水溶液定容,混匀。
1 μg/mL 硒的标准溶液:精确吸取 1.00 mL的100 μg/mL硒的标准溶液于100 mL容量瓶中,5 %(V/V)的盐酸-水溶液定容,混匀。
硒元素标准曲线:分别取1 μg/mL的硒的标准溶液 0 mL、0.1 mL、0.2 mL、0.3 mL、0.4 mL、0.5 mL 于 100 mL 容量瓶中,加入 100 g/L的 K3[Fe(CN)6]-H2O 溶液 10 mL,用 5 %(V/V)盐酸-水溶液定容,混匀,待测。
1.3.4 数学模型的建立和不确定度来源分析
绞股蓝茶中硒的含量X按公式(1)计算[21-22]

式中:X—绞股蓝茶中硒的含量,mg/kg;c —待测液中硒含量,ng/mL;V—待测样品定容体积,mL;m—绞股蓝茶称样质量,g;f—稀释倍数。
影响绞股蓝茶中硒含量测定结果的不确定度来源[23-25]及评定见表1。

表1 不确定度来源及评定方法Table 1 Source of uncertainty and method of evaluation
2 结果与分析
2.1 绞股蓝茶中硒含量的测定
2.1.1 微波消解升温程序优化
由于现行标准GB/T 5009.93—2017在消解、赶酸时温度、时间等条件凭现象及经验,具有一定的不稳定性,故笔者通过试验对微波消解过程及赶酸过程进行了优化,当升温程序按照表2设定,消解完成后在170℃条件下加热至近干时,消解时间最短,溶液澄清透明,效果最好,回收率较高。
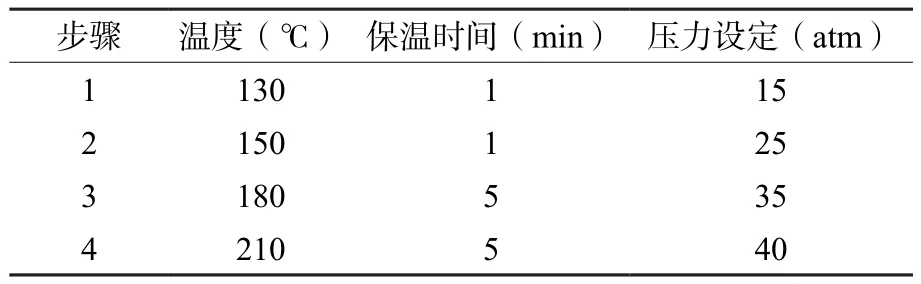
表2 微波消解程序Table 2 Procedure of microwave digestion
2.1.2 负高压对硒元素荧光值的影响
按照1.3.2设定仪器检测条件,将负高压分别设定为 230 V、250 V、270 V、290 V、310 V,灯电流为50 mA,载液为5 %(V/V)盐酸-水溶 液,还原剂为8 g/L硼氰化钾碱溶液(称取8 g 硼氰化钾溶解于1 L的5 g/L的KOH-H2O溶液中,下同),载气流速为400 mL/min,屏蔽气流速为 600 mL/min,在该条件下测定 0.75 ng/mL 硒的标准溶液,平行测定三次,结果取平均值,结果如图1所示。
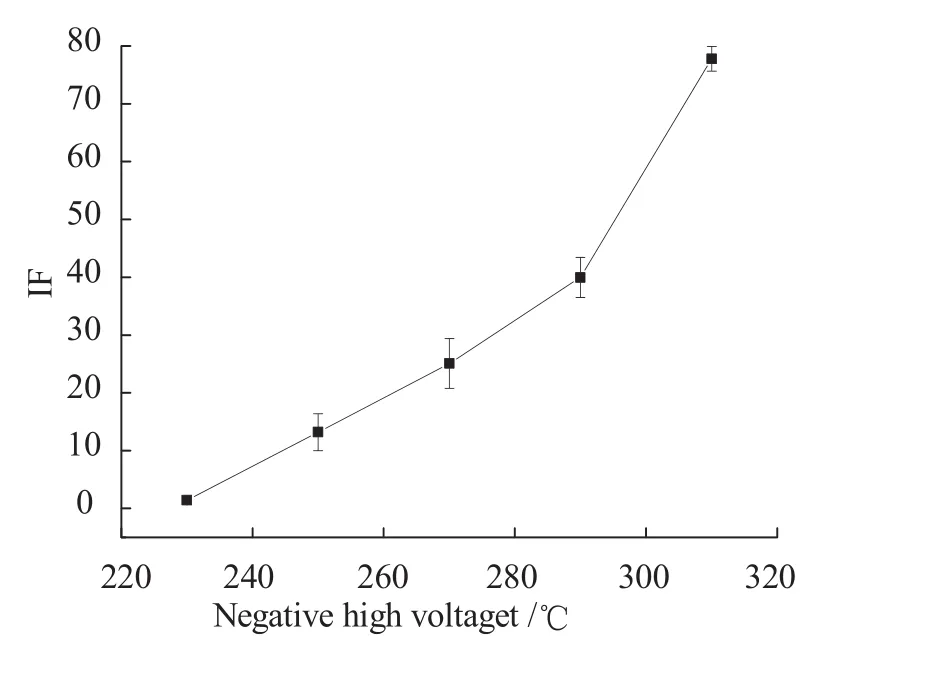
图1 负高压对荧光值的影响Figure 1 Effect of negative high voltage on fluorescence value
由图1可知,随着电压的增加,荧光值明显加强,当负高压大于290 V时,由于仪器测量噪声明显导致样品峰形不稳定[26],重现性良好,故本实验负高压选择270V。
2.1.3 灯电流对硒元素荧光值的影响
按照1.3.2设定仪器检测条件,将灯电流分别设定为 30 mA、35 mA、40 mA、45 mA、50 mA,负高压为270 V,载液为5 %(V/V)盐酸-水溶液,还原剂为8 g/L的硼氰化钾碱溶液,载气流速为400 mL/min,屏蔽气流速为600 mL/min,在该条件下测定0.75 ng/mL硒的标准溶液,平行测定三次,结果取平均值,结果如图2所示。
由图 2可知,灯电流在 30 ~ 45 mA 范围内荧光值随灯电流的增大快速升高,当灯电流大于45 mA后趋于稳定,过高的灯电流会缩短硒灯的寿命,重现性良好,故本实验灯电流选择45 mA。
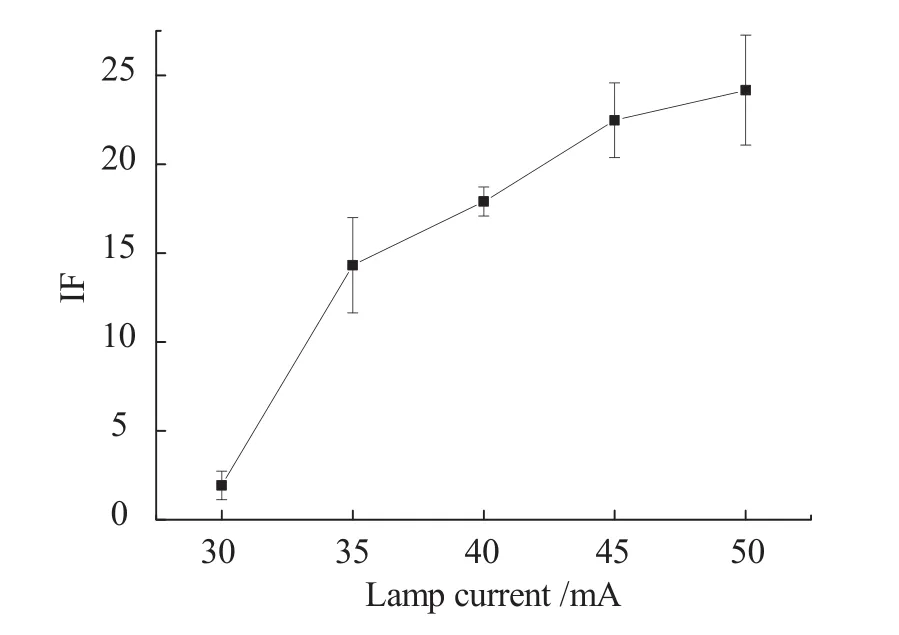
图2 灯电流对荧光值的影响Figure 2 Effect of lamp current on fluorescence value
2.1.4 载气流速对硒元素荧光值的影响
按照1.3.2设定仪器检测条件,将载气流速分别设定为 100 mL/min、200 mL/min、300 mL/min、400 mL/min、500 mL/min、600 mL/min、700 mL/min、800 mL/min,负高压为 270 V,灯电流为50 mA,载液为5 %(V/V)盐酸-水溶液,还原剂为8 g/L的硼氰化钾碱溶液,屏蔽气流速为 600 mL/min,在该条件下测定 0.75 ng/mL 硒的标准溶液,平行测定三次,结果取平均值,结果如图3所示。
由图3可知,载气流速越大对硒元素氢化物的推动作用越大,荧光值越高,当载气流量在 300 ~ 600 mL/min 时,荧光值较为稳定,重现性良好。实验中可以观察到由于载气流量过大,硒元素氢化物气液分离效果变差,造成荧光值不稳定,故本实验载气流速选择400 mL/min。
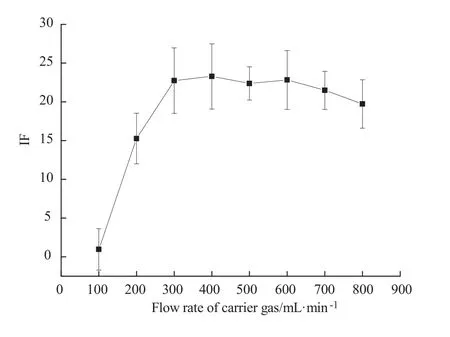
图3 载气流速对荧光值的影响Figure 3 Effect of flow rate of carrier gas on fluorescence value
2.1.5 屏蔽气流速对硒元素荧光值的影响
按照1.3.2设定仪器检测条件,将屏蔽气流速 分 别 设定 为 200 mL/min、400 mL/min、600 mL/min、700 mL/min,负高压为 270 V,灯电流为50 mA,载液为5 %(V/V)盐酸-水溶液,还原剂为8 g/L硼氰化钾碱溶液,载气流速为400 mL/min,在该条件下测定 0.75 ng/mL 硒的标准溶液,平行测定三次,取平均值,结果如图4所示。
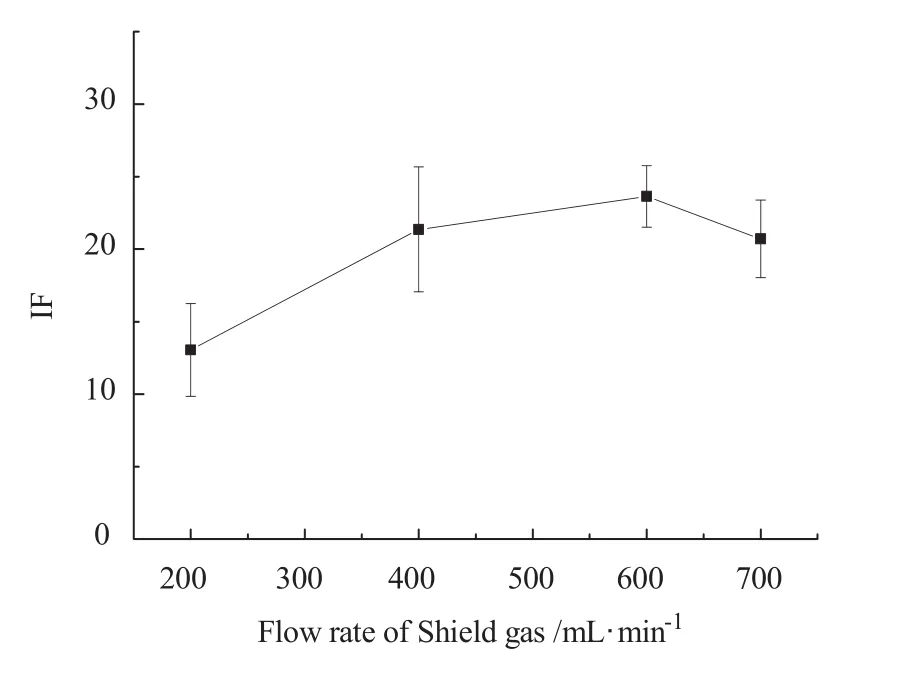
图4 屏蔽气流速对荧光值的影响Figure 4 Effect of flow rate of shield gas on fluorescence value
由图4可知,屏蔽气流速对荧光值影响呈先上升后下降趋势,但屏蔽气流速范围在200 ~ 700 mL/min范围内,荧光值变化范围不大,重现性良好。故本实验屏蔽气流速选择600 mL/min。
2.1.6 载液浓度对硒元素荧光值的影响
按照1.3.2设定仪器检测条件,将载液盐酸-水溶液浓度分别设定为2 %(V/V,下同)、4 %、5 %、8 %、9 %,负高压为 270 V,灯电流为 50 mA,载液为5 %(V/V)盐酸-水溶液,还原剂为8 g/L硼氰化钾碱溶液,载气流速为400 mL/min,屏蔽气流速为600 mL/min,在该条件下测定0.75 ng/mL硒的标准溶液,平行测定三次,取平均值,结果如图5所示。
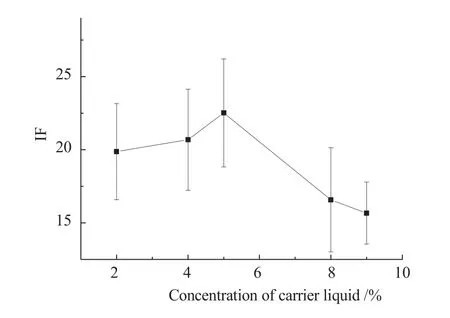
图5 载液浓度对荧光值的影响Figure 5 Effect of concentration of carrier liquid on fluorescence value
由图5可知,由于低浓度的酸与还原剂反应温和,且空白值较小,所以随着载液浓度的增加,荧光值先缓缓上升,当浓度大于5 %后,由于空白值变大,实验稳定性下降,荧光值急速下降。实验重现性良好,故本实验载液为5 %(V/V)盐酸-水溶液。
2.1.7 还原剂浓度对硒元素荧光值的影响
按照1.3.2设定仪器检测条件,还原剂为硼氰化钾碱液,浓度分别设定为4 g/L(配置溶液的碱液及定容的溶液均为5 g/L的KOH-H2O溶液,下同)、6 g/L、8 g/L、10 g/L、12 g/L、14 g/L、 16 g/L,负高压为 270 V,灯电流为 50 mA,载液为5 %(V/V)盐酸-水溶液,载气流速为400 mL/min,屏蔽气流速为 600 mL/min,在该条件下测定0.75 ng/mL硒的标准溶液,平行测定三次,取平均值,结果如图6所示。
由图6可知,随着还原剂中硼氰化钾浓度增加,荧光值逐渐升高,但硼氢化钾浓度超过10 g/L时,产生H2量过大,气液分离效果变差,可以看到部分液滴通过管道进入炉体,实验稳定性下降。实验重现性良好,故实验还原剂为10 g 硼氰化钾 / L (5 g/L KOH-H2O)溶液。
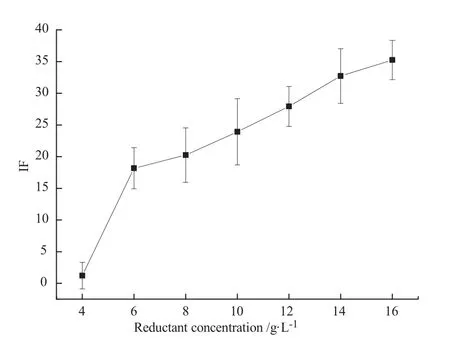
图6 还原剂浓度对荧光值的影响Figure 6 Effect of concentration of reductant on fluorescence value
2.1.8 标准曲线范围、灵敏度及检出限
按照1.3.3中方法配置系列标准溶液,进行测定,以硒浓度(x)为横坐标,荧光值(y)为纵坐标,绘制标准曲线如图7所示。
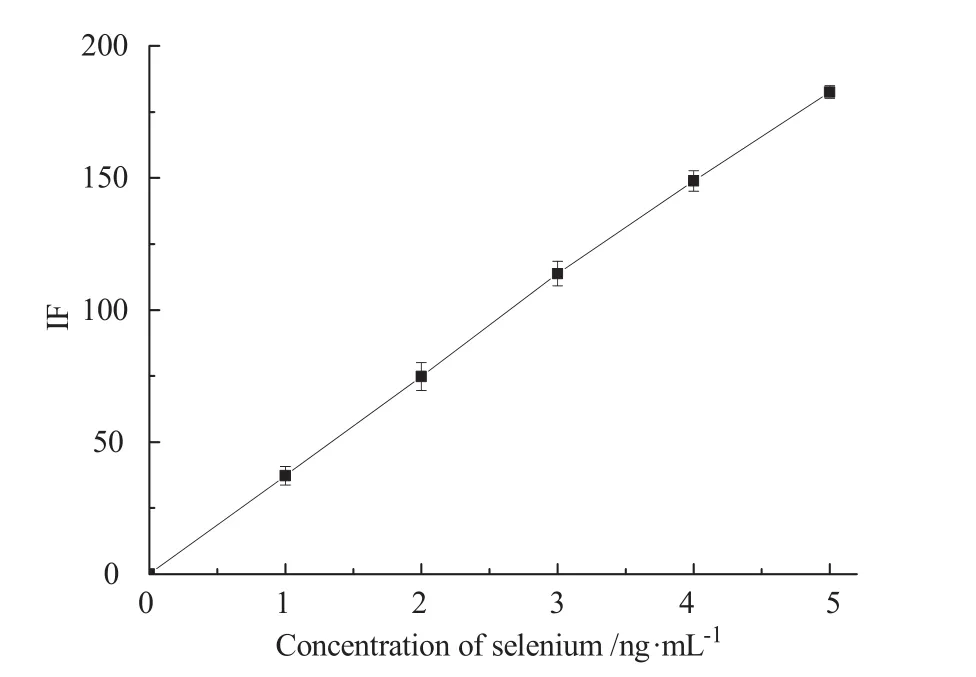
图7 硒的标准曲线Figure 7 The standard curve of selenium
硒标液浓度范围为0 ~ 5 ng/mL,硒标液浓度吸光度标准曲线方程为:y = 36.7791x+0.9248,R2= 0.9994。根据食品卫生检验方法测定并计 算[27],检出限为0.07956 μg/L,标线重现性良好。
2.1.9 方法精密度、准确度及重现性
平行称取 0.5 g(精确至 0.0001 g)绞股蓝茶6份,按照1.3.1中方法进行消解,同时进行全溶剂空白及生物质成分分析标准物质芹菜进行消解,取1、2、3、4、5、6号样品置于25 mL容量瓶中,分别加入25 ng/mL硒标准溶液0 mL、 0 mL、0 mL、0.85 mL、1.70 mL、3.40 mL 混匀、定容,每组样品平行测定10次,测定值取平均值,结果见表3。
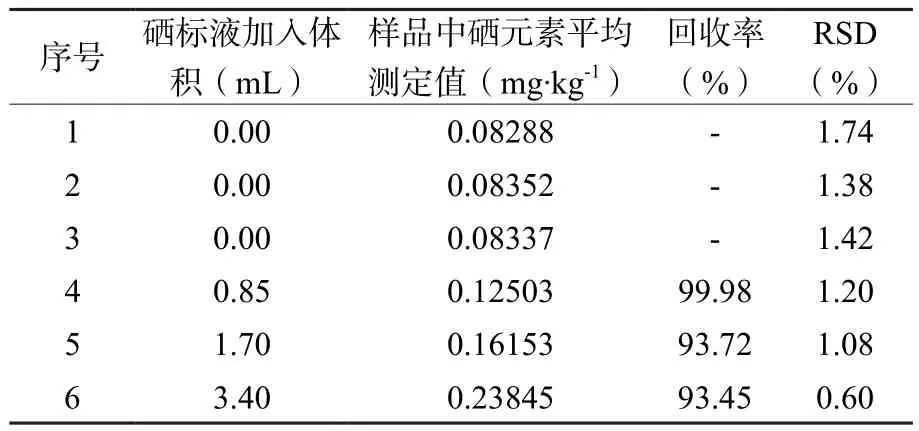
表3 方法精密度、准确度及重现性测定结果 (n=10)Table 3 Determination results of precision, accuracy and repeatability of the method (n=10)
通过计算,该方法测定绞股蓝茶中硒的回收率范围为 93.45 % ~ 99.98 %,相对标准偏差RSD 范围为 0.60 % ~ 1.74 %。通过 1 ~ 3 号三次平行消解后测定结果较为接近,绞股蓝茶叶中硒的平均值为0.08325 mg/kg,证明该分析方法是稳定的,具有可重复性。同时,用该方法 测定标准物质芹菜中硒含量为0.117 mg/kg,认定证书中查阅芹菜中硒含量认定值为(0.118± 0.017) mg/kg,芹菜的测定值在推荐值(真实值)范围内,准确性高,符合分析实验要求。
2.2 绞股蓝茶中硒含量测定的不确定度评定
2.2.1 样品前处理引入的不确定度urelsam
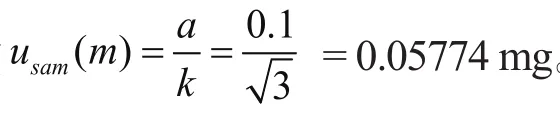
样品消解引入的不确定度urelsam(v)。25 mL容量瓶带来的不确定度urelsam(v)1:根据常用玻璃量器检定规程[28],定容样品的25 mL容量(A级),为B类评定,最大允许误差±0.03 mL,按均匀分布计算,usam(v)1= 0.03/31/2= 0.01732 mL。所以相对不确定度 urelsam(v)1= usam(v)1/V= 0.0006928。
温度引起体积变动带来的不确定度urelsam(v)2。 假设水温为(20±3) ℃,此时水的膨胀系数为2.1× 10-4℃-1,按均匀分布计算,usam(v)2=体积×膨胀系 数 ×ΔT/k = 25×2.1×10-4×3/31/2= 0.009093 mL。 所以相对不确定度urelsam(v)2= usam(v)2/V= 0.0003637。

2.2.2 标准储备液配置及标准曲线拟合引起的不确定度urelstd
标准储备液引入的不确定度urelstd1。实验所用硒的标准溶液证书标注扩展不确定度为4 μg/mL,即区间半宽度a = 4,为B类评定,按照均匀分布计算,所以其相对标准不确定度urelstd1=a/k/体积 = 4/31/2/1000 = 0.002309。
标准溶液配置引入的不确定度urelstd2。配置系列标准溶液时,使用到1 mL吸量管、10 mL容量瓶、100 mL容量瓶,均为A级,为B类评定,按均匀分布计算,使用次数及相对标准不确定度urelstd2-x,以1 mL吸量管的相对标准不确定度为例,urelstd2-1mL=容量允差/31/2/量程= 0.008/31/2/1 = 0.004619,结果见表 4。
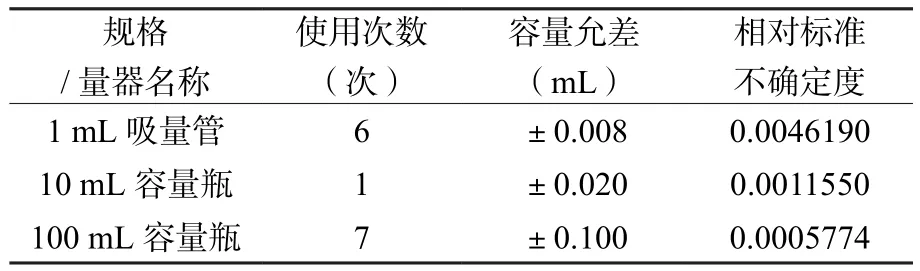
表4 标准溶液配置容量器具引入的不确定度Table 4 Results of uncertainty of standard solution configuration volumetric apparatus
使用 1 mL 吸量管、10 mL 容量瓶、100 mL 容量瓶移取、定容溶液时,由于温度引起体积变动,属于B类评定,按均匀分布计算,故温度引起体积变动的相对不确定度urelstd2-T = 2.1×10-4×3/31/2= 0.009093。
所以标准溶液配置的相对不确定度为urelstd2=
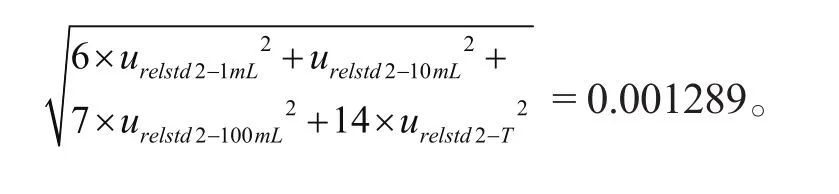
标准曲线拟合引入的不确定度urelstd3。按照1.3.3方法配置标准溶液,拟合出标准曲线方程 为y= 36.7791x+0.9248,R2= 0.9994, 即a= 36.7791,b= 0.9248。标准曲线各点平均测定3次,即 N = 18,样品重复测定 10 次,即p= 10。待测样品中硒浓度平均值= 1.6613 ng/mL。拟合曲线的相对不确定度计算公式urelstd3见公式(2),中间计算结果见表5。
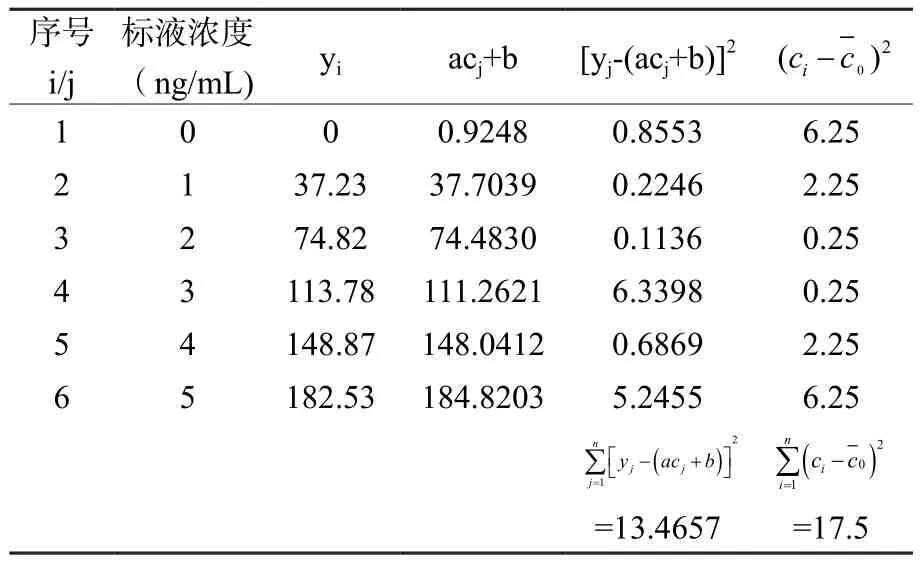
表5 标准曲线及中间计算结果Table 5 Standard curve and intermediate calculation results
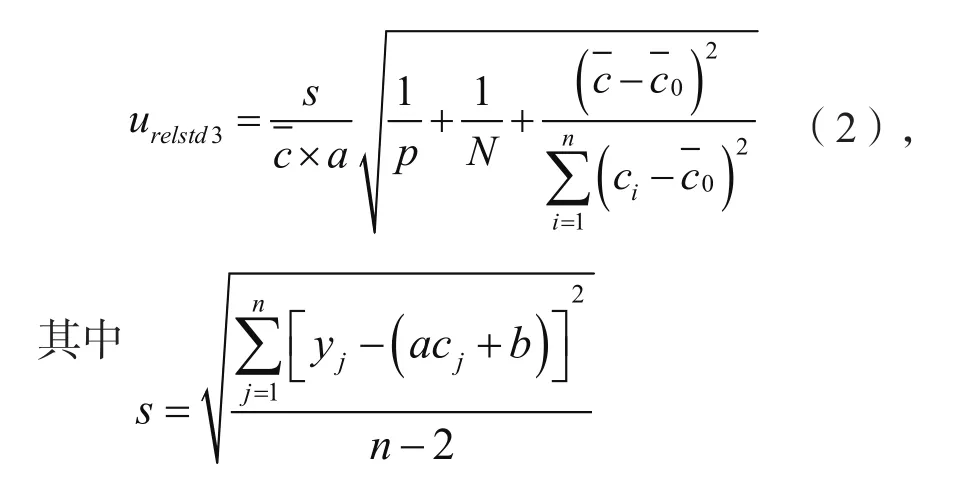
式中:s—拟合曲线的偏差;a—斜率;p—样品重复的次数,次;N—拟合曲线上的点总个数,个;—样品浓度的平均值,ng/mL;—标准曲 线浓度的平均值,ng/mL;—标准曲线上第i或j点浓度值,ng/mL;—标准曲线上第j点的实测荧光值。
所以标准曲线拟合的相对不确定度urelstd3= 0.01329。
2.2.3 测定过程中的随机效应引入的不确定度urelrep
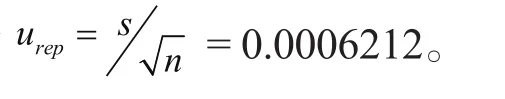
2.2.4 绞股蓝茶中硒含量的合成不确定度ucom
2.2.5 绞股蓝茶中硒含量的扩展不确定度U及报告结果
根据扩展不确定度公式U = k×ucom,取包含概率约为95 %,故k = 2,所以绞股蓝茶中硒含量的扩展不确定度 U = 0.003 mg/kg。
根据《测量不确定度评定与表示》(JJF 1059.1—2012)报告结果:原子荧光法测定绞股蓝茶中硒含量为 (0.083±0.003) mg/kg;k = 2。
3 结论与讨论
研究通过优化仪器检测时的负高压、灯电流、载液浓度、还原剂浓度、载气流速、屏蔽气流速等条件,分析了样品前处理、标准储备液配置及标准曲线拟合、测定过程中的随机效应等方面引入的不确定度,综合分析得到如下结论:
仪器检测参数的最优检测条件为:负高压270 V、灯电流(主灯电流、辅灯电流设定值相同)45 mA、载液为5%(V/V)的HCl-H2O溶液、还原剂为 10 g 硼氰化钾 / L(5 g/LKOH-H2O)溶液、载气流速400 mL/min、屏蔽气流速600 mL/min下进行测定,读数时间12 s,延迟时间3 s,原子化器温度200℃,炉高8 mm,载液第一次进样量1.5 mL,载液第二次进样量1.5 mL,样品进样量1.0 mL,采用自动进样方式,测定波长为 196.0 nm。在该条件下,硒在 0 ~ 5 ng/mL的范围内,浓度和荧光值线性关系良好R2= 0.9994,检出限为0.07956 μg/L,相对标准偏差RSD 范围为 0.60 % ~ 1.74 %,加标回收率范围为 93.45 % ~ 99.98 %。三次独立平行实验结果较为接近,重现性良好,绞股蓝茶叶中硒的平均值为0.08325 mg/kg。用该方法同时测定的标准物质芹菜中硒的测定值为0.117 mg/kg,认定证书中查阅芹菜中硒含量认定值为0.118±0.017 mg/kg。
原子荧光法测定绞股蓝茶中硒含量为(0.083±0.003)mg/kg;k = 2。研究证明与 GB/T 5009.93—2017相比,采用微波消解—原子荧光法测定绞股蓝中硒含量方法具有高效、准确、重复性好、操作简便的特点。在测定绞股蓝茶中硒含量的过程中,标准曲线拟合是影响合成不确定度最大的来源,在检测过程中应注意加强对标准曲线质量的控制,降低检测过程对结果准确性的影响,提高测量精度。本试验结果能够为绞股蓝茶生产厂家硒含量测定与分析提供技术指导,对第三方检测、食品、环境等行业具有借鉴意义。
