老年Ⅱ型糖尿病病人经利拉鲁肽治疗后外周血IGF-1及IGF-1R的表达变化
2021-06-08何雪花杨晓玲梁元碧
何雪花,张 玲,杨晓玲,梁元碧
(广元市第一人民医院内分泌老年内科,四川 广元 628017)
作为一种常见的内分泌失调代谢性疾病,Ⅱ型糖尿病不仅累及血管病变,也可合并神经、眼部等并发症,严重影响病人的生活质量,不利于预后[1,2]。二甲双胍是Ⅱ型糖尿病首选治疗药物,效果一直受到肯定,但近几年的研究指出二甲双胍治疗过程中易受病人身体基础代谢、饮食习惯及遗传等因素影响,临床疗效往往无法达到预期,血糖控制难度大[3]。利拉鲁肽是人胰高糖素样肽-1类似物,其是现阶段新的Ⅱ型糖尿病治疗方法,研究指出将利拉鲁肽与二甲双胍联合使用可显著提高降糖效果[4]。报道显示,利拉鲁肽能对胰岛β细胞及α细胞产生作用,调节胰岛功能,从而达到降低血糖的目的,同时还可显著降低糖尿病病人体重,应用价值高[5]。但老年Ⅱ型糖尿病病人多病程长、病情顽固,将该药与二甲双胍联合用于老年病人的治疗是否能获得理想效果尚不清楚。胰岛素样生长因子1(IGF-1)是一种在分子结构上与胰岛素类极为相似的多肽蛋白物质,可增强机体对葡萄糖、氨基酸的吸收能力,促进糖原的合成及乳酸分泌,增加人体对胰岛素的灵敏度,提高胰岛素的作用效率,但当糖尿病病人血糖水平过高时,促使IGF-1水平显著升高,增加胰岛素抵抗风险,不利于预后[6]。目前,临床上关于利拉鲁肽治疗糖尿病的研究主要集中在糖尿病病人的胰岛功能、脂联素及抵抗素等方面,而对糖尿病病人外周血IGF-1及其受体IGF-1R的相关研究较少。故本研究主要观察老年Ⅱ型糖尿病病人经利拉鲁肽治疗后IGF-1及胰岛素样生长因子1受体(IGF-1R)表达变化情况,以探讨利拉鲁肽治疗老年Ⅱ型糖尿病的价值,为未来老年Ⅱ型糖尿病的治疗提供新思路。现报告如下。
1 资料与方法
1.1 一般资料
选取2017-01~2019-02期间于我院门诊82例老年Ⅱ型糖尿病病人,采用数字奇偶法将入选者分为观察组(奇数)与对照组(偶数),各41例。两组一般资料比较(见表1)。本次研究内容经我院伦理委员会批准同意。
1.2 入选标准
1.2.1 纳入标准(1)Ⅱ型糖尿病符合《中国2型糖尿病防治指南(2013年版)》[7]内相关诊断标准;(2)符合利拉鲁肽适应症的病人;(3)既往无利拉鲁肽使用史的病人;(4)近3个月内未使用减肥类药物的病人;(5)病人及其家属知晓本次研究内容,且签署知情同意书;(6)年龄≥60周岁的病人。
1.2.2 排除标准(1)Ⅰ型糖尿病的病人;(2)合并重要脏器疾病的病人;(3)合并严重精神障碍影响治疗依从性的病人;(4)合并感染性、传染性疾病的病人;(5)近1周内服用过糖皮质激素类药物的病人。
1.3 方法
全部病人均接受常规治疗,包括:指导病人控制体重,制定营养均衡的膳食计划,满足病人对微量元素的需求,控制含糖食物的摄入量;同时给予病人盐酸二甲双胍片(中美上海施贵宝制药有限公司,国药准字H20033370,规格0.5g/片)口服治疗,初始服用剂量0.5g/次,2次/天,后根据病人血糖水平调整剂量,一般1~1.5g/天,最多不超过2g/天,餐前30min服用;观察组病人在此基础上使用利拉鲁肽注射液(丹麦诺和诺德公司,国药准字J20160037,规格18mg/mL)经皮下注射治疗,治疗前均病人进行利拉鲁肽注射液使用方法的相关培训,初始剂量为0.6mg/次,1次/天,治疗1周后,剂量应增加至1.2mg/次,1次/天。治疗时间为6个月。
1.4 评价指标
(1)实验室指标:分别于治疗前、治疗6个月后,早晨空腹抽取两组病人外周肘静脉血5mL,经自动离心机(湘智离心机仪器有限公司,TGL-20M型),以4000r/min的速度离心10min后取血清,置于-80℃的环境中保存待检:①IGF-1及IGF-1R:使用酶联免疫吸附法(ELISA)检测,试剂盒由上海晶抗生物工程有限公司提供;②空腹C肽(Fasting C-peptide,FC-P):使用化学发光法检测;③脂联素、抵抗素水平:使用ELISA法检测;(2)分别于治疗前、治疗6个月后,抽取两组病人餐后2h外周肘静脉血5mL,采用自动离心机,以4000r/min的速度离心10min后取血清,经化学发光法,试剂盒由深圳子科生物科技有限公司提供,检测餐后两小时C肽(Two Hours Postprandial C-peptide,2hC-P)水平;(3)胰岛素抵抗指数(HOMA-IR):分别于治疗前、治疗6个月后,空腹抽取病人5mL空腹静脉血,经自动离心机,以3000r/min的速度离心取血清待,采用ARCHITECT c16000生化检测仪(上海寰熙医疗器械有限公司)对病人的空腹血糖、空腹胰岛素水平进行检测,HOMA-IR=空腹血糖(mmol/L)×空腹胰岛素(mIU/L)/22.5;(4)体 质 量 指 数(body mass index,BMI)与腰围:分别记录两组病人治疗前、治疗6个月后,体重、身高、腰围,并计算BMI,BMI=体重(kg)/身高(m2);(5)不良反应:记录两组病人治疗过程中不良反应发生情况,包括低血糖(血糖水平≤3.9 mmol/L)、头痛(病人主诉)、上呼吸道感染(经咽拭子培养显示)、胃肠道不适(病人出现恶心、腹泻等情况)。
1.5 统计学方法
采用SPSS 24.0软件进行数据处理,计量资料均经正态性检验,符合正态分布以表示,组间用独立样本t检验,组内用配对样本t检验,计数资料用百分比表示,采用χ2检验,若期望值<5,则采用连续校正检验,P<0.05为差异具有统计学意义。
2 结果
2.1 一般资料
两组一般资料对比,差异无统计学意义(P>0.05)(见表1)。
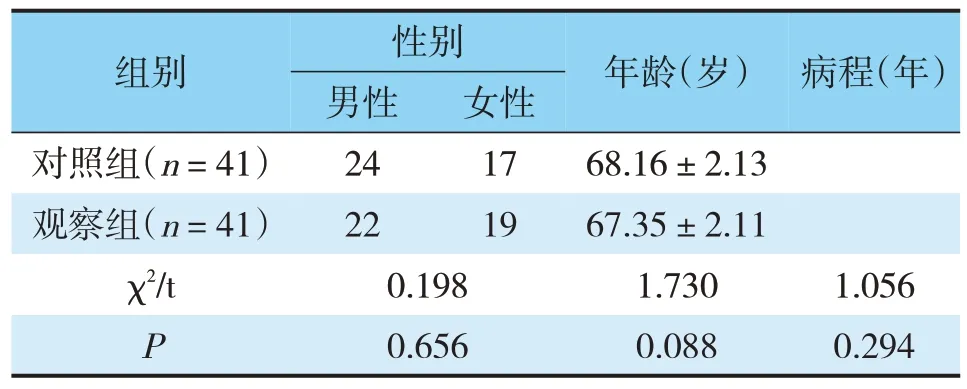
表1 两组一般资料比较Tab.1 Two groups of general data comparison
2.2 病例脱落或剔除情况
在治疗过程中,无脱落或剔除病例。
2.3 IGF-1及IGF-1R水平
治疗6个月后,两组IGF-1及IGF-1R水平均较治疗前降低,且观察组IGF-1及IGF-1R水平低于对照组,差异有统计学意义(P<0.05)(见表2)。
表2 两组病人IGF-1及IGF-1R水平比较(±s)Tab.2 Two groups of patients level of IGF 1 and IGF 1 r is(±s)
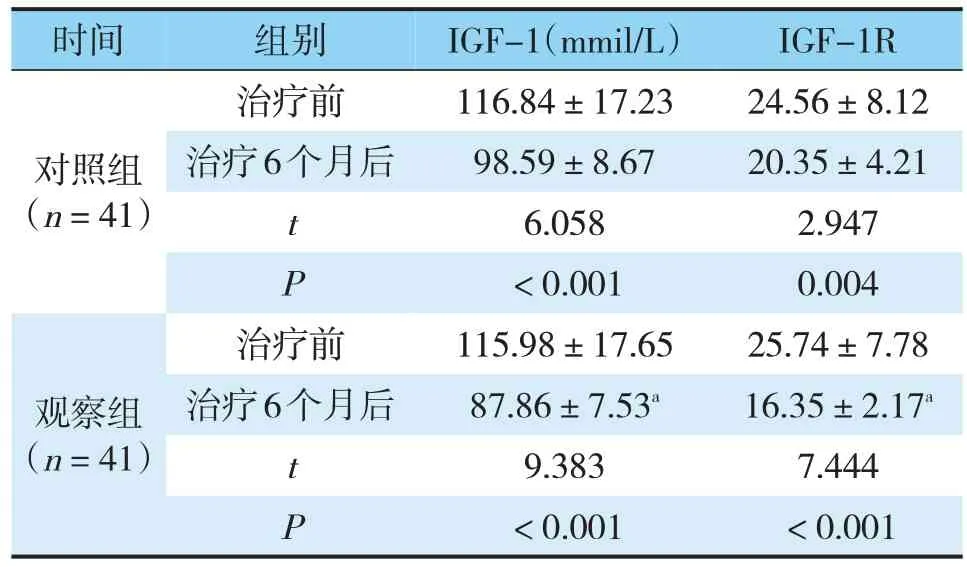
表2 两组病人IGF-1及IGF-1R水平比较(±s)Tab.2 Two groups of patients level of IGF 1 and IGF 1 r is(±s)
注:与对照组治疗6个月后同指标治疗前对比,aP<0.05
时间 组别IGF-1(mmil/L)IGF-1R治疗前116.84±17.2324.56±8.12对照组 治疗6个月后98.59±8.6720.35±4.21(n=41)t6.0582.947 P<0.0010.004治疗前115.98±17.6525.74±7.78观察组 治疗6个月后87.86±7.53a16.35±2.17a(n=41)t9.3837.444 P<0.001<0.001
2.4 BMI、腰围
治疗6个月后,对照组BMI、腰围与治疗前比较,差异无统计学意义(P>0.05);治疗6个月后,观察组BMI值较治疗前降低、腰围较治疗前缩小,且观察组BMI低于对照组,腰围小于对照组,差异有统计学意义(P<0.05)(见表3)。
2.5 胰岛功能
治疗6个月后,对照组FC-P、2hC-P、HOMA-IR水平与治疗前对比,差异无统计学意义(P>0.05);治疗6个月后,观察组FC-P、2hC-P、HOMA-IR水平均较治疗前升高,且均高于对照组,差异有统计学意义(P<0.05)(见表4)。
表3 两组病人BMI、腰围比较(±s)Tab.3 Two groups of patients with BMI,waist circumference comparison(±s)
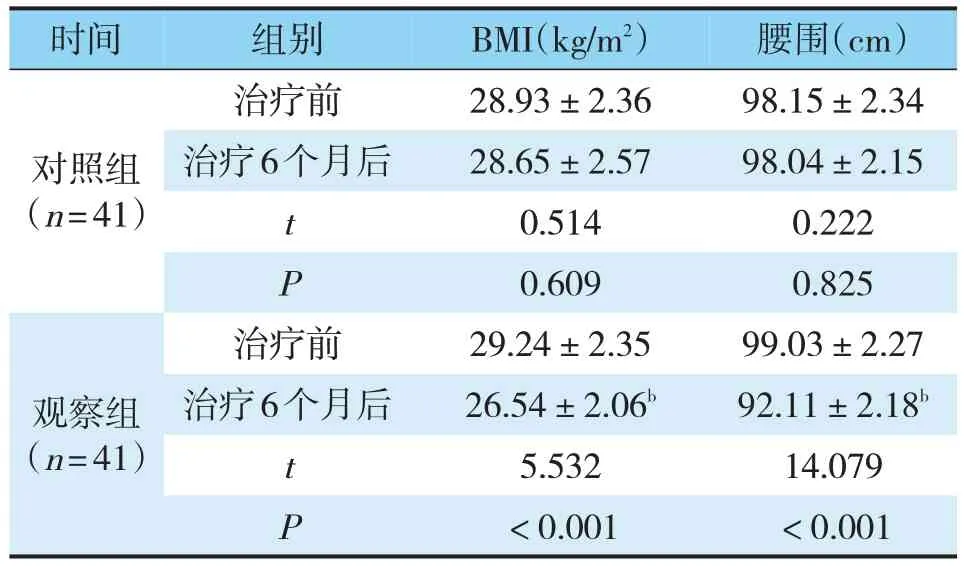
表3 两组病人BMI、腰围比较(±s)Tab.3 Two groups of patients with BMI,waist circumference comparison(±s)
注:与对照组治疗6个月后同指标治疗前对比,bP<0.05
时间 组别BM(Ikg/m2) 腰围(cm)治疗前28.93±2.3698.15±2.34对照组 治疗6个月后28.65±2.5798.04±2.15(n=41)t0.5140.222 P 0.6090.825治疗前29.24±2.3599.03±2.27观察组 治疗6个月后26.54±2.06b92.11±2.18b(n=41)t5.53214.079 P<0.001<0.001
表4 两组病人胰岛功能比较(±s,ng/mL)Tab.4 Islet function in patients with two groups of comparison(ng/mL,±s)
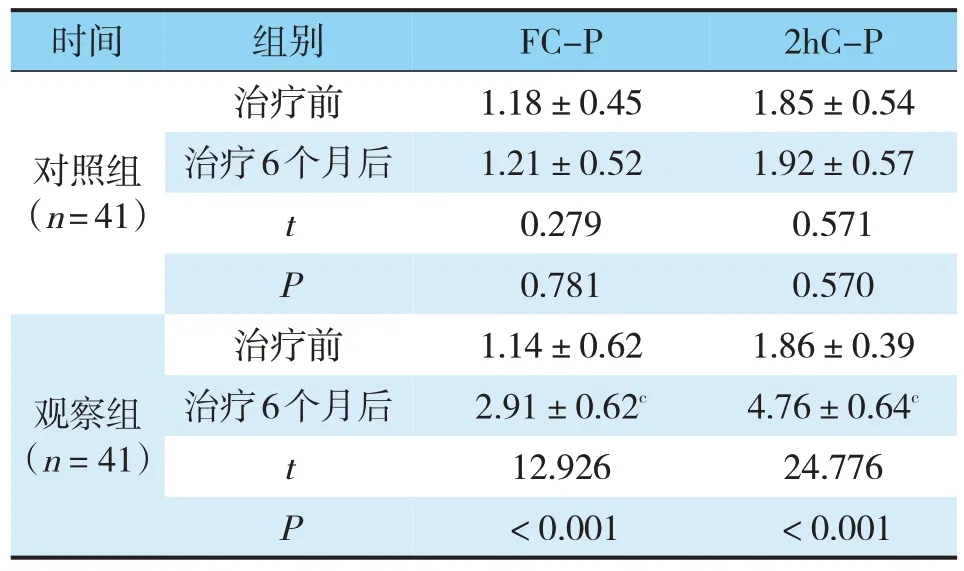
表4 两组病人胰岛功能比较(±s,ng/mL)Tab.4 Islet function in patients with two groups of comparison(ng/mL,±s)
注:与对照组治疗6个月后同指标治疗前对比,cP<0.05
时间 组别FC-P2hC-P治疗前1.18±0.451.85±0.54对照组 治疗6个月后1.21±0.521.92±0.57(n=41)t0.2790.571 P 0.7810.570治疗前1.14±0.621.86±0.39观察组 治疗6个月后2.91±0.62c4.76±0.64c(n=41)t12.92624.776 P<0.001<0.001
2.6 脂联素、抵抗素水平
治疗6个月后,对照组脂联素、抵抗素水平与治疗前对比,差异无统计学意义(P>0.05);治疗6个月后,观察组脂联素水平较治疗前升高、抵抗素水平较治疗前降低,且脂联素水平高于对照组、抵抗素水平低于对照组,差异有统计学意义(P<0.05)(见表5)。
表5 两组病人脂联素、抵抗素水平比较(±s)Tab.5 patients with two groups of adiponectin,resistin level comparison(±s)
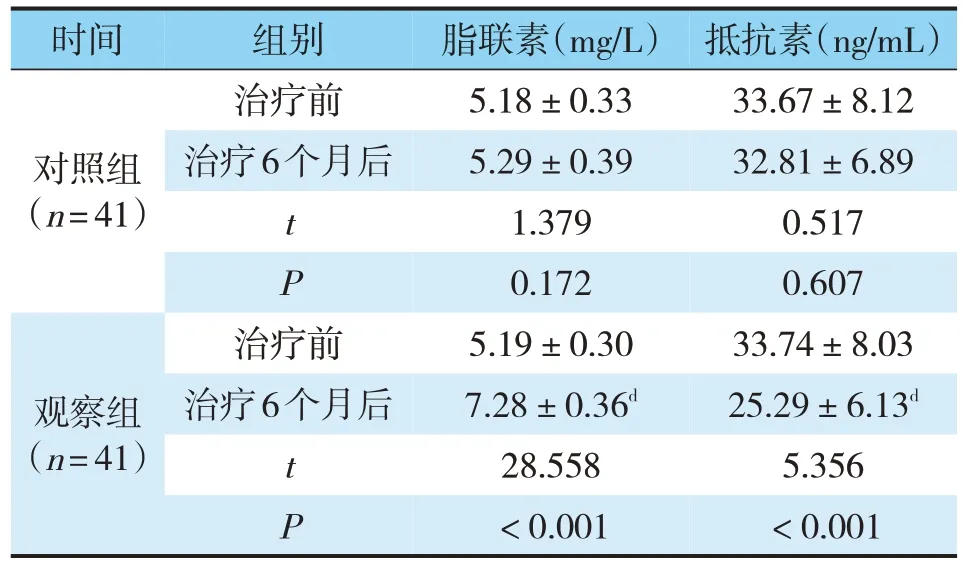
表5 两组病人脂联素、抵抗素水平比较(±s)Tab.5 patients with two groups of adiponectin,resistin level comparison(±s)
注:与对照组治疗6个月后同指标治疗前对比,dP<0.05
时间 组别 脂联素(mg/L) 抵抗素(ng/mL)治疗前5.18±0.3333.67±8.12对照组 治疗6个月后5.29±0.3932.81±6.89(n=41)t1.3790.517 P 0.1720.607治疗前5.19±0.3033.74±8.03观察组 治疗6个月后7.28±0.36d25.29±6.13d(n=41)t28.5585.356 P<0.001<0.001
2.7 不良反应发生情况
治疗期间,两组低血糖、头痛、上呼吸道感染、胃肠道不适发生率对比,差异无统计学意义(P>0.05)(见表6)。
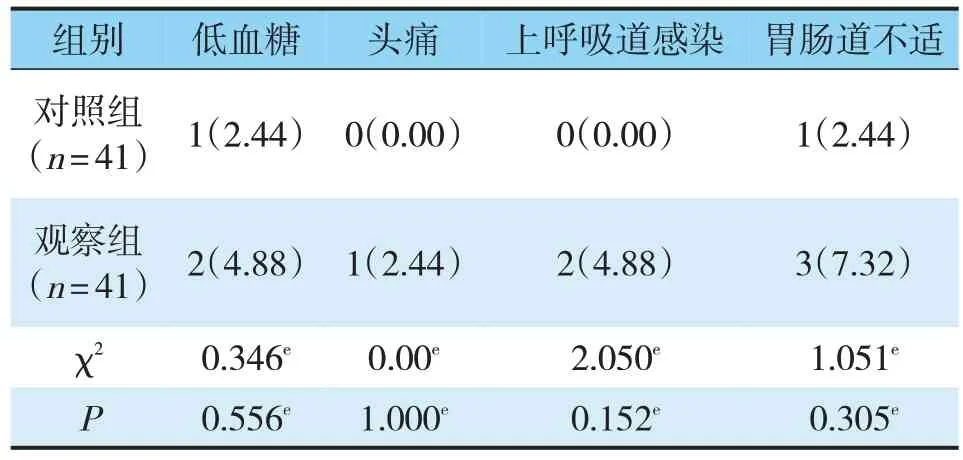
表6 两组病人不良反应发生情况对比(n,%)Tab.6 adverse reactions occurred in patients with two groups of contrast(n,%)
3 讨论
Ⅱ型糖尿病是一种因多种因素引起胰岛素分泌绝对或相对不足以及靶细胞对胰岛素敏感性降低,致使体内糖、蛋白质和脂肪等发生代谢异常的疾病,可加重组织损害,增加血管及神经病变风险,严重影响病人生活质量,尤其老年人群最为突出[8,9]。老年人因合并各类基础疾病,治疗难度更大,常规用药可能无法带来理想获益,因此,如何采取合理、有效的治疗方案提高老年Ⅱ型糖尿病病人获益,对改善老年病人生活质量意义重大。
研究表明,二甲双胍广泛用于Ⅱ型糖尿病的治疗,药物的使用能够提高Ⅱ型糖尿病病人血糖耐受性,降低基础和餐后血糖水平[10]。但其长期使用时,易出现药物浓度积累现象,增加乳酸性中毒风险,加之老年糖尿病病人病程长、病情严重程度相对高、治疗难度大,故药物单独使用对于老年Ⅱ型糖尿病可能无法获益甚至增加安全性风险。研究指出,大部分老年Ⅱ型糖尿病病人均合并肥胖,其体内易产生大量脂肪因子,打破原有的平衡状态,进而对胰岛β细胞造成损伤,影响胰岛功能[11]。故急需找到一种可以辅助二甲双胍使用帮助病人控制体重的药物,已获得胰岛功能改善的效果,提高治疗获益。大量相关报道显示,利拉鲁肽是一种治疗效果极佳的降糖药物,该药物能够最大程度降低Ⅱ型糖尿病病人体重、腰围,改善其胰岛功能,且治疗后低血糖的发生率低,安全性高[12,13]。孙晓方等[14]研究显示,对肥胖Ⅱ型糖尿病病人使用利拉鲁肽治疗,可明显改善胰岛细胞功能,减轻体重,降糖效果极佳。为指导未来老年Ⅱ型糖尿病病人安全有效的治疗方式,本研究在使用常规治疗及二甲双胍的基础上为观察组联合利拉鲁肽治疗,结果显示,观察组BMI、腰围均小于对照组,表明利拉鲁肽可显著降低病人体重,帮助病人腰围缩小。诸多研究表明,超过50%的老年Ⅱ型糖尿病病人均有超重或肥胖现象,而对于该类糖尿病病人单纯通过降糖治疗效果往往差强人意,减轻体重可在获得较好的降糖效果的同时降低低血糖、心血管等不良反应发生风险[15,16]。
IGF-1与Ⅱ型糖尿病病人胰岛素抵抗、内分泌代谢能力密切相关;IGF-1R是IGF-1受体,其表达情况与IGF-1有关,正常情况下IGF-1与IGF-1R结合后可对细胞产生相应刺激,对细胞的糖代谢能力与胰岛素极为相似,可调节细胞多种代谢及转运过程,但当Ⅱ型糖尿病病人长期处于高血糖状态时,机体胰岛素分泌过量,会引发胰岛素抵抗,促使机体血糖水平显著升高,造成IGF-1及IGF-1R过表达,引发高甘油三酯和高游离脂肪酸血症等脂代谢紊乱发生风险,进一步减弱内分泌代谢能力[17]。而脂代谢紊乱又可进一步加重胰岛素抵抗,影响老年Ⅱ型糖尿病病人预后。但IGF-1及IGF-1R与Ⅱ型糖尿病代谢之间的关系目前尚不明确,相关研究也不多。本研究结果显示,观察组治疗后IGF-1及IGF-1R水平均低于对照组,提示利拉鲁肽能显著改善老年Ⅱ型糖尿病病人IGF-1及IGF-1R水平,进而改善病人胰岛素抵抗状态,提高降糖效果。脂联素能够对胰岛β细胞产生保护作用,改善胰岛素抵抗状态,且脂联素的改变远早于糖、脂代谢紊乱,不仅是胰岛素敏感性评估指标之一,还是胰岛素抵抗发生发展的重要标志物[18]。抵抗素是一种特异性多肽,可对骨骼肌细胞、干细胞及脂肪细胞产生作用,降低其对胰岛素的敏感性,能够显著降低胰岛β细胞对葡萄糖的摄取能力,影响胰岛素释放,导致体内高血糖状态长期保持,可造成胰岛细胞严重损伤[19]。本次研究中,观察组脂联素水平高于对照组,抵抗素水平低于对照组,表明利拉鲁肽对老年Ⅱ型糖尿病病人脂联素、抵抗素具有调节作用,减轻胰岛素抵抗,降低胰岛细胞功能的损害程度。C肽(C-P)由胰岛β细胞分泌,因其不容易被肝脏降解,故检测C肽水平可准确反映胰岛细胞的功能[20]。本次研究结果显示,观察组FC-P、2hC-P、HOMA-IR水平高于对照组,提示利拉鲁肽改善胰岛功能效果确切。此外,本次还对利拉鲁肽的安全性进行研究,结果显示,两组低血糖、头痛、上呼吸道感染、胃肠道不适发生率对比无差异,表明利拉鲁肽治疗老年Ⅱ型糖尿病具有较高的安全性。现阶段,临床关于利拉鲁肽治疗老年Ⅱ型糖尿病对IGF-1及IGF-1R水平研究较少,其能否通过改善IGF-1及IGF-1R水平达到调节胰岛素抵抗状态目前仍尚未完全明确,仍需要在未来展开大样本、长时间的研究加以验证。
综上所述,老年Ⅱ型糖尿病病人经利拉鲁肽治疗获益明显,病人外周血IGF-1及IGF-1R水平明显改善,有利于调节病人胰岛功能、降低BMI、缩小腰围,病人脂联素、抵抗素水平显著改善,临床应用价值高。此外,由于老年Ⅱ型糖尿病病人多合并高血压、高血脂等多种基础性疾病,致使合并用药多,如调脂药及降压药等,进而可对本次研究中临床指标测定的准确性造成一定影响,在应用价值方面仍有局限,还需在未来展开大样本、长时间的研究加以佐证本次研究结果。
