硒纳米颗粒的生物合成及其对孔雀石绿吸附性能的研究
2021-06-04程园园
陈 喆,曹 凯,程园园
(1.安徽大学 资源与环境工程学院,安徽 合肥230601;2.湿地生态保护与修复安徽省重点实验室(安徽大学),安徽 合肥230601;3.安徽大学 生命科学学院,安徽 合肥230601)
近年来,染料作为使织物获得色泽的有机化合物,在生产活动中使用愈加频繁.然而,染料的广泛使用对环境中的水体造成了污染[1-2].三苯甲烷类染料废水是典型的化工业废水,具有致癌、致畸、致突变等特点.其中,孔雀石绿就是典型的三苯甲烷类染料,由于其高效的杀菌性,一度被广泛利用在渔业生产中.对环境水体造成了巨大的污染.因此,去除废水中的染料迫在眉睫.
众多物理化学生物的方法已被应用于净化染料废水.其中,吸附作为一种简单、灵活、高效的方法一直备受青睐.近年来,具有良好吸附量、快吸附速率的吸附材料得到越来越多的关注,纳米颗粒由于其高比表面积,常作为高效的吸附剂来使用,如Se-NPs、纳米ZnO和AgNPs[3-5].然而,现有制备方法常存在环境污染大、成本高、合成过程复杂、反应条件苛刻且易团聚等缺点,故寻求操作简单、经济实用、绿色环保的合成方法尤为重要.部分微生物如某些细菌、真菌和酵母菌能够在一定浓度的金属离子溶液中存活、生长并氧化还原这些金属离子,将其转换成对应的纳米颗粒[6].故利用微生物还原氧化污染物,合成所需要的纳米颗粒无疑是获得纳米颗粒的一种绿色环保的方式.
本实验室从浙江舟山双峰盐场的土壤中分离出菌株胶红酵母R.mucilaginosaPA-1,该菌株在亚硒酸盐的还原中展现了较高的能力.以孔雀石绿为模型,研究了合成的Se-NPs吸附废水中染料的能力,为污染物的治理提供新思路.
1 实验材料和方法
1.1 材料
1.1.1 菌株 本实验菌株R.mucilaginosaPA-1筛选自浙江舟山双峰盐场的土壤中[7].
1.1.2 试剂 菌株PA-1用R2A培养基(酪蛋白氨基酸0.5 g/L、可溶性淀粉0.5 g/L、蛋白胨0.5 g/L、酵母提取物0.5 g/L、七水硫酸镁0.05 g/L、磷酸氢二钾0.3 g/L)在30 ℃、180 r/min条件下进行培养.在厌氧培养基(磷酸氢二钾0.225 g/L、磷酸二氢钾0.225 g/L、氯化钠0.46 g/L、硫酸铵0.255 g/L、七水硫酸镁0.024 g/L、葡萄糖10 g/L、4-羟乙基哌嗪乙磺酸4.766 g/L、微量元素5 mL/L)中还原.本实验中采用的试剂纯度均为分析纯,Na2SeO4采购自Sigma-Aldrich公司.
1.2 Se(Ⅳ)的测定方法亚硒酸盐浓度的测定参照文献[8].样品经离心(10 000 r/min,10 min)后,取400μL的上清液,加入200μL的4 mol/L HCl和200μL的1 mol/L抗坏血酸,显色10 min,在紫外分光光度计500 nm下测定Se(Ⅳ)的浓度.
1.3 Se-NPs的生物合成细菌在30℃、180 r/min好氧培养12 h.离心收集(6 000 r/min,5 min),用厌氧培养基重悬.以初始浓度OD600=0.5 将菌株接种至含有不同浓度Na2SeO3的厌氧培养基中.以葡萄糖作为唯一碳源,Na2SeO3作为电子受体[9].
1.4 Se-NPs的原位表征取还原24 h后的4 mL样品,1 000 r/min离心10 min去上清,以乙醇固定.
利用TEM观察样品的形貌特征. 再取还原24 h后的样品,12 000 r/min离心收集后冷冻干燥,EDS、FTIR分析样品.
1.5 Se-NPs还原条件的优化厌氧条件下,考查底物浓度(0.5,1,2,5,10,15 mmol/L Na2SeO3)、pH值(2,4,6,8,10)、温度(25,30,35℃)对硒还原的影响.
1.6 染料吸附实验取定量吸附剂(0.3 g/L Se-NPs)于锥形瓶中,向其加入质量浓度5~40 mg/L的模拟印染废水(MG),调节pH值(5~10),在转速200 r/min,室温条件下进行吸附.样品经1 h吸附后离心(12 000 r/min,5 min).在617 nm处测其吸光度.MG的吸附量计算如下:

其中,qt是t时的吸附量,ρ0是初始质量浓度,ρt是吸附t时的质量浓度,V是溶液体积,m是Se-NPs的质量.
染料吸附后,10 000 r/min离心10 min,收集Se-NPs.用100 mmol NaCl重悬,循环利用Se-NPs.脱附效率由以下方程计算:

为了实验Se-NPs的重复利用性,进行了5个连续的吸附/脱附循环.循环去除效率计算如下:

2 结果与分析
2.1 Se-NPs的还原如图1所示,厌氧条件下,接入菌株PA-1培养24 h后,培养基由无色变为红色,对照组颜色不变.有研究指出,反应溶液呈红色即代表有Se-NPs的生成[10-11].因此,推测菌株PA-1具有合成Se-NPs的能力.

图1 菌株PA-1还原Se(Ⅳ)Fig.1 The reduction of Se(Ⅳ) by PA-1
为了进一步证明生成了硒纳米颗粒,进行了一系列的物理表征.如图2所示,TEM表明,形成的纳米颗粒呈现规则的圆形,直径范围为30~100 nm,平均粒径为60 nm左右.如图2(c)所示,EDS分析证实了纳米颗粒的主要成分为元素硒.此外,观测到C、N、O的峰,可能是源于生物分子,如酶、细菌生物材料或包裹在Se-NPs上的多糖和蛋白质.Cu信号来源于铜片. 如图2(e)所示,Se-NPs在261 nm处有明显的吸收峰,表明Se-NPs的合成.
文献[12]中所述,胞外聚合物(EPS)等细胞分泌物会附着在Se-NPs的表面,EPS有助于Se-NPs的分散并阻止其聚集,因此,无需添加外部稳定剂即可以提高纳米材料的稳定性.通过比较菌株PA-1与生物合成的硒纳米颗粒(Bio-Se NPs)的FTIR,如图2(f)所示,二者光谱形状类似.3 413 cm-1为胺基和羧酸基团的伸缩振动,证明了葡萄糖中O-H基团和蛋白质中N-H基团的存在[12-14].1 652、1 556、1 244 cm-1的特征峰对应于酰胺I、酰胺Ⅱ、酰胺Ⅲ,证明了蛋白质的存在[15].1 070~1 085 cm-1处的多种峰,证明了碳水化合物的存在.FTIR谱图表明,Bio-Se NPs的表面包裹了EPS.据报道,Se-NPs表面的EPS在硒还原反应过程中起着重要的作用.EPS中的蛋白质和其他生物大分子被用作元素Se的还原剂,其中膜表面上的蛋白质主要属于还原酶和氧化还原酶,负责将Se(Ⅳ)还原为Se-NPs[16].整个还原过程是通过电子传递链上的氧化还原酶由NADPH/NADH电子传递开始的.蛋白质表面电子和Se(Ⅳ)之间的静电相互作用,导致还原反应,从而形成Bio-Se NPs.
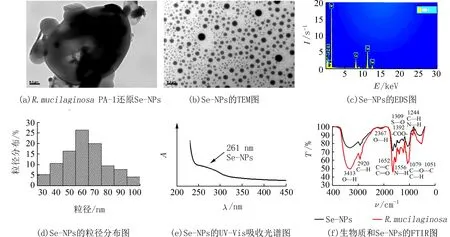
图2 Se-NPs的物理表征Fig.2 Physical characterization of Se-NPs
2.2 硒还原条件的优化Bio-Se NPs的生物合成也受到一些环境参数的影响,包括底物浓度、pH和温度.如图3所示,菌株PA-1只在0.5 mmol/L的Na2SeO3中还原完全.在pH=8的条件下,Se(Ⅳ)的还原效率优于其他,28 h即能完全还原.在一定范围内,温度的提高对硒的生物还原具有显著的促进作用.菌株PA-1在35℃下还原最快,20 h即可还原97%,24 h完全还原.
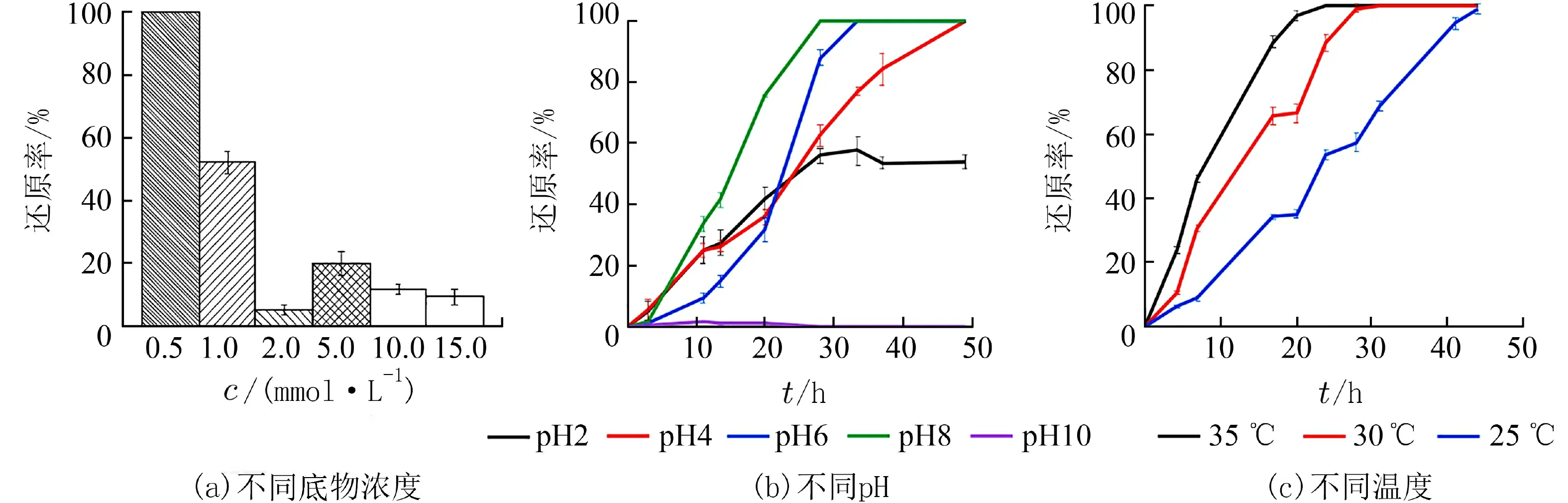
图3 不同条件下Se(Ⅳ)的还原效率Fig.3 Se(Ⅳ)reduction efficiency under different conditions
2.3 染料吸附与脱附实验本研究探究了不同条件下Bio-Se NPs对MG的吸附能力.如图4(a)所示,10 mg/L的MG由蓝色变为无色,表明MG被Bio-Se NPs吸附.UV-Vis也证实了MG被吸附脱色.据报道[5-17],材料的吸附性能往往受体系内pH值变化的影响. pH值的变化不仅会影响吸附剂的表面性质,还会对吸附质的溶解度及其质子化程度产生重要影响.例如体系在高pH值时,溶液中存在大量的OH-,使得Bio-Se NPs带负电荷,从而使得材料对阳离子染料(MG)的吸附能力增强.而当pH值变低时,材料上带正电荷的吸附位点增多,从而与阳离子染料之间产生库伦斥力,不利于材料对染料的吸附.如图4(b)所示,MG的去除效率随pH的增加明显提高,与之前的报道结果一致.说明材料Bio-Se NPs与阳离子染料MG之间主要吸附机理是静电作用.吸附剂的再生及重复利用能力可以大大降低其使用成本并且使吸附过程变得更具竞争力.因此,我们探究了Bio-Se NPs的循环再利用性.实验结果表明,经5次吸附-脱附循环过后,Bio-Se NPs的吸附效率仍高达82.12%(图5(c)).
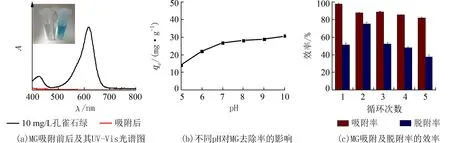
图4 MG的吸附及脱附实验Fig.4 MG adsorption and desorption experiment
如图5(a)、(b)所示,pH=10、30℃条件下,探究了MG的接触时间对吸附容量的影响.实验结果表明,MG的吸附速率极快,不同浓度的MG均能在10 min内达到吸附平衡.此外,还建立了准一级、准二级和Elovich动力学模型,以阐明其吸附机理.
准一级动力学模型:

其中qe和qt分别是平衡和时间t时的吸附量(mg·g-1).k1、k2分别是准一级、准二级速率常量(h-1),A、k是Elovich方程的常量.动力学参数如表1所示,MG的准一级动力学方程的R2为0.999,高于准二级和Elovich模型.即Bio-Se NPs对MG的吸附动力学符合准一级模型,是一种反应速率与一种反应物浓度呈线性关系的扩散控制的吸附反应过程.
了解平衡吸附等温线对于充分了解Bio-Se NPs吸附性能具有重要意义.我们用如下模型来拟合.
Langmuir方程:

其中,qm(mg·g-1)是吸附剂最大容量,KL(L·mg-1)平衡吸附常量;KF(L·mg-1)和1/n是代表吸附容量和吸附强度的Freundlich常量,A和B是Temkin常量.吸附等温线及其拟合参数如图5(d)及表2所示.其中,Langmuir的相关系数最高,说明吸附剂表面均匀,吸附物不能在表面上迁移,吸附质之间没有相互作用,吸附是单层的.且当吸附剂表面被单层吸附物覆盖时,发生最大吸附[18].根据Langmuir模型,303、313、323 K下MG的qm分别为1 355.39、1 095.49、898.62 mg/g.Freundlich常量(n>2)说明吸附容易进行[19].
热力学参数能够分析吸附过程的自发性、随机性、吸热性以及放热性.根据
Van’t Hoff方程:
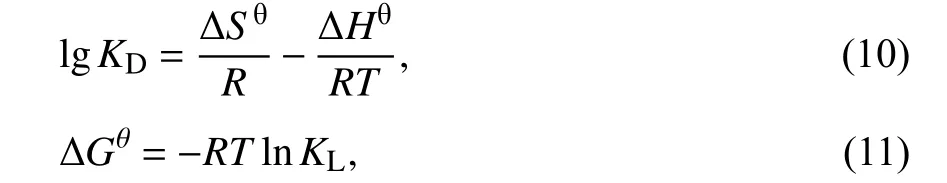
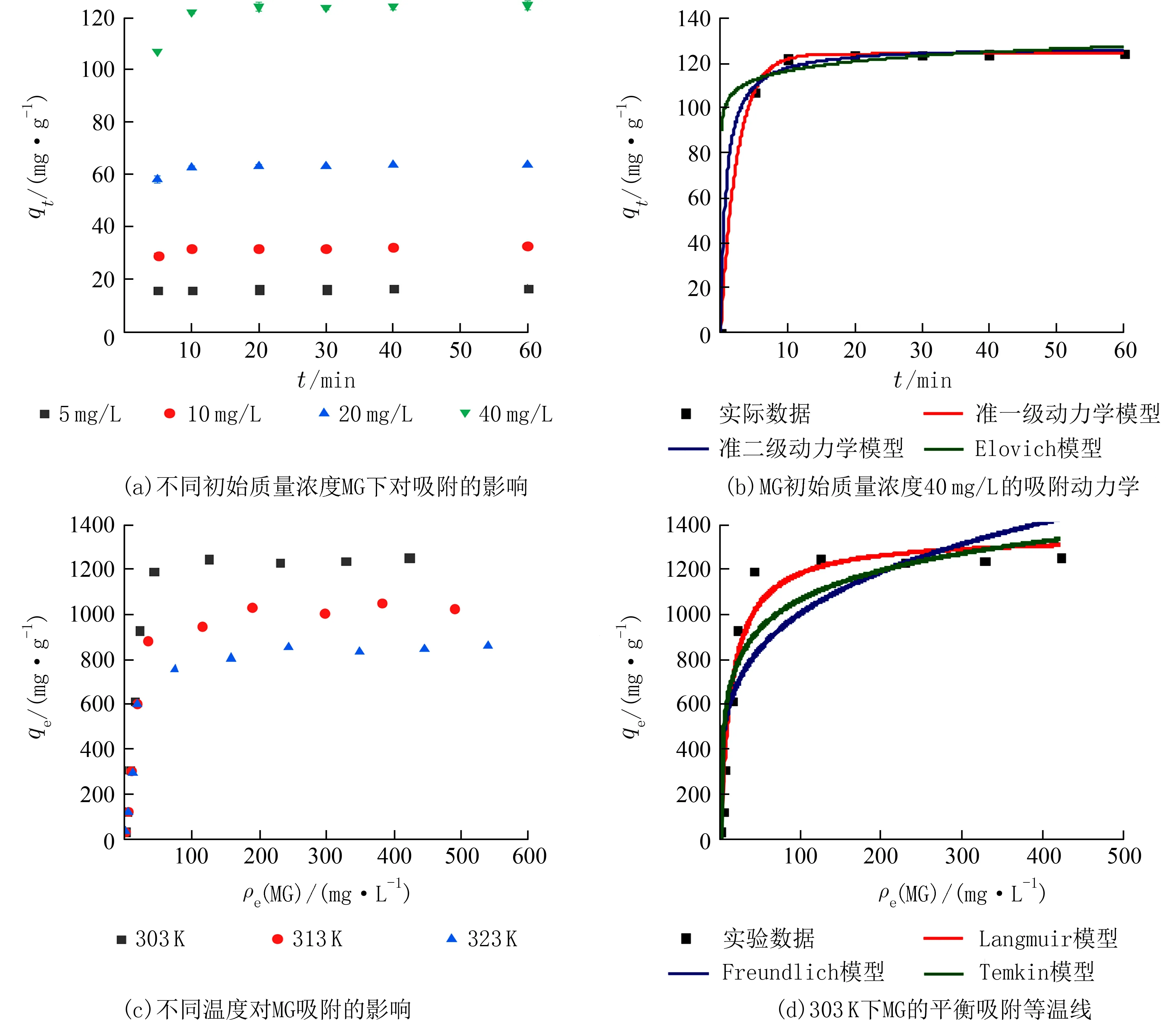
图5 Bio-Se NPs对MG的吸附性能Fig.5 Adsorption performance of Bio-Se NPs for MG

表1 Bio-Se NPs吸附MG的动力学模型参数Tab.1 Parametersof kinetic model of Bio-Se NPs for the MG adsorption

表2 Langmuir,Freundlich and Temkin吸附等温线的常量、相关系数和q mTab.2 Langmuir,Freundlich and Temkin adsorption isotherm constant,correlation coefficient and q m
其中,KD=Ke/ρe,R为通用气体常量(8.314 J/(mol·K));T为热力学温度(K);∆Hθ为焓(J/mol),∆Sθ为熵(J/mol),∆Gθ(kJ/mol)为自由能.热力学参数的值见表3.不同温度下,∆Gθ值为负.这表明MG在Bio-Se NPs上的吸附是一种自发的过程.随着温度的升高,ΔGθ的增高,表明在较高的温度下,MG的吸附过程更不利.MG的吸附反应是放热反应(ΔHθ<0),ΔSθ<0,说明MG 被吸附到Bio-Se NPs上,使得吸附质分子失去部分自由度(包括但不限于平动和转动),从而使熵减小,表明此过程是一个趋于有序的吸附过程[20].

表3 Bio-Se NPs吸附MG的热力学参数Tab.3 Thermodynamic parameters for MG adsorption onto Bio-Se NPs.
为了更好地解释反应的吸附机理,将Bio-Se NPs吸附脱附循环5次,利用FTIR、XPS及XRD对吸附前后的Bio-Se NPs进行分析.如图6(c)所示,Bio-Se NPs吸附前后的XRD衍射光谱的数据符合硒的JCPDS(编号:06-0362)标准卡片,且吸附前后并无明显变化. 如图6(f)所示,吸附MG后的Bio-Se NPs样品的FTIR谱图出现了MG分子的特征峰,其原因是在材料表面吸附了大量MG分子,使得吸附后的样品兼具Bio-Se NPs和MG的特征峰.图6(a)、(b)、(d)、(e)为吸附前后的Bio-Se NPs的XPS谱.Se 3d5/2峰分别处于56.7、55.9 eV和55.5 eV,说明Bio-Se NPs中的Se元素为0价硒. 此外,吸附MG后的Bio-Se NPs谱图(图6(b))中,出现了 Na 1s、Cl 2p的新峰,说明有部分脱附剂吸附在了吸附剂表面,除此之外谱图没有明显变化,表明吸附MG之后吸附剂的化学组成并没有发生变化,说明吸附过程为物理吸附.

图6 Bio-Se NPs吸附MG前后的表征谱图Fig.6 Characterization of Bio-Se NPs before and after MG adsorption
3 结论
(1) 通过R.mucilaginosaPA-1合成Bio-Se NPs.波谱表征结果表明,合成的为表面包裹着EPS、分散性良好的、球形Bio-Se NPs.其颗粒粒径大小分布范围为30~100 nm,平均粒径为60 nm左右.进一步探究了Bio-Se NPs合成的最适条件:OD600=0.5,0.5 mmol Na2SeO3,pH=8,35℃.最适条件下,Bio-Se NPs的合成仅需24 h.
(2)研究了Bio-Se NPs对MG的吸附能力以及影响因素,如pH、温度.Bio-Se NPs在pH=10下对阳离子染料具有很大的去除潜力.吸附动力学研究表明,准一级动力学模型可以很好地拟合Bio-Se NPs对MG的动力学吸附,吸附过程为物理吸附. 等温吸附研究表明,MG在Bio-Se NPs上的吸附等温线符合Langmuir模型,属单分子层吸附.303~323 K范围内,染料去除率随温度的升高而降低,吸附量分别为1 355.39、1 095.49 mg/g和898.62 mg/g,对MG的去除能力优于传统生物质材料.吸附热力学研究表明,MG在Bio-Se NPs上的吸附是一种自发的放热反应.此外,Bio-Se经5次循环后,吸附能力依然优异,MG去除率高达80%以上.
