还原态吡咯喹啉醌清除氮自由基能力研究
2021-06-04吴贞贞杨雪鹏
马 科 吴贞贞 杨雪鹏
(郑州轻工业大学食品与生物工程学院,河南 郑州 450008)
吡咯喹啉醌(Pyrroloquinoline quinone,PQQ),是一种含有3个羧基的水溶性醌类化合物,是继核黄素和烟酰胺后的第三类辅酶[1],广泛存在于母乳、植物、动物组织、某些单细胞真核生物和许多细菌中[2]。作为许多重要酶的辅基,PQQ对生物体具有多种生物功能,如调控基因表达和蛋白质功能[3]、神经保护作用[4]、调节机体自由基水平[5]和信号转导、修复DNA功能[6]等。
在自然界中,吡咯喹啉醌存在醌型(PQQ,氧化态)、半醌型(PQQH)和氢醌型(PQQH2,还原态) 3种可以互相转化的稳定状态(见图1)[7-8]。氧化态PQQ呈醌形式,PQQH2呈邻二酚形式。PQQ可以通过从底物转移两个质子和两个电子转化为PQQH2[9]。作为氧化还原酶的辅基,PQQ 3种状态的转化在底物的氧化还原反应中起到电子传递作用。
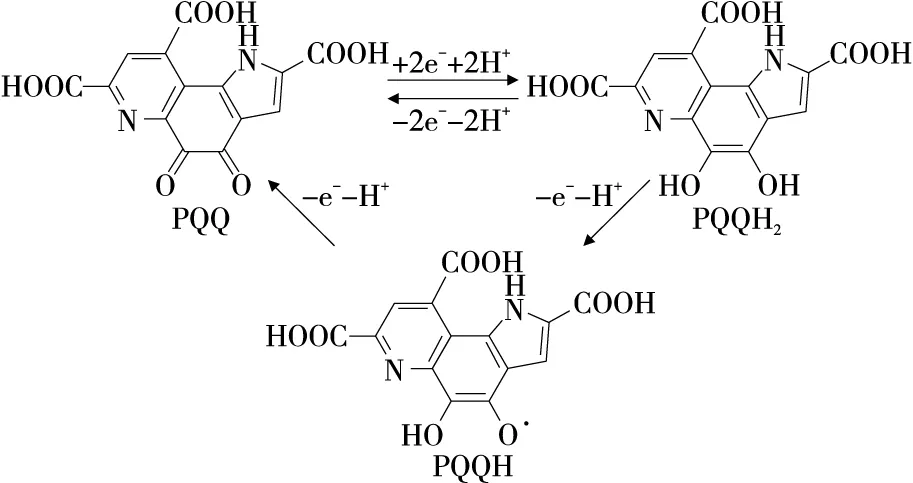
图1 PQQ氧化态与还原态转化及电子传递功能Figure 1 PQQ oxidation state and reduction state transformation and electron transfer function
已有研究[10]表明,PQQH2具有良好的抗氧化性,可以有效清除机体活性氧自由基。但是,PQQ对于活性氮(如:ABTS)自由基的清除作用,未见文献报道。活性氮自由基是机体内氧化应激过程的产物,在机体过多地积累会导致慢性炎症,进而引发很多疾病,例如癌症、糖尿病、动脉粥样硬化等[11-12]。试验拟以ABTS自由基的清除能力为指标对PQQH2的抗氧化性进行研究,以期为其作为抗氧化剂在食品中的应用提供理论依据。
1 材料与方法
1.1 材料与仪器
1.1.1 材料与试剂
PQQH2标品:色谱纯,阿拉丁试剂公司;
维生素C标品:色谱纯,郑州派尼化学试剂公司;
ABTS:分析纯,麦克林生物科技有限公司;
其余试剂均为分析纯。
1.1.2 仪器设备
分析天平:AB256-S型,宁波新芝生物科技股份有限公司;
精密pH计:PHS-3D型,上海雷磁仪器厂;
紫外—分光光度计:2300型,尤尼克(上海)有限公司。
1.2 试验方法
1.2.1 清除ABTS自由基的反应动力曲线测定 分别配制PQQH2标准溶液10,30,50,70 mg/L。将PQQH2溶液与0.1 mmol/L的ABTS工作液进行自由基反应,间隔一定时间,测定吸光度,研究PQQH2清除ABTS自由基的速度与时间变化的关系,试验重复3次,以时间为横坐标,清除率为纵坐标绘制反应动力曲线图,按式(1)计算ABTS自由基清除率。
(1)
式中:
a——ABTS自由基清除率,%;
A0——空白对照组的吸光度;
A1——1 mL PQQH2和 ABTS工作液的吸光度。
根据文献[13],建立反应动力学模型:
(1) 准一级反应动力学方程:
(2)
式中:
Ct——ABTS自由基在t时刻的质量浓度,mg/mL;
C0——ABTS自由基在t=0时的质量浓度,mg/mL;
k1——一级反应速率常数,mg/(mL·min)。
ABTS自由基剩余率:
(3)
式中:
w——ABTS自由基的剩余率,%。
结合式(2)和式(3)得准一级反应动力学方程式:
ln(1-a)=-k1t,
(4)
(2) 准二级反应动力学方程:
(5)
结合式(3)和式(5)得准二级反应动力学方程式:
(6)
式中:
a——ABTS自由基清除率,%;
k2——二级反应速率常数,mg/(mL·min)。
1.2.2 清除ABTS自由基能力半数清除率(IC50)的测定
以维生素C为阳性对照,计算ABTS自由基清除率达到50%时样品的质量浓度。分别配制PQQH2标准溶液10,30,50,70,90 mg/L。将1 mL PQQH2溶液与3 mL 0.1 mmol/L 的ABTS自由基反应,试验重复3次。半数清除率浓度的计算,运用Oringin 9.1进行。
1.2.3 热稳定性研究
(1) 加热温度对PQQH2稳定性的影响:配制30,50,70 mg/L PQQH2标准溶液,分别在相同时间(4 h)、不同温度(30,50,75,100 ℃)水浴下反应,测定PQQH2对ABTS自由基的清除率。
(2) 加热时间对PQQH2稳定性的影响:配制30,50,70 mg/L PQQH2标准溶液,分别在相同温度(100 ℃)、不同时间(4,8,12,24 h)下进行水浴反应,测定PQQH2对ABTS自由基的清除率。
试验重复3次,测定方法参照1.2.1,以维生素C为阳性对照,对PQQH2各项指标作出评价。
2 结果分析
2.1 清除ABTS自由基的反应动力曲线
如图2所示,反应前10 min内,ABTS自由基清除率随反应时间的延长显著提高,PQQH2质量浓度越高,清除效率越高,10 min后ABTS自由基清除速率降低,清除率无显著变化,反应逐渐趋于平衡。并且相同反应条件下,提高PQQH2的质量浓度,ABTS自由基清除率也显著提高,70 mg/L PQQH2相较于10 mg/L PQQH2对ABTS自由基的清除率提升了约3倍,达到了95%左右。试验结果表明,ABTS自由基清除率与PQQH2的质量浓度呈正比。

图2 不同浓度PQQH2清除ABTS自由基的反应动力曲线Figure 2 Kinetic curves of scavenging effects of different concentrations of PQQH2 on ABTS radical
对不同质量浓度PQQH2清除ABTS自由基反应进行准一级、准二级动力学方程拟合,结果见图3、图4,相应动力学参数见表1。准一级动力学模型拟合相关系数均在0.9以下,线性相关较差。而准二级动力学模型拟合的线性相关系数为0.959~0.996,因此,PQQH2清除ABTS自由基采用准二级动力学模型,二级反应速率常数随PQQH2质量浓度的增加而增大。二级反应速率常数能够反映抗氧化物质的自由基清除能力,其值越大,清除自由基的能力越强。
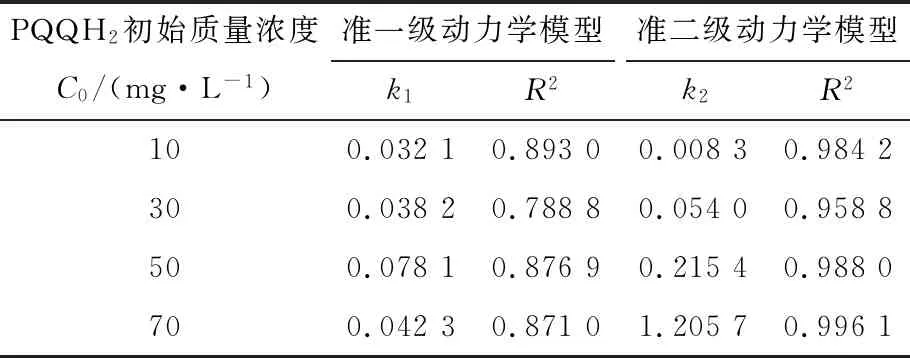
表1 动力学模型拟合参数Table 1 Kinetic parameters for PQQH2 to ABTS·
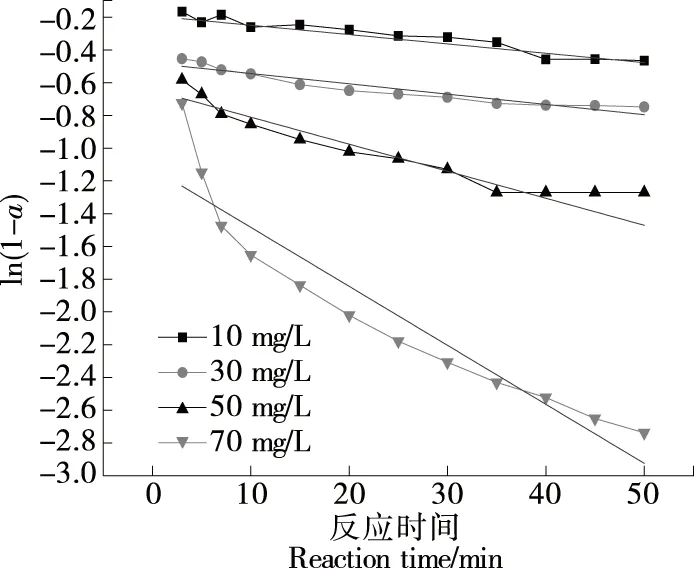
图3 PQQH2清除ABTS自由基准一级反应动力学方程的拟合图线Figure 3 Fitting curve of the kinetic equation of the quasi-first order reaction of PQQH2 clearing ABTS radical
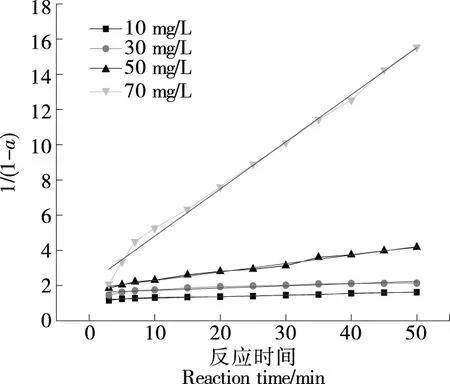
图4 PQQH2清除ABTS自由基准二级反应动力学方程的拟合图线Figure 4 Fitting curve of the kinetic equation of the quasi-second order reaction of PQQH2 clearing ABTS radical
2.2 清除ABTS自由基的IC50值
如图5所示,ABTS自由基清除率与PQQH2和维生素C在一定质量浓度范围内呈线性关系,ABTS自由基清除率与PQQH2、维生素C的质量浓度呈正比。当PQQH2质量浓度为0~90 mg/L时,对ABTS自由基的清除率随着质量浓度的增大而升高,清除率可高达95%左右,但之后随着PQQH2质量浓度的增加,清除率虽然也在增加,但增长速率显著降低,清除率最终保持平稳不变。PQQH2清除ABTS自由基IC50值约为30 mg/L,即90 μmol/L,而维生素C清除ABTS自由基的IC50值约为38 mg/L,即176 μmol/L。PQQH2的IC50值是维生素C的51.14%,说明PQQH2比维生素C更适合作为一种快速清除自由基的抗氧化剂。

图5 PQQH2、维生素C对ABTS自由基清除能力的变化Figure 5 ABTS radical scavenging capacity of PQQH2,VC
2.3 PQQH2与维生素C清除ABTS自由基的反应动力学比较
通过研究相同质量浓度(70 mg/L)的PQQH2与维生素C清除ABTS自由基的反应动力学,结果见图6。由图6 可知,相同质量浓度时,PQQH2的抗氧化性要高于维生素C的。反应25 min时,PQQH2对ABTS自由基的清除率可达到90%以上,而维生素C对ABTS自由基的清除率仅能达到78%。

图6 PQQH2和维生素C清除ABTS自由基的反应动力曲线Figure 6 Kinetic curves of scavenging effects of PQQH2 and VC on ABTS radical
2.4 热稳定性研究
2.4.1 加热温度对PQQH2稳定性的影响 如图7所示,在加热时间相同的条件下,随着加热温度的升高,PQQH2和维生素C对ABTS自由基的清除能力均呈下降趋势,可能是由于加热导致抗氧化活性基团损失。加热温度由30 ℃升高到100 ℃,相同质量浓度的维生素C对ABTS自由基清除能力损失比PQQH2多2~3倍。说明PQQH2表现出的热稳定性要高于维生素C,当加热时间相同时,PQQH2的稳定性更高,对ABTS自由基清除能力损失更小,PQQH2即使在高温条件下,也依然能够保持自身结构的稳定性,从而展现突出的抗氧化特性。

图7 加热温度对清除率的影响Figure 7 The effect of heating temperature on removal rate
2.4.2 加热时间对PQQH2稳定性的影响 如图8所示,当加热温度一定,随着加热时间的延长,维生素C表现出的抗氧化活性能力的降低幅度显著高于PQQH2,约为PQQH2的3~7倍。相较于维生素C,PQQH2具有稳定的结构,在高温条件下,依然能够保持优良的抗氧化性能。维生素C因其具备的抗氧化特性被广泛应用于食品中,但基于自由基清除能力、热稳定性等指标,PQQH2比维生素C更适合作为食品抗氧化剂。
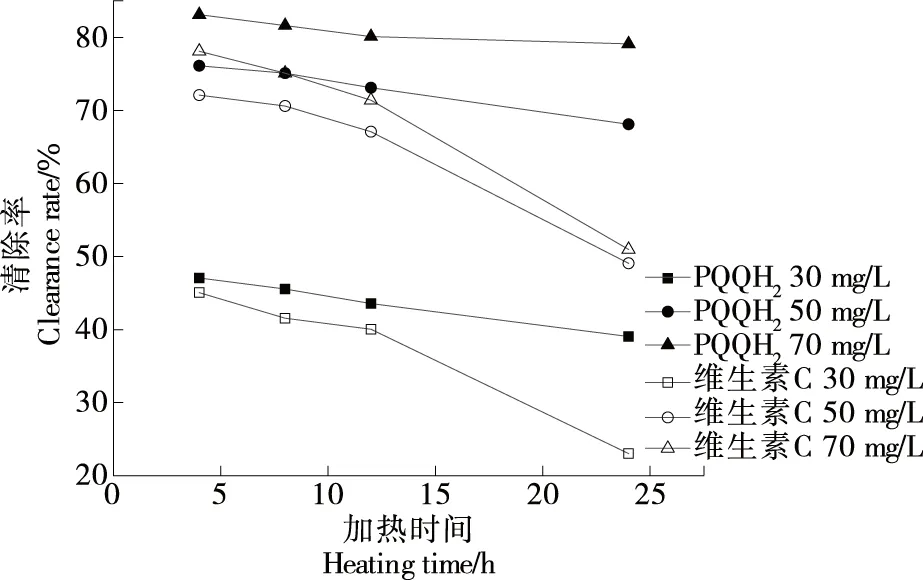
图8 加热时间对清除率的影响Figure 8 Effect of heating time on removal rate
3 结论
研究检测了10,30,50,70 mg/L 4种质量浓度下还原态吡咯喹啉醌对ABTS自由基的清除能力,结果表明,浓度越高,清除能力就越强。当还原态吡咯喹啉醌的质量浓度为70 mg/L时,反应25 min,ABTS自由基的清除率可达到90%以上,说明还原态吡咯喹啉醌具有一定的抗氧化能力。根据反应动力学模型,二级动力学拟合方程更能描述还原态吡咯喹啉醌对ABTS自由基的清除能力,相关系数为0.959~0.996。还原态吡咯喹啉醌比维生素C具有更好的抗氧化活性,有望将其开发为一种天然的抗氧化剂。
