气相色谱法快速测定婴幼儿配方奶粉中肌醇含量
2021-06-04薛敏敏陈文璋程孟雅袁列江吴海智
朱 礼 何 浩 薛敏敏 陈文璋 程孟雅 袁列江 吴海智
(湖南省产商品质量监督检验研究院,湖南 长沙 410007)
肌醇又名环己六醇,广泛分布于动物和植物体内,是动物、植物和微生物的生长因子[1]。肌醇在婴幼儿配方奶粉中是可选择性成分指标,可促进细胞新陈代谢、促进发育、增进食欲、促进毛发健康生长,预防湿疹等,其含量应在1.0~9.0 mg/100 kJ[2]。目前,检测食品中肌醇含量的方法有气相色谱法[3-5]、微生物法[3,6]、液相色谱法[7-8]、气质联用法[9]、液质联用法[10]、毛细管电泳法[11]、离子色谱法[12-13]、化学法[14]等。其中气相色谱法和气质联用法是利用硅烷化试剂与肌醇反应,使肌醇反应生成硅烷化肌醇衍生物,增加了肌醇的挥发性,以利于用气相色谱或气质联用仪进行分析。在适当的条件下,肌醇的6个羟基均被硅烷化试剂衍生,反应产物单一,可以定量进行分析[15-16]。曾静等[4]为了减少杂质对肌醇含量测定的影响,采用固相萃取技术,样品经LC-Florisil小柱净化处理,浓缩、硅烷化后以正己烷提取,以提高气相色谱法检测婴幼儿配方奶粉中肌醇含量的准确性。周玮婧等[5]引入内标法减少了衍生过程给肌醇检测带来的误差,并将该方法应用于奶粉检测中,利用肌醇在酸性条件下与乙酸酐生成不溶于水而溶于三氯甲烷的六乙酰肌醇,测定奶粉中肌醇的含量,该方法的定量限为6 mg/kg。以上气相色谱法分别是研究通过优化前处理方法减少杂质对肌醇含量测定的影响,以及采用内标法减少衍生过程给肌醇检测带来的误差。
目前,检测婴幼儿配方奶粉中肌醇含量的方法主要是GB 5009.270—2016的微生物法(第一法)和气相色谱法(第二法)。微生物法是利用葡萄汁酵母菌对肌醇的特异性和灵敏性,定量测定食品中的肌醇含量,步骤繁琐、检测周期长、易受外部因素干扰。气相色谱法灵敏度高,但样品前处理过程中选择的旋转蒸发方式、硅烷化等操作繁琐耗时,反应时间长,不利于批量样品的检测[17]。试验拟在GB 5009.270—2016第二法的基础上进行改进,通过优化前处理步骤和仪器色谱条件,缩减前处理时间和批处理分析时间,以期实现实验室间大批量样品的快速检测。
1 材料与方法
1.1 试验材料
1.1.1 标准物质与试剂
肌醇(CAS号:87-89-8):纯度99.0%,上海安谱实验科技有限公司;
婴幼儿配方乳粉质控样品:肌醇特性值131.1 mg/100 g,中国检验检疫科学研究院;
N,N-二甲基甲酰胺:分析纯,国药集团化学试剂有限公司;
三甲基氯硅烷:GC级,纯度≥99.0%,上海麦克林生化科技有限公司;
六甲基二硅胺烷:分析纯,纯度98%,上海麦克林生化科技有限公司;
二水乙酸锌、亚铁氰化钾、无水乙醇:分析纯,国药集团化学试剂有限公司。
1.1.2 仪器与设备
气相色谱仪:Agilent-7890A型,配分流/不分流进样口、FID检测器,美国安捷伦科技有限公司;
石英毛细管柱:ZB-5ms型(15.0 m×0.25 mm×0.50 μm),北京艾杰尔科技有限公司;
超纯水仪:ELIX3 Essential+Reference型,广东丹利科技有限公司;
台式高速离心机:TG16-WS型,湖南湘仪离心机有限公司;
多通道平行浓缩仪(氮吹仪):MV5型,莱伯泰科仪器股份有限公司;
数显恒温水浴锅:HH.S11-2型,天津泰斯特仪器有限公司;
电热鼓风干燥箱:DHG-9420A型,上海一恒科学仪器有限公司;
涡旋混合器:美国Talboys EOFO-945007基本型,上海安谱实验科技股份有限公司。
1.2 试验方法
1.2.1 试样处理与衍生 准确称取5 g试样于50 mL小烧杯中,加入约40~50 ℃的超纯水30 mL,充分搅拌至完全溶解。将试样处理液转入50 mL容量瓶中,加入5 mL 亚铁氰化钾(106 g/L)溶液和5 mL乙酸锌(220 g/L)溶液,加入超纯水定容,充分振摇后静置30 min,过滤。准确吸取5 mL滤液至20 mL螺纹口比色管中,加入无水乙醇至约10 mL,涡旋混匀,氮吹剩至约2~3 mL,再加无水乙醇至约10 mL,氮吹至干后再加入5 mL 无水乙醇,继续氮吹至干。在100 ℃电热鼓风干燥箱中加热30 min,冷却后依次加入0.5 mL三甲基氯硅烷、1.0 mL六甲基二硅烷和4 mLN,N-二甲基甲酰胺,涡旋混匀2 min。将样品处理液在80 ℃的水浴锅中衍生20 min,衍生化反应中其间振摇2~3次,衍生化反应结束后冷却至室温。用10 mL超纯水分3次将衍生化反应后的处理液水洗至50 mL离心管中,加入5.0 mL正己烷,涡旋混匀充分萃取,5 000 r/min离心3 min,取上清液进气相色谱分析。
1.2.2 肌醇标准溶液的配制 称取101.0 mg经105 ℃烘干2 h的肌醇标准品于100 mL容量瓶中,用超纯水定容后摇匀,配制成1.0 mg/mL的肌醇储备液。吸取10.0 mL 肌醇储备液,用超纯水定容至100 mL容量瓶中,摇匀,得到100 μg/mL的肌醇使用液。分别吸取0.050,0.250,1.000,2.500,5.000,10.000 mL肌醇标准使用液至20 mL螺口比色管中,同1.2.1同步处理与衍生。
1.2.3 气相色谱条件 色谱柱:ZB-5ms石英毛细管柱(15.0 m×0.25 mm×0.50 μm);进样口温度260 ℃;进样体积1.0 μL,分流比5∶1;色谱柱流速1.48 mL/min;程序升温条件:120 ℃保持0 min,10 ℃/min升温至190 ℃,保持7 min,然后50 ℃/min升温至280 ℃,保持4.2 min,共20 min;检测器温度280 ℃;载气:高纯氮气,纯度≥99.999%;高纯氢气,纯度≥99.999%,流量30 mL/min;高纯空气,流量400 mL/min。
1.2.4 方法学验证 选择测定低限、常规含量水平、最高残留量(maximum residue limit,MRL)3个水平浓度进行三水平六平行的加标回收率测定,同时选择3个不同阶段奶粉及中国检验检疫科学研究院提供的奶粉质控样进行方法学验证。
2 结果与讨论
2.1 前处理方法的改进
2.1.1 提取溶剂、提取方式和净化方式对肌醇提取效率的影响 GB 5009.270—2016第二法用70%乙醇和30%超纯水配制肌醇储备液和标准使用液。试验发现,肌醇储备液在4 ℃存放10 d,将会有肌醇絮状物析出。考虑到肌醇在水中溶解度较好,在乙醇中只能微量溶解,试验方法用超纯水配制肌醇储备液和标准使用液,存放时间3个月以上均无肌醇絮状物析出。
GB 5009.270—2016第二法规定,用40 ℃温水溶解奶粉后超声10 min,用95%的乙醇定容。静置20 min后用4 000 r/min离心5 min。试验用40 ℃温水浸泡奶粉后,涡旋充分混匀,加入亚铁氰化钾和乙酸锌溶液,定容、摇匀,静置30 min后过滤。肌醇在水中溶解度显著优于在乙醇中的溶解度,因此,推测试验方法提取效率应优于国标方法。该推测在方法学试验中得到了验证。
2.1.2 滤液除水干燥方式对衍生结果的影响 GB 5009.270—2016第二法规定,取5 mL待干燥滤液至旋转蒸发浓缩瓶中,加入5 mL无水乙醇旋转浓缩至干,转移至烘箱中100 ℃烘干1 h。加入10.0 mLN,N-二甲基甲酰胺,超声溶解5 min后转移至25 mL有螺纹盖的离心管中,加入硅烷化试剂3.0 mL,在80 ℃水浴中衍生75 min。
试验方法取5 mL待干燥滤液于20 mL螺口比色管中,加入无水乙醇至10 mL,涡旋混匀,氮吹至约1~2 mL刻度处,补加无水乙醇至10 mL,氮吹至干后于100 ℃烘干0.5 h。冷却后加入0.5 mL三甲基硅烷、1 mL六甲基二硅烷和4 mLN,N-二甲基甲酰胺,涡旋混匀2 min,于80 ℃水浴中衍生20 min。
试验方法与GB 5009.270—2016第二法相比,干燥方式由旋转蒸发干燥改为氮吹干燥,旋转蒸发干燥只能小批量进行处理,样品数量多则耗时较长,而氮吹干燥可实现大批量样品的同时干燥。试验方法使用多通道可调节氮吹仪可同时干燥处理54个样品,极大地降低了大批量样品的干燥时间,同时省去了干燥后的样品由旋转蒸发浓缩瓶转移至离心管的步骤。试验采用添加乙酸锌和亚铁氰化钾的方式净化,该方法较国标方法能除去更多蛋白质和其他杂质,通过观察试验现象,试验方法氮吹后剩下的固体要显著少于国标方法旋转蒸发后剩下的固体物质。
试验方法通过在GB 5009.270—2016第二法基础上进行改进,减少了在烘箱中的干燥时间,干燥时间缩短0.5 h;同时,试验方法也缩短了在水浴锅中的衍生时间,衍生时间缩短了55 min。肌醇标准样品衍生物气相色谱图见图1,婴幼儿配方奶粉肌醇衍生物气相色谱图见图2。试验结果表明,在烘箱中烘干0.5 h已能完全去除水分,通过图2可知肌醇衍生反应产生的色谱峰无鼓包峰,且试验方法测定得到的奶粉质控样结果与其特性值十分接近。表明水分去除干净,衍生反应完全。试验表明,试验方法即使缩短了干燥及衍生时间,仍能达到较好的干燥及衍生效果。
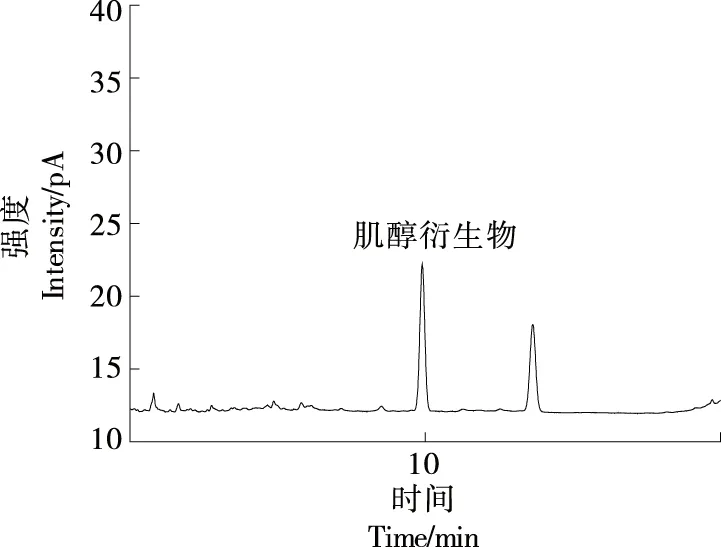
图1 肌醇标准样品衍生物气相色谱图Figure 1 Gas chromatogram of the standard derivative of inositol (100 μg/mL)
2.2 气相色谱条件的优化
GB 5009.270—2016第二法采用填料为50%氰丙基-甲基聚硅氧烷的60 m毛细管柱(DB-23),试验方法采用5%苯基-甲基聚硅氧烷(ZB-5ms)的15 m毛细管柱。GB 5009.270—2016第二法与试验方法程序升温条件比较见表1。由表1可知,试验方法单个样品分析时间缩短了43 min。这主要是因为试验方法采用的色谱柱比GB 5009.270—2016第二法采用的色谱柱长度短了3倍,因此出峰时间较快;同时由于肌醇衍生物极性较小,试验方法采用的5%苯基-甲基聚硅氧烷(ZB-5ms)为弱极性色谱柱,而GB 5009.270—2016第二法采用填料为50%氰丙基-甲基聚硅氧烷的60 m毛细管柱(DB-23)为中等极性色谱柱,因此试验方法肌醇衍生物出峰时间较快,程序升温时间减短。试验方法即使大大缩短了分析时间,但由奶粉质控样的肌醇衍生物色谱图可知(见图2),肌醇衍生物与其他杂质色谱峰分离较好,分离度都在1.5以上。试验方法极大地缩短了分析时间延长了色谱柱的使用寿命,大大地提高了检验效率。
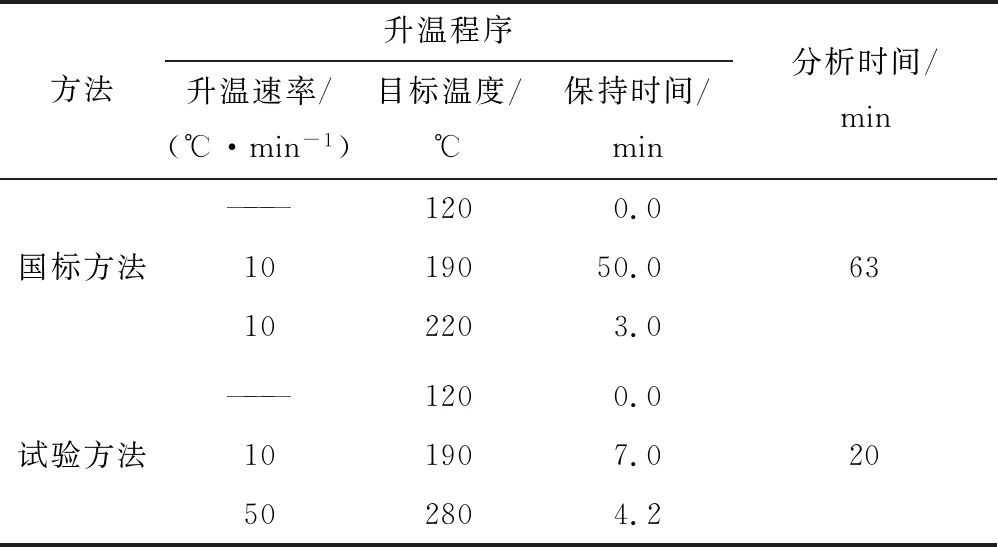
表1 试验方法与国标方法色谱柱分析程序对比Table 1 Thecomparison of chromatographic column’s analytical procedure between this paper and the national standard method
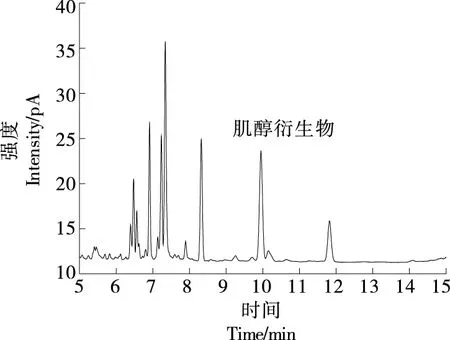
图2 婴幼儿配方奶粉肌醇衍生物气相色谱图Figure 2 Gas chromatogram of the inositol derivative of infant formula sample
2.3 方法学验证
以肌醇质量浓度(μg/mL)为横坐标,峰面积(pA·s)为纵坐标绘制标准曲线,试验方法在1~200 μg/mL范围内线性范围良好,相关系数为0.999 9,线性方程为y=3.023x-0.518,对应样品的检测范围为1~200 mg/100 g。试验方法中肌醇衍生物的3倍平均信噪比对应的质量浓度为检出限(LOD),10倍平均信噪比对应的质量浓度为定量限(LOQ),平行测定3次,取平均值获得该方法的LOD及LOQ,对应质量浓度分别为1,3 μg/mL。按照前处理方法可知,样品检出限为1.0 mg/100 g,定量限为3.0 mg/100 g。分别取一、二、三段阴性奶粉,进行三水平六平行加标试验。加标水平分别为测定低限水平、常规含量水平、MRL水平,加标量分别为3,100,190 mg/100 g。由表2可知,三水平加标回收平均回收率为97.4%~100.5%,符合GB/T 27404—2008要求。
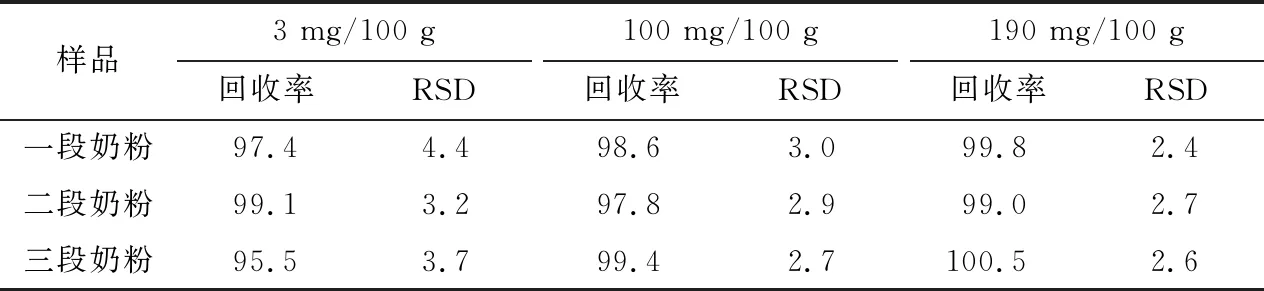
表2 准确度和精密度试验Table 2 Accuracy and precision tests (n=6) %
3个奶粉样品和1个质控样品分别用试验方法和GB 5009.270—2016第二法测定,检验结果见表3。由表3可知,试验方法测定样品肌醇含量相对标准偏差(RSD,n=6)<2.1%,运用试验方法和国标方法测定同一奶粉肌醇含量的相对偏差为1.2%~2.2%,奶粉质控样6次平行试验数据的平均值(131.9 mg/100 g)与质控样品特性值(131.1 mg/100 g)的相对偏差为0.6%。由此可知,试验方法检测结果与国标方法相近,质控样结果与真值十分接近。
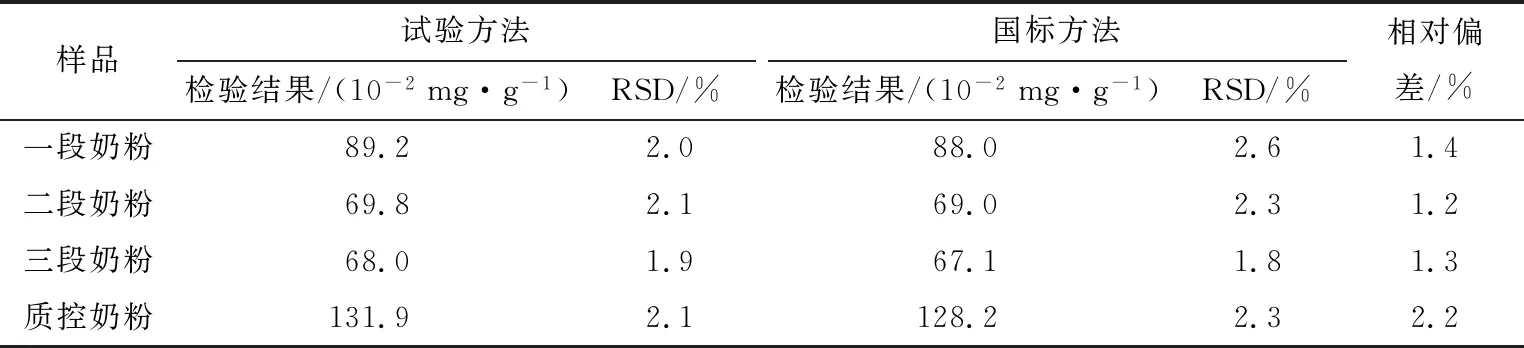
表3 试验方法与国标方法检验结果比较†Table 3 The test results of this paper and the national standard method (n=6)
3 结论
通过对GB 5009.270—2016第二法进行前处理步骤及仪器色谱条件的优化,建立了可用于实验室大批量婴幼儿配方奶粉中肌醇含量快速检测的气相色谱方法。该方法各项指标均符合GB/T 27404—2008《实验室质量控制规范 食品理化检验》要求。将该方法运用到婴幼儿配方奶粉肌醇含量的检测中,其检测结果与国标方法相近,相对偏差为1.2%~2.2%;质控样检测结果与真值十分接近,相对偏差为0.6%。该方法与已有的气相色谱方法相比,前处理时间和上机时间短、前处理简单、结果准确、可重复性好,可实现批量化样品检测。
