核壳结构米粒状FeS2/C纳米材料制备及储锂性能研究
2021-06-03夏青徐宇兴周运成纪雪倩冯海兰王鹏飞谭强强
夏青,徐宇兴,周运成,纪雪倩,冯海兰,王鹏飞,谭强强,4
(1中国科学院过程工程研究所多相复杂系统国家重点实验室,北京100190;2中科廊坊过程工程研究院,河北廊坊065001;3中国科学院绿色过程制造创新研究院,北京100190;4河北省先进能源材料技术创新中心,河北廊坊065001)
引 言
锂离子电池因具有能量密度高、无记忆效应、循环寿命长等优点,已经成为使用最为广泛的便携能源装置[1-2]。目前,以锂金属氧化物为正极,石墨为负极的商业锂离子电池已接近应用瓶颈,逐渐不能满足日益增长的能源需求,开发具有高能量密度的正负极材料已经成为当务之急[3-4]。近几十年间,科学家对一系列新型负极材料进行了研究探索,诸如合金类的硅基[5-6]、锡基[7-8],以及转换型的过渡金属氧化物[9-11]、过渡金属硫化物[12-14]等。其中,二硫化铁(FeS2)具有高理论比容量(894 mA·h·g-1)、低成本以及环境友好等优点,被认为是一种非常具有潜力的高能量密度锂离子电池负极材料[15]。然而,在放电过程中,FeS2材料与锂发生转换反应生成高活性的纳米Fe单质和绝缘的Li2S。纳米Fe单质发生团聚,以及多硫化物原位溶解生成硫单质,导致电极容量的衰减[16]。同时,FeS2材料面临着电子电导低、循环过程中体积变化大等问题,使得其电化学循环性能较差、容量保持率较低,限制了它的商业化应用[17]。
针对这些问题,大量研究通过减小材料颗粒尺寸来改善其电化学性能,如纳米线[18]、纳米立方体[19]等。制备纳米FeS2材料或构造特殊形貌FeS2颗粒,可缩短锂离子传输路径,缓冲材料在充放电过程中的结构应力变化,增大与电解液的接触面积,以及减少循环过程中的硫穿梭效应。如荣华等[20]采用水热法一步合成了由纳米片堆积的FeS2微球,在2 A·g-1的大电流密度条件下,500次循环后依然稳定保持350 mA·h·g-1的可逆比容量。除此之外,将FeS2材料与碳基材料复合,也可有效改善其电化学性能,如石墨烯[21]、碳纳米管[22]等。碳基材料可起到提高材料电子电导的作用,同时稳定电极结构,避免活性物质在循环过程中剥落。与碳基材料复合的FeS2材料多具有良好的结构稳定性,表现出稳定的循环性能。如Fan等[23]通过水热法合成类葡萄簇结构的FeS2/碳纳米纤维复合材料,能够在5 A·g-1电流密度下循环1000次后保持573.4 mA·h·g-1的可逆比容量。Jing等[24]制备出FeS2/碳/石墨烯复合材料,利用两种碳的保护作用,构建二元的锂离子/电子传输通道。所合成的材料在2 A·g-1电流密度下循环400次后比容量为678 mA·h·g-1,容量保持率为93.8%。Yin等[25]合成的FeS2@多孔碳八面体复合负极材料,表现出优异的倍率性能和循环稳定性,在5 A·g-1电流密度下可逆比容量为381 mA·h·g-1,100 mA·g-1电流密度下循环100次可逆比容量为1071 mA·h·g-1。Xi等[26]合成了纳米花状缺陷富集型FeS2@三维多层级结构杂原子掺杂碳复合材料,在0.1 C电流密度下首次比容量达到841 mA·h·g-1,在4 C大电流密度下循环3000次容量衰减率仅为每圈0.020%。
虽然针对FeS2负极材料的改性已有大量研究,但具有均匀碳包覆结构超细FeS2纳米颗粒的合成仍然是一个难点,FeS2的电化学性能也有待进一步提升。有鉴于此,本文通过阴离子置换反应制备出具有核壳结构的米粒状FeS2/C纳米材料,并对其电化学性能进行了研究。
1 实验材料和方法
1.1 材料制备
实验中采用分析纯级药品为试剂原料。具体制备过程如下:将50 ml浓度为5.4 mol·L-1的NaOH水溶液在75℃下逐滴滴入50 ml浓度为2 mol·L-1的Fe(NO3)3·9H2O溶液,混合搅拌5 min后,将溶液转移至100℃下干燥陈化4 d。将所得粉体用去离子水和无水乙醇洗涤数次后烘干获得前体材料。将0.32 g前体材料加入400 ml浓度为10 mmol·L-1的三羟甲基氨基甲烷缓冲液(pH=8.5)中,超声分散30 min。将0.16 g盐酸多巴胺缓慢溶解于上述溶液中,并保持搅拌3 h。将所得粉体收集,离心洗涤烘干得到棕色粉末。将0.2 g棕色粉末与0.8 g升华硫混合研磨,转移至密封管中在N2气氛下400℃处理3 h,获得FeS2/C材料。作为对比样的FeS2材料由直接将0.2 g前体材料与0.8 g升华硫混合,转移至密封管中在N2气氛下400℃处理3 h而获得。
1.2 材料表征
采用X射线衍射技术(XRD,Smartlab,Cu靶,入射波长0.15406 nm)分析样品物相;通过拉曼光谱仪(Raman,inVia)采集材料的拉曼光谱;采用场发射扫描电子显微镜(FESEM,SU8020)和高分辨透射电子显微镜(TEM,JEM-2100F)技术观测样品形貌;通过热重(TG/DSC,TG-DTA6300,升温速率10℃·min-1)表征材料的组分含量。
1.3 电池组装与电化学性能测试
将所制备样品与乙炔黑、聚偏氟乙烯(PVDF)按照质量比70∶15∶15的比例于N-甲基吡咯烷酮溶剂中均匀混合搅拌,获得均匀浆料。将浆料涂覆于铜箔集流体上,并在真空条件下120℃干燥12 h。将烘干后的电极裁剪为直径为10 mm的极片进行电池组装,活性物质在极片上的面载量为1 mg·cm-2左右。以直径为16 mm的金属锂片为对电极,直径为16 mm的聚丙烯微孔膜Celgard 2400为隔膜,1 mol·L-1LiPF6/EC+DEC+DMC(体积比1∶1∶1)为电解液在氩气气氛下组装半电池,电池型号为2025。采用LAND电池测试系统对电池进行恒流充放电测试,电压范围为0.01~3.0 V;采用Arbin测试系统对电池进行循环伏安测试分析,扫描速率0.1 mV·s-1;采用IM6电化学工作站对电池进行电化学阻抗谱测试,频率范围为1 MHz到100 mHz。
2 实验结果与讨论
2.1 样品的物相及形貌分析
图1为所制备FeS2/C复合物和纯FeS2的XRD谱图。所制备样品各衍射峰与FeS2(JCPDSNo.42-1340)的标准谱图吻合度高,证实已成功获得FeS2,且样品中不含杂质相。样品属于立方晶系,在28.5°、33.1°、37.1°、40.8°、47.4°、56.3°、59.0°、61.7°和64.3°处的衍射峰分别对应(111)、(200)、(210)、(211)、(220)、(311)、(222)、(023)以及(321)晶面。

图1 所制备FeS2/C复合材料和纯FeS2的XRD谱图Fig.1 XRDpatterns of the as-prepared FeS2/Ccompositeand pure FeS2
为了表征FeS2/C复合材料中碳的状态,对材料进行了拉曼光谱分析,结果如图2所示。由图可知,在1405 cm-1和1542 cm-1位置有两个明显的特征峰,分别对应着碳的D峰和G峰[27]。其中,D峰与碳的原子晶格缺陷有关,而G峰则是由sp2杂化的伸缩振动引起[28]。

图2 FeS2/C复合材料的拉曼光谱Fig.2 Raman spectrum of the FeS2/Ccomposite
为了得到FeS2/C复合材料中各组分的含量,对样品进行了热重测试。FeS2/C样品在空气中的TGA结果如图3所示。所得曲线证明材料存在两个分解过程,分别为300~400℃之间失重12.7%以及550~700℃之间失重26.9%。其中,300~400℃之间的失重对应着碳的气化,而550~700℃之间的失重则归因于FeS2到Fe2O3的转换反应[29]。随着温度的继续升高,样品不再发生质量变化,可知最终所得Fe2O3的质量比为60.4%。根据结果可计算出FeS2/C复合材料中碳的质量比为9.2%,FeS2的质量比为90.8%。
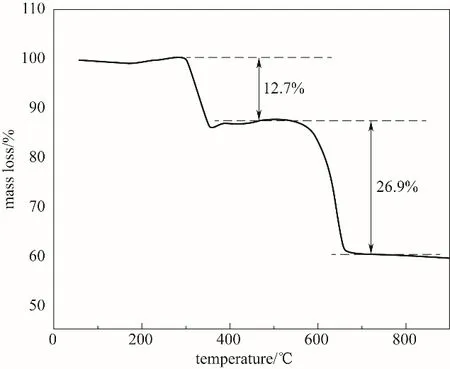
图3 FeS2/C样品在空气中的TGA结果Fig.3 TGA result of FeS2/Csample under air atmosphere
图4(a)~(c)分别为前体、FeS2样品以及FeS2/C样品的场发射电镜照片。由图可知,前体为米粒状纳米颗粒,形貌均匀,分散程度高,颗粒长约150~180 nm,宽约为100~130 nm。FeS2样品颗粒形貌不均匀,呈现严重团聚状态。FeS2/C样品则保持了前体的米粒状颗粒形貌,大小均匀,分散度高。图4(d)~(f)为FeS2/C样品的透射电镜照片。在图4(d)中,可以观察到FeS2/C样品表面有一层均匀的碳膜。由图4(e)可知,碳膜的厚度小于10 nm。从形貌分析可知,FeS2和表面碳膜实现了较好的复合,碳膜的包覆能够保持材料形貌,避免颗粒的团聚,从而提高材料的循环稳定性。图4(f)为FeS2/C样品的高分辨透射电镜照片。从图上可以看出,FeS2/C材料的晶面条纹清晰规整,表现出良好的结晶性。其放大图对应晶格条纹的晶面间距为0.242 nm,对应FeS2的(210)晶面。

图4 前体(a)、FeS2样品(b)以及FeS2/C样品(c)的场发射电镜照片;FeS2/C样品的透射电镜照片[(d)~(f)]Fig.4 FESEMimages of the precursor(a),FeS2 sample(b),and FeS2/Csample(c);TEM images of FeS2/Csample[(d)—(f)]
FeS2/C复合材料的合成过程如图5所示。首先,Fe2O3前体通过液相反应被均匀包覆一层聚多巴胺(PDA),获得Fe2O3/PDA。随后,将所得Fe2O3/PDA与单质硫均匀混合,在N2气氛下热处理进行硫化,热处理过程中PDA碳化,最终获得具有核壳结构的米粒状FeS2/C纳米复合材料。在材料制备过程中,分两步制备硫化铁材料,先进行PDA包覆,再利用阴离子置换反应对前体进行硫化。这种方法可以使材料保持其原始形貌,避免在硫化反应过程中的形貌破坏,同时在材料表面原位包覆均匀碳层,提高与FeS2之间的结合力,改善材料电子电导,使其具有更高的电化学活性。此外,均匀的碳层可协助材料在循环过程中生成更为稳定的固体电解质(SEI)膜,阻碍转换反应产物多硫化物在电解液中的溶解,提高材料的循环稳定性。
2.2 电化学性能分析


图5 米粒状FeS2/C复合材料合成过程示意图Fig.5 Schematic illustration of the formation process for rice-like FeS2/Ccomposite
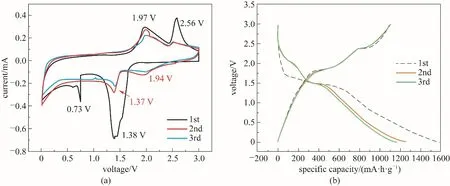
图6 FeS2/C电极的循环伏安图和容量电压曲线图Fig.6 CV curves and charge-discharge profilesfor FeS2/Celectrode

图6(b)为FeS2/C电极在100 mA·g-1电流密度下的前三圈容量电压曲线图,扫描电压范围为0.01~3.0 V。首次放电过程中,FeS2/C电极在1.5 V左右出现一个较为明显的放电平台,对应于循环伏安曲线中的首次放电还原峰(1.38 V)。在1.0 V以下出现的斜坡平台则对应首次不可逆固体电解质膜的生成。首次循环后,FeS2/C电极的容量电压曲线基本重合,与CV测试结果一致,样品表现出良好的结构稳定性。FeS2/C电极的首次放电比容量和充电比容量分别为1575 mA·h·g-1以及1091 mA·h·g-1,首次库仑效率为69.3%。首次不可逆主要是由材料表面不可逆固体电解质膜的生成以及Li2S的不完全分解引起[32]。在随后的两次循环中,FeS2/C电极的充电比容量为1100.7 mA·h·g-1以及1104.5 mA·h·g-1,库仑效率逐渐升高到87.8%和95%,体现了良好的循环可逆性。
图7(a)为FeS2/C电极以及FeS2电极在0.01~3.0 V电压范围内,100 mA·g-1电流密度下的循环性能。由图可知,FeS2/C电极在循环初期容量表现出缓慢上升趋势,之后保持稳定。容量的缓慢上升归因于材料在循环初期的活化过程中,随着锂离子的嵌入/脱出,表面产生了更多的活性位点,以及新暴露材料表面固体电解质膜的再次生成,这种情况在过渡金属硫化物、过渡金属氧化物等电极材料中十分常见[33]。FeS2/C电极循环80圈之后容量仍保持在1100 mA·h·g-1,远高于FeS2的理论比容量。这种情况可能由于材料在低电位下,还原产物Fe金属纳米颗粒可以存储大量自旋极化的电子,产生大量额外电容,以及表面胶状固体电解质膜的可逆生成引起[34]。为了进行对比,将未进行碳包覆直接硫化所得的FeS2电极在同样条件下进行了循环测试,结果如图7(a)所示。30次循环之后,FeS2电极的比容量迅速衰减到了582 mA·h·g-1。实验结果证实,所制备的FeS2/C材料在作为电极时,由于其具有碳包覆核壳结构,拥有更加优异的循环稳定性。
图7(b)为FeS2/C电极在不同电流密度下的阶梯倍率循环性能。随着电流密度的增大,充放电比容量逐步下降。在100、200、500以及1 A·g-1电流密度下的可逆比容量分别为1217、1196、1090以及1015 mA·h·g-1。即使在2 A·g-1的大电流密度下,可逆比容量仍能保持在866 mA·h·g-1。在经过多个电流密度循环后,当电流密度从2000 mA·g-1回复至100 mA·g-1时,FeS2/C电极的电流密度能够立刻回复到1202 mA·h·g-1,体现了较好的回复性能和抗大电流冲击能力。
对FeS2/C和FeS2电极进行交流阻抗谱(EIS)测试,结果如图8所示。两个电极的交流阻抗谱均由半弧形的高/中频段以及与实轴(Z′)呈一定角度的低频斜线段组成。其中,高/中频段的弧对应与固体电解质膜相关的膜阻抗(Rf)以及电荷转移电阻(Rct),低频段的斜线则主要与电化学扩散过程有关,代表锂离子的扩散阻抗(W)。由图可知,FeS2/C电极的电荷转移电阻明显小于FeS2电极,说明FeS2/C电极中的电荷转移过程更为容易,电化学活性较高,具有较快的电极反应动力。

图8 FeS2/C和FeS2电极的阻抗谱Fig.8 Nyquist plots of FeS2/Cand FeS2 electrodes
通过上述分析可知,FeS2/C表现出良好的电化学稳定性和倍率性能,主要归因于其独特的设计理念和微观结构,可归纳为以下几个方面:(1)外层的碳壳和内部的FeS2构建了均匀的核壳结构,内部FeS2提供了高比容量,外层的碳壳可以提高复合材料的电子电导,同时可缓解材料在充放电过程中因应力不均引起的开裂现象,从而提高材料的结构稳定性;(2)均匀包覆的碳层可协助生成更为稳定的SEI膜,阻碍多硫化物在电解液中的溶解,提高材料的循环稳定性;(3)通过先包覆碳层后硫化的方式,可使材料保持其纳米级颗粒尺寸,阻止材料的团聚;(4)纳米级颗粒为材料的电极反应提供了较大的表面积,有利于电解液的充分浸润,为材料表面电荷的传输提供了较短的离子和电子的传输路径,加速了电极反应动力学过程;(5)纳米级颗粒能够缓解材料在电化学反应过程中的结构应变应力,从而使其具有优异的结构稳定性。
3结 论
本文通过阴离子置换反应制备出具有核壳结构的米粒状FeS2/C纳米材料。因具有独特的微观结构,所合成的FeS2/C材料具有较高的离子和电子电导,优异的电解液浸润特性,以及缓冲材料体积变化的能力。在作为锂离子电池负极材料时,FeS2/C电极具有较高的可逆比容量以及优秀的倍率性能,100 mA·g-1电流密度下可逆比容量高达1100 mA·h·g-1,在2 A·g-1的大电流密度下,依然有866 mA·h·g-1可逆比容量。研究结果表明,通过阴离子置换的方式可以构建具有特殊结构的纳米材料,避免在硫化过程中材料形貌的变化,从而改善其电化学性能。该结果为其他高性能金属硫化物核壳材料的制备提供了新的思路和方法。
