混合盐模板法制备超级电容器用氮掺杂分级多孔碳纳米片
2021-06-03焦帅杨磊武婷婷李宏强吕辉鸿何孝军
焦帅,杨磊,武婷婷,李宏强,吕辉鸿,何孝军
(安徽工业大学化学与化工学院,安徽马鞍山243002)
引 言
随着化石燃料的大量消耗,带来的能源和环境问题不容忽视。因此,近年来人们致力于开发高效的能量转换与存储设备(如二次电池、太阳能电池等),以收集可再生能源(如风能、太阳能等)[1-4]。基于亥姆霍兹双电层理论,出现了一种新型储能元件-超级电容器(也称电化学电容器),它是通过电位驱动的离子积累来存储能量,以平衡多孔电极的表面电荷。超级电容器是一种高效的储能元件,具有广泛的应用前景[5-6]。但是,超级电容器的电荷存储仅发生在电极表面(或近表面),这导致其容量远低于电池,从而限制了超级电容器的推广应用[7]。
电极材料对超级电容器储电性能起着至关重要的作用。常用的电极材料包括多孔碳材料、导电聚合物和金属氧化物等[8-11]。其中,多孔碳材料因导电性好、比表面积大、化学稳定性好等优点受到了研究者的广泛关注。例如,Zhang等[12]从煤焦油沥青出发,通过溶剂萃取-温和改性-活化过程制备了具有可调介孔的蜂窝状多孔碳纳米片。作为超级电容器电极材料,分级多孔碳材料比单一孔径的碳材料具有明显的优势[13-14]。分级多孔结构不仅能显著促进电解液离子的传输,而且能提供大的表面积,保证了大量的离子吸附,从而提高电容器的容量[14]。目前,将模板法与活化法相耦合是制备分级多孔碳材料最有效的策略之一[15-17]。例如,本课题组[18]使用纳米ZnO模板法结合KOH原位活化技术直接从煤沥青制备了具有丰富微孔/中孔的相互连接的石墨烯纳米囊。但该策略在材料制备过程中需使用一定量的酸和碱,对环境有污染。因此,亟需开发一种无酸无碱制备分级多孔碳的技术[19]。
基于此,本文报道了一种NaCl和Na2CO3混合盐模板法,以煤沥青为碳前体,K2CO3为活化剂,在NH3气氛下制备超级电容器用氮掺杂分级多孔碳纳米片(NHCNs)。其中,以热塑性煤沥青作为碳源时,NaCl和Na2CO3混合盐模板起到了占位造孔的作用,最后,通过水洗去除模板后,可以形成分级孔碳[20]。文中还考察了混合盐模板中NaCl和Na2CO3的质量比对NHCNs的结构及其电化学性能的影响。
1 实验材料和方法
1.1 试剂与材料
煤沥青(马鞍山钢铁股份有限公司);无水碳酸钾(K2CO3,上海阿拉丁生化科技股份有限公司,AR);氯化钠(NaCl,上海阿拉丁生化科技股份有限公司,AR);无水碳酸钠(Na2CO3,上海阿拉丁生化科技股份有限公司,AR);聚四氟乙烯(PTFE,太原力之源有限公司)。
1.2 NHCNs的制备
首先,称取2 g煤沥青、10 g K2CO3、X(X=3、4、5)g NaCl、1 g Na2CO3放入研钵中充分研磨。然后将混合物转移到管式炉中,并用NH3以30 ml·min-1的流量将炉内的空气排尽。随后以5℃·min-1的速率将混合物从室温加热至150℃,并恒温30 min,继续加热至850℃,并恒温60 min,在NH3气氛下自然冷却至室温。取出产物,放入蒸馏水中并搅拌12 h,然后再反复洗涤除去杂质。最后,在110℃烘箱中干燥12 h后获得样品。所制样品命名为NHCNs,按照加入NaCl的质量分别命名为NHCNX,下标X为NaCl的质量。
1.3 表征
采用场发射扫描电子显微镜(FESEM,Hitachi,S4800)、透射电子显微镜(TEM,JEOL-2100)、比表面分析仪(ASAP 2020)、X射线粉末衍射仪(XRD,Ultima IV,Japan)、拉曼光谱仪(JYLab-Raman HR800)对氮掺杂分级多孔碳纳米片(NHCNs)进行了表征。利用Brunauer-Emmett-Teller(BET)方法在0.05~0.30的相对压力下计算样品的比表面积(SBET)。采用密度泛函理论(DFT)方法计算孔径分布。在0.99的相对压力下,获得了总孔隙体积(Vt)。用tplot法估算了微孔体积(Vmic)。采用Dap=4Vt/SBET方程计算NHCNs的平均孔径(Dap)。用X射线光电子能谱仪(XPS,Thermo ESCALAB250)分析了NHCNs中碳、氧、氮元素的含量和化学键状态。
1.4 电化学测试
将NHCNs[85%(质量)]和聚四氟乙烯[15%(质量)]调成浆料并碾压成膜。随后用冲孔机将膜制成直径为12 mm的碳片(负载量约为2.0 mg·cm-2),置于110℃真空干燥箱内干燥2 h。将质量、形状相似的两个碳片压在泡沫镍上,随后在真空条件下将两电极片浸泡于6 mol·L-1KOH电解液中保持2 h,然后组装成对称的纽扣式超级电容器。在CHI760E电化学工作站(上海辰华仪器有限公司)上用循环伏安法对超级电容器进行了评价。在超电容测试系统(SCTS,美国Arbin仪器公司)上进行了充放电性能测试。电化学阻抗(EIS)是在输力强阻抗分析仪(SI1260,英国Solartron Analytical)上测试的,阻抗测试的频率范围为10-3~105Hz,交流信号振幅电压为5 mV。
根据式(1)由GCD曲线计算NHCNs电极比电容:
式中,C是单电极的比电容,F·g-1;I是放电电流,A;m是两电极中活性物质的总质量,g;ΔV是放电电压,V;Δt是放电时间,s。
根据式(2)、式(3)分别计算NHCNs电容器的能量密度和功率密度:
式中,E是电容器的能量密度,W·h·kg-1;P是电容器的功率密度,W·kg-1;Δtd是放电时间,s。
2 实验结果与讨论
图1是NHCNs的制备流程示意图。首先,将煤沥青、NaCl、Na2CO3、K2CO3按照一定比例均匀混合,随后放入管式炉中,在NH3气氛下进行加热。当温度达到150℃时,煤沥青开始软化并包裹模板和活化剂。随着温度的升高,煤沥青中芳香环自由基开始发生聚合反应,从而形成相互连接的碳纳米片。当温度超过700℃时,K2CO3与碳纳米片开始反应形成孔隙[21]。最后,使用蒸馏水洗去杂质,得到NHCNs。活化机理如式(4)~式(7)所示:

通过场发射扫描电子显微镜(FESEM)和透射电子显微镜(TEM)对材料形貌进行表征,研究混合盐模板中NaCl与Na2CO3的质量比对材料微观形貌的影响。从图2(a)~(c)中可以看出,NHCNs呈现三维互连的片状结构。随着NaCl质量的增加,NHCNs三维结构中的空腔变大,并且碳纳米片尺寸增大。三维互连的片状结构可以增加电解液与活性物质之间的接触面积,有助于电解液的浸润[22]。从透射电镜图[图2(d)]可以看出,NHCN4含有许多褶皱,这些褶皱可以防止片与片之间的堆叠,促进电解液离子的传输,提高孔隙利用率[22]。图2(e)表明NHCN4三维互连的片状结构由二维的薄片构成。

图1 NHCNs的制备流程示意图Fig.1 The schematic for the preparation of NHCNs

图2 NHCN3(a),NHCN4(b),NHCN5(c)的扫描电镜图;NHCN4的透射电镜图(d);NHCN4的高分辨率透射电镜图(e)Fig.2 FESEM images of NHCN3(a),NHCN4(b),NHCN5(c);TEM image of NHCN4(d);High resolution TEM image of NHCN4(e)
采用N2吸脱附、X射线光电子能谱(XPS)等表征手段,研究混合盐模板中NaCl与Na2CO3的质量比对材料孔隙结构与表面元素组成的影响。从NHCNs的N2吸脱附等温线[图3(a)]可以看出,三个样品的吸脱附等温线均为Ⅳ型曲线,在相对压力P/P0<0.1的条件下,出现较高的吸附量;在P/P0为0.4~0.99时,吸脱附等温线出现明显的滞后环。上述结果表明NHCNs中存在大量的微孔和中孔。薄片上的中孔可以为离子传输提供通道,微孔提供了大量的活性位点用于离子吸附[23]。图3(b)为NHCNs的孔径分布图。可见,微孔主要分布在0.4~2.0 nm之间,中孔分布在2.0~7.0 nm之间。表1为NHCNs样品的孔结构参数。随着NaCl质量的增加,NHCNs的比表面积 先 由1453 m2·g-1(NHCN3)增 大 到1597 m2·g-1(NHCN4),随 后 降 低 到1324 m2·g-1(NHCN5)。同 时,NHCN4具有最大的Dap(2.63 nm)和Vt(1.05 cm3·g-1),说明改变NaCl与Na2CO3的质量比可以调控NHCNs材料的孔结构参数。图3(c)为NHCNs的X射线衍射(XRD)谱图。NHCNs在24°和44°处出现两个较宽的衍射峰,分别对应于碳的(002)和(100)面[24]。从NHCNs的拉曼光谱图[图3(d)]中可以看出,所有的样品均在1348、1593、2670 cm-1处出现峰,分别表示D峰、G峰和2D峰。其中,D峰是由无定形碳结构引起,G峰是由石墨化碳结构引起,而2D峰是由三维石墨烯结构引起[25]。此外,ID/IG(D峰与G峰的强度比值)可以表示碳材料石墨化度。NHCN3、NHCN4、NHCN5的ID/IG值分别为0.92、0.94、0.96,说明材料的石墨化程度较高,导电能力较强[25]。
如图4(a)所示,NHCNs的XPS光谱在285.0 eV、400.0 eV、531.0 eV处存在三个特征峰,分别对应C、N、O三种元素[26]。NHCN4的N 1s谱图[图4(b)]中显示了三种含氮官能团,分别为吡啶N(N-6,398.9 eV)、吡咯N(N-5,400.1 eV)、石墨化N(N-Q,401.0 eV)[27]。通过表2可知,NHCN4的N含量最高,为3.72%,且N-5的含量也最高。碳材料骨架表面的含氮官能团有助于提高电极材料在电解液中的润湿性;此外,N-5和N-6可以通过法拉第反应产生赝电容,N-Q可以改善碳材料表面的电子云密度,有利于电子转移,提高材料导电性[26,28]。

表1 NHCNs的孔结构参数Table 1 The pore structure parameters of NHCNs
将NHCNs组装成对称的超级电容器,在0~1 V的电压区间、6 mol·L-1KOH电解液中对其电化学性能进行评估。如图5(a)所示,NHCNs电极在2 mV·s-1扫描速率下的CV曲线均呈现类矩形,说明NHCNs电极具有理想的双电层电容行为[29]。其中,NHCN4电极的CV曲线面积最大,表明其比电容最高。图5(b)为NHCN4电极在不同扫描速率下的CV曲线。可见,即使在200 mV·s-1的扫速下,CV曲线仍为类矩形,表明NHCN4电极具有优异的倍率性能[15]。图5(c)为NHCNs电极的GCD曲线,三条曲线均呈线性、对称分布,且压降较小(NHCN4电极的压降仅为0.0014 V),表明其具有较好的电导率[30]。NHCNs电极在不同电流密度下的比电容如图5(d)所示。在电流密度为0.05 A·g-1下,NHCN4电极的比电容(239 F·g-1)高于NHCN3(209 F·g-1)和NHCN5(185 F·g-1)电 极。当 电 流 密 度 为40 A·g-1时,NHCN3、NHCN4、NHCN5电极的比电容分别为151、151、95 F·g-1。NHCN4电极的比电容高于文献报道值(表
3)[31-35]。在相同电流密度下,NHCN4电极的比电容较大,这归功于NHCN4具有较高的比表面积(表1),可以提供大量的活性位点用于离子吸附;此外,NHCN4的N含量最高(表2),能提供更多的赝电容。然而,NHCNs电极的比电容值随着电流密度的增大均呈下降的趋势,这是因为在较小的电流密度下,电解液离子扩散较慢,能够很好渗透到电极材料孔隙当中,进而形成双电层。随着电流密度增大,电解液离子扩散加快,使得电极材料中部分孔隙难以被充分利用,从而导致比电容下降[36-37]。
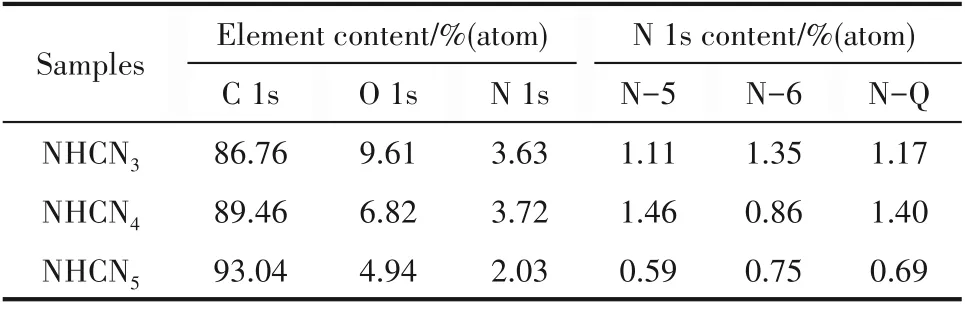
表2 NHCNs中碳、氧和氮元素含量Table 2 Contents of carbon,oxygen and nitrogen elements in NHCNs
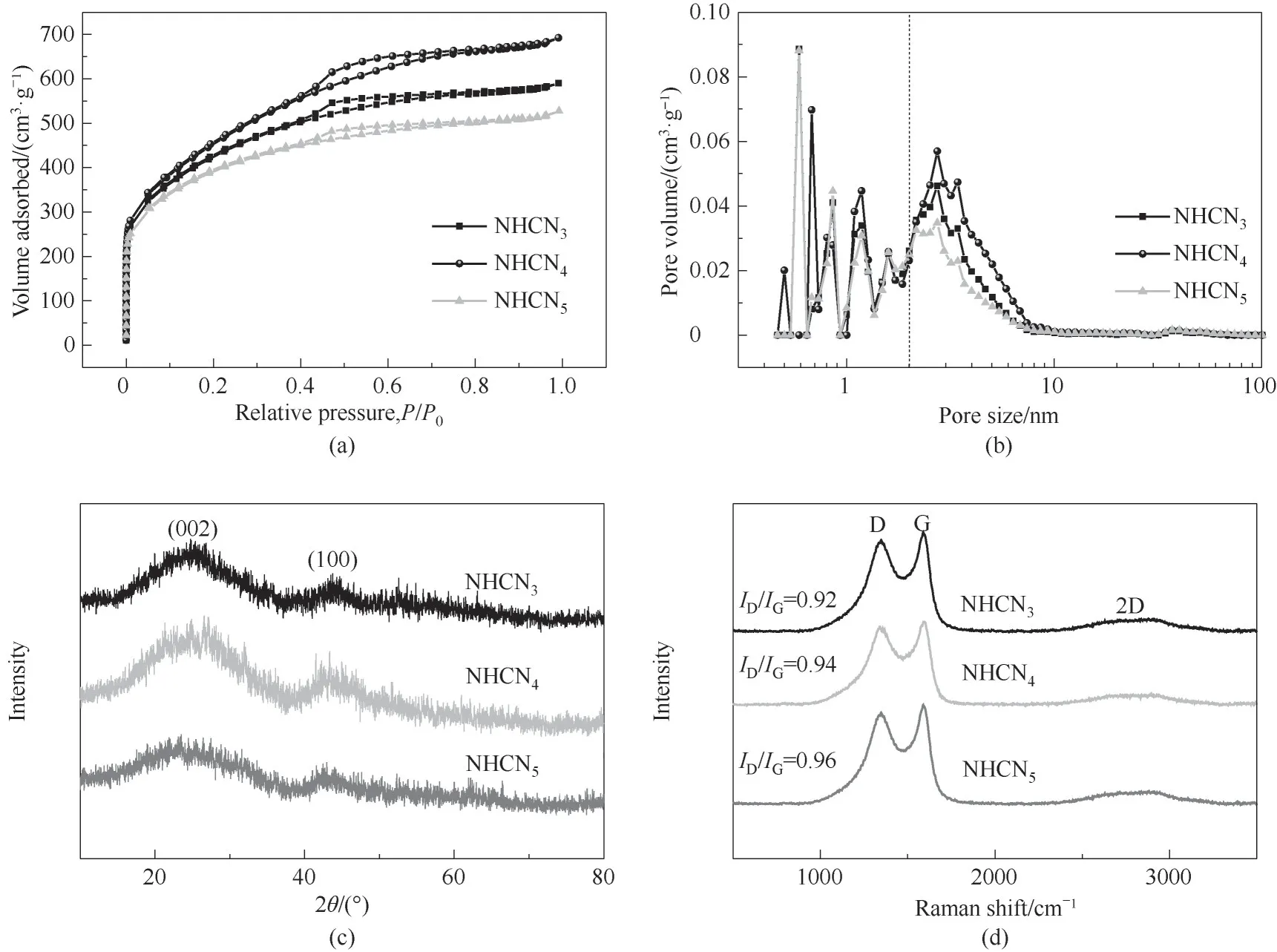
图3 NHCNs的N2吸脱附等温线(a);孔径分布(b);XRD谱图(c);Raman谱图(d)Fig.3 Nitrogen adsorption-desorption isotherms(a);Pore size distribution(b);XRDpattern(c);Raman spectra of NHCNs(d)
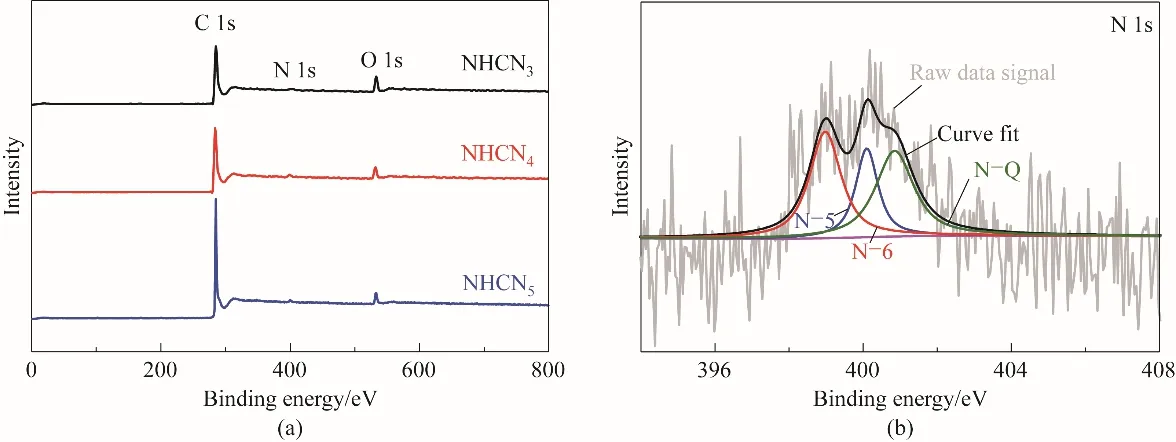
图4 NHCNs的XPS全谱图(a);NHCN4的N 1s谱图(b)Fig.4 Full XPSspectra of NHCNs(a);N 1s spectrumof NHCN4(b)

图5 NHCNs电极在扫描速率为2 mV·s-1下的CV曲线(a);NHCN4电极在不同扫描速率下的CV曲线(b);NHCNs电极在0.05 A·g-1电流密度下的GCD曲线(c);NHCNs电极在不同电流密度时的比电容图(d)Fig.5 CV curves of NHCNelectrodes at the scan rate of 2 mV·s-1(a);CV curves of NHCN4 electrode at different scan rates(b);GCD curves of NHCNelectrodes at 0.05 A·g-1(c);Specific capacitance of NHCNelectrodes at various current densities(d)

表3 不同碳电极材料的比电容Table 3 The specific capacitance of different carbon electrode materials
图6(a)为NHCNs电容器的Ragone图,当平均功率密度为26 W·kg-1时,NHCN4电容器的能量密度为9.4 W·h·kg-1,高于NHCN3(8.6 W·h·kg-1)和NHCN5(6.2 W·h·kg-1)电容器的能量密度。为了对NHCNs电容器的电化学性能进一步地评估,对其进行了交流阻抗测试。通过NHCNs电极的Nyquist图[图6(b)]可知,NHCN4电极的内部欧姆电阻(Rs)和电荷转移电阻(Rct)分别仅为0.5、2.0Ω,说明NHCN4具有快速的电子传导和离子传输能力[38]。在低频区,三条Nyquist曲线均近似垂直横坐标,表明电解液能够充分浸润到NHCNs的孔隙中,使NHCNs电极具有理想的双电层电容行为[39-40]。图6(c)为NHCNs电极的Bode图,可见NHCN4电极在-45°相位角处对应的松弛时间(τ0=1/f0)仅为1.3 s,较小的松弛时间再次证实了NHCN4电极具有快速的离子传输能力[30]。通过图6(d)可知,NHCN4电极经过在10000次充放电测试后,可获得96.9%的高比电容保持率,说明该电极具有优异的循环稳定性。综上所述,NHCNs电极的优异性能可归因于材料的结构优势:(1)三维互连的褶皱碳纳米片为电子转移提供了导电的sp2碳网,从而加快了电子的转移,增强材料导电性;(2)分级多孔结构(中孔可作为离子传输通道,微孔可吸附大量离子)不仅能显著促进电解液离子的传输,而且能提供大的表面积,保证了大量的离子吸附,从而提高电容器的容量;(3)表面的含氮官能团可提高材料亲水性,并贡献赝电容。

图6 NHCNs电容器的Ragone图(a);NHCNs电极的Nyquist图(b);NHCNs电极的Bode图(c);NHCN4电极在5 A·g-1电流密度下循环10000次的比电容保持率(d)Fig.6 Ragone plots of NHCNcapacitors(a);Nyquist plots of NHCNelectrodes(b);Bode plots of NHCNelectrodes(c);Capacitance retention of NHCN4 electrode at 5 A·g-1 after 10000 cycles(d)
3结 论
(1)本文采用混合盐模板法制备了氮掺杂分级多孔碳纳米片(NHCNs)。得益于其较高的比表面积(1597 m2·g-1)、丰富的N含量(3.72%)和三维互连的褶皱片状结构,NHCN4电极具有优异的超级电容性能。
(2)在6 mol·L-1KOH电解液中,0.05 A·g-1电流密度时,NHCN4电极比电容为239 F·g-1;10000次循环后电容保持率为96.9%,展现出优异的循环稳定性。
(3)本文为超级电容器用氮掺杂分级多孔碳纳米片的制备提供了一种无酸无碱的技术。
