沙门氏菌LAMP检测方法的建立及其在蔬菜栽培土壤中的应用
2021-05-31刘兰英陈丽华李玥仁
吕 新,刘兰英,陈丽华,李玥仁
(1. 福建省农业科学院农业质量标准与检测技术研究所,福建 福州 350003;2. 福建省农产品质量安全重点实验室,福建 福州 350003)
0 引 言
【研究意义】沙门氏菌是最主要的病原微生物之一,由其引起的食物中毒占食物中毒病例的第1或第2位[1]。仅在2005—2011年,国外发生的19起蔬菜因病原微生物污染而引起的食源性疾病案例中,有11起是由沙门氏菌污染引起的,占比高达58%[2]。沙门氏菌也是我国食源性疾病的主要病原体,我国发生的细菌性食源性中毒事件中有80%左右由沙门氏菌引起[3]。国内已有多篇研究文献发现胡萝卜、香菜、香葱、生菜等新鲜蔬菜中存在沙门氏菌污染风险[4−6]。蔬菜的沙门氏菌污染可能发生在从农田到餐桌的每个环节[7−8],近年来,随着对蔬菜供应链主要环节中沙门氏菌污染风险和来源的深入研究,发现沙门氏菌污染风险虽然贯穿供应链的每个主要环节,但仍以栽培环节,特别是蔬菜栽培土壤中沙门氏菌污染风险最大,也是沙门氏菌检测和风险控制的重点[8−11]。【前人研究进展】目前环介导等温扩增技术(loop-Mediated Isothermal Amplification,LAMP)已经运用到多种食品中沙门氏菌的快速检测中,因其具有快速、灵敏的优点备受关注。Hara-Kudo等[12]采用环介导等温扩增技术,可以检出沙门氏菌最低含量为2.2 CFU·管−1,并在1 h以内获得检测结果;张宏伟等[13]采用环介导等温扩增技术检测食品样品中沙门氏菌最低检出限为1.5 CFU·hg−1;王瑾等[14]采用实时荧光环介导等温扩增技术,可检测沙门氏菌最低含量为6 CFU·管−1,人工污染鸡肉的检出限为450 CFU·g−1,全程用时约7 h;Wu等[15]利用实时荧光定量环介导等温扩增技术对生菜中沙门氏菌进行检测,灵敏度达到了4 CFU.g−1,而检测过程仅需3 h左右;庞心怡等[16]采用环介导等温扩增技术快速检测肉类中沙门氏菌,对人工污染的沙门氏菌肉样检测灵敏度达98 CFU·mL−1,而全程仅用时15 h。【本研究切入点】目前对沙门氏菌检测多采用国标《食品安全国家标准 食品微生物学检验 沙门氏菌检验》(GB 4 789.4—2016)方法,但该方法需要对待检样品进行预增菌、选择性分离和生化试验鉴定,操作繁琐,耗时费力,仅筛选出沙门氏菌可疑菌落就需要3~4 d,后续的生化试验还需2~3 d[17],满足不了沙门氏菌快速检测的要求。而环介导等温扩增技术(loop-mediated isothermal amplification,LAMP)最早在2000年由日本科学家Notomi[18]发明,该技术可在恒温条件下(60~65 ℃)1h内完成核酸的高倍扩增,灵敏度比PCR技术高2~7个数量级,反应产物不仅可以通过琼脂糖电泳、浊度仪和定量PCR进行检测,也可以通过钙黄绿素、羟基萘酚蓝、SYBR Green I显色后观察[19,20],目前已成功应用于沙门氏菌、蜡样芽孢杆菌、副溶血弧菌、志贺氏菌等多种病原微生物的检测[14,21−23],但国内尚未见有关蔬菜栽培土壤中沙门氏菌LAMP检测方法的研究报道。【拟解决的关键问题】本研究以沙门氏菌特有侵袭蛋白A (invA)基因序列设计可视化LAMP检测引物,建立基于钙黄绿素显色的蔬菜栽培土壤中沙门氏菌可视化快速检测方法,以期为蔬菜栽培土壤中沙门氏菌的防控提供技术支撑。
1 材料与方法
1.1 试验材料
1.1.1 蔬菜栽培土壤 供试蔬菜栽培土壤样品集自闽清县东桥镇绿辉蔬菜种植农场,样品按S型多点采集土壤表层(0~20 cm)的混合样,采样后立即用冰袋包装新鲜样品带回实验室,人工除去植物残体、根系和石头,过2 mm筛后测定土壤理化指标。供试蔬菜栽培土壤具体理化指标如下:土壤类型为黄红壤,0~20 cm土层pH值5.31,有机质含量16.61 g·kg−1,碱解氮含量126.54 mg·kg−1,速效磷含量 18.25 mg·kg−1,速效钾含量113.79 mg·kg−1。
1.1.2 材料与试剂 胰蛋白胨大豆肉汤(TSB)、胰蛋白胨大豆琼脂(TSA)(北京陆桥技术有限责任公司),DL2000 Marker、dNTP(Takara公司),Bst 2.0 DNA polymerase(美国NEB公司),琼脂糖(西班牙Biowest),Betaine、Tween-20(上海生工),MnCl2、NaCl、Calcein(阿 拉 丁 公 司),FastDNA®Spin Kit for Soil试剂盒(美国MP Bio公司),无菌均质袋( 北京陆桥)。
1.1.3 仪器与设备 PCR仪(BIO-RADTMS1000),凝胶成像系统(BIO-RADTMGel Doc XR+),FastPrepTMFP120核酸提取仪(美国MP Bio公司),easyMixTM拍击式均质器(法国AES Chemunex公司),电泳仪及电源(北京六一仪器厂),恒温水浴锅(上海一恒 ),恒温培养箱(上海一恒)。
1.1.4 菌株 表1为供试7种微生物菌株,分别来自中国工业微生物菌种保藏管理中心(CICC)、中国普通微生物菌种保藏管理中心(CGMCC)和美国典型 培养物保存中心(ATCC)。
1.2 试验方法
1.2.1 引物设计 根据Genbank登录的沙门氏菌特有侵袭蛋白A (invasion protein A,invA)基因序列(Accession: M90846.1),在网站(http://primerexplorer.jp/e/)上使用Primer Explorer 5.0在线软件设计3对LAMP引物用于沙门氏菌检测,包括1对外引物(F3/B3)、1对内引物(FIP/BIP)和1对环引物(Loop F/Loop B)。检测引物交由上海生工合成。具体检测引物序列见表2。

表 1 供试菌株Table 1 Bacteria used for testing

表 2 环介导等温扩增引物Table 2 Primers of LAMP
1.2.2 沙门氏菌培养、计数及基因组DNA提取 将TSA平板内活化的沙门氏菌,挑取单个菌落接种于5 mL TSB液体培养基中,37 ℃、180 r·min−1过夜培养15~18 h,以1∶100比例转接于100 mL TSB液体培养基,37 ℃、180 r·min−1培养3 h左右至细菌对数生长期(OD600≈0.55)。菌液使用生理盐水按10倍梯度依次稀释后,分别取100 μL不同浓度稀释液涂于TSA平板上,37 ℃倒置培养18~24 h计数。
沙门氏菌DNA模板采用热裂解法提取,取1 mL沙门氏菌菌液在台式离心机上10 000 r·min−1离心5 min,弃上清液,沉淀重悬于0.5 mL生理盐水,加入等体积2×TZ裂解液,于99.5 ℃加热10 min,冰上冷却2 min后,在10 000 r·min−1离心5 min,取上 清液即为沙门氏菌DNA模板,−20 ℃保存备用。
1.2.3 LAMP反应体系和反应条件优化 分别对LAMP反应体系中dNTPs浓度、MgSO4浓度以及Betaine浓度,反应条件中反应温度和反应时间进行优化,其中dNTPs终浓度分别为0.8、1.2、1.6、2.0、2.4 mmol·L−1,MgSO4终浓度分别为2、4、6、8、10、12 mmol·L−1,Betaine终 浓 度 分 别 为0.6、0.8、1.2、1.4、1.6 mol·L−1;反 应 温 度 分 别 设 置58、59、60、61、62、63、64、65 ℃,反应时间分别为30、40、50、60、70、80、90 min。选用50 μmol·L−1Calcein-500 μmol·L−1MnCl2作 为 指 示 剂[24],阳 性 反 应 显 绿色,阴性反应显橘黄色,每个因子设置3个重复,以 确定最佳反应体系和反应条件。
1.2.4 LAMP反应特异性检测 分别以鼠伤寒沙门氏菌、金黄色葡萄球菌、大肠埃希氏菌、产气肠杆菌、大肠埃希氏菌O157:H7、单核细胞增生李斯特氏菌和英诺克李斯特氏菌菌株为材料,以热裂解法制备各菌株DNA,验证所建立LAMP检测方法的特异性。取1 μL各菌株的DNA作为模板,采取已优化的反应体系和条件进行特异性分析,反应结束后,以管内颜色变化来判断阴阳性,阳性为绿色,阴性为橘黄色;或将扩增产物在1.5%琼脂糖电泳上检测,阳性反应可观察到特征性梯形带,阴性反应则没有出 现扩增条带。
1.2.5 LAMP反应灵敏度检测 以10倍递减将沙门氏 菌 浓 度 稀 释 为7×108~7×102CFU·mL−17个 梯度,以热裂解法提取沙门氏菌DNA,然后取1 μL不同含量的沙门氏菌DNA作为模板,对LAMP反应灵敏度进行检测。结果直接肉眼观察,阳性反应显绿色,阴性反应显橘黄色,同时在2%琼脂糖凝胶电泳上检 测。
1.2.6 人工污染沙门氏菌的栽培土壤样品检测 取10 g经国标方法检测沙门氏菌阴性的蔬菜栽培土壤样品,置于装有90 mL蛋白胨缓冲水(BPW)的无菌均质袋中,分别加入灭菌生理盐水稀释至适宜含量的沙门氏菌0.5 mL,以制备含沙门氏菌含量为0、5×101、4×102、1×103、4×103、1×104、4×104、1×105CFU·g−1的人工污染样品,将均质袋放置在拍击式均质器中拍打1 min,置37 ℃的恒温培养箱中预增菌4 h。预增菌后重新混匀土壤样品,吸取1 mL混匀土壤样品至FastDNA®Spin Kit for Soil试剂盒中的土壤裂解管中,12 000 r·min−1离心3 min,吸弃上清,然后在FastPrepTMFP120核酸提取仪上提取土壤微生物总DNA,100 μL溶解土壤微生物总DNA,取1 μL作为LAMP反应扩增模板。
1.2.7 蔬菜栽培土壤中沙门氏菌污染的检测 利用所建立的蔬菜栽培土壤中沙门氏菌LAMP检测方法对采自全省不同蔬菜产区的41份土壤样品进行沙门氏菌检测,同时采用国标方法(GB 4789.4—2016《食品微生物学检验 沙门氏菌检验》)进行检测分 析。
2 结果与分析
2.1 LAMP检测方法的建立
通过反应温度和时间进行优化,确定LAMP最适反应温度为65 ℃,反应时间为1 h。优化后蔬菜栽培土壤中沙门氏菌LAMP检测最佳反应体系25 μL包括:2.5 μL 10×Isothermal Amplification Buffer,1.4 mmol·L−1dNTPs,0.2 μmol·L−1F3-B3,1.6 μmol·L−1FIPBIP,0.4 μmol·L−1Loop F~Loop B,0.8 mol·L−1Betaine,6.0 mmol·L−1MgSO4,8 U Bst 2.0 DNA polymerase,50 μmol·L−1Calcein和500 μmol·L−1MnCl2,DNA模板1 μl,灭菌超纯水补足25 μL体积。优化的LAMP反应 效果如图1所示。

图 1 LAMP体系检测沙门氏菌Fig. 1 Detection of Salmonella using optimized LAMP assay
2.2 特异性检测结果
分别以鼠伤寒沙门氏菌菌株和非沙门氏菌菌株的DNA为模板进行LAMP反应特异性分析,结果表明,在Calcein-MnCl2指示剂的作用下,65 ℃温育1 h后,鼠伤寒沙门氏菌LAMP反应产物显绿色,而供试6个非沙门氏菌菌株的LAMP反应产物均显橘黄色(图2-A)。进一步取2 μL扩增产物用2%的琼脂糖凝胶电泳检测,结果除鼠伤寒沙门氏菌LAMP扩增产物出现梯形条带外,其他6个菌株均未出现任何条带(图2-B)。结果表明,本研究所建立的可视化LAMP检测方法对沙门氏菌具有良好的特 异性。
2.3 灵敏度检测结果
分别以7个不同含量沙门氏菌DNA为模板进行扩增来验证LAMP体系的灵敏度,琼脂糖凝胶电泳检测结果显示,在每管25 μL LAMP反应体系中沙门氏菌DNA含量为7×105~7 CFU时均可以出现LAMP产物特有的梯形条带(图3-A),而当沙门氏菌DNA含量为7 ×10−1CFU时没有出现任何条带。可视化显色结果与琼脂糖凝胶电泳结果一致(图3-B),说明L AMP反应体系可以检测到7 CFU沙门氏菌DNA。
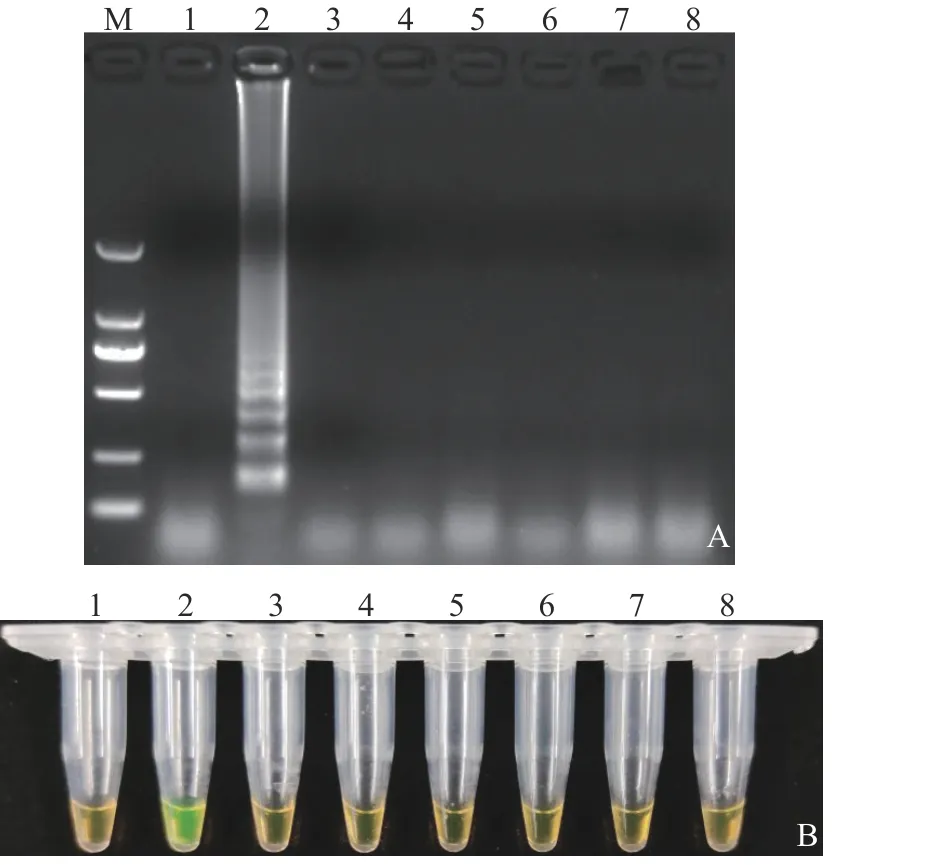
图 2 LAMP方法检测沙门氏菌的特异性Fig. 2 Specificity of LAMP assay in detecting Salmonella
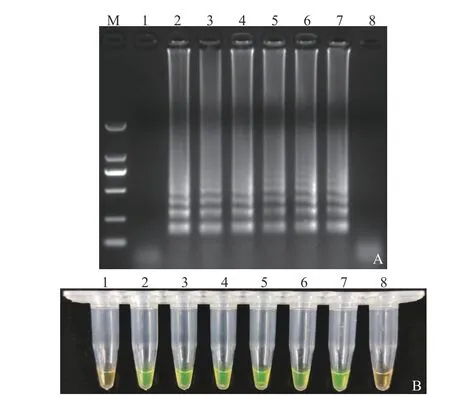
图 3 LAMP方法检测沙门氏菌的灵敏度Fig. 3 Sensitivity of LAMP assay in detecting Salmonella
2.4 人工污染沙门氏菌的栽培土壤样品检测结果
人工污染沙门氏菌的栽培土壤样品经37 ℃预增菌4 h后,提取土壤微生物总DNA进行扩增检测。分别设置0、5×101、4×102、1×103、4×103、1×104、4×104、1×105CFU·g−1共7组 不 同 梯 度 进 行LAMP扩增检测。琼脂糖电泳结果显示,当LAMP反应体系中沙门氏菌含量为4×102~1×105CFU·g−1时均可以出现LAMP产物特有的梯形条带(图4-A),而当沙门氏菌含量为5×101CFU·g−1时没有出现任何条带。可视化显色结果与琼脂糖凝胶电泳结果一致(图4-B),说明本LAMP反应体系检测蔬菜栽培土壤 样品灵敏度为4×102CFU·g−1。
2.5 蔬菜栽培土壤中沙门氏菌污染的检测结果
应用上述LAMP检测方法和国标检测法,同时对全省不同蔬菜产区的41份土壤样品进行沙门氏菌检测,结果见表3。2种方法都检测到2份沙门氏菌阳性样品和39份沙门氏菌阴性样品,LAMP检测方法与国标方法(GB 4789.4—2016《食品微生物学检验 沙门氏菌检验》)检测结果一致,而LAMP检测将国标方法检测时间由5~7 d缩短至8 h内,大幅减轻 了检测强度,提高了检测效率。

图 4 LAMP方法检测人工污染沙门氏菌的栽培土壤样品Fig. 4 LAMP assay for detecting artificially inoculated Salmonella in soil samples

表 3 2种方法对比检测蔬菜栽培土壤沙门氏菌污染结果Table 3 Salmonella detection in soil by two different methods
3 讨论与结论
快速检测技术是监测和防控沙门氏菌等食源性疾病最重要的环节之一,而衡量快速检测技术性能最关键指标是检测用时与灵敏度。目前采用的国标检测方法《食品安全国家标准 食品微生物学检验 沙门氏菌检验》(GB 4789.4—2016),需要对待检样品进行预增菌、选择性分离和生化试验鉴定等步骤,操作繁琐;最终拿到鉴定结果需要5~7d,耗时费力,难以满足沙门氏菌快速检测的要求。PCR方法虽然具有检测时间短、灵敏度高的特点,但需要专门的检测仪器(普通PCR仪或荧光定量PCR仪),而环介导等温扩增技术(loop-mediated isothermal amplification,LAMP)由于具有更高的灵敏度和视觉判断性的优点,且检测过程不需要专门的检测仪器,弥补了国标检测方法和PCR方法检测沙门氏菌的不足。
沙门氏菌侵袭蛋白(invasion protein)基因簇是沙门氏菌编码吸附和侵袭上皮细胞表面蛋白的基因,与沙门氏菌对肠道上皮细胞的侵袭有关,包括invA、invB、invC、invD、invE等基因,其中以invA基因应用最为广泛,目前根据invA基因序列设计特异性引物已成功应用于乳品、肉类、蔬菜等食品中沙门氏菌的检测[14,15,21]。本研究根据沙门氏菌侵袭蛋白A (invA)基因序列设计特异性LAMP引物,建立了一种基于颜色判定的简单、快速和灵敏的蔬菜栽培土壤中沙门氏菌的快速检测方法,对沙门氏菌纯菌检测灵敏度可达7 CFU/25 μL,人工污染的栽培土 壤 样 品 检 测 灵 敏 度 为4×102CFU·g−1。采 用 该LAMP方法与国标检测方法对比检测蔬菜栽培土壤中沙门氏菌污染,结果表明LAMP检测结果与国标方法检测结果一致,说明该方法能成功应用于蔬菜栽培土壤中沙门氏菌的快速检测,可为蔬菜栽培土壤中沙门氏菌污染的及时防控提供技术支撑。
