邻二氮菲测定铁含量实验的扩充与改进
2021-05-29宋文璟
宋文璟,刘 畅
(大连理工大学化工学院,辽宁盘锦 124221)
0 引言
邻二氮菲分光光度法测定铁含量实验是一项非常经典的仪器分析实验,利用间接紫外-可见分光光度法(UV-Vis),有助于学生理解相关知识并掌握实验技能,几乎所有的实验教材中都有此实验[1-6]。该实验原理为:在pH=2~9 的溶液中,邻二氮菲与Fe2+按照3∶1的摩尔关系生成稳定的橙红色络合物,其最大吸收波长为510 nm,摩尔吸收系数ε=11 kL·(mol·cm)-1,通过使用紫外-可见分光光度计测定该橙红色络合物的吸光度值(A)来确定待测溶液中Fe2+的含量。这个实验视情况可以安排4~8 个学时,若只定量待测Fe2+溶液需4 个学时,再进行实验条件的优化则另外增加4 个学时。
然而该实验只涉及UV-Vis 的使用,测试仪器单一,大部分时间消耗在溶液的配制上,达不到仪器分析实验的教学目标和初衷,还抑制了学生的学习兴趣。随着社会的不断进步和经济的迅速发展,越来越多的研究单位和企业都配备了众多的分析仪器,这就要求学生在本科学习阶段尽量多的掌握各种分析仪器的基本理论和操作技能,具备毕业后进入工作岗位独立开展仪器分析实验的能力[7-9]。目前仪器分析实验内容主要涵盖电化学分析法、光谱分析法(以UV-Vis 和红外光谱法IR为主)和色谱法,极少涉及原子吸收光谱法(AAS)实验的教学和应用[10]。AAS 能够分析元素周期表中绝大多数的金属与非金属元素,在医药、食品和环境领域均有广泛的应用[11-13],因此十分有必要在本科阶段的仪器分析实验中开展AAS 实验的教学内容。我校是“211”和“985”工程建设重点高校,也是世界一流大学A 类建设高校。为了提高仪器分析实验的教学质量,充分发挥分析仪器在培养学生核心竞争力中的作用,结合现有的基础条件和仪器设备,深度挖掘经典实验,在“邻二氮菲测定铁含量”的实验中增设利用AAS对待测Fe2+溶液进行定量的教学内容,让学生采用UV-Vis和AAS两种分析方法对同一样品进行对比试验,更加深刻地掌握这两种仪器的性能特点和优劣。在将该实验内容扩充的同时,还更新了一些操作方法和数据分析技术,大大提高了该实验的教学效果。
1 实验部分
1.1 仪器与试剂
UV8000 紫外-可见分光光度计,上海元析仪器有限公司;AA6100 原子吸收分光光度计,天美(中国)科学仪器有限公司;ME104 电子天平,梅特勒-托利多国际贸易(上海)有限公司;1~10 mL单道可变量程移液器,赛默飞世尔科技(中国)有限公司;1~10 mL 可调定量加液器;智能数显恒温电加热套,上海予星仪器设备有限公司。
100 μg/mL 标准Fe2+溶液:取0.702 g(NH4)2Fe(SO4)2·6H2O固体溶解于500 mL 去离子水中,加入浓硫酸约2 mL,转移至1 L 容量瓶中,用去离子水定容至刻度。
1 g/L邻二氮菲溶液:精密称取1,10-邻二氮杂菲固体1 g至烧杯中,加入去离子水后在电加热套上温热搅拌12~24 h,全部溶解后将溶液冷却,用容量瓶定容至1 L。
10 g/L盐酸羟胺溶液:精密称取NH2OH·HCl固体10 g,加入去离子水溶解,用容量瓶定容至1 L,临用时现配。
1 mol/L醋酸钠溶液:称取CH3COONa·3H2O 固体136.08 g,用去离子水定容至1 L,避光保存。
1 mol/L 硫酸溶液:由浓硫酸用去离子水稀释而成。
以上所用试剂均为分析纯。
待测样品为含铁复合维生素片(Multivitamins Plus Iron),购自TESCO,含铁标示量为14 mg/片。
1.2 系列标准Fe2+溶液的制备
用移液枪分别精密量取100 μg/mL 标准Fe2+溶液1、2、3 和4 mL于100 mL容量瓶中,依次用可调加液器加入盐酸羟胺溶液、醋酸钠溶液和邻二氮菲溶液各10 mL,用去离子水定容至刻度,摇匀。4 份标准Fe2+溶液的浓度值分别为1、2、3 和4 μg/mL。
另取一只100 mL容量瓶,不加标准Fe2+溶液,只用可调加液器加入体积均为10 mL的盐酸羟胺溶液、醋酸钠溶液和邻二氮菲溶液,用去离子水定容至刻度,摇匀,作为试剂空白溶液。
1.3 待测溶液的制备
由于此部分需要较长时间,要求学生在实验中优先于“1.2”项进行。
取含铁复合维生素片1 片,精密称定其质量(g)并记录,用研钵研磨成粉状后置于400 mL 大烧杯中,加入200 mL 0.1 mol/L硫酸溶液(让学生使用量筒自行稀释1 mol/L 硫酸溶液得到)。然后将大烧杯放在电加热套上微热使Fe2+完全溶解(溶解的这段时间学生可进行“1.2”项的操作),冷却后将溶液转移至1 L容量瓶中,用去离子水淋洗大烧杯3~4 次,并将淋洗液全部收集到容量瓶中,用去离子水定容容量瓶至刻度,摇匀。此时,容量瓶底残留有未溶解的药片包衣,属正常现象,不会影响测量结果的准确度。最后,用移液枪精密移取上清液10 mL至100 mL容量瓶中,用可调加液器依次加入盐酸羟胺溶液、醋酸钠溶液和邻二氮菲溶液各10 mL,用去离子水定容至刻度,摇匀,作为待测溶液。
1.4 UV-Vis法实验条件
以试剂空白为参比溶液,采用1 cm 比色皿在350~800 nm波长范围内扫描系列Fe2+标准溶液和待测溶液的光谱图,记录最大波长(λmax)处的A值。
1.5 AAS法实验条件
采用铁空心阴极灯和空气-乙炔火焰原子化器。狭缝宽度为0.2 nm,灯电流为5.0 mA,空气流量为6.8 L/min,乙炔流量为1.7 L/min,燃烧器高度为6 mm。在248.3 nm波长处测定并记录系列标准Fe2+溶液和待测溶液的A值。
1.6 铁含量的测定方法
UV-Vis法和AAS 法均采用标准曲线法测定待测样品中Fe2+的含量。以系列标准Fe2+溶液的浓度值(μg/mL)为横坐标,所对应的A值为纵坐标,用Origin软件绘制标准曲线并使之通过原点,建立拟合方程式。将待测溶液的A值代入拟合方程式,计算容量瓶中待测溶液Fe2+的浓度(μg/mL)。再结合稀释倍数和称样质量计算得到复合维生素片中的铁含量(mg/g)。
2 结果与讨论
2.1 采用UV-Vis法测定铁含量
系列标准Fe2+溶液所测得的A 值见表1,A 值全部在0~1 范围内。用Origin 2019 软件作出A 值与Fe2+浓度的关系图如图1 所示。图中表明,溶液的A值随溶液中Fe2+浓度的增加而增大,呈线性相关趋势。采用线性拟合的方式处理实验数据,图1 的内插表格为数据拟合参数和误差分析结果。拟合方程式为y=0.201x+0.010 8,校正决定系数为0.999 47。

表1 UV-Vis法测定系列标准Fe2+溶液的吸光度(A)值

图1 UV-Vis法测得吸光度(A)与Fe2+浓度线性关系图

取1 片复合维生素片,精密称定其质量m=0.359 0 g,按照“1.3”项下操作制备待测溶液,测得其A1=0.292,代入拟合方程式得容量瓶待测溶液Fe2+的浓度为1.40 μg/mL,通过下式计算该复合维生素片的含铁量为39.0 mg/g,代入取样量得该片复合维生素片中铁质量是14.0 mg/片。经与标示量(14 mg/片)比较,建立的UV-Vis 方法能够准确测定出复合维生素片中的铁含量。此外,系列标准Fe2+溶液和待测溶液的λmax均为510 nm,通过拟合方程式的斜率计算得邻二氮菲-Fe2+络合物的εmax=11.2 kL/(mol·cm),与经验值完全一致。
2.2 采用AAS法测定铁含量
采用AAS法测定“2.1”项下的系列标准Fe2+溶液和待测溶液,系列标准Fe2+溶液的A 值如表2 所示,待测溶液A2=0.029。图2 所示用Origin 2019 软件绘制的A值与Fe2+浓度的关系,溶液的A值同样随着溶液中Fe2+浓度的增加而增大,呈线性相关趋势。拟合方程式为y=a2x +b2=0.021 4x -0.000 6,校正决定系数为0.999 65。计算得到该片复合维生素片中含铁量为38.5 mg/g,相当于13.8 mg/片。结果表明,所建立的AAS法同样能够准确测定出复合维生素片中的铁含量。
表2 AAS法测定系列标准Fe2+溶液的吸光度(A)值
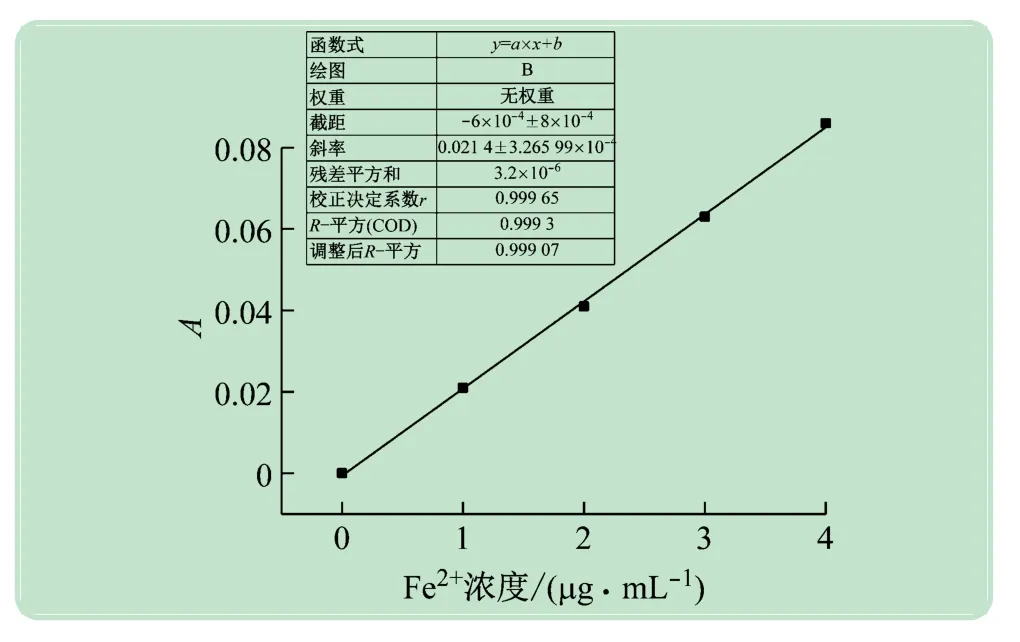
图2 AAS法测得吸光度(A)与Fe2+浓度线性关系图
3 改进内容与讨论
3.1 丰富实验教学内容
原实验设计只采用UV-Vis一种定量方法,改进后扩充了AAS法定量。由于AAS法与UV-Vis法使用的是同一份系列标准Fe2+溶液和待测溶液,相比于单独开设一个AAS法实验省略了溶液配制的过程,如此设计“性价比”很高。此外,待测样品通常是教师配制好的模拟样品,学生直接取用。待测样品采用商品化含铁复合维生素片,学生通过简单的前处理操作即可测定,共存的其他成分不干扰测定,使学生对完整的样品分析过程有更为切身的体会。通过对比学生的检测结果和样品标示量,还能够检验学生实验操作的准确性。将样品前处理引入实验教学中,有助于提升学生综合运用所学样品前处理技术解决实际应用问题的能力[14-16]。虽然相对原实验设计增加了两个环节,但通过调整实验方案,如“1.3 项”制备待测溶液的同时进行“1.2 项”配制系列标准Fe2+溶液,将课堂数据处理和完成实验报告改为课下,可在不增加学时的情况下丰富实验教学内容。
3.2 采用Origin软件处理数据
数据处理是仪器分析实验教学中的重点之一。原实验中采用Excel软件绘制标准曲线、拟合方程式,相比于Excel,Origin 能够直接显示拟合结果和误差分析,更加具有指导意义。实验指导教师则依据工作曲线的校正决定系数、相对偏差、数据精度等信息更合理地评定学生的实验数据。
3.3 引进最新实验仪器
原实验设计要求使用吸量管移取标准Fe2+溶液,考虑到现代科研和实际工作中,吸量管已经被移液枪所取代[17],改进的实验中增加了移液枪的使用内容,操作快速、准确。此外,原实验中盐酸羟胺、邻二氮菲和醋酸钠3种试剂的加入量不同,分别为2、3 和5 mL,学生容易出错,改进的实验将盐酸羟胺、邻二氮菲和醋酸钠的加入体积均改为10 mL,并相应修改它们的浓度,同时采用可调加液器取代量筒。通过引进新的小型实验仪器,极大地提升了学生配制溶液的效率,学生可将时间和注意力集中于大型仪器的操作和使用。
3.4 增加实验趣味性
相比于模拟样品,让学生分析真实的与生活贴近的复合维生素片,且研磨、溶解、定容、定量测定等的每一个环节都有可能影响最终结果的准确性,更能够激发学生实验的兴趣和求知欲。
4 结语
对邻二氮菲测定铁含量这个经典实验内容进行深度挖掘,分别采用UV-Vis 法和AAS 法两种方法测定同一片复合维生素片剂中的含铁质量(mg/g),内容包括标准溶液的配制、标准曲线的建立、样品溶液的制备、样品溶液的测量和Origin 数据处理等一套完整的分析过程。实验可安排4 学时,每次指导16 名学生,每个学生自成1 组,独立完成所有的实验内容。实验室为学生提供16 台紫外-可见分光光度计和2 台原子吸收光谱仪,学生在课堂上只需获取原始数据,课后处理、计算和撰写实验报告。为了防止学生课后窜改数据,要求学生在实验中将原始数据书写到二联复写纸上,离开实验室前提交复写联。通过1 年多的实践,改进后的实验取得了良好的教学效果。
