白术种质资源遗传多样性及连作障碍研究进展
2021-05-26朱香梅石雨荷李晴周日宝童巧珍
朱香梅 石雨荷 李晴 周日宝 童巧珍
摘要:白术是我国常用的大宗类药材,在我国已有上百年的栽培历史。随着白术市场需求量的扩大及药用植物遗传多样性检测手段逐渐成熟和多样化,关于白术种质资源的研究也逐步深入。分别介绍不同白术种质及其同属间形态水平上的差异和DNA水平上的差异。形态标记法能简单筛选出种质优良种株的表型特征,而分子鉴定技术直接分析遗传物质DNA的多态性来推断物种内在的遗传变异。白术栽植过程中除了DNA水平上存在的性状差异影响着白术品质,土壤因子的变化、化感自毒作用也是重要的影响因素,就白术连作障碍发生的原因及其解决措施展开讨论。综述白术种质资源遗传多样性及栽植过程中连作障碍问题的研究进展,为白术优质种质筛选鉴定、遗传多样性保护及药材产业化的发展提供参考。
关键词:白术;遗传多样性;连作障碍;种质资源;形态标记法;分子鉴定;变异
中图分类号:S567.23+3.03;S567.23+3.04文献标志码: A
文章编号:1002-1302(2021)08-0043-06
收稿日期:2020-08-14
基金项目:中央引导地方科技发展专项资金(编号:2019XF5069);湖南省教育厅重点项目(编号:19A367)。
作者简介:朱香梅(1996—),女,湖南邵阳人,硕士研究生,研究方向为中药资源与质量。E-mail:2785384490@qq.com。
通信作者:童巧珍,博士,教授,博士生导师,从事中药资源与质量研究。E-mail:qztong88@126.com。
白术为菊科苍术属(Atractylodes DC)植物白术(Atractylodis macrocephala Koidz.)的干燥根莖,是著名的地道药材“浙八味”之一,其味苦、甘,性温,归脾、胃经,有健脾益气、燥湿利水、止汗、安胎等功效[1]。张仲景《伤寒杂病论》中提到白术还具有祛风逐湿、温中止利、润肠通便之效[2]。现代研究表明,白术富含挥发油和内酯类成分,具有抗肿瘤、保护胃黏膜、抗炎、保肝、改善记忆力、免疫调节等多种作用[3],在临床应用中使用广泛。白术属于异花授粉的多年生草本植物,主要产于浙江、安徽、福建、四川、江西、湖南等地,以北纬29°50′~30°50′亚热带常绿阔叶林的浙江於潜、安徽皖南山区一带为其道地产区[4]。虽在浙江新昌、嵊县,湖南平江、衡阳,安徽歙县、宁国,江西修水、铜鼓等地区均有移植栽培[5],但由于白术长期不同区域间的移植、杂交,以及种间、居群间的杂交繁殖,造成了白术的种质混乱,品种不明,使得白术资源逐渐减少、遗传多样性降低,品种质量得不到保障[6]。遗传多样性是生物多样性的基础,决定了物种对外界不良环境的抵御能力和进化能力,遗传多样性降低表明物种遗传变异水平和对生存环境的适应能力降低[7]。另外,白术为宿根植物且忌连作,具有很强的忌地性,栽培过程中容易出现连作障碍问题[8]。种植过白术的土壤通常须间隔3~5年才能重新栽植白术。这不仅给白术种植户带来了非常大的经济损失,而且制约了道地药材的产业化生产。
目前,国内外对白术化学成分及药理作用研究报道较多,还未见白术遗传多样性和连作障碍问题的报道。笔者首先从白术形态多样性、分子多态性方面对白术种质资源遗传多样性进行综述,其次,总结白术种植过程中连作障碍发生的原因及其解决措施。
1 白术遗传多样性研究进展
为更好地保护和开发利用白术的种质资源,国内外研究者对白术种质资源遗传多样性和种群结构特征做了许多工作,主要是从形态水平和分子水平2个方面进行研究。形态学研究能快速地对白术进行形态学性状的评价,是白术居群内或居群间分类的重要依据之一,而分子标记能直接反映不同产地的白术在DNA水平上的差异。随着多种分子标记技术的出现,分子标记技术在白术种质资源的遗传多样性研究中占有重要地位。
1.1 形态学水平研究
形态学检测药用植物的遗传变异是目前最直接的方法。一般检测性状有2种:一种是单基因决定的质量性状,另一种是由多基因决定的数量性状[9]。这种根据表型特征进而对白术遗传多样性分析的研究方法,除了在水稻[10]、大豆[11]等农作物上应用广泛,在药用植物领域也有应用,如骨碎补类[12]、菝葜属[13]药用植物等。张杰等利用体视显微镜通过种子大小、冠毛颜色及直径在内的5个特征性状将白术与苍术种子区分开来[14]。方程吉等采用主成分和聚类分析法对6类表型白术样品进行分析,认为宽叶高杆浓密,茎枝裸露而易见的白术质量最好[15]。白术种质资源丰富复杂,在移栽过程中,田间出现许多不同表型性状,通常是由环境引起的性状差异。黄有军等通过显微镜观察白术根茎的横切面,发现浙江临安淤潜的白术与其他产地的差异较大[16]。白术一般是通过单基因控制性状,从而影响其质量,进一步研究其种群的遗传多样性。形态学分析对白术近缘物种居群(北苍术)或其变种个体很难界定,其主要还是用于属或组的水平。但仅仅依赖形态特征是不完整的,还须要进一步分析白术的分子水平。
1.2 DNA分子水平多态性研究
1.2.1 RAPD标记技术
随机扩增引物多态性DNA(random amplified polymorphic DNA,简称RAPD)是由Williams等研究者于1990年建立并发展起来的一种本质是聚合酶链式反应(polymerase chain reaction,简称PCR)的二代标记技术[17]。该技术的样品采集方便、操作简便安全,最重要的是没有种群的特异性,适用性强,多用于白术种质资源的辨别。王宗宽等利用RAPD技术对浙江省3个不同居群的白术进行分析,发现不同居群白术的RAPD多态性的差异和它的遗传变异与亲缘关系相吻合,表明RAPD标记技术可以很好地将不同产区的白术进行分类[18]。朱振洪等的研究结果表明,安徽亳州、河南郸城、浙江天台等地区的居群和湖北恩施地区的4个居群均表现出较高的遗传多样性,且不同地区的白术在DNA水平上有明显遗传差异[19]。RAPD作为一种显性的分子标记技术,能很好地检测出不同来源白术的DNA差异,但其重现性较差,须慎重选择。
1.2.2 SCAR标记技术
特征性扩增片段区域(sequence characterized amplified regions,简称SCAR)就是在RAPD筛选标记过的条带序列两端设计特异引物从而进行PCR反应,最终获得稳定的SCAR分子标记[20]。SCAR标记重现性好、准确度高、没有假阳性,目前在黄花白及、牛膝、金线莲等药用植物的分子鉴定、筛选优良育种中广泛应用[21-22]。李敏等成功获得了浙白术、河北小白术的SCAR标记物,而平术和徽术没有特异性扩增条带[23]。SCAR标记技术对于亲缘关系近、基因相似度较高的药用植物很难鉴别出来。
1.2.3 SSR和ISSR标记技术
简单重复序列(simple sequence repeat,简称SSR)标记的原理就是根据生物基因组中串联的重复序列,通过比较稳固的侧翼序列设计特异引物,通过聚合酶链式反应技术扩增出重复的DNA序列,进一步获得长度多态性[24]。简单序列重复区间(inter simple sequence repeat,简称ISSR)标记是在SSR的基础上,对重复SSR DNA序列区间进行检测[25]。其优点是不需要像SSR标记提前预知序列信息,成本低、试验简便、稳定性好,但两者均是共显性遗传,多用于植物遗传多样性分析、药用植物真伪鉴定、优良基因探索等方面[26]。中药白术在用ISSR进行PCR扩增时,须要找到适合的反应体系,白术种质遗传多样性分析时才会更加便利。马辉等分别优化了於术、咸丰白术的ISSR-PCR反应体系,表明不同产地的白术都有特定的反应体系,白术的道地品种分子鉴定、指纹图的构建都有了依据[27-28]。郑丽利用SSR标记野生白术和栽培白术,结果表明,栽培白术种群内个体间的遗传分化小,遺传变异相对较低[29],这与孙靓等的研究结果[6]一致,表明栽培的白术比野生白术对环境的适应性要强,产生这种遗传分化差异可能与其育种的来源有关。
1.2.4 AFLP标记技术
扩增片段长度多态性(amplified fragment length polymorphism,简称AFLP)标记[30]是由荷兰科学家Pieter等在1992年首次提出来的分子标记技术。它既继承了RAPD操作简单、检测快速的优点,又具有SCAR、ISSR重现性好、稳定性好、准确度高的优点,目前广泛用于动植物遗传育种、种植资源遗传多样性分析和遗传指纹图谱的构建中,但由于成本高、试验操作复杂使其应用受到限制[31]。王红娟等的研究表明,AFLP技术可以鉴定出白术二倍体和四倍体试管苗形态上的差异[32]。王志安等建立了浙江省磐安县白术AFLP指纹图谱体系[33]。AFLP分子标记技术可以为白术多倍体育种、种质的保存提供帮助。
1.2.5 其他标记技术
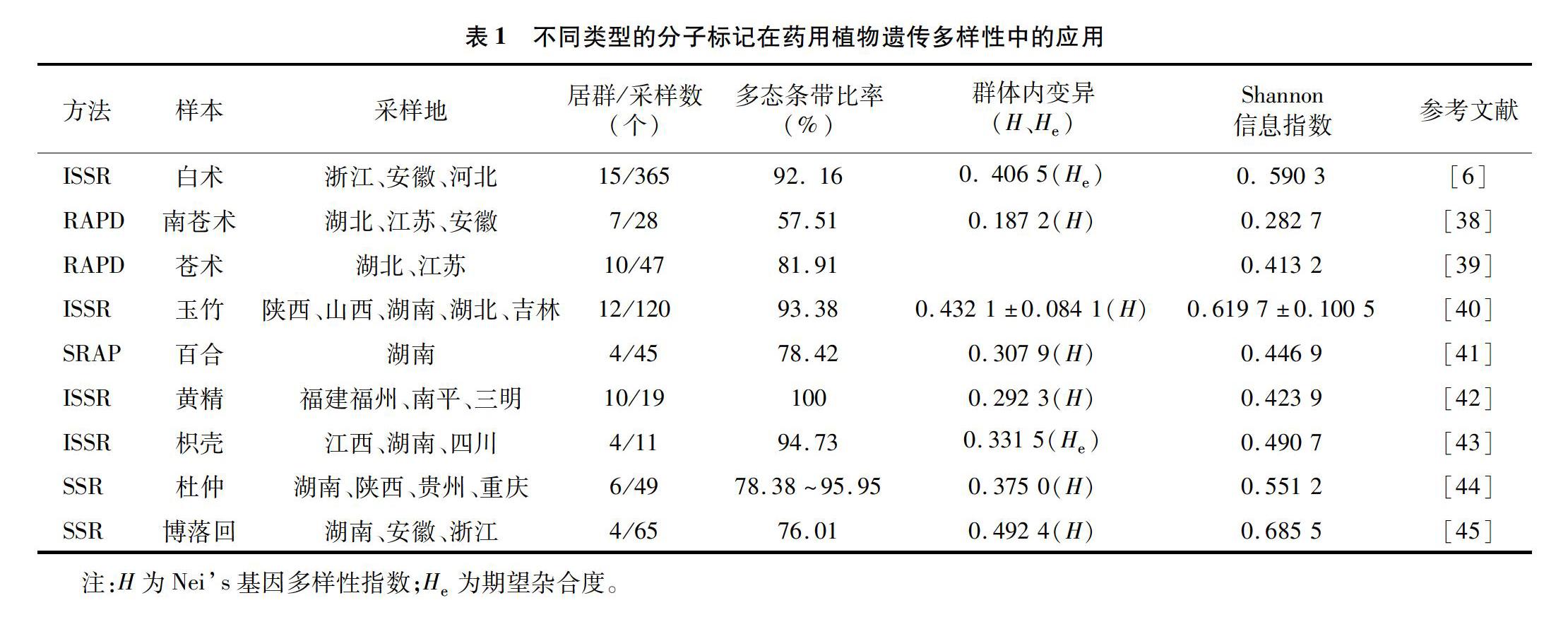
DNA条形码标记技术是利用在植物中核基因内转录间隔区(internal transcribed spacer,简称ITS)和叶绿体的部分片段对物种进行鉴定的一种技术[34]。此法常用于苍术属药用植物及其伪品的鉴定。余亚东等利用ITS2 序列,将药材白术和其他苍术属及仿冒品各聚分一支,DNA条形码标记技术鉴定遗传信息缺失的药用植物效果较好[35]。第3代标记技术——单核苷酸多态性(single nucleotide polymorphism,简称SNP )标记主要用于白术部分基因片段的SNP分析[36]。曹亮等的研究表明,通过psbA-trnH序列比对,对白术和苍术的种子进行鉴别[37]。因此,将不同的遗传标记技术结合应用于白术,可以很好地解决白术种质混淆的问题。目前,DNA分子标记技术还用于苍术属和其他湘产药材的遗传多样性研究中,由表1可以看出,白术的遗传多样性处于较高水平。
2 白术连作障碍的研究进展
药用植物中约70%的根和根茎类药材均存在严重的连作障碍[8],如人参(Panax ginseng)、三七(Panax notoginseng)、地黄(Rehmannia glutinosa)[46-47]。有研究表明,土壤因子(土壤的理化性质、土壤生物学性状)的变化和化感自毒作用是引发栽培过程中白术连作障碍问题的潜在原因[48]。
2.1 白术连作障碍的原因
2.1.1 土壤因子的变化
1983年日本研究者泷岛提出植物连作障碍的五大原因,即土壤养分亏缺 、土壤反应异常、土状恶化、植物的有害物质以及土壤微生物的变化[49]。陈慧等在研究中发现,浙江地区根际土壤的酸性、金属离子累积量与白术连作年限成正比,连作白术根际土壤中微生物总量和细菌、放线菌数量呈倒“U”形趋势,真菌数量变化趋势呈“U”形,二年生白术的酶活性比一年生白术低[50],这与宋荣等研究的连作下的平江白术[48]一致。细菌和放线菌是根际土壤中的有益微生物,土壤酶活性也是作为衡量土壤肥力的有效指标。根茎中含有大量的挥发油,连作下的白术土壤呈强酸性,长期连作有害的根际分泌物会刺激大量有害病原微生物的快速生长,从而导致白术植株病害越发严重。苏翠芬等的研究结果表明,重茬白术易患根腐病,死苗率严重时达70%~80%,甚至绝收[51]。根腐病和白绢病均是土传病害,是成株期白术根茎部死苗率、发病率最高的病害,尤其是在连作下的白术,其他危害白术苗期的病害也有研究,如铁叶病[52]、枯斑病[53]。
2.1.2 化感自毒作用
澳大利亚生物学家Molisch在1937年提出,植物化感作用是植物本身通过释放化学物质对其他植物产生某种影响的现象[54]。后来研究者发现,这种化学物质是药用植物产生的次级代谢产物,别称化感物质。植物通过淋溶 、根系分泌物、挥发和植株腐解等方式释放的化感物质对正茬或下茬同种或同科植物的生长产生抑制作用称为自毒作用[55]。白术在连作过程中,其茎、叶、根须等残留体在农田被分解后,产生对白术自身生长发育有害的化学物质。徐建中等研究发现,白术根系土壤有机溶剂浸提物、白术地上部和地下部水浸液对自身幼苗生长有抑制作用,表明白术根系分泌物中可能存在着抑制白术幼苗生长的化感物质,推测白术这种自毒效应可能是造成连作障碍的原因[56]。有研究表明,药用植物的化感物质会抑制细胞的生长、影响细胞膜透性、影响植物体内激素水平、影响酶的活性[57]。陈秋强等的研究结果表明,连作下白术根际分泌的2,6-二叔丁基对甲酚四甲基联苯、对二甲苯以及对氯苯基-6,8-二氯-7-苯并吡啶等化感物质会导致连作下白术死苗[58]。
2.2 解决白术连作障碍的措施
2.2.1 土壤消毒,合适的肥料
土壤消毒是解决白术连作障碍的重要方法之一。作物连作后土壤中速效氮、速效磷含量降低,土壤肥力、关键酶的活性严重下降[59]。此外,连作后土壤过度酸化,导致大量有害病菌及线虫等有害生物繁殖。有研究发现,西洋参[60]、地黄[46]和三七[61]等药用植物采用土壤消毒和施肥配合使用的方法,减缓了连作障碍的发生。石灰对土壤有灭菌、消毒的作用,能提高土壤pH值,是药用植物土壤消毒中最常用的消毒剂[62]。唐乐等的研究结果表明,在连续种植过的白术土壤中同时施以生石灰和腐植酸颗粒肥,可以使白术白绢病、根腐病的发病率降低,土壤酶的活性上升,白术苗存活率增加,而单独使用效果不佳[63]。石雷磊等利用高效液相色谱法(high performance liquid chromatography,简称HPLC)检测出连作2年的白术土壤经石灰、蚕沙发酵肥和生物菌肥处理后白术药材的白术内酯Ⅰ、Ⅲ含量最高,白术药材鲜产量也是最高的。化学肥料是药用植物施肥中最常用的肥料之一,而化学肥料对植株土壤有残留危害,逐渐被微生物肥料替代[64]。目前,根际促生菌已成为国内外微生物肥料研究领域中的一个热点,最早发现是在马铃薯根际中,它能促进植物生长,增强植物抗性,提高植物产量,并且还能减少化肥与农药的用量,多应用于克服植物连作障碍研究[65]。陈慧的研究表明,根际促生菌肥处理,对连作下白术幼苗起到了一个很好的修复作用[66]。
2.2.2 轮作
药用植物轮作的种植方式与连作相反,在同一块田地上有顺序地轮流种植不同作物从而减少药用植物病虫害,提高药材的质量和产量。轮作是解决白术连作障碍最便捷、最经济和最有效的方法。不同地区轮作方式不同,如浙江的玉米—白术轮作,长江流域的白术—紫云英轮作[67]。药—农轮作和药—药轮作是我国药用植物普遍应用的轮作模式。合理的轮作模式可以有效地将2种作物根系分泌的化感物质进行有益结合,减少连作下白术植株土传病害和自毒现象的发生,提高药材的产量。徐建中等的研究结果表明,白术—农作物轮作比与其他药用植物轮作的白术植株死苗率和根腐病的发病率都要低,且轮作间隔年限也缩短了[67]。利用白术的生长特性进行轮作可以提高土地和光能利用率,如白术—栝楼轮作,是一种高效绿色的轮作方式[48]。轮作的作用机制主要是平衡土壤养分吸收、优化土壤微生物群体、调控土壤中酶活性、降低病虫害的发生[68-69]。
3 结论与展望
遗传多样性的研究在种质资源的保护和开发利用中占有重要的位置,以此对物种提出較为有效的保护措施,如南方野生稻保护区的建立[70]。刘逸慧等利用ISSR分子标记技术对浙江磐安3个白术栽培群体和浙江、贵州、福建、湖北等白术栽培群体遗传多样性进行分析,认为浙江磐安仁川、凌峰、光明的白术遗传多样性比其他地区要好,应优先重点保护[71]。形态多样性研究提供的位点多样、分析简单,而分子生物学方法精确、可靠,但分析起来比较复杂。因此,形态学与分子生物学相结合是鉴定白术种质的有效途径。运用不同的DNA分子标记技术对白术种质遗传多样性进行分析,研究结果发现,於术、平术的遗传分化的水平普遍偏低,遗传分化主要存在于各个栽培群体内个体间,居群内遗传变异大于居群间,因此应该在遗传多样性较高的地区如浙江临安、磐安县建立保护区,同时选择资源数量多的进行大范围的就地保护,在白术的种质保存和栽培生产中,建立单独的制种、育苗,对栽植的园圃进行保护。可能对白术植物遗传种质资源的探索、遗传多样性保护的挖掘有着重要价值。
白术连作障碍分2种类型:一类是物理型障碍,一类是生物学障碍。采用土壤消毒,合理施肥措施,主要解决连作下的白术土壤理化性质、养分损耗的问题。轮作可以防止连作期白术产生的自毒效应和土传病菌的繁殖。白术产量的形成是一个非常复杂的过程,在其生长过程中,很多因素均可能影响白术药材产量和质量的改变。通过对白术种质遗传多样性的分析,采用分子手段,选育出抗性高的白术品种进行连作,这也是克服白术连作障碍的有效措施。目前,白术连作障碍机制和原因尚不完全清楚,对连作白术死苗根际分泌物组分结构的深入研究,可以为白术连作障碍的解决提供新发掘点,促进我国道地药材产业的发展及为其他药用植物连作障碍研究提供参考。
参考文献:
[1]国家药典委员会. 中华人民共和国药典:一部[S]. 北京:中国医药科技出版社,2015:103-104.
[2]王朝阳. 《伤寒杂病论》中白术临床运用及证治规律研究[D]. 武汉:湖北中医药大学,2015:1-78.
[3]陈 静,冉小库,孙云超,等. 白术止汗作用药效物质研究[J]. 辽宁中医药大学学报,2016,18(9):22-24.
[4]彭华胜,王德群. 白术道地药材的形成与变迁[J]. 中国中药杂志,2004,29(12):1133-1135.
[5]孙志国,程东来,刘成武,等. 道地药材咸丰白术的国家地理标志产品保护分析[J]. 时珍国医国药,2010,21(10):2650-2652.
[6]孙 靓,郑玉光,袁 媛,等. 白术遗传多样性ISSR分析[J]. 中国中药杂志,2012,37(22):3381-3385.
[7]王洪新,胡志昂. 植物的繁育系统、遗传结构和遗传多样性保护[J]. 生物多样性,1996,4(2):92-96.
[8]郭兰萍,黄璐琦,蒋有绪,等. 药用植物栽培种植中的土壤环境恶化及防治策略[J]. 中国中药杂志,2006,31(9):714-717.
[9]钱迎倩,马克平. 生物多样性研究的原理与方法[M]. 北京:中国科学技术出版社,1994.
[10]陈 越,张敦宇,丁明亮,等. 多个省份水稻资源的表型多样性与优异资源的筛选[J]. 浙江农业学报,2019,31(11):1779-1789.
[11]赵朝森,王瑞珍,李英慧,等. 江西大豆种质资源表型及品质性状综合分析与评价[J]. 大豆科学,2019,38(5):686-693.
[12]尹子丽,许银凤,王 茂,等. 药用骨碎补类植物孢子形态特征研究[J]. 时珍国医国药,2017,28(10):2431-2434.
[13]李官政,邹 运,孙稚颖.山东菝葜属药用植物叶微形态学研究[J]. 中药材,2017,40(7):1563-1566.
[14]張 杰,周修腾,杨 光,等. 白术和苍术种子的显微鉴别研究[J]. 现代中药研究与实践,2019,33(5):4-6.
[15]方程吉,王春荣,田 薇,等. 不同表型白术质量评价及优株筛选[J]. 时珍国医国药,2014,25(3):712-714.
[16]黄有军,汪培军,沈天鹏,等. 不同产地白术根茎解剖比较[J]. 浙江林学院学报,2008,25(2):153-157.
[17]Williams J G,Kubelik A R,Livak K J,et al. DNA polymorphisms amplified by arbitrary primers are useful as genetic markers[J]. Nucleic Acids Research,1990,18(22):6531-6535.
[18]王宗宽,曹 炜,夏强强,等. 白术不同居群亲缘关系RAPD分析[J]. 安徽林业科技,2011,37(1):14-17,22.
[19]朱振洪,刘文洪,余 勤,等. 四种不同产地白术的DNA随机扩增多态性研究[J]. 浙江中医药大学学报,2011,35(4):575-577.
[20]周 涛,谢 宇,张丽艳,等. 基于SCAR分子标记的头花蓼分子鉴定研究[J]. 中国中药杂志,2013,38(16):2577-2580.
[21]王剑锴,李明杰,王建明,等. 金线莲RAPD-SCAR标记的开发和种质遗传多样性评价[J]. 中草药,2016,47(1):122-129.
[22]田孟良,官 宇,刘 帆,等. 基于RAPD标记的SCAR分子标记技术鉴定川牛膝及其混淆品[J]. 中国中药杂志,2010,35(8):953-956.
[23]李 敏,陈 强,茅学群. 中药白术SCAR分子鉴定标记的筛选和克隆[J]. 浙江工业大学学报,2015,43(2):148-153.
[24]王玲玲,陈东亮,黄丛林,等. SSR分子标记技术在植物研究中的应用[J]. 安徽农业科学,2017,45(36):123-126,130.
[25]巨秀婷,阿啟兰,侯志强,等. 基于ISSR分子标记的郁金香品种遗传多样性分析[J]. 基因组学与应用生物学,2017,36(7):2934-2939.
[26]杨春芳,曾 阳,郭凤霞,等. 分子标记技术在獐牙菜属植物研究中的应用进展[J]. 中草药,2017,48(15):3238-3244.
[27]马 辉,张智俊,罗淑萍,等. 药用植物白术ISSR-PCR反应体系的正交体系的正交优化研究[J]. 新疆农业科学,2009,46(1):40-45.
[28]卢 超,何银生,艾伦强,等. 道地药材咸丰白术ISSR反应体系优化及多态性引物筛选[J]. 分子植物育种,2018,16(22):7423-7428.
[29]郑 丽. 苍术属系统发育及药用植物白术的群体遗传和栽培起源研究[D]. 杭州:浙江大学,2013:1-174.
[30]Vos P,Hogers R,Bleeker M,et al. AFLP:a new technique for DNA fingerprinting[J]. Nucleic Acids Research,1995,23(21):4407-4414.
[31]沈 亮,徐 荣,陈 君,等. 我国肉苁蓉寄主梭梭种质资源多样性的AFLP分析[J]. 中国中药杂志,2014,39(6):959-964.
[32]王红娟,李雅婷,向增旭. 白术四倍体试管苗形态学及AFLP分析[J]. 中国中药杂志,2015,40(3):404-409.
[33]王志安,徐 行,沈晓霞,等. 白术种质AFLP指纹图谱分析体系的建立和应用[J]. 中药材,2008,31(4):483-487.
[34]陈士林,姚 辉,韩建萍,等. 中药材DNA条形码分子鉴定指导原则[J]. 中国中药杂志,2013,38(2):141-148.
[35]余亚东,石林春,马晓冲,等. 白术与苍术及其混伪品DNA条形码鉴定研究[J]. 中国中药杂志,2014,39(12):2194-2198.
[36]姚丹青,楼坚锋,顾芹芹. SNP在农作物遗传分析中的应用[J]. 上海农业科技,2015,354(6):26-27,41.
[37]曹 亮,蒋 超,彭华胜,等. 白术、苍术种子位点特异性PCR鉴别方法研究[J]. 中国中药杂志,2013,38(16):2567-2570.
[38]郭建林,葛燕芬,孙小芹,等. 基于RAPD标记的南苍术居群遗传多样性分析[J]. 植物资源与环境学报,2012,21(4):35-40.
[39]郭兰萍,黄璐琦,蒋有绪,等. 苍术遗传结构的RAPD分析[J]. 中国药学杂志,2006,41(3):178-181.
[40]卜 静,王冬梅,李登武. 不同产地野生玉竹种质资源多样性与亲缘关系的ISSR分析[J]. 中草药,2012,43(9):1824-1828.
[41]童巧珍,高 昱,刘平安,等. 基于SRAP标记的湘产百合核心种质库构建[J]. 江苏农业科学,2016,44(1):56-60.
[42]徐惠龙,汪英俊,陈 鸣,等. 基于ISSR标记的福建省多花黄精与长梗黄精种质鉴别及遗传多样性分析[J]. 福建农业学报,2017,32(6):619-624.
[43]罗光明,陈 岩,李 霞,等. 枳壳道地产区主流品种遗传多样性的ISSR分析[J]. 江西农业大学学报,2007,29(1):124-128.
[44]糜亞男,张水寒,蔡 媛,等. 杜仲SSR标记的遗传多态性及其亲缘关系分析[J]. 时珍国医国药,2015,26(10):2507-2509.
[45]朱鹏程,柳亦松,黄 鹏,等. 博落回SSR引物的开发以及遗传多样性分析[J]. 生命科学研究,2013,17(2):120-124.
[46]Tan Y,Cui Y S,Li H Y,et al. Rhizospheric soil and root endogenous fungal diversity and composition in response to continuous Panax notoginseng cropping practices[J]. Microbiological Research,2017,194:10-19.
[47]檀国印,杨志玲,袁志林,等. 药用植物连作障碍及其防治途径研究进展[J]. 西北农林科技大学学报(自然科学版),2012,40(4):197-204.
[48]Song R,Deng K,Zhu X Q,et al. Analysis of the causes of continuous cropping obstacles for Atractylodes macrocephala Koidz in Pingjiang county and its control methods[J]. Agricultural Science & Technology,2015,16(3):462-466.
[49]泷 岛. 防治连作障碍的措施[J]. 日本土壤肥科学杂志,1983(2):170-178.
[50]陈 慧,杨志玲,袁志林,等. 白术连作根际土壤的理化性质及微生物区系变化[J]. 植物资源与环境学报,2014,23(1):24-29.
[51]苏翠芬,刘留建,孙 静. 白术根腐病的发生与防治[J]. 河北农业,2014(5):37-38.
[52]蒋 平,刘光霞,汪丰琴. 白术铁叶病的发生及防控技术[J]. 植物医生,2017,30(9):43-44.
[53]张佳星,李 玲,戴德江,等. 白术枯斑病原鉴定、生物学特性及其对不同药剂的敏感性研究[J]. 植物病理学报,2018,48(5):682-692.
[54]Molish H B. Der einfluss einer pflanze auf die andere,allelopathie[J]. Verlag von Gustav Fischer,1937:13-20.
[55]张爱华,郜玉钢,许永华,等. 我国药用植物化感作用研究进展[J]. 中草药,2011,42(10):1885-1890.
[56]徐建中,王志安,孙乙铭,等. 白术自毒作用研究[J]. 中国现代中药,2011,13(11):25-27,48.
[57]熊鹏飞. 不同连作年限白术的化感作用及其对生长与产质量的影响[D]. 贵阳:贵州大学,2016.
[58]陈秋强,胡朝晖,徐建中,等. 白术发生连作障碍后土壤理化性质及根泌物的变化[J]. 中国科技纵横,2016,12(24):204-208.
[59]汤 民,张进忠,张 丹,等. 土壤改良剂及其组合原位钝化果园土壤中的Pb、Cd[J]. 环境科学,2012,33(10):3569-3576.
[60]陈 娟,张雪松,杨家学,等. 连作西洋参根际真菌群落差异及其在土壤药剂处理后的初步分析[J]. 中国中药杂志,2012,37(23):3531-3535.
[61]张子龙,孙 萌,李凯明,等. 基于TOPSIS-RSR法的三七连作障碍消减效应综合评价[J]. 中国生态农业学报,2015,23(6):713-724.
[62]张 燕,樱井美希,陈美兰,等. 不同石灰处理对苍术生长、产量和挥发性成分影响的研究[J]. 中药材,2015,38(3):429-432.
[63]唐 乐,曹国璠,李金玲,等. 土壤改良剂对连作白术质量、病害及土壤酶活性的影响[J]. 河南农业科学,2020,49(3):54-62.
[64]石雷磊,徐建中. 土壤处理对白术连作障碍的调控效应研究[J]. 中国现代应用药学,2018,35(5):693-697.
[65]Griffiths B S,Ritz K,Ebblewhite N,et al. Soil microbial community structure:effects of substrate loading rates[J]. Soil Biology and Biochemistry,1998,31(1):145-153.
[66]陈 慧. 连作白术根际土壤变化及PGPR菌肥缓解白术连作障碍研究[D]. 北京:中国林业科学研究院,2014.
[67]徐建中,孙乙铭,王志安,等. 白术—玉米轮作对白术植株生长及产量影响研究[J]. 中国现代中药,2012,14(2):40-42.
[68]刘文静,张建伟,邱崇文,等. 水旱轮作对土壤微生物群落构建过程的影响机制[J]. 土壤,2020,52(4):710-717.
[69]刘益珍,姜振辉. 稻田水旱轮作生态效应研究进展及发展建议[J]. 江苏农业科学,2019,47(20):19-23.
[70]黄依南,黄国勤. 东乡野生稻的发现、价值与保护[J]. 农业环境与发展,2012,29(1):13-15.
[71]刘逸慧,陈斌龙,周晓龙,等. 药用植物白术栽培群体的遗传多样性研究[J]. 中国中药杂志,2008,33(23):2756-2760.
