有机氯对乙烯环氧化反应性能的影响
2021-05-26吴同旭胡远明郭秋双孟广莹李晓云孙彦民于海斌
吴同旭,胡远明,郭秋双,孟广莹,李晓云,孙彦民,于海斌
(1.中海油天津化工研究设计院有限公司, 天津 300131;2.中国石油吉林石化公司化肥厂,吉林 吉林 132000)
环氧乙烷属于一种杂环化合物,是重要的石油化工有机中间体[1],银催化剂是目前用于乙烯不完全氧化制环氧乙烷的唯一催化剂。银催化剂的选择性对生产环氧乙烷的乙烯消耗起决定性的作用。由于环氧乙烷产量巨大,选择性若提高1%,即可节省大量乙烯原料,意味着巨大的经济效益。已有研究[2]认为,以有机氯化合物提供氯元素作为反应抑制剂,加入反应体系能够显著提高乙烯氧化反应的收率。
一些理论和实验已经证明添加适量的1,2-二氯乙烷,可有效改变银催化剂的表面吸附性能,有利于吸附氧与乙烯发生选择性氧化反应的进行,提高生成目标产物环氧乙烷选择性[3]。本文考察有机氯作为抑制剂对乙烯环氧化性能的影响,并且对抑制剂作用机理进行研究。
1 实验部分
1.1 催化剂制备
筛选合适的氧化铝前驱体,通过加入不同种类的造孔剂并筛选合适的添加方式,优化焙烧条件,实现构造出银载体所需大孔的同时,优化载体孔分布,并提高载体强度。
银载体物性:比表面积(1.5~1.8) m2·g-1;平均孔径(1 200~1 500) nm;强度(55~70) N;孔容(0.5~0.6) cm3·g-1;吸水率80%~100%;堆积密度(0.5~0.6) g·cm-3。XRD晶型:α相。
称取一定质量的硝酸银溶解后与草酸溶液反应得白色草酸银沉淀,采用负压过滤取其沉淀物草酸银滤饼。称取适量水置于烧杯中,依次加入一定量的乙二胺、少量乙醇胺,之后缓慢加入草酸银滤饼,得到银胺络合溶液。采用真空浸渍方法将所得银胺溶液浸渍于α-Al2O3载体上,浸渍液体积为载体吸水率的2~4倍,沥滤除去多余的溶液后,将其放入烘箱干燥,随后在氮气气氛210 ℃活化制成银催化剂。
1.2 催化剂表征
通过XRD、SEM、TEM、BET以及压汞法等测试表征手段对载体及银催化剂进行表征分析。图1为银催化剂载体XRD图。由图1的XRD峰形态可知,银催化剂载体为纯α-Al2O3晶相。
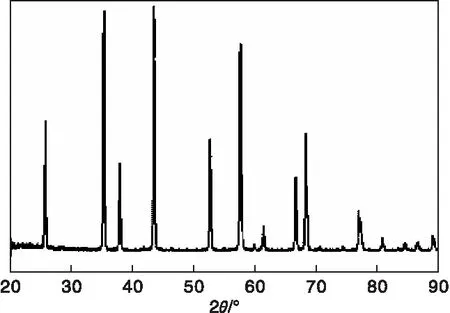
图1 银催化剂载体的XRD图Figure 1 XRD pattern of silver based catalyst support
图2为银催化剂载体的SEM照片。

图2 银催化剂载体的SEM照片Figure 2 SEM image of silver based catalyst support
由图2可以看出,银催化剂载体具有疏松的大孔隙的蠕动虫状的结构。
硝酸银与草酸铵在溶液中反应的反应方程式为:

由于银催化剂制备使用惰性大孔氧化铝材料,催化剂制备过程中要特别注意活性组分的负载。在银催化剂上活性组分是以银单质形式存在,银颗粒均匀覆盖于载体上,银颗粒的大小对温度影响较敏感。图3和图4分别为银催化剂的SEM和TEM照片。由图3和图4可以看出,银催化剂中的活性组分银颗粒在载体上均匀分散。

图3 银催化剂SEM照片Figure 3 SEM image of silver based catalyst

图4 银催化剂TEM照片Figure 4 TEM image of silver based catalyst
1.3 催化剂性能评价
采用10 mL固定床反应器,在反应压力(1.9~2.1) MPa、原料气流量50 L·h-1、反应原料气体积组成为乙烯13%、氧气7%、甲烷为系统平衡气的标准反应条件下,评价制备的银催化剂对乙烯环氧化反应的催化性能。考察抑制剂种类及用量对乙烯环氧化性能的影响,进而对有机氯化合物作为抑制剂的作用机理进行研究。
图5为银催化剂微反评价流程。抑制剂进料方式为恒温恒压下采用鼓泡法使用甲烷气带入。采用安捷伦公司7890B气相色谱仪对反应气体组成进行定量分析,配备HP-PLOT Q毛细色谱柱和热导池(TCD)检测器,用以分离和检测气体组成。

图5 银催化剂微反评价流程Figure 5 Micro reaction evaluation process of silver catalyst
2 结果与讨论
2.1 氯含量
在乙烯环氧化制环氧乙烷的反应条件下,控制反应温度225 ℃,加入四氯乙烯,考察氯含量对乙烯氧化性能的影响,结果如表1所示。
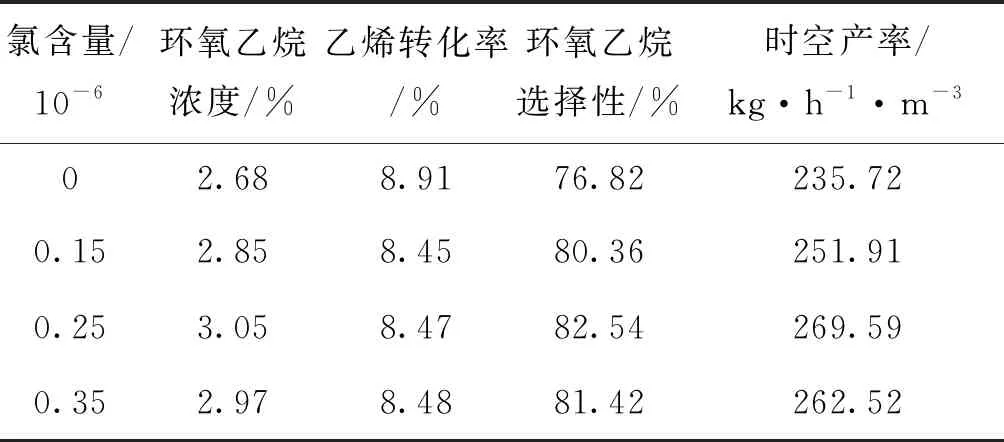
表1 不同氯含量对乙烯氧化性能的影响
由表1可以看出,以四氯乙烯为反应抑制剂,随着氯含量升高,环氧乙烷选择性和时空产率先升高后降低。当氯含量为0.25×10-6(以氯元素物质的量计,下同)时,目标产物环氧乙烷的选择性及时空产率最高。这是因为氯离子表面修饰金属银,可提高乙烯环氧化反应中环氧乙烷选择性,同时降低了催化剂的催化活性。因此,抑制剂的加入能够明显提高环氧乙烷选择性,抑制反应速率。
2.2 抑制剂类型
其他反应条件不变,考察氯含量为0.25×10-6时,不同抑制剂对乙烯氧化性能的影响,结果如表2所示。
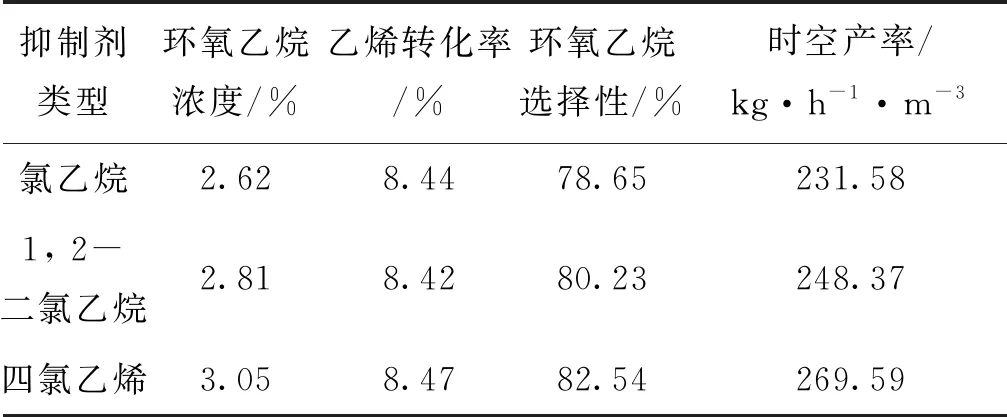
表2 不同抑制剂对乙烯氧化性能的影响
由表2可以看出,相同反应条件下,控制氯含量为0.25×10-6,分别选择氯乙烷、1,2-二氯乙烷、四氯乙烯作为氯源,四氯乙烯的反应效果明显优于氯乙烷和1,2-二氯乙烷。根据该实验结果,以四氯乙烯为例,对其作为抑制剂的作用机理进行研究。
2.3 抑制剂四氯乙烯反应机理
2.3.1 四氯乙烯在银催化剂及其载体上的反应
在反应器中装入10 mL未负载活性组分的α-Al2O3载体,相同反应条件下,通入含有四氯乙烯物质的量为0.25×10-6的气体(甲烷作平衡气)。改变反应温度,检测反应器出口气体中四氯乙烯含量,结果见表3。

表3 四氯乙烯在α- Al2O3载体上的分解反应
由表3可知,随着反应温度增加,反应器出口气体中四氯乙烯含量未发生实质性变化。由此可见,在(200~260) ℃,四氯乙烯在未负载活性组分的α-Al2O3载体上几乎不发生任何反应。
相同反应条件下,将同一气体通入装有相同粒度银催化剂的10 mL反应器中,依次设定反应温度为200 ℃、210 ℃、220 ℃、230 ℃、240 ℃、250 ℃、260 ℃,对反应器出口气体进行连续48 h取样分析。结果发现,反应器出口气体中均未检测到四氯乙烯,表明四氯乙烯在200 ℃时已在银催化剂表面完全分解。
2.3.2 氧气对四氯乙烯在银催化剂表面吸附分解的影响
将四氯乙烯物质的量0.25×10-6、氧气物质的量分数7%的气体(甲烷作平衡气)通入装有银催化剂的10 mL反应器中,在不同反应温度下,检测出口气体中四氯乙烯含量,结果见表4所示。

表4 氧气对四氯乙烯分解的影响
从表4可以看出,出口气体中四氯乙烯含量随反应温度的升高而降低,结合2.3.1研究结果,表明在氧存在下,氧气与四氯乙烯在银催化剂表面发生竞争性吸附,占据了部分银催化剂活性位,从而抑制四氯乙烯在催化剂表面的吸附及分解。随着反应温度升高,四氯乙烯的吸附作用越来越强。氧气占据银催化剂活性位的能力越来越弱,抑制四氯乙烯在银催化剂表面吸附分解的能力也越来越弱。
2.3.3 乙烯对四氯乙烯在银催化剂表面吸附分解的影响
相同实验条件下,将四氯乙烯物质的量0.25×10-6、乙烯物质的量分数28%的气体(甲烷作平衡气)通入装有银催化剂的10 mL反应器中,依次改变反应温度,检测反应器出口气体中四氯乙烯含量,结果见表5所示。

表5 乙烯对四氯乙烯分解的影响
由表5可以看出,乙烯存在下,反应器出口气体中含有四氯乙烯,其含量随反应温度的升高而逐渐降低。
2.3.4 抑制剂分解可逆性的研究
为考察由于抑制剂的分解而新产生的氯是否会与乙烯发生化学反应,进行如下实验:分别以氯乙烷、四氯乙烯及1,2-二氯乙烷为抑制剂,配制氧气、乙烯、甲烷混和气,抑制剂含量以氯元素计算,均为0.25×10-6,待完全混和均匀后,通入装有10 mL银催化剂的反应器中。在实验条件下,分别连续测定反应器出口气体中氯乙烷、四氯乙烯及1,2-二氯乙烷含量。结果发现,在反应温度为200 ℃时,装有银催化剂的反应器出口气中氯乙烷和四氯乙烯物质的量均为零,而1,2-二氯乙烷物质的量换算成氯元素的物质的量为0.23×10-6。由此证明,在乙烯环氧化制环氧乙烷反应条件下,由于有高浓度乙烯的存在,乙烯与游离氯发生加成反应,生成几乎等量的1,2-二氯乙烷。相当于1,2-二氯乙烷的分解为可逆反应,而不能生成氯乙烷和四氯乙烯,相当于氯乙烷和四氯乙烯的分解是不可逆反应。这也是虽然四氯乙烯抑制乙烯完全氧化的作用效果优于氯乙烷和1,2-二氯乙烷,但工业上大多选用1,2-二氯乙烷的原因。
3 结 论
(1)在原料气中添加微量的氯乙烷、1,2-二氯乙烷、四氯乙烯等含氯有机物作为抑制剂,可有效抑制乙烯完全氧化反应的进行,减少二氧化碳的生成,提高环氧乙烷选择性。氯含量为0.25×10-6(以氯原子物质的量计)时的抑制作用效果最佳。
(2)在相同的氯含量下,四氯乙烯的抑制效果优于氯乙烷和1,2-二氯乙烷。
(3)在乙烯环氧化制环氧乙烷反应条件下,由于大量乙烯存在,1,2-二氯乙烷的分解是可逆反应,氯乙烷和四氯乙烯的分解是不可逆反应。
