超高效液相色谱串联质谱法检测晨尿中儿茶酚胺及其代谢产物的价值
2021-05-26闫亚娟刘慧琳伦立民
闫亚娟,黄 猛,张 丹,刘慧琳,伦立民△
1.青岛大学医学部,山东青岛266000;2.青岛大学附属医院检验科,山东青岛266000
尿液儿茶酚胺及其代谢产物的检测对嗜铬细胞瘤的诊断具有重要意义[1-2]。近年来,国内外已建立了多种液相色谱串联质谱法(LC-MS/MS)用于定量检测尿液中的儿茶酚胺及其代谢产物[3-6]。这些方法大多留取患者24 h的尿液进行检测,存在诸多不足之处,如标本用量多、检测耗时长、标本前处理操作复杂等,限制了儿茶酚胺及其代谢产物检测的临床应用。因此,本研究旨在建立一种快速且可同时检测尿液儿茶酚胺及其代谢产物的超高效液相色谱串联质谱法(UPLC-MS/MS),采用简单、特异的微量尿样固相萃取,一次进样同时检测尿液中多种儿茶酚胺及其代谢产物,并建立健康成年人群尿液儿茶酚胺及其代谢产物的参考区间,为临床嗜铬细胞瘤的诊断提供帮助。
1 资料与方法
1.1一般资料 选择青岛大学附属医院体检健康者100例为研究对象,其中男51例,年龄19~65岁;女49例,年龄22~52岁。纳入研究对象均同时满足以下条件:(1)2020年1—7月来青岛大学附属医院健康体检的18~65岁成人;(2)经体格检查未见异常;(3)血常规、尿常规、血清生化检测均未见异常;(4)影像学检查肾上腺未见异常。纳入研究对象排除具有以下任意一项条件者:(1)有严重心、肺、肝、肾等器质性疾病,身体状况差;(2)不愿意参与本研究,拒绝签署知情同意书;(3)既往或目前患有或疑似患有肾上腺疾病。本研究获得青岛大学附属医院医学伦理委员会的批准,所有研究对象均自愿参与本研究,并签署知情同意书。
1.2仪器与试剂 Agilent Technologies 1290 Infinity Ⅱ超高效液相色谱仪(安捷伦,美国);QTRAP 5500三重四极杆质谱仪(AB SCIEX,美国);色谱柱(Agilent Pursuit PFP 2×150 mm);PWCX 96孔固相萃取板。试剂:标准品肾上腺素(E)盐酸盐、去甲肾上腺素(NE)盐酸盐、多巴胺(DA)盐酸盐、甲氧基肾上腺素(MN)盐酸盐、甲氧基去甲肾上腺素(NMN)盐酸盐、3-甲氧酪胺(3-MT)盐酸盐、高香草酸(HVA)、香草扁桃酸(VMA)及其对应的同位素内标E-d3、NE-d6、DA-d4、MN-d3、NMN-d3、3-MT-d4、HVA-d3、VMA-d3(Sigma,美国),醋酸铵(北京化工,中国),乙腈(色谱级,anaqua,美国),甲醇(色谱级,anaqua,美国),实验用水为超纯水(18.2 MΩ·cm,25 ℃),由BureWATER超纯水仪制备。尿肌酐检测采用日立7180全自动生化分析仪,试剂盒购自北京利得曼生化股份有限公司。
1.3方法
1.3.1工作液制备及质控品 采用0.2 mol/L的盐酸溶液配制10 μg/mL的儿茶酚胺及其代谢产物的储备液,并配制成不同浓度的标准品,浓度范围为0.5~1 000.0 ng/mL。
1.3.2标本采集 嘱所有研究对象在研究过程中不食用或饮用任何富含儿茶酚胺的食物及饮料,不服用任何药物,不进行剧烈运动,并保持日常生活方式,嘱其体检前一天晚上8点后禁食、禁饮,体检当天清晨6:00采集晨尿,并选择其中20例志愿者采集24 h尿液,采用6 mmol/L盐酸防腐,标本于—80 ℃冰箱保存。
1.3.3标本前处理 将标准品、质控品及尿液标本取出放置至室温,并混匀,将96孔固相萃取板预先用甲醇和水各1 mL进行活化和平衡。(1)患者标本:采用0.22 μm尼龙滤膜过滤得到尿滤液,取480 μL,加入20 μL内标工作液和1 mL 0.5 mol/L的乙酸铵溶液,涡旋5 s。(2)标准品及质控品:取20 μL不同浓度的标准品和质控品,加入 460 μL超纯水,混匀后分别加入20 μL混合内标工作液和1 mL 0.5 mol/L的乙酸铵溶液,涡旋5 s。将尿液标本、标准品及质控品分别加入96孔固相萃取板中,之后分别用1 mL 20 mmoL/L的乙酸铵溶液和1 mL甲醇进行洗脱,最后用500 μL的乙腈水溶液进行洗脱,收集洗脱液70 μL至96孔固相萃取板内,上机检测。
1.3.4色谱分析条件 色谱柱柱温为40 ℃,流速为600 μL/min,流动相A为水(0.1%甲酸),流动相B为乙腈(0.1%甲酸),梯度洗脱程序为0 min,5%B;2.5 min,50%B;3.0 min,95%B;3.5 min,5%B;5.0 min,5%B。
1.3.5质谱分析条件 电喷雾离子源(ESI),正离子 MRM 扫描分析,使用气体为高纯氮气,离子源电压为5 500 V,脱溶剂气温度为500 ℃,气帘气为25 psi,雾化气(GS1)为60 psi,辅助加热气(GS2)为55 psi,碰撞气(CAD)为medium,取上清液上机检测,每次进样量15 μL,其他部分质谱检测参数见表1。
1.4方法验证
1.4.1检出限(LOD)及定量下限(LOQ) 用标准曲线的最低浓度连续重复检测10次,可计算出LOD和LOQ,公式如下,LOD=3×SD/Slope,LOQ=10×SD/Slope。其中SD为这10次最低浓度的响应标准差,Slope为校准曲线的斜率。
1.4.2线性评估和标准曲线的建立 使用不同浓度的标准品,每个浓度重复检测3次,对6种分析物分别建立多元回归方程进行线性评估,分别记录6种分析物的线性方程和相关系数。
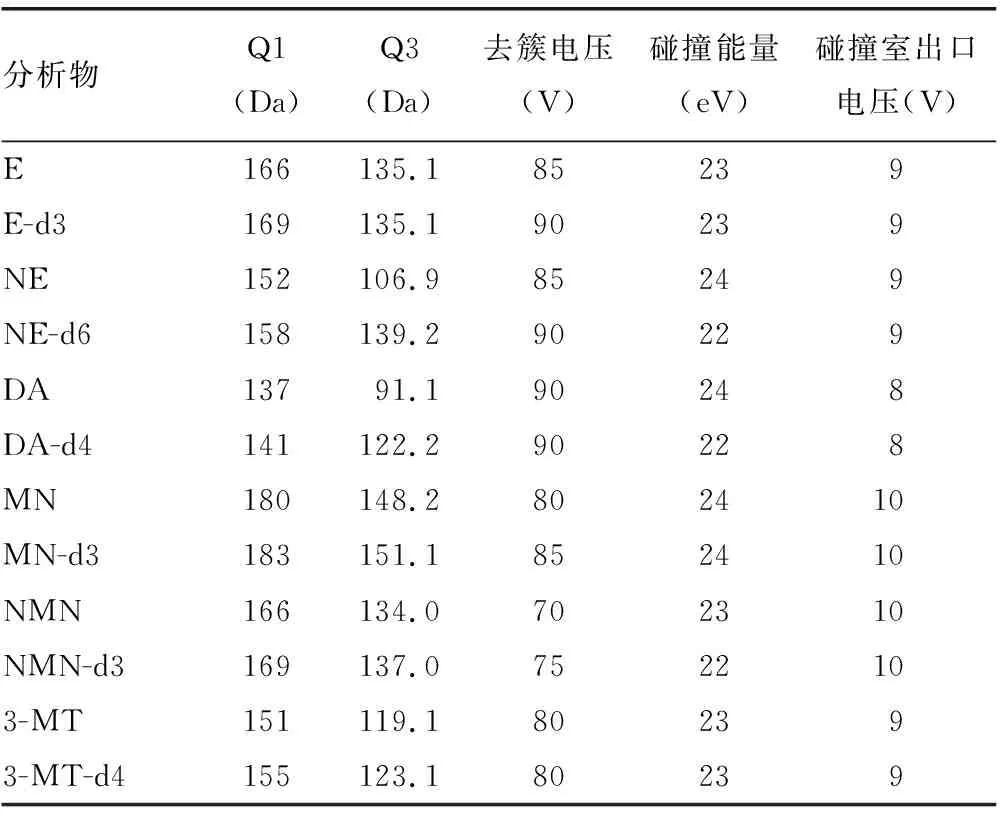
表1 儿茶酚胺及其代谢产物质谱参数优化
1.4.3精密度 取5例体检健康者的尿液标本分成3等份,分别加入高、中、低3个浓度的标准品,每个浓度每天重复检测5次,连续检测3 d,用重复检测的变异系数(CV)表示精密度。
1.4.4准确度 用回收实验进行评估,取5例体检健康者的尿液标本分成3等份,检测目的分析物浓度后,分别加入高、中、低3个浓度的标准品,检测加入标准品后的浓度。检测值应在理论值的±15%以内,低浓度点在理论值的±20%以内。准确度=尿液标本加入标准品后测定的浓度/样品中内源性分析物与加入标准品浓度之和。
1.4.5基质效应 尿样和空白溶剂用相同的固相萃取程序处理,取5例体检健康者的尿液标本分成3等份,检测目的分析物浓度后,分别加入高、中、低3个浓度的标准品,检测加入标准品后的浓度,比值应为0.85~1.15。基质效应=(本底加入标准品后的目的分析物浓度—本底中目的分析浓度)/溶剂中目的分析物浓度。
1.4.6稳定性 取10例体检健康者的尿液标本,分成5等份,1份立即检测,1份室温下放置24 h后检测,1份于4 ℃冰箱中保存24 h后检测,1份于4 ℃冰箱中保存48 h后检测,1份于—80 ℃冰箱中保存7 d后检测。分别分析标本在室温及4 ℃冰箱的短期稳定性及—80 ℃长期保存的稳定性。一般认为浓度变化<15%时分析物是稳定的。稳定性(%)=(放置后检测的浓度—立即检测的浓度)/立即检测的浓度。
1.5临床应用
1.5.1晨尿检测儿茶酚胺及其代谢产物的有效性 分析晨尿与24 h尿液收集这两种不同采样方法之间检测结果的相关性,选择20例研究对象,收集其晨尿及24 h尿液,根据肌酐输出值对稀释差异进行归一化,表示为分析物与肌酐的比值(μg/g Cr)。
1.5.2参考区间 采用建立的方法检测100例研究对象晨尿中各种儿茶酚胺及代谢产物,每种分析物的尿排泄量以其浓度与肌酐浓度的比值表示,单位为μg/g Cr。
1.6统计学处理 所有数据处理和量化均采用AB-SCIEX公司的Analyst 1.6.1软件包进行,使用SPSS26.0进行其他统计分析。采用K-S正态性检验对检测结果进行正态性检验,由于6种目的分析物均呈非正态分布,因此参考区间采用P2.5和P97.5分别作为下限值、上限值,采用Pearson相关和Logistic线性回归分析评价晨尿与24 h尿分析物的相关性。
2 结 果
2.1LOD、LOQ和线性评估 LC-MS/MS检测各种儿茶酚胺及其代谢产物的LOD和LOQ,在相应的浓度范围内,比较各种分析物浓度及其响应的线性和二次多项式回归,经1/x加权拟合的二次多项式回归显示,线性评估决定系数(r2)均>0.99,且标准偏差均较小,因此所有6种分析物均采用1/x加权的二次多项式回归。每种分析物的LOD、LOQ和线性参数见表2。
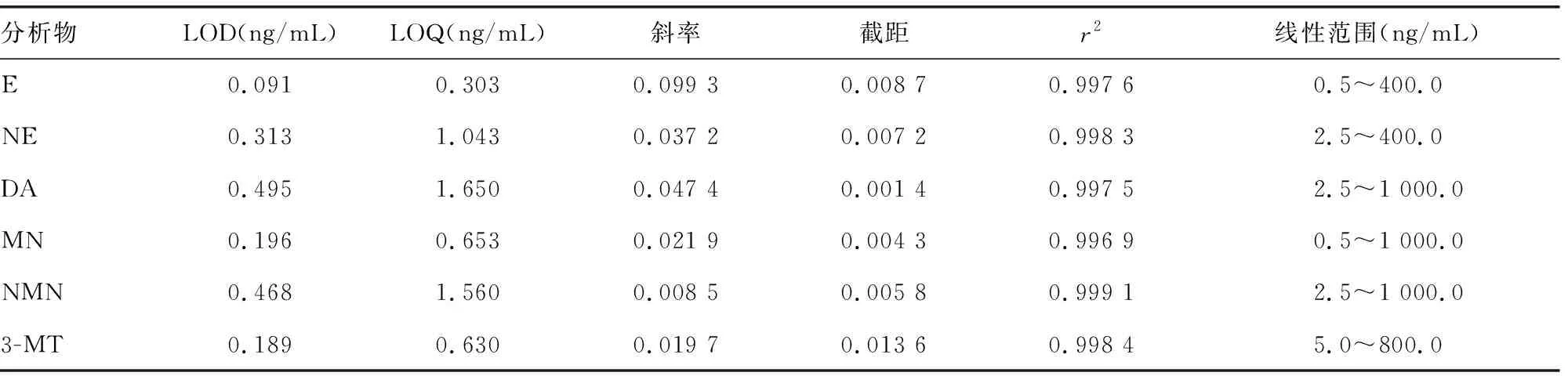
表2 儿茶酚胺及其代谢产物的LOD、LOQ和线性参数
2.2精密度 LC-MS/MS 检测6种分析物在3种浓度下的重复性均较好,批内精密度和总精密度为1.1%~8.5%,均能满足临床检测要求,见表3。
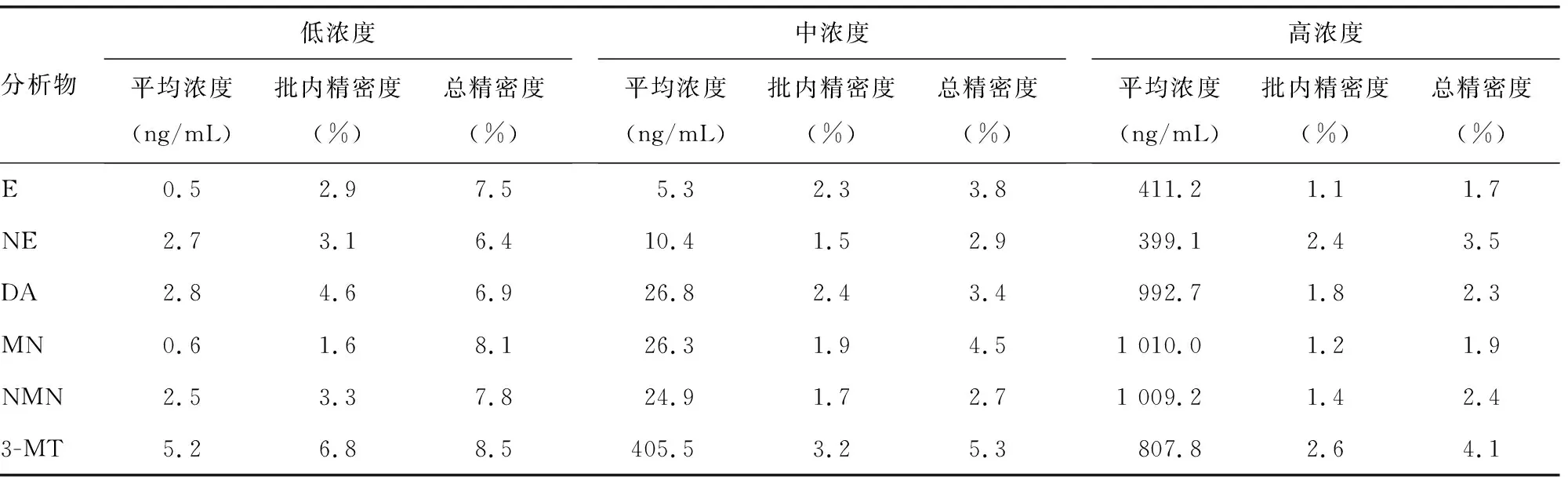
表3 LC-MS/MS检测儿茶酚胺及其代谢产物的精密度
2.3准确度和基质效应 6种儿茶酚胺及其代谢产物的准确度为97.2%~108.5%,s均在10%以内,均符合检测值应该在靶值的±15%以内的标准,见表4。6种分析物的基质效应为93.7%~108.5%,基质效应的CV为3.4%~7.3%,符合基质效应的CV应小于15%的标准,见表4。
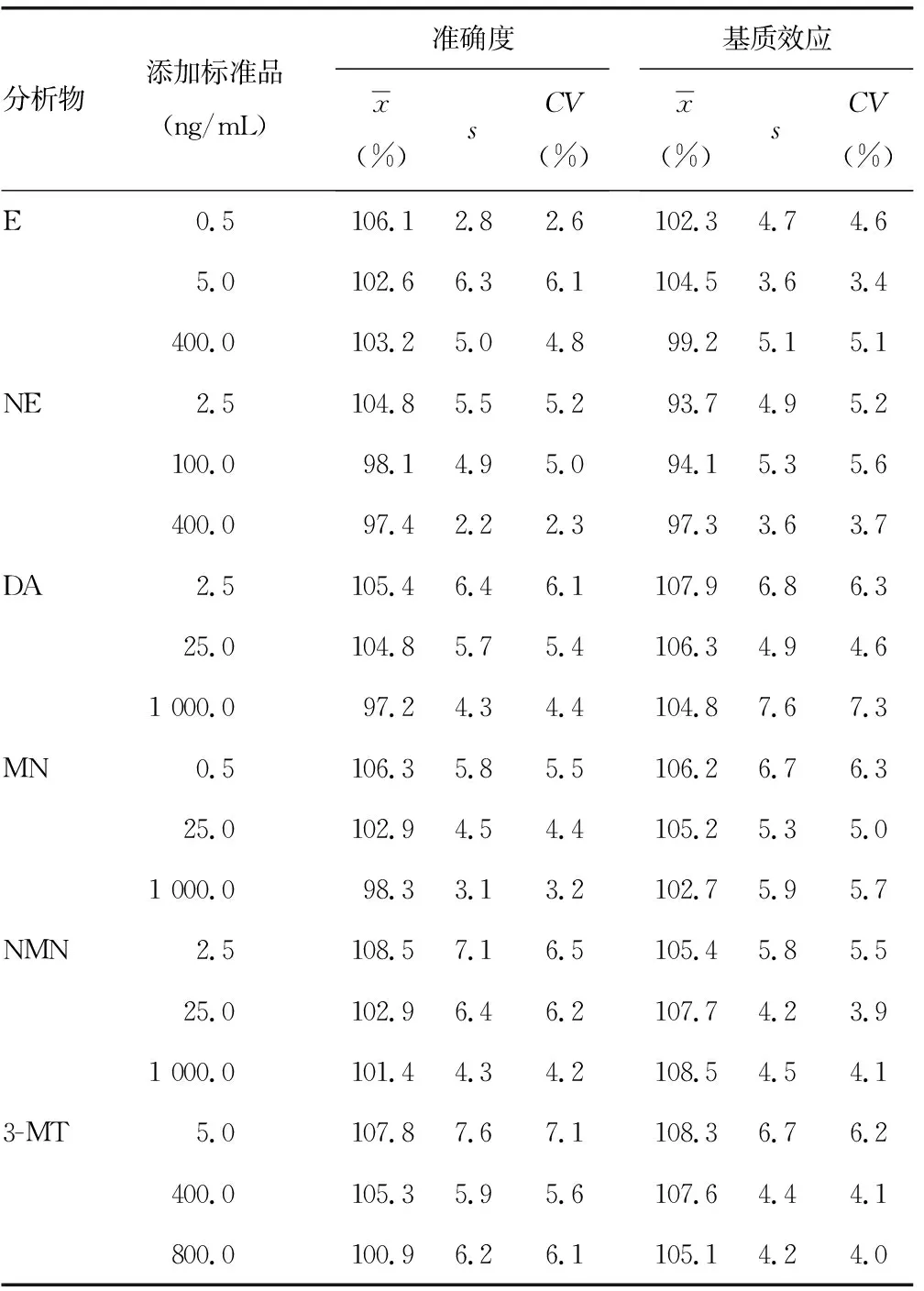
表4 LC-MS/MS检测儿茶酚胺及其代谢产物的准确度和基质效应
2.4稳定性 不同情况下尿液标本中儿茶酚胺及其代谢产物的稳定性,见表5。稳定性均较好,所有目的分析物浓度变化均≤6.2%。
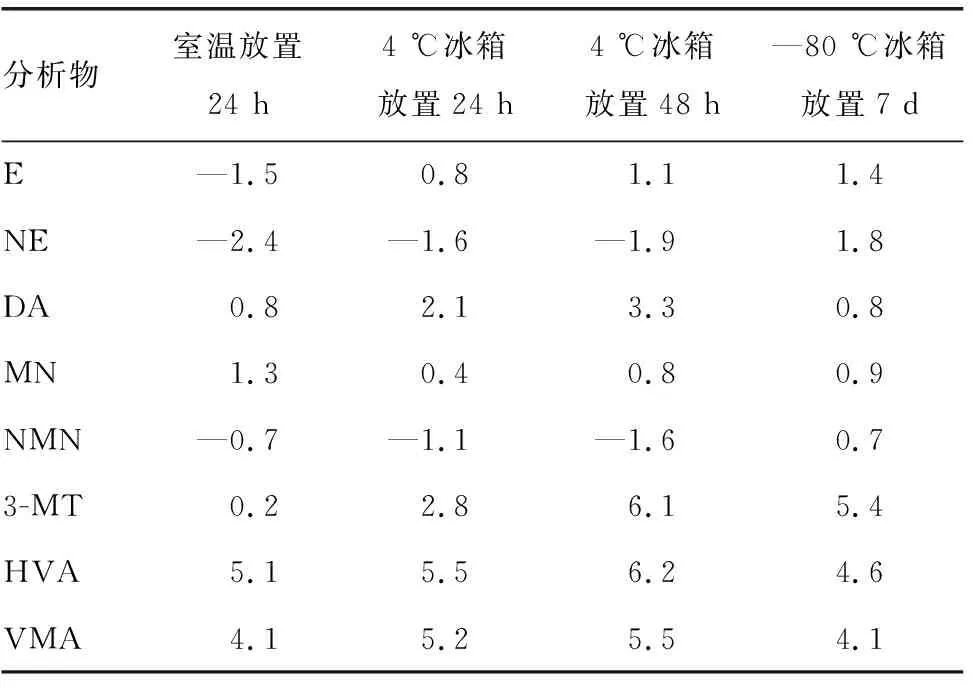
表5 儿茶酚胺及其代谢产物的稳定性(%)
2.5临床应用
2.5.1晨尿检测儿茶酚胺及其代谢产物的有效性 晨尿与24 h尿液收集这两种采样方法之间所有的分析物检测结果呈正相关(n=20,P<0.000 1,r:0.93~0.97,斜率:0.52~1.05)。晨尿与24 h尿儿茶酚胺及其代谢产物的相关性结果如下:NE线性回归分析斜率为0.683,r=0.952,P<0.000 1;E线性回归分析斜率为0.522,r=0.905,P<0.000 1;DA线性回归分析斜率为0.941,r=0.964,P<0.000 1;3-MT线性回归分析斜率为0.980,r=0.963,P<0.000 1;NMN线性回归分析斜率为0.622,r=0.937,P<0.000 1;MN线性回归分析斜率为1.050;r=0.969,P<0.000 1。
2.5.2参考区间 儿茶酚胺及其代谢产物检测结果箱形图见图1,取P2.5和P97.5建立参考区间,参考区间NE为2.6~140.4 μg/g Cr,E为0.3~37.2 μg/g Cr,DA为43.4~561.8 μg/g Cr,3-MT为18.0~165.7 μg/g Cr,NMN为15.1~241.5 μg/g Cr,MN为6.8~192.0 μg/g Cr。
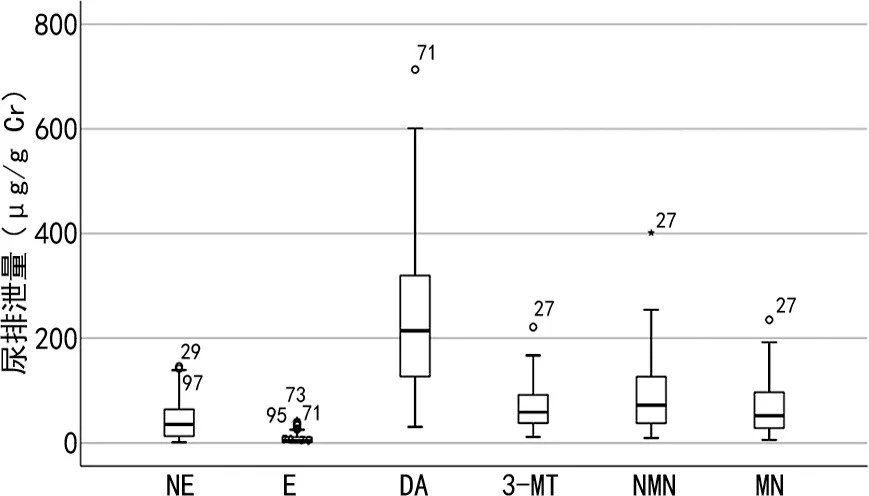
图1 100例健康体检者儿茶酚胺及其代谢产物检测结果箱式图
3 讨 论
嗜铬细胞瘤是一种罕见的神经内分泌肿瘤,起源于肾上腺髓质细胞,发病率约为0.05%[7]。嗜铬细胞瘤可大量释放儿茶酚胺,因此患者可出现各种严重的并发症,如果不能尽早诊断和治疗,会导致致命的后果[8-10]。儿茶酚胺及其代谢产物的联合检测可提高对嗜铬细胞瘤诊断的敏感性和选择性,可辅助诊断仅分泌DA的特殊类型嗜铬细胞瘤,对不同生化表型嗜铬细胞瘤的鉴别也发挥着重要作用[11-12]。临床通常通过检测尿液或血浆中的儿茶酚胺对疑似嗜铬细胞瘤患者进行筛查。然而,由于儿茶酚胺在体液中水平极低、极性高,使其准确检测十分困难[13]。另一方面,血浆儿茶酚胺水平很低,受试者采集标本时的姿势对检测结果影响很大,准确检测采集条件要求高,如不能充分满足采集条件则不能达到临床检测性能要求[14]。24 h尿液采集繁琐,收集过程非常耗时且容易出错,与其相比,晨尿的留取更加方便,并且利用了与夜间卧床休息时交感肾上腺系统活性降低的优势,避免了较多原因造成的交感肾上腺系统的激活,可以提高诊断性能[15-16]。
目前,用于儿茶酚胺及其代谢产物检测的常用方法有酶免疫检测法、液相色谱电化学分析法、LC-MS/MS。LC-MS/MS较前两者具有诸多优势,与酶免疫检测法相比,LC-MS/MS的灵敏度和特异度更高,前处理时间更短,并且能够准确检测前者无法检测的3-MT;与液相色谱电化学分析法相比,LC-MS/MS采样更便捷,标本前处理更简单,并且能够避免前者在分析时无法避免的干扰。本研究建立了检测晨尿儿茶酚胺及其代谢产物的UPLC-MS/MS,该方法具有简单、快速、灵敏度高、选择性高的优点,用晨尿标本代替24 h尿液收集进行检测,使标本采集更加简单方便,简化了pH值调节过程,并获得了更高的萃取效率,优化了梯度洗脱程序,在较短的运行时间内将潜在的干扰降至最低,并能获得较好的分离效果。
本研究建立了一种简单、快速,同时检测尿儿茶酚胺及其代谢产物的UPLS-MS/MS,并且进行了方法评价。这种方法采用晨尿标本替代24 h尿液收集,标本采集更加简单、方便。良好的验证数据和对实际尿样检测的成功应用表明,该方法灵敏、特异、可靠,可用于儿茶酚胺及其代谢产物排泄量的监测和嗜铬细胞瘤的鉴别及辅助诊断。
