肿瘤患者输液港并发感染和血栓形成的药学监护*
2021-05-26龚金红孙志强
龚金红,孙志强
(南京医科大学附属常州第二人民医院1.药学部;2.放疗科,常州 213000)
静脉输液港(central venous port,CVP)植入作为一种稳定、有效的静脉通道建立方式,与经外周静脉穿刺中心静脉置管(peripherally inserted central catheter,PICC)相比,可在体内置留更长时间,给肿瘤患者化学治疗(化疗)、肠外营养支持治疗带来极大方便。该技术的使用既避免了化疗药物对静脉内膜的刺激,又减轻了多疗程化疗穿刺的痛苦,但因CVP导管长期留置于血管内,存在导管折曲移位、感染、血栓形成等[1]相关并发症风险。笔者参与1例食管癌并发导管相关性静脉血栓及感染患者的治疗,并施行药学监护,保障了患者药物治疗安全、有效。
1 病例资料
患者,男,62岁,身高180 cm,体质量65 kg,体表面积1.82 m2。因“进食哽噎1个月余”于2019年8月6日入院。患者1年前诊断为食管癌,曾行同步放化疗(紫杉醇270 mg 第1天+顺铂42 mg 第1~3天×4周期)。2个月前患者出现进食哽噎,胃镜、PET-CT检查提示食管癌复发、转移。2019年7月26日经右侧颈内静脉植入输液港,次日行白蛋白结合型紫杉醇400 mg 第1天+奈达铂140 mg 第2天化疗。近1周来,患者仍感进食哽噎,进食后感疼痛,收住入院。体检:体温36.9 ℃,脉搏72次·min-1,呼吸16次·min-1,血压110/74 mmHg(1 mmHg=0.133 kPa),卡氏功能状态评分80分。辅助检查:白细胞(WBC)计数13.70×109·L-1,中性粒细胞比例82.30%,空腹血糖3.06 mmol·L-1,血钾3.32 mmol·L-1,C反应蛋白(CRP)23.8 mg·L-1,D-二聚体2.08 mg·L-1。
2 主要治疗经过与药学监护
2.1主要治疗经过患者入院后予抑酸、补液、依替米星抗感染、营养支持等治疗。入院6 d内体温正常,痰培养、血培养阴性,停用依替米星。第9天患者食欲明显好转,停用肠外营养并加强经口饮食。考虑患者食管鳞癌放化疗后复发,给予卡瑞利珠单抗免疫治疗联合紫杉醇化疗,辅以抑酸、护胃、保肝等对症支持治疗。患者输注卡瑞利珠单抗后约6 h出现高热,最高达39.7 ℃,医师考虑卡瑞利珠单抗引起不良反应[2],给予吲哚美辛、复方氨林巴比妥、地塞米松、物理降温等处理。患者入院血钾偏低,且卡瑞利珠单抗、地塞米松均可导致低钾血症,目前血钾较前进一步降低,予氯化钾缓释片口服补钾。入院第12天,患者仍有发热,无咳嗽咯痰,无腹痛、腹泻,无尿频尿痛。体检:右侧颈部稍肿胀。辅助检查:WBC 8.35×109·L-1,中性粒细胞 6.43×109·L-1,中性粒细胞比例 77.01%,血钾3.38 mmol·L-1。患者连续3 d出现高热,吲哚美辛栓、复方氨林巴比妥、物理降温处理无明显缓解,注射地塞米松后好转,医师考虑卡瑞利珠单抗引起的免疫性反应。入院第14天,患者右侧颈部肿胀加重,输液港内回抽无回血。动静脉彩色B超检查提示右侧颈内静脉腔内折叠的输液港导管强回声影,周围不均质混合回声影充填,近心段未见明显血流显示,提示右侧颈内静脉血栓形成。临床药师会诊探讨抗栓方案,建议立即予“依诺肝素4000 U、q12 h”抗凝,医师采纳,拟数字减影血管造影术下明确血栓情况并评估导管拔除或导管内溶栓的可行性。对药师选择阿替普酶溶栓[3-4]的建议,医师考虑患者治疗成本,未采纳,选择了尿激酶。
入院第15天数字减影血管造影术提示输液港导管脱落移位至右侧颈内静脉内,右侧颈内静脉及头臂静脉血栓形成,长度约10 cm,遂行“上腔静脉滤器置入+溶栓导管置入术”,术中注入“尿激酶10万U”,术后导管泵入“尿激酶10万U,q6 h×3 d”。入院第16天患者右侧颈部肿胀较前消退,无皮下、牙龈出血。体检:血压 96/57 mmHg,心率79次·min-1,律齐,未闻及病理性杂音。辅助检查:WBC19.41×109·L-1,中性粒细胞 17.88×109·L-1,降钙素原(procalcitonin,PCT)0.21 ng·mL-1,血钾4.22 mmol·L-1,D-二聚体>40 mg·L-1。医师考虑血栓形成应激引起血常规等异常,未予关注。临床药师提醒:患者昨日术后有高热(39.2 ℃)、白细胞及PCT升高,存在感染可能,建议予“头孢曲松2 g,qd,静脉滴注”经验性抗感染治疗,医师采纳。患者血压偏低,加强补液扩容,同时予“贝前列素钠、丹参注射液”改善循环。导管内溶栓后72 h复查血管造影提示血栓已明显消失,血管通畅,予拔除输液港及溶栓导管,并取输液港导管尖端送细菌培养。入院第21天,患者无发热、畏寒。辅助检查:WBC 5.91×109·L-1,中性粒细胞3.51×109·L-1,丙氨酸氨基转移酶(ALT)90.0 U·L-1,天冬氨酸氨基转移酶(AST)69.0 U·L-1,γ-谷氨酰转肽酶(γ-GGT)97.0 U·L-1,血钾3.73 mmol·L-1,D-二聚体3.70 mg·L-1。加用异甘草酸镁、多烯磷脂酰胆碱保肝治疗,并停用补钾药物。入院第22天,患者一般情况良好,右股静脉穿刺置管行原方案化疗,同时抑酸护胃、止吐、保肝,药师密切监护化疗相关不良反应。入院第23天,导管细菌培养检出金黄色葡萄球菌(苯唑西林敏感),头孢曲松敏感且治疗有效,继续原抗感染方案。入院第25天患者一般情况良好,未出现明显不良反应。抗感染治疗10 d,近日体温、血常规等均恢复正常,无其他感染相关体征,停用头孢曲松,出院。出院后继续利伐沙班15 mg,po,bid,服用21 d后调整为20 mg,qd。药师对患者出院带药进行用药指导,如出现牙龈出血、皮肤瘀斑、胃部不适、黑便、尿血等出血症状,及时就诊。患者住院期间主要治疗药物见表1。
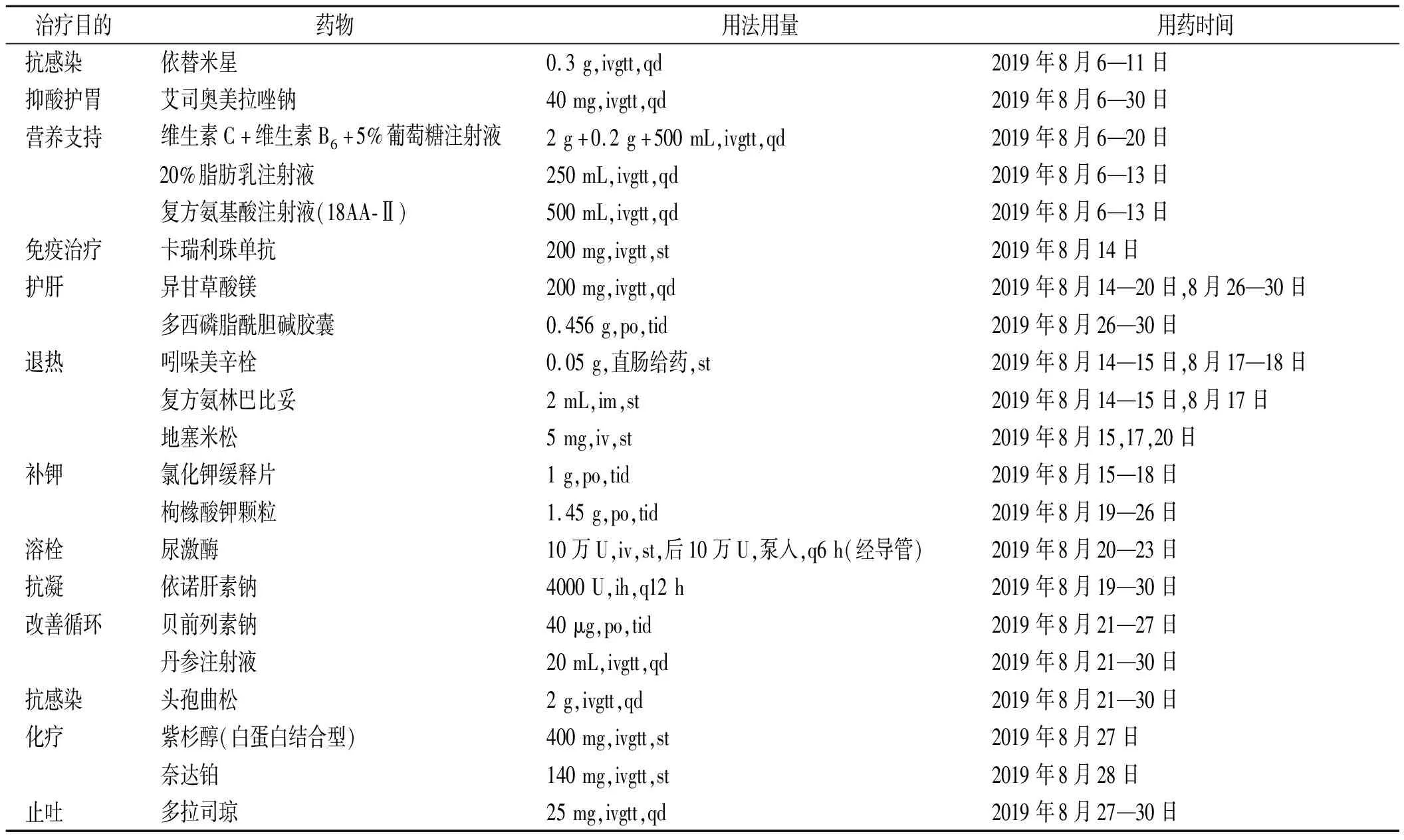
表1 患者住院期间主要用药情况
2.2药学监护临床药师在患者发生血栓后对其实施密切的药学监护,抗栓治疗监护:患者予依诺肝素钠抗凝联合尿激酶导管溶栓出血风险较高,药师每日2次查看溶栓导管局部是否有血肿形成,观察并询问患者是否有牙龈出血、胃部不适、头痛、血尿、黑便等症状,监护凝血功能、D-二聚体、血小板计数等检验指标。该患者抗凝、溶栓治疗期间未发生出血不良反应,凝血功能及血小板计数均在治疗可接受范围内。抗感染治疗监护:每日监测患者体温、血常规,并及时跟踪导管及血培养结果。培养及药敏结果示金黄色葡萄球菌,头孢曲松敏感,药师认为无需调整抗感染方案。患者血培养阴性、体温及血常规等感染指标均正常后72 h停用抗菌药。化疗监护:患者改从右股静脉穿刺置管行紫杉醇+奈达铂化疗,药师监护患者静脉置管局部是否有肿胀等异常情况、化疗前后肝功能、D-二聚体等指标。化疗期间未发生明显不良反应。
3 讨论
3.1导管相关性感染输液港港体或导管感染是CVP常见的并发症,可导致住院时间延长、费用增加、死亡率上升。一项系统评价分析显示,导管每个月使用时间、住院治疗、姑息化疗、肠外营养、中性粒细胞减少、血液系统恶性肿瘤等是成人植入式输液港相关感染的危险因素[5]。该患者存在导管每个月使用时间长、住院治疗、化疗、肠外营养等多种危险因素,此次住院治疗期间有发热,行上腔静脉滤器及导管溶栓后,白细胞较前明显升高,可能与激素、血栓应激有关,临床药师考虑不排除感染,感染部位及病原菌不明确,导管相关性感染亦不能排除。徐惠芳等[6]报道老年恶性肿瘤患者静脉导管相关性血流感染病原菌中,革兰阳性菌占40.96%,以凝固酶阴性葡萄球菌、金黄色葡萄球菌为主;革兰阴性菌占54.22%,以大肠埃希菌、肺炎克雷伯菌为主。头孢曲松对金黄色葡萄球菌、凝固酶阴性葡萄球菌、肺炎链球菌等革兰阳性菌及大多数革兰阴性菌有较好的杀菌效果,此外对消化性链球菌等厌氧菌也有抗菌活性,因此建议选择头孢曲松。数字减影血管造影术显示导管血栓负荷较重,立即移除可引起其他血栓事件风险,抗凝、溶栓3 d后成功移除导管。经治疗,患者体温、血常规等均趋于正常,输液港导管尖端培养提示金黄色葡萄球菌(苯唑西林敏感),血培养阴性,提示存在导管感染,头孢曲松敏感且治疗有效,继续原方案治疗10 d,好转出院。
3.2肿瘤患者静脉血栓栓塞症(venousthromboem-bolism,VTE)
3.2.1肿瘤患者VTE风险评估肿瘤相关静脉血栓栓塞症发病率4%~20%,与非肿瘤患者相比,肿瘤患者血栓形成风险升高4~7倍。肿瘤患者发生VTE风险因素较复杂,肿瘤自身因素(如部位、分期、转移等),手术,化疗,内分泌治疗,中心静脉置管等均可影响肿瘤患者VTE的发生[3]。本例患者食管癌复发转移,经输液港行白蛋白结合型紫杉醇联合奈达铂化疗,在输液港植入后约3周发生血栓,与文献[7]报道的中心静脉置管后前6周VTE风险最高一致。目前肿瘤VTE风险评估常用的工具主要有Khorana评分、Caprini评分以及Padua评分[8]。Khorana评分[9]是针对肿瘤患者设计的静脉血栓预测模型,纳入肿瘤类型、血小板计数、血红蛋白、白细胞计数、体质指数等5项指标,评分0分、1~2分、≥3分分别预示VTE风险级别为低危、中危、高危,美国临床肿瘤学会指南指出Khorana评分≥3分或胰腺癌、肺癌、胃癌患者,在患者知情基础上可使用预防剂量的低分子肝素或普通肝素。Caprini评分[10-11]广泛应用于所有住院患者VTE风险评估,由于该模型考虑了肿瘤相关的多种风险因素,被我国肿瘤相关VTE防治指南推荐使用[12]。依据评分将患者VTE风险分为低危(0~1分)、中危(2分)、高危(3~4分)和极高危(≥5分),>3分即建议予肝素预防性抗凝。Padua评分是主要用于评估内科住院患者VTE风险的模型,被国内外多个指南[13-14]推荐应用,包括11个危险因素,按评分结果分为低危组(<4分)和高危组(≥4分)。研究认为Padua风险模型对肿瘤患者VTE的识别有较好的特异性[15]。
本例患者按Khorana评分(2分)属于中危患者,按Caprini评分(7分)和Padua评分(4分)均属于高危患者,因此有VTE预防指征。对肿瘤患者常规进行动态Caprini评分筛查将有助于早期识别VTE高危患者,从而及早干预,改善肿瘤患者的不良结局。目前我院已在骨科、胃肠外科等多个科室引入Caprini评分筛查工具,但肿瘤科还未正式开展。临床药师正在同肿瘤科医师、护士沟通,为肿瘤患者制订Caprini评分筛查流程,对高危患者进行早期VTE预防。此外,该患者初始出现右颈部肿胀时未引起重视,直至2 d后输液港体回抽无回血才进行血栓排查,提示医护人员在肿瘤患者VTE防治方面的意识仍有待加强,临床药师与肿瘤科医生、护士就此进行了交流,对血栓形成相关的症状体征(如发热、置管局部红肿)以及检验指标异常(如WBC、血小板、D-二聚体等升高)引起高度警惕,做到早发现、早诊断、早治疗。
3.2.2肿瘤患者VTE治疗近年来,新型口服抗凝药(new oral anticoagulant,NOAC)因应用方便、安全等优势,在髋关节或膝关节置换术VTE预防、非瓣膜性心房颤动患者卒中和全身性栓塞预防等领域应用逐渐普及,其在肿瘤患者VTE防治方面也引起了广泛关注。美国临床肿瘤学会癌症患者VTE防治指南[16]不推荐对同时患有恶性肿瘤和静脉血栓的患者使用NOAC。2018加拿大专家共识[17]指出NOAC用于肿瘤相关性血栓治疗不劣于低分子肝素,但直接凝血酶抑制剂达比加群对肿瘤相关性血栓疗效证据不足。2019年美国国立综合癌症网络指南[3]对利伐沙班、阿哌沙班、依度沙班、达比加群均有推荐。本例患者不愿意口服华法林并进行国际标准化比值(INR)监测,根据2019年美国国立综合癌症网络指南,临床药师建议该患者住院期间采用依诺肝素4000 U、皮下注射、q12 h方案,出院后予利伐沙班口服抗凝,每次15 mg,每天2次,服用3周后调整为每天1次,每次20 mg,至少3个月,后根据患者3个月后动态Caprini评分确定是否延长抗凝。随访至今,患者未发生血栓或出血事件。
3.3“专科”临床药师“专域”化由于慢病早龄化、人口老龄化以及手术等因素,目前临床各科室收住患者往往合并多种疾病或并发症,如内分泌科糖尿病患者、心内科冠心病患者、风湿疾病科强直性脊柱炎患者、肾内科膜性肾病患者、肿瘤以及外科大手术患者等在住院治疗过程中并发急性脑梗死、静脉血栓栓塞症,创伤外科、神经外科等术后并发癫,外科手术后感染……对于这些非本专科疾病,医生一般通过会诊的方式处理,但会诊医生通常给予常规急性期处理意见,缺乏远期评估与监护,专科临床药师在抗栓、抗癫、抗感染等药物治疗方面能发挥协助治疗、药学监护的作用。本例CVP植入食管癌患者出现静脉血栓及感染,通过神经内科临床药师参与治疗方案制订及药学监护,保障了肿瘤患者发生特殊并发症时药物治疗的安全、有效,改善了患者的临床结局。为临床药师探索参与专科外的重点患者相关疾病的临床治疗,逐步建立“专域化”药学服务模式提供了参考。
