2.2 mm与3.0 mm透明角膜切口白内障超声乳化吸除术对角膜屈光度和角膜散光的影响鲍迅
2021-05-26林云志朱靖姚勇
林云志 朱靖 姚勇
当今世界,白内障超声乳化吸除(phacoemulsification,phaco)联合人工晶状体(intraocular lens,IOL)植入手术是治疗白内障的经典方法,伴随手术技巧的提高、手术设备的发展以及患者对视觉质量的期待,白内障手术后患者不仅看的见、看的清,还看的舒服、看的持久。角膜的切开不可避免的会使角膜表面完整性受到破坏,引起角膜散光[1]。角膜散光是影响白内障手术后视觉质量的重要因素,即使是微小切口仍会产生手术源性散光(surgically induced astigmatism,SIA),引起视力下降、复视、头晕等症状[2]。由此看来,研究phaco+IOL植入术中透明角膜切口大小对角膜屈光度和角膜散光的作用,有利于改善患者术后视觉质量。
资料与方法
一、一般情况
本实验采取的方法为前瞻性双盲随机对照研究。严格遵守本单位医学伦理委员会的相关章程,在向患者及家属详细说明实验情况后,自愿签署实验知情同意书。随机选择2019年1月至2020年1月在我医疗机构就诊的年龄相关性白内障患者70例(70只眼),分为研究组35例(35只眼):男性16例(16眼),女性19例(19只眼),年龄(66.21±4.13)(52~85)岁和对照组35例(35只眼):男性17例(17只眼),女性18例(18只眼),年龄(68.17±3.49)(50~88)岁,前者行2.2 mm透明角膜切口Phaco+IOL植入术,后者行3.0 mm透明角膜切口phaco+IOL植入术。手术前对所有患者行眼科全面体格检查,并用Pentacam眼前节测量仪测量每位患者的角膜屈光度、角膜散光等指标。所有手术检查均由特定的经验丰富的医技检查人员进行。除外合并有干燥综合征、强直性脊柱炎、结缔组织病等全身性疾病者和合并有角膜炎、青光眼、视网膜疾病、葡萄膜炎等其他眼部手术史者以及既往行内眼手术者。
二、手术步骤
手术过程均由同一名高年资经验丰富的白内障手术医生完成。术前连续3 d用可乐必妥滴眼液(参天,日本)滴眼,1 d 4次。手术开始前用倍诺喜滴眼液(参天,日本)滴眼,5 min1次,点3次。研究组同时用2.2 mm角膜穿刺刀(sharepoint,美国)和15°角膜穿刺刀(sharepoint,美国)在10点和2点做透明角膜主、侧切口,然后用黏弹剂加深前房、扩大瞳孔,连续环形撕囊,直径为5.5 mm,钝针头行水分离,拦截劈裂乳化核块,注吸(I/A)皮质,抛光针头行后囊膜抛光,再次注入黏弹剂,用推注器将折叠式人工晶状体注射于囊袋内,I/A头吸净前房和IOL前后的黏弹剂,水密透明角膜主、侧切口,指测眼压正常,典必殊眼膏涂眼,聚维酮碘消毒上下眼睑,无菌纱布封眼。术后用典必殊滴眼液(爱尔康,美国)涂眼,2 h 1次持续1周,然后1 d 4次持续至1个月,典必殊眼膏(爱尔康,西班牙)涂眼,持续1个月。参考组除用3.0 mm穿刺刀制作透明角膜主切口,其余步骤均相同。
三、术后分析指标
研究组和参考组所有患者,术后4个月均用Pentacam眼前节测量仪检测,分析参与的患者手术前和手术后4个月角膜前表面屈光度、角膜后表面屈光度、角膜前表面散光、角膜后表面散光、角膜总散光的变化。
四、统计学分析
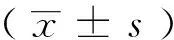
结 果
一、研究组患者手术前后角膜屈光度及角膜散光统计
研究组手术前后角膜前表面屈光度及前表面散光比较均无统计学意义(P=0.468,0435),角膜后表面屈光度和后表面散光比较均有统计学意义(P=0.0005,0.017),具体情况见表1。

表1 研究组手术前后角膜屈光度及散光变化(D)
二、参考组患者手术前后角膜屈光度及角膜散光统计
参考组患者手术前后角膜前表面屈光度及前表面散光比较均无统计学意义(P=0.758,0.476),角膜后表面屈光度及后表面散光比较均有统计学意义(P=0.023,0.0003)。见表2。

表2 参考组手术前后角膜屈光度及散光变化
三、两组患者手术前后角膜屈光度及散光变化值统计
两组患者手术前后角膜前表面屈光度差值、角膜前表面散光差值比较分析后均无统计学意义(P=0.524,0.867),研究组手术前后角膜后表面屈光度差值、角膜后表面散光差值均小于参考组(P=0.003,0.025)。见表3。

表3 两组患者手术前后角膜屈光度和散光差值比较
四、角膜总屈光度、总散光统计
两组患者手术前后角膜总屈光度差异均无统计学意义(P=0.529,0.313),两组患者手术前后角膜总散光比较均有统计学意义(P=0.039,0.027)。见表4。

表4 两组患者手术前后角膜总屈光度和总散光比较
讨 论
现如今,白内障手术切口越来越小,对眼球创伤也越来越小,手术后视功能恢复很快。但是即使切口再小,都不可避免的会对眼球完整性和弯曲度产生变化,引起术后散光,其中以角膜散光最常见。手术源性散光产生原因多种多样,常见的如手术切口的位置、形态和长度,手术器械反复进出眼球,超声能量释放等因素,其中切口是影响角膜散光最重要的因素[3]。相关研究显示[4],散光度数若超过0.75 D,就会引起视力下降、视物模糊、复视、头晕等症状。因此,散光矫正是屈光性白内障手术的必然要求。研究显示[5],透明角膜切口每减少0.5 mm,SIA减少约0.25 D。但SIA不会随着切口的变小而越来越小,据相关研究报道[6,7],2.2 mm透明角膜切口和1.8 mm透明角膜切口产生的SIA无统计学意义。
临床上测量角膜屈光度的方法多种多样,常见的有角膜曲率计、电脑自动验光仪、波前像差仪、IOL-master光学眼生物测量仪、Lenstar测量仪、Pentacam眼前节测量仪等。Pentacam眼前节测量仪是建立在Scheimpflug光学理论上,进行三维扫描和旋转测量,其摄像系统具有整合功能,测量时摄像系统可以拍摄50张图片,每张图片包含有角膜前后表面共500个点,可以获得角膜前后表面形态结构。Pentacam测量的是高度信息,与轴位和方位的变化无关,最终由高度演算成角膜屈光度信息,其中包括了角膜前后表面的屈光度信息[8]。由于Pentacam测量与测量方向和参考点的轴位无必然的联系,因此具有更好的可重复性和精准度[9]。
本研究统计分析显示,2.2 mm与3.0 mm透明角膜切口白内障超声乳化手术对角膜前表面屈光度和前表面散光的作用较小,但是角膜后表面屈光度和后表面散光因切口变化较大,且3.0 mm透明角膜切口对角膜后表面屈光度作用更大,说明越大的角膜切口,对角膜的生物学特性影响更大,角膜的恢复时间更长,这与先前文献报道相吻合[10,11]。另外,我们在手术前在计算IOL度数时如果没有将角膜后表面屈光度包括在内,那术后角膜屈光状态就会与预测的产生偏差。目前临床上角膜后表面屈光度很难精确计算,常理想化的认为角膜后表面屈光度与前表面屈光度为一常数。由于角膜后表面界面由内皮细胞和房水组成,因此角膜后表面的屈光度明显小于前表面,从而引起对角膜后表面的忽略。随着Pentacam的广泛应用,角膜后表面对角膜屈光度的影响受到越来越多关注。相关学者研究发现[12],角膜后表面产生的SIA为(0.33±0.28)D,其中SIA大于0.5 D者占比为28%。Nemeth等[13]研究表明,手术切口对角膜后表面可以产生显著作用,忽视这种影响会影响屈光手术的精准性,使得屈光性人工晶状体不能发挥应有的效果。综上看来,因为透明角膜切口为全层切口,SIA也要考虑到角膜后表面散光。Hayashi等[14]研究表明,在角膜陡峭上做主切口,可以显著降低术后角膜散光并减轻手术前角膜散光,但也有文献报道[15],在陡峭轴上做切口并没有引起术前角膜散光减轻,而这是由于没有考虑到角膜后表面散光的作用。因此,角膜后表面散光会对术后屈光状态产生重大影响。
伴随医疗技术的提升、医疗设备的改进、患者手术期望值的上升,屈光性白内障摘除手术会不断发展。通过研究手术后角膜屈光度和角膜散光的变化,手术医生可以更好的进行手术设计,减小甚至规避散光对术后视觉质量的影响,提升患者视功能。
