基于DCE-MRI影像组学和临床特征的列线图在乳腺MRI BI-RADS 4类病灶中的诊断价值
2021-05-25赵悠帆陈中伟周洁洁缪海卫李建策王美豪
赵悠帆,陈中伟,周洁洁,缪海卫,李建策,王美豪
温州医科大学附属第一医院 放射影像中心,浙江 温州 325015
乳腺癌是女性人群中最常见的癌症,也是癌症相关死亡的第二位原因[1]。早期诊断和治疗能够延长患者的生存期甚至达到治愈的效果。磁共振成像(magnetic resonance imaging,MRI)是目前检查乳腺癌敏感性最高的影像学检查,但特异性有待提高[2]。美国放射学会(American College of Radiology,ACR)发布的第五版乳腺影像报告与数据系统(BI-RADS)中,依据病灶的形态学特征及动态增强曲线特征将乳腺病变分为7类,其中第4类定义为可疑恶性病变,其恶性概率为2%~95%,但跨度较大,通常需要活检来明确诊断,这使部分患者接受了没有必要的有创活检检查,增加了额外的费用。传统的BI-RADS主观评分,其结果一致性不高,且准确性依赖医师的临床经验[3]。影像组学使用高级数学算法从医学图像中提取和分析肉眼无法识别的定量特征来获得更客观、全面的信息,从而能够提高诊断的准确性[4]。另外,乳腺癌是一种多因素相关的疾病,局限于影像资料可能会限制疾病诊断的准确性。已有研究表明乳腺癌可能与年龄、代谢等临床因素相关[5-7]。多方面综合考虑可能有利于疾病的准确诊断。本研究旨在建立基于动态增强磁共振(dynamic contrast-enhanced magnetic resonance imaging,DCE-MRI)影像组学和临床相关风险因素的列线图,并评价其鉴别乳腺MRI BI-RADS 4类病灶良恶性的效能。
1 资料和方法
1.1 一般资料 收集2017年1月至2019年6月在温州医科大学附属第一医院行术前乳腺MRI检查及血生化检查的女性患者。所有患者均行穿刺或手术,并获得病理结果。纳入标准:①患者在行乳腺MRI检查前未接受穿刺活检或手术,包括淋巴结及对侧乳腺;②患者未经化疗等任何治疗措施;③在MRI检查后1个月内经穿刺活检或手术获得病理结果;④MRI影像诊断报告中被归为BI-RADS 4类(包括4A、4B、4C)。排除标准:①因压脂不充分、伪影等原因导致DCE图像质量较差;②序列扫描不全;③对侧乳腺有乳腺癌病史;④血生化检查与病理检查间隔时间大于14 d。本研究共纳入185例患者,良性病变患者69例,年龄23~78(44±11)岁,良性病灶71个;恶性病变患者116例,年龄22~72(49± 9)岁,恶性病灶118个。本研究获温州医科大学附属第一医院伦理委员会批准。
1.2 临床特征 收集患者各项临床特征,包括年龄、绝经状态及血生化指标。所有血液样本均在空腹条件下采集。血生化指标包括总胆红素、直接胆红素、总蛋白、白蛋白、丙氨酸氨基转移酶、天冬氨酸氨基转移酶、碱性磷酸酶、γ-谷氨酰转移酶、血糖、尿素、肌酐、估算肾小球滤过率、尿酸、总胆固醇、甘油三酯、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇、载脂蛋白A1、载脂蛋白B、肌酸激酶、乳酸脱氢酶、脂蛋白(a)。
1.3 MRI检查方法 所有患者MRI图像均采用GE Signa HDxt 3.0T MR扫描仪和乳腺专用8通道相控阵线圈获得。扫描时患者取俯卧位,两侧乳腺自然悬垂于乳腺线圈内,扫描范围包括两侧乳腺组织及腋窝软组织。嘱咐患者扫描过程中自由呼吸、保持不动,尽可能减少因呼吸、心跳等产生的伪影。乳腺完全扫描序列包括,轴位和矢状位STIR序列、T1WI同反相位序列、轴位DWI序列及轴位DCE。DCE扫描序列具体参数如下:采用VIBRANT序列,TR:5 ms;TE:2 ms;FA:10°;层厚:1.2 mm;FOV: 340 mm×340 mm;矩阵:416×416。DCE-MRI序列共包括6期,于注射对比剂前先行蒙片扫描,再经静脉以2.5 m L/s高压注射器注射造影剂钆喷酸葡胺(Gd-DTPA),剂量为0.1 mmol/kg,注射对比剂后连续扫描5期,每期扫描时间90 s。
1.4 感兴趣区域(region of interest,ROI)分割 由2名经验丰富的高年资放射科医师在不知道病理结果的情况下,参考手术部位,使用ITK-SNAP软件(版本3.4.0,http://www.itksnap.org/)在MRI增强后第一期图像上病灶最大层面,协商达成一致共同手动勾画ROI。对于非肿块病灶,选择单个连续病灶的最大层面进行ROI勾画。ROI略小于病灶边缘,以减少部分容积效应的影响。随后将ROI投影到其他参数图上。
1.5 特征提取与特征选择 通过GE AW4.2后处理工作站计算获得以下3种DCE参数图:信号增强比率(signal enhancement ratio,SER)、最大上升斜率(maximum slope of increase,MSI)、最大下降斜率(maximum slope of decrease,MSD)。所有参数图以DCIOM格式保存,并导入Artificial Intelligence Kit软件[通用电气医疗(中国)有限公司]进行影像组学分析。分别从每个病灶的DCE参数图及其衍生图像[高斯拉普拉斯算子(laplacian of gaussian,LoG)、小波(wavelet)和局部二值模式(local binary p attern,LBP)]中提取特征。每幅图像提取18个一阶特征、24个灰度共生矩阵(gray-level co-occurrence matrix,GLCM)特征、14个灰度相关矩阵(gray level dependence matrix,GLDM)特征、16个灰度游程矩阵(graylevel run-length matrix,GLRLM)特征、16个灰度区域大小矩阵(gray-level size zone matrix,GLSZM)特征和5个邻域灰度差矩阵(neighbourhood gray-tone difference matrix,NGTDM)特征。最终从一个病灶中共提取3 948个影像组学特征。根据7:3的比例,随机将所有病例分成训练集和测试集。所有提取的特征进行z-score标准化后,在训练集中采用最大相关最小冗余(max-relevance and min-redundancy,mRMR)和最小绝对值收缩和选择算子(least absolute shrinkage and selection operator,LASSO)算法组合的方式选择最优特征子集,并计算特征相应的系数。
1.6 统计学处理方法 所有统计分析均使用R语言(版本3.6.4,https://www.r-project.org/)完成。首先,通过对所选影像组学特征按其系数加权求和来计算影像组学评分(rad-score),使用Wilcoxon秩和检验进行影像组学评分的组间比较。接着采用单因素logistic回归分析寻找预测乳腺癌的相关临床因素。选择单因素分析中P<0.05的临床特征,并采用向后逐步logistic回归进行多因素分析,筛选独立临床风险因素,建立临床模型。最后,运用多因素logistic回归方法基于临床风险因素和影像组学评分构建组合模型,绘制列线图。绘制各模 型ROC曲线,并采用Delong检验比较其ROC曲线下面积(AUC)。使用Hosmer-Lemeshow拟合优度检验评价组合模型的校准度。最后通过决策曲线分析评价模型的临床实用性。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料 在本研究的189个病灶中,恶性病灶共118个,其中浸润性导管癌82个(占69.5%),导管内原位癌28个(占23.7%),其他类型恶性病变8个(占6.8%);良性病灶共71个,其中腺病46个(占65%),导管内乳头状瘤14个(占11.4%),乳腺炎5个(占7.0%),其他良性病变6个(占8.5%)。
2.2 列线图构建结果 经过特征筛选后,最终保留了11个特征用于计算影像组学评分,见图1和表1。在训练集和测试集中,恶性病灶的影像组学评分均显著高于良性病灶,差异有统计学意义(P<0.001)。单因素分析显示年龄、总胆红素、直接胆红素、估算肾小球滤过率、总胆固醇、低密度脂蛋白胆固醇、载脂蛋白B、乳酸脱氢酶是乳腺癌发生的影响因素(P<0.05)。多因素分析显示年龄、总胆红素和低密度脂蛋白胆固醇水平增高是乳腺癌的危险因素(见表2)。根据影像组学评分、年龄、总胆红素和低密度脂蛋白胆固醇构建组合模型,绘制列线图,见图2。该组合模型在训练集和测试集中的Hosmer-Lemeshow检验结果显示差异无统计学意义(P=0.59、0.48),表明该组合模型的拟合度较好。
2.3 各模型的诊断效能 临床模型、影像组学模型和组合模型训练集ROC曲线的AUC值分别为0.73、0.86和0.93。组合模型的AUC值显著高于临床模型(P<0.001)和影像组学模型(P=0.014)。在测试集中,临床模型AUC值为0.73,影像组学模型AUC值为0.80,组合模型的AUC值为0.88。组合模型AUC值高于影像组学模型(P=0.037),而与临床模型差异无统计学意义(P=0.057)。见图3。表3罗列了3种模型分别在训练集和测试集中乳腺癌的诊断效能。组合模型相较于临床模型和影像组学模型,准确性、阳性预测值和阴性预测值均有所提高。决策分析显示,组合模型的临床实用性高于临床模型及影像组学模型(见图4)。

表1 筛选出的影像组学特征及其相应系数

图1 LASSO特征降维过程

表2 临床特征的单因素和多因素logistic回归分析
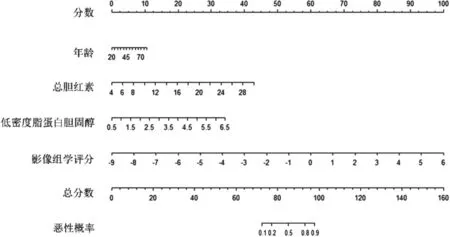
图2 鉴别诊断乳腺MRI BI-RADS 4类病灶良恶性的列线图
3 讨论
在本研究中,我们结合DCE-MRI影像组学和临床特征建立了列线图,并评估了其在乳腺MRI BIRADS4类病灶中的诊断效能。结果表明,基于影像组学和临床相结合的列线图在乳腺MRI BI-RADS 4类病灶的诊断中具有较好的应用价值。
MRI是乳腺的重要影像学检查方法,而DCE-MRI是乳腺MRI检查的重要序列,它通过注射造影剂,提高病灶与正常组织的对比度,获得更准确的病变形态特征,此外还能反映病灶内新生血管等微循环的特征,对乳腺癌有较好的诊断效能[8]。虽然BI-RADS通过对影像征象的主观性解读,能够为乳腺病变临床决策提供帮助,但是其结果一致性不佳限制了临床使用价值。而影像组学能够通过定量分析,做出客观的判断。已有研究证明,从DCE图像中提取的定量影像组学特征能够较好地用于区分乳腺良恶性病变,甚至可以区分乳腺癌的不同分子亚型[9]。 ZHANG等[10]进行了基于多参数MRI的乳腺癌诊断影像组学分析,结果表明,与基于其他序列的影像组学模型相比,基于DCE-MRI的药代动力学参数图的影像组学具有最高的诊断效能(AUC为0.84)。但是由于药代动力学参数的结果受较多的因素影响[11-12],它在常规临床检查中并没有得到广泛的应用。而在本研究中,基于常规乳腺DCE-MRI序列半定量参数的影像组学模型就能获得与定量药代动力学参数相近的诊断效能(在训练和测试集中的AUC分别为0.86和0.80)。该方法容易推广使用。另外,CHEN等[13]从DCE-MRI注射造影剂后第三期图像(约114 s)中提取影像组学特征来鉴别钼靶上仅表现微钙化的BI-RADS 3-5乳腺病变的良恶性。其所构建的DCEMRI影像组学模型灵敏度为75%,特异度为78%,准确性为76.5%,AUC为0.88,但缺乏验证。本研究提取了DCE-MRI半定量参数图的特征用于构建影像模型,相比单期图像特征,更能够反映肿瘤内部微循环特征及其异质性。

图3 各模型的ROC曲线

表3 不同模型对乳腺癌的诊断效能
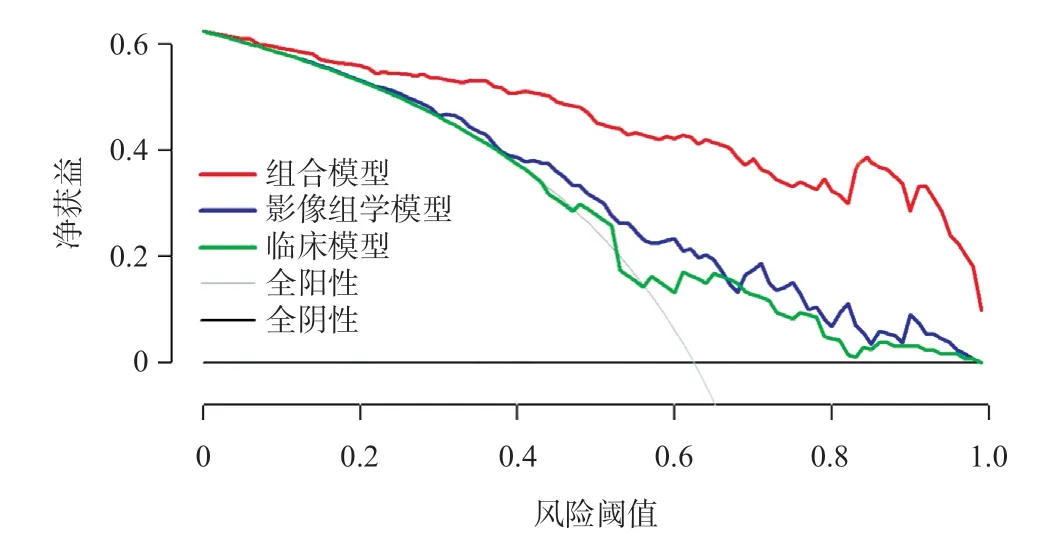
图4 各模型决策曲线
本研究显示年龄、低密度脂蛋白水平和总胆红素水平是预测乳腺癌的独立风险因素。流行病学研究显示年龄是乳腺癌的危险因素。在80岁前,乳腺癌的发生率随着年龄增长而几乎呈线性增长[14]。另有临床研究表明低密度脂蛋白水平与乳腺癌发生风险呈正相关[15-17]。低密度脂蛋白能够影响细胞的增殖和迁移,进而促进疾病的发展[16,18-19]。此 外,本研究显示总胆红素水平也是乳腺癌的独立危险因素之一。然而目前关于胆红素与乳腺癌之间的潜在联系尚未明确,仍需进一步探索。
乳腺癌的发生受多种因素影响。综合患者各方面信息综合考虑,有助于更准确的诊断和个体化治疗。正如我们所设想的,结合临床与影像特征的列线图能进一步提高在乳腺MRI BI-RADS 4类病灶中的诊断效能。另外,乳腺DCE-MRI和血生化检查是常规的术前检查,结果容易获得,本研究于此基础上建立的列线图在具有较高诊断效能的同时而没有给患者额外增加其他检查。
本研究尚有一些不足之处。首先,这是一项来自单中心的回顾性研究,样本量有限,本研究中开发的列线图仍需要大样本多中心研究进一步验证。其次,本研究中采用在病灶最大层面上勾画二维ROI,而不是三维立体勾画病灶,这可能会导致部分抽样偏差。再次,虽然手动勾画ROI的方式在目前各种病灶分割方式中最为精确,但在一定程度上也会受到主观因素的影响。相信随着计算机技术的飞快发展,在不久的将来能够实现病灶准确的自动分割。
综上,基于临床风险因素和乳腺DCE-MRI影像组学的列线图,能够较好地鉴别乳腺MRI BI-RADS 4类病灶的良恶性,为临床提供了一种无创且有效的诊断工具来更好地帮助乳腺病灶术前定性。
