PEG/GO-CuSO4-硫脲复合相变材料的制备及性能
2021-05-19邓聪
邓 聪
(江西省聚合物微纳制造与器件重点实验室,化学生物与材料科学学院,东华理工大学,江西 南昌 330013)
引言
利用太阳能有望获得可再生和清洁能源,可以分别通过光电效应、光化学效应和光热效应将光转换为电能、化学能和热能[1-4]。其中,光热材料的核心是选择合适的光热转换材料,通过选择合适的光热材料,提高光热转换效率,将光能高效地转化为所需的热能。转换后的太阳能通常以显热的形式出现,表现为明显的温度升高。显热的容量相对较低,不适合用于储能。同时,当太阳辐射停止时温度迅速下降,考虑到太阳辐射是断断续续的,因此有必要将光热材料与储热材料结合起来以可持续地利用太阳能。相变材料被证明是太阳能转换为热能后的良好储热材料[5-9]。常见的相变材料,例如石蜡和聚乙二醇(PEG),依靠可逆的固液转化来存储和释放潜热。由于熔化和结晶,相变材料表现出高的热容量,相变材料分子量不高,熔融后易于液体流动。因此,在固液可逆转化过程中防止液体泄漏十分重要[10-16]。一种简便的策略是将相变材料加载到多孔支架中,在该支架中,分子迁移率和泄漏在很大程度上受到表面张力和毛细作用力的限制。源自碳纳米管,石墨烯和其他碳材料的碳气凝胶/泡沫被广泛用于制造几乎不泄漏的相变复合材料[17-25]。此外,碳材料具有显著的光热效应,使相变复合材料能够收集和储存太阳能。实际上,碳气凝胶/泡沫通常通过冷冻干燥,水热合成和高温碳化来制造。
氧化石墨烯(GO)纳米片是通过氧化从天然石墨中衍生出来的,在边缘和基面上具有丰富的含氧基团。它使GO纳米片具有高度亲水性但具有电绝缘性[26]。因此,需要还原GO纳米片以恢复sp2杂交从而增强光热效应。另一方面,相互连接的GO纳米片比孤立的对应物更有利于抑制液体泄漏。迄今为止,在高温下对GO纳米片进行水热处理已普遍用于制备具有互连结构的还原GO纳米片[27]。
在这里,以CuSO4和硫脲的混合溶液对GO进行交联改性,Cu2+交联氧化石墨烯(GO)而且引入硫脲对GO表面的羧基进行酰胺化改性,得到GO-CuSO4-硫脲材料与有机相变组分PEG原位复合,制备了PEG/GO-CuSO4-硫脲复合定形相变材料。GO-CuSO4-硫脲材料具有较好的光热效应和对PEG的强限制,所得相变复合材料极少泄漏且具有较高的光热转换效率。
1 实验部分
1.1 实验原料与实验设备
氧化石墨烯(苏州恒球科技有限公司)、聚乙二醇4000(国药集团化学试剂有限公司)、硫酸铜(国药集团化学试剂有限公司)、硫脲(西陇科学股份有限公司)。
分析天平(奥豪斯仪器有限公司)、Nova Nano SEM 450型场发射扫描电镜。
Thermo Nicolet 380型傅里叶红外光谱仪、D20型恒温加热台、Q2000型差示扫描量热仪、SM206-SOLAR型太阳能功率计、HT-18型红外热成像仪、SHZ-D(Ⅲ)型循环水市式真空泵、手机、手扳式压片机、DHG-9146A型电热恒温鼓风干燥箱、LJ-16型离子溅射仪。
1.2 样品制备
先配置1 mol/L的硫酸铜和1 mol/L硫脲,在三个烧杯中按CuSO4:硫脲=1 mol:4 mol进行配制,先取10 mL、4 mL、2 mL硫脲分别稀释到100 mL、40 mL、20 mL再分别加入1 mol/L硫酸铜2.5 mL、1 mL、0.5 mL后立即加入取10 mg/mL氧化石墨烯(GO)10 mL、4 mL、2 mL放入三个烧杯中,静置24 h后,将所得物质用水洗涤过滤后,按质量比95:5 、98:2、99:1分别加入聚乙二醇(PEG4000),搅拌等聚乙二醇溶解后放于热台烘干,样品干燥后压片处理备用。
1.3 表征及测试
利用扫描电镜对样品表面的微观形貌进行观察分析,利用傅里叶红外分析化学成分及结构,性能测试包括渗漏率测试、相变性能测试和光热转换性能测试。
2 结果与讨论
2.1 材料的微观形貌和结构
对于二价阳离子,由于其氢氧根亲和能力处于[-20,-15]的自由能范围内,与GO表面基团的能力接近,其反应过程比较复杂。Cu2+与GO表面的羟基之间的行为是一个不断变化和调整的平衡过程:一方面,由于对羟基(氢氧根)结合能力的较大差异,靠近GO表面的二价阳离子会趋于直接“夺取”表面的单个羟基基团,形成新的水合离子结构[Cu(OH)]+(H2O)5,体现出高价阳离子对GO的还原性;另一方面,溶液pH环境的变化也在诱导着二价阳离子的第一水合层中的质子转移,在酸碱平衡过程中将Cu2+水解为这种[CuOH]+(H2O)5离子,或者反过来恢复到Cu2+状态。在这样的平衡过程中,同时存在着未发生变化的Cu2+与变化后的[CuOH]+离子与GO表面基团的交联情况,Cu2+本身与氢氧根结合的能力与双羟基一致,因此能形成稳定的配位交联,而与环氧基的交联则会导致最多1个环氧基团发生开环反应。在Cu2+离子络合氢氧根(或水解)形成[CuOH]+后,其结合额外氢氧根的能力有所减弱,遇到单个羟基时就不会再发生络合反应,此时,[CuOH]+同样能与双羟基形成稳定交联,只是其极化作用己不足以导致环氧的开环[135]。图2.1b中GO纳米片可以通过边缘处的羟基和Cu2+形成稳定的化合物,而混合溶液中的硫脲小分子可以与羧基反应形成酰胺基。图2.1c中的FT-IR光谱表明,GO纳米片在1726 cm-1附近的羧基拉伸振动在GO-CuSO4-硫脲中减弱了,而后面的酰胺基在1689 cm-1和1351 cm-1附近的峰加强了。Cu2+和GO的络合作用形成稳定物质并且导致一个环氧基团的开环反应振动,3000 cm-1-3500 cm-1的波数区域的吸光度变化主要是Cu2+与羟基的络合作用使羟基伸缩振动。硫脲还含有N-H键,这使得GO-CuSO4-硫脲在2923 cm-1处的吸收峰明显加强,其次,由于GO和硫脲的静电作用使1738 cm-1处的-COOH峰强度减少,GO-CuSO4-硫脲在1585 cm-1处出现了特征峰,这说明Cu2+与GO发生了环氧开环反应。且由图2.1b可知,反应后的物质还是呈淡黄色,说明该混合液体还原性较弱。

图2.1 (a)GO原液图片(b)用Cu2+和硫脲混合液处理后的GO(c)FT-IR光谱
靠近GO表面的二价阳离子会趋于直接“夺取”表面的单个羟基基团,形成新的水合离子结构[Cu(OH)]+(H2O)5,由于Cu2+的络合作用使GO纳米片之间相互连接,再加上硫脲的作用,GO-CuSO4-硫脲簇表现为层状堆叠(图2.2c),结合的Cu2+分布在GO纳米片的基面上,并由Cu元素的EDS映射支持(图2.2c中的插图)。基于C、O、N、S和Cu元素的总质量,N元素的质量比约为5.56%,Cu元素的质量约占8.45%。相反,没有用混合溶液处理的GO纳米片在通过冷冻干燥除水后表现为单独的弯曲层(图2.2b)。GO-CuSO4-硫脲簇和GO纳米片之间在微观尺度上的形态学差异与图中的视觉观察结果一致。
图2.2a比较了基于PEG的复合材料的形状稳定性和液体渗漏与填充剂类型和填充量的关系。纯的PEG在90 ℃时变为流体,并因其低熔点和极低的粘度而完全扩散。纯PEG的漏液率为100%,不适合实际应用。当加入GO-CuSO4-硫脲或GO纳米片时,可以缓解这一难题。形状稳定性随着填充物载荷的增加而增强,同时减少了液体泄漏。另一方面,就相同填料填充量下的液体泄漏而言,GO-CuSO4-硫脲优于GO纳米片。而且,在GO-CuSO4-硫脲的5wt%负载下,液体泄漏几乎被完全抑制(图2.2a)。它应与GO-CuSO4-硫脲中的层状堆积相关,其中PEG的分子迁移受到很大限制。限制作用类似于在其他多孔材料(如碳气凝胶/泡沫)中观察到的限制作用。
实际上,GO-CuSO4-硫脲的负载量为5wt%时,GO-CuSO4-硫脲诱导的多层结构可以对熔融的PEG链施加显着的表面张力和毛细作用力,从而有效地防止液体泄漏。相反,GO纳米片很好地分散在PEG基质中,没有多层结构观察到的复合材料(图2.2d)。因此,其导致较弱的限制作用以及更严重的液体泄漏。

图2.2 (a)相变复合材料在30℃、60℃、90℃下保持30分钟后与所述填充物各掺量下的渗透情况,(b)相变复合材料在90℃下保持30分钟后与所述填充物各掺量下的渗透百分率,(c)GO扫描电镜图像,(d)GO-CuSO4-硫脲的SEM图像,(e)GO纳米片负载5%的相变复合材料的SEM图像,(f):GO-CuSO4-硫脲负载5%的相变复合材料的SEM图像
2.2 复合相变材料的热性能
如图2.3的DSC曲线所示,PEG在加热和冷却后分别经历约55 ℃的可逆熔融和约32 ℃的结晶。同时,关于熔融和结晶的相变焓分别为162.6 J/g和161.4 J/g(表2.1)。填料的负载,无论是GO-CuSO4-硫脲还是GO纳米片,都会降低熔化和结晶焓。在所采用的温度范围内,填料不能发生相变是有意义的。当GO纳米片负载为5wt%时,熔融和结晶焓分别为150.3 J/g和146.7 J/g。它们约为纯PEG的92%和90%,略低于期望值(95%)。结果表明,由于分子限制,PEG的结晶在一定程度上受到GO纳米片的阻碍。而当GO-CuSO4-硫脲负载为5wt%的情况下,熔融和结晶焓分别为150.6 J/g和148.7 J/g。它们分别约为纯PEG的92.6%和92.1%,略低于预期值(95%)。这表明由于分子限制,PEG的结晶在一定程度上受到GO-CuSO4-硫脲的阻碍。相应地,由于结晶延迟,熔融焓略有降低。即便如此,其焓值仍高于其他基于PEG的形状稳定的相变复合材料[28-30,31-33]。

表2.1 分别是纯PEG和有GO-CuSO4-硫脲或GO纳米片负载的复合材料融化焓和结晶焓
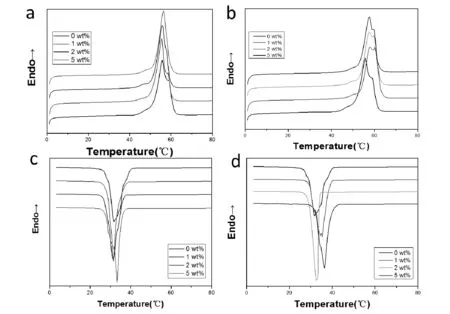
图2.3 (a)纯PEG和负载各比例GO的复合相变材料的融化曲线,(b)纯PEG和负载各比例GO-CuSO4-硫脲的复合相变材料的融化曲线,(c)纯PEG和负载各比例GO的复合相变材料的结晶曲线,(d)纯PEG和负载各比例GO-CuSO4-硫脲的复合相变材料的结晶曲线
另一方面,熔化和结晶的温度范围几乎不受填料类型和填充量的影响。而且,在熔融和结晶方面,GO-CuSO4-硫脲和GO纳米片之间也没有太大差异。这意味着PEG的固液转化几乎与填料类型无关,这不同于上述液体泄漏。简而言之,高相变焓与极少的液体泄漏相结合,使相变复合材料的GO-CuSO4-硫脲负载量为5wt%,可用于存储和释放热能。
2.3 热能存储性能研究
图2.4a分别显示了纯PEG以及具有GO纳米片和GO-CuSO4-硫脲复合材料的温度曲线,同时打开和关闭了光。对于三个样品,由于显热的增加,在光照下温度在初始阶段迅速升高。之后,温度曲线在40 ℃以上发生偏转,温度升高变慢。它对应于PEG的熔化,并且潜热通过固液转化来存储。在60 ℃左右完全熔化后,温度再次急剧上升,由于光热转换和向周围环境散热之间的平衡,温度几乎达到饱和。当灯熄灭时,温度下降。由于PEG的结晶,潜热的释放开始于40 ℃左右。温度曲线表明,光的开关可以介导热能的存储和释放,因为光转换的热量可以触发PEG的熔化。

图2.4 (a)纯PEG和GO纳米片和GO-CuSO4-硫脲负载量分别为5wt%的复合材料的温度分布,(b)光热转换效率。光照射密度为1 kW/m2
另一方面,PEG在与GO-CuSO4-硫脲的复合材料中的熔化速度相对较快,这是从温度分布中的偏转区域判断的。具有GO-CuSO4-硫脲的复合材料的熔融持续时间仅为55 s,远短于纯PEG(76 s)和具有GO纳米片(99 s)的复合材料。从[117,119-121,131,134]可以推导出光热转换效率公式(1)。
(1)
m样品质量、ΔH熔化焓、L辐照密度、A样品面积和Δt持续时间。
如图2.4b所示,与GO-CuSO4-硫脲的复合材料略高于GO的光热转换效率,光热效率只有67.2%。相反,纯PEG和与GO纳米片的复合材料分别仅达到18.9%和63.2%。由于光热转换相对高于GO,PEG在复合材料中与GO-CuSO4-硫脲的熔化相对快于GO,导致了显著的热积累。同时,GO/PEI团簇复合材料的饱和温度约为91 ℃,也高于纯PEG(~65℃)和GO纳米片(~78℃)的复合材料。由GO-CuSO4-硫脲诱导的优光热效应使相变复合材料同时收获太阳能和储存热能,进一步考虑了高的相变焓和良好的形状稳定性。
3 结论
以CuSO4和硫脲的混合溶液对GO进行交联改性,Cu2+交联氧化石墨烯(GO)而且引入硫脲对GO表面的羧基进行酰胺化改性,得到GO-CuSO4-硫脲材料与有机相变组分PEG原位复合,制备了PEG/GO-CuSO4-硫脲复合定形相变材料。将GO-CuSO4-硫脲材料和PEG在常温水溶剂中混合,PEG 被填充在聚合物 GO-CuSO4-硫脲材料层状结构中。研究GO-CuSO4-硫脲材料在复合相变中的含量对复合相变性能的影响。通过一系列表征得出以下结论:
(1)SEM 测试表明,PEG 能够均匀填充在聚合物GO-CuSO4-硫脲材料多层网络结构中。且PEG与GO-CuSO4-硫脲材料的相容性较好,没有发现相分离的现象。
(2)通过FT-IR和DSC分析表明,靠近GO表面的二价阳离子会趋于直接“夺取”表面的单个羟基基团,形成新的水合离子结构[Cu(OH)]+(H2O)5,体现出高价阳离子对GO的还原性;另一方面,溶液p(环境的变化也在诱导着二价阳离子的第一水合层中的质子转移,在酸碱平衡过程中将Cu2+水解为这种[CuOH]+(H2O)5离子,或者反过来恢复到Cu2+状态。在这样的平衡过程中,同时存在着未发生变化的Cu2+与变化后的[CuOH]+离子与GO表面基团的交联情况,Cu2+本身和氢氧根结合的能力与双羟基一致,因此能形成稳定的配位交联,而与环氧基的交联则会导致最多1个环氧基团发生开环反应。GO-CuSO4-硫脲材料的存在对PEG的结晶能力不产生影响,PEG和GO-CuSO4-硫脲材料之间未发生化学反应,保证PEG的相变潜热储能特性。
(3)通过渗漏率测试表明,由于GO-CuSO4-硫脲材料的多层结构的存在,对PEG具有优异的防泄漏作用,其渗漏率的改变随PEG含量的改变而变化。在90 ℃下测试0.5 h 后渗漏率最大仅为1.24%。
(4)通过光热性能测试表明,GO-CuSO4-硫脲的负载量为5wt%,液体泄漏少,光热转换效率为67.2%,优于GO纳米片。PEG/GO-CuSO4-硫脲复合相变材料是一种较好的储热材料。
