锂离子电池高容量合金基含锂负极材料的研究进展
2021-05-17毛尔洋孙永明
毛尔洋,王 莉,孙永明
(1.华中科技大学武汉光电国家研究中心,武汉430074;2.清华大学核能与新能源技术研究院,北京100084)
21世纪以来,科技日新月异,经济飞速发展,人类文明也迎来了飞跃发展,随之而来的世界能源危机不断加剧,地球环境问题也愈发凸显,人们亟待发展以太阳能、风能、潮汐能等间歇性发电的新型可再生清洁能源,而这些能源的有效利用首先必须高效存储;另一方面,消费电子领域及电动交通工具,如电动汽车、无人机等皆需要先进的储能器件. 因此,人们迫切需要开发具有更高能量密度、更高功率密度、更长寿命、更低成本、更高安全性的可充放储能技术[1~4].
在过去200年里电化学储能技术取得了长足发展,从伏打电池、铅酸电池、镍镉电池、镍氢电池,再到锂离子电池,能量密度也显著提高. 1991年首次商业化的锂离子电池因有能量密度高、能量效率高、循环寿命长、无记忆效应、快速放电、自放电率低、工作温度范围宽和安全可靠等显著优点,已成为当今各国科学家研究的重要前沿方向[5~7]. 然而,当前基于嵌入反应机制、由石墨负极和锂过渡金属氧化物正极组成的传统锂离子电池的能量密度仅为200~260 W·h·kg-1,已经接近理论极限,且近20多年来年均增长不到5%,已远不能满足日益增长的储能要求[8~12]. 因此,亟需发展下一代可充放锂电池技术,通过探索新型的反应机制与电极材料,进一步提高电池能量密度、倍率性能、循环寿命和安全性[13~19].
在现有的锂离子电池中,由过渡金属氧化物或磷酸盐作为正极为电池循环提供锂离子源,其有限的比容量(通常<200 mA·h·g-1)严重限制了全电池的能量密度. 而不含锂的正极材料通常比上述含锂正极材料能提供更高的理论锂离子比容量,如S(1675 mA·h·g-1)[20~23],V2O5(441 mA·h·g-1)[24~26]和FeF3(712 mA·h·g-1)[27~30]等. 因此,若使用高容量不含锂正极材料与高容量含锂负极材料匹配,则有望实现更高能量密度的锂离子电池.
金属锂负极因其具备最高的理论容量(3860 mA·h·g-1,2061 mA·h·cm-3),最低的氢标准电势(-3.04 V)与最低的密度(0.59 g/cm3),是最终的含锂负极,被认为是电化学储能技术中的“圣杯”,而近年来人们开展了大量的相关研究并取得了重要进展[31~35]. 早在1970年,Exxon 公司的Whittingham等率先开展了锂二次电池的研究. 在之后的80年代,Moli Energy公司致力于推动锂金属电池的商业化.但是金属锂负极充放电循环过程中不可控的锂枝晶的形成及其高的化学反应活性频繁造成短路、热失控等严重的安全事故,导致当时所有电池被召回,锂金属电池商业化宣告失败[5]. 此外,金属锂负极库仑效率(Coulombic efficiency,CE)低(在商用碳酸盐电解液中通常<95%)和固态电解质界面(Solid electrolyte interface,SEI)膜不稳定等一系列问题,使其长期停留在研发阶段[36~38].
20世纪70年代,Dey[39]证实了在室温下锂金属可以与其它金属在有机电解液中发生电化学合金反应. 在过去几十年中,人们开展了大量的关于锂与其它金属、半金属以及其化合物的合金化反应的研究,正式开启了一类基于合金反应机制的含锂负极材料LixMy(M为能够和锂发生合金化反应的元素)的研究. 早期的研究,以Huggins 等[40~48]为代表,围绕Li-Si[40~48]与Li-Al[49~53]两大体系,以及其它类似的二元合金(Li-Sn,Li-Sb 和Li-Ge 等)、Li-Si-M(M 为活性或惰性金属或非金属,如Cr,Sn)三元混合导电基体合金等[54~59],采用熔盐、无机及有机等多种电解质,在高温、较高温乃至室温等条件下,对锂合金的热力学、相图和近平衡条件下电化学性质等基本原理进行大量的研究. 如在与金属硫化物正极(如FeS2)匹配的高温熔融盐锂热电池中,Lai[56],Seefurth等[57~59],Wen等[40]和Huggins等[41]利用金属锂和硅在高温(775 K及以上)下定比反应制备了多种Li-Si合金负极(包括Li22Si5,Li15Si4,Li21Si8和Li2Si),并在650~750 K高温范围内实现了电流密度在50~400 mA/cm2范围内的可逆充放电,负极的利用率在60%~90%之间. 由于Li-Si 合金熔点比金属锂高,且化学活性比Li 低,可避免高温下锂金属负极与隔膜材料、电极材料等发生反应的问题,从而显著提高锂基电池的安全性和电化学性能. 然而当时的研究随基于石墨负极更为安全的嵌入型反应机制的锂离子电池成功商业化逐渐不再被关注.
近年来,由于人们对下一代高比能锂离子电池的迫切需求,基于合金反应机制的含锂负极材料LixMy(M为能够和锂发生合金化反应的元素)作为一类极具潜力的锂离子电池负极材料,又重新受到人们的注意. 其研究从前期的高温体系,重点转向了室温条件下相关研究,并与多种高容量正极材料相匹配,如过渡金属氧化物或氟化物正极、S正极和O2正极等,开发了不同的电池体系且取得了一定进展[60~72]. 该类高容量合金基含锂负极材料LixMy具备多种共性优势:(1)允许较多的锂离子发生可逆电化学反应,具有数倍于石墨(372 mA·h·g-1,基于石墨的质量计算)和含锂过渡金属氧化物[如钛酸锂(Li4Ti5O12)、钴酸锂(LiCoO2)、锰酸锂(LiMn2O4)、磷酸铁锂(LiFePO4)、三元(LiNi1-x-yCoxMnyO2)等]的储锂比容量;(2)其嵌锂电位低且平稳,锂化电位适当而合理,略高于石墨(约0.1 V)及锂析出电位,在保证较高的全电池输出电压前提下,能够在过充或快充中避免金属锂析出或枝晶形成,展现出其安全性高的特性和可快充的前景.(3)能为全电池提供活性锂源,可与不含锂的高容量正极材料(如S,O2,FeF3,V2O5和MnO2等)相匹配,构建新型高比能电池体系(图1).

Fig.1 Novel battery mechanism coupling highcapacity Li-containing anode and Li-free cathode based on alloy-dealloy reaction,illustrating the advantages of utilizing high-capacity Li-containing anodes
以LixMy的最高锂化态为例,图2显示了基于合金反应机制的含锂负极材料的工作电位和理论比容量与其它传统负极、正极材料的对比. 如Li4.4Si 的平均锂化工作电位约为0.3 V(vs.Li/Li+),理论质量比容量高达2011 mA·h·g-1(基于Li4.4Si计算,若基于Si计算则为4200 mA·h·g-1),是所有含锂负极中最高的;而Li4.4Sn的上述2个参数则分别约为0.4 V(vs.Li/Li+),790 mA·h·g-1(基于Sn为994 mA·h·g-1);Li3P的上述参数约为0.7 V(vs.Li/Li+),1552 mA·h·g-1(基于P为2596 mA·h·g-1);Li2.25Al的上述参数约为0.2 V(vs.Li/Li+),1416 mA·h·g-1(基于Al 为2235 mA·h·g-1),Li4.4Ge 的上述参数约为0.5 V(vs.Li/Li+),1155 mA·h·g-1(基于Ge 为1640 mA·h·g-1)等,这些负极的理论比容量均远高于锂化石墨(339 mA·h·g-1,基于LiC6质量计算)[73,74].
此外,不同的LixMy基的含锂负极除了具有高容量、合理的工作电位等以上共性优势外,它们各自具备独特的优缺点,如LixSi基负极普遍具有较高的理论质量比容量[68,70];LixSn基负极具有高的体积比容量(如Li4.4Sn 基于Sn 计算为1990 mA·h·cm-3)和优异的电子/离子导电性[71];Li3P 基负极的约0.7 V(vs.Li/Li+)的锂化电位能够避免在快速充电过程中或低温环境下电池产生较大的过电位导致负极表面的实际电位到达0 V(vs.Li/Li+),进而引起金属锂枝晶的析出问题,因而可作为一种理想的快充负极材料[72,75];LixAl基材料工作电位较低(约0.2 Vvs.Li/Li+),接近于石墨,能够使全电池具有高的能量密度,且拥有优异的电子导电性和相对较小的体积效应(约为100%)[69,76];同时,Al与Si具有丰富的储量和低廉的价格,以及成熟的工业研究体系[77,78].
因此,高容量合金基含锂负极材料LixMy作为一类具备独特优势和巨大潜力的新型负极材料,有望成为下一代高比能、高安全性、可快充锂离子电池的负极材料的选择.
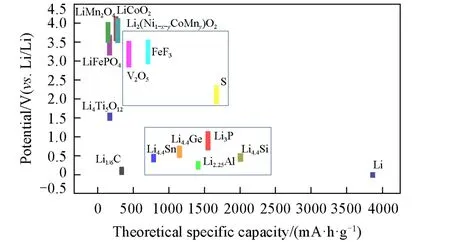
Fig.2 Theoretical specific capacity and potential(vs. Li/Li+) of various high-capacity Li-containing anodes and Li-free cathodes,in contrast to the conventional intercalation-type electrodes
1 高容量合金基含锂负极材料存在的问题和挑战
负极是锂离子电池的核心部件之一,性能优异的负极材料的设计与制备须满足一系列共性[79,80],包括:(1)嵌锂电位低且平稳,以保证较高的全电池输出电压;(2)允许较多的锂离子可逆脱嵌,比容量较高;(3)在充放电过程中材料及电极结构稳定,具有较长的循环寿命;能够与电解液形成稳定的固体电解质界面膜(SEI),获得较高的库仑效率;(4)较高的电子电导率和离子电导率,以实现较小的极化和良好的倍率性能;(5)环境稳定性和化学稳定性好,安全性高,能够在环境中稳定存放和进行安全运输或存放;(6)与现有电极和电池制备工艺相匹配,能够直接使用现有工艺进行电池制备;(7)材料合成工艺简单,原材料资源丰富,材料制备过程不会对环境造成严重污染,易于产业化等.
然而,有关高容量合金基含锂负极材料LixMy的研究在尚处于起步尚未成熟阶段,尤其是其合金基多电子脱嵌机理、含锂态的高化学活泼性以及合成困难等本征特性,导致其在诸多方面尚不能满足实用性负极的系列共性要求. 因此,制备性能优异的高容量含锂负极面临着多种挑战(见图3),主要表现在:
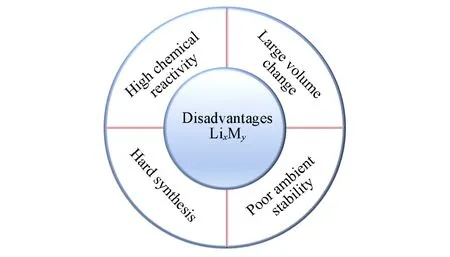
Fig.3 Challenges faced by scientific research and practical fabrication on high-capacity Li-containing anode materials
材料合成和电极制备. 现有高容量含锂合金负极材料的合成方法(热力学、动力学层面),主要有高温热熔合金方法[65,68,70,72,81~85]、高能机械球磨合金方法[67,78,86~89]、电化学锂化[60~63,66,90,91]等方法. 此类方法合成条件往往比较苛刻,伴随着高温、高能、高压,有一定的危险性或复杂性,因而难以规模化.因此,亟待开发安全、高效的合金合成方法,同时探索更加温和、安全的工艺. 此外,在电极制备层面,高容量含锂负极材料的高化学活泼性导致其易与常规使用的极性溶剂[如1-甲基2-吡咯烷酮(NMP)]或环境中的水等发生反应,引起材料失活或电极制作失败,因而不能与现有电池电极制备工艺相兼容. 因此,需要开展独特且适合的新型电极制备工艺,如干法电极制备工艺,以避免传统工艺中匀浆、涂布、干燥等流程中极性溶剂的使用.
多体系全电池匹配兼容与功能性应用领域的拓展. 高容量合金基含锂负极可以应用在多个全电池体系中,如常规锂离子电池[67,68,72,92]、锂离子-硫电池[61,69,90,93]、锂离子-空气电池[63,66,94~96]等. 不同的电池体系具备特殊性问题,如硫电池的穿梭效应、空气电池开放体系的电极腐蚀性问题等,都需要在负极设计时综合考虑和解决. 此外,从长期研究来看,可挖掘高容量含锂负极的独特性质,研制具备如高倍率[18]、高低温[97]、高电压等特殊功能的电池,并将其用于多种领域.
电化学性能的调控优化. 目前报道的基于高容量合金基含锂负极的电池电化学性能表现普遍较差,由于其合金基反应机制与高化学活性,在充放电循环中面临多种挑战,如:(1)材料体积变化大.与石墨(约为10%)相比,高容量含锂电极材料,如Li4.4Si,Li4.4Sn,Li3P和Li2.25Al的理论体积变化分别达到约420%,260%,300%和100%[32]. 一方面将导致材料表面SEI 不稳定,在充放电过程中SEI 不断发生破裂和重新生成,继而引起循环过程中库仑效率较低,电解液和活性锂不断消耗,最终使电池的循环寿命较短;另一方面,材料体积变化引起电极结构重整、厚度变化,造成极片粉化或从集流体脱落,因材料的电接触失活使电池性能劣变.(2)电子/离子导电率低. 高容量含锂负极在其锂化状态(如Li4.4Si,Li4.4Sn,Li3P和Li2.25Al)和去锂化状态(如Si,Sn,P和Al)之间进行转化,这些电极材料在不同的锂化状态具有不同的电子和离子导电性. 如Si,P为半导体和绝缘体,具有较差的电子电导性;而锂化后,电子电导增加. 因此,在实际应用中,需综合地从抑制体积变化、提升电子/离子导电性、电极表面改性、SEI 膜的形成和调制、电解液体系的改进及研发、提高CE等多角度综合考虑和协同设计.
规模生产和实际应用. 从实验室探索到实际生产,高容量含锂负极的高化学活泼性导致其面临环境稳定性差等严峻挑战,尤其是对存储和使用环境要求苛刻,常常需要惰性气体氛围或极低露点环境. 其与空气中的水、氧发生反应,不但会引起材料失去活性,剧烈的反应还可能引发严重的安全隐患. 通过表面保护等策略提高其环境和化学稳定性是解决其存储及实际应用难题的重要技术途径和核心关键. 此外,探究如何规模化生产、降低成本等也是研究的必由之路.
2 高容量合金基含锂负极材料的合成与制备方法
近年来,高容量合金基含锂负极材料的合成方法使用较多的是传统的高温热熔合成[65,68,70,72,81~85]与高能机械球磨合成[67,78,86~89]. 此外,随着预锂化的深入研究并引申作为负极应用在电池中,一类通过电化学接触短路或电化学锂化方法制备含锂负极的报道也逐渐增多[60~63,66,69,90,91,98]. 同时也出现一些新型的辊压机械合金[71]、化学溶剂还原合金[93]、等离子烧结合金[99]、化学合成[64]等方法以及多种方法的综合利用. 此外,该类材料高的化学活性和差的环境稳定性使电极制备面临挑战. 目前,电极制备方法主要有针对粉末材料的湿法涂覆制备方法[68],以及干法压片制备方法[48,86]、针对箔材电极的机械辊压制备法[71]等. 当前,亟待依据各种合金基高容量含锂负极的特性,开发更多的新型材料合成与电极制备方法[100],并探索更加温和、安全、低成本的工艺等.
2.1 高温热熔合金法
锂金属熔点(180 ℃)低,且化学性质活泼,沿用高温热熔合金的传统合金制备方法,通过将锂金属直接与Si,Sn,P等材料或与其化合物SiO2,SiO,其复合物P/C等混合、熔炼、退火处理,即得到合金基含锂负极材料. 其主要优点在于设备和工艺简单,早期的研究多是通过此方法制备[101]. 近年来,代表性研究主要有2014年美国斯坦福大学崔屹课题组[65]通过将硅纳米颗粒(粒径约50 nm)与熔融态金属锂反应[图4(A)],制备硅化锂合金纳米颗粒(LixSi NPs). 在材料制备过程中,由于少量氧的存在生成Li2O包覆的核壳结构(LixSi-Li2O NPs),并实现了首次高的脱锂比容量(1310 mA·h·g-1),该界面层能在一定程度上提高材料在环境中的稳定性,可在干燥空气(露点-50 ℃,相对湿度<0.1%)暴露1 d后容量保持率为91%,5 d后为70%. 2016年该课题组通过使用更低成本的SiO或SiO2作为起始材料,与熔融的锂金属合金制备了环境稳定性更高且对湿度兼容更好的LixSi/Li2O复合负极材料[81],由于将活性LixSi纳米畴均匀分散嵌入在稳定的Li2O基体中,该独特结构使得所制备的复合含锂负极材料可暴露于相对湿度约为40%的潮湿环境中6 h,容量仍然保持1240 mA·h·g-1(容量保持率约为58%).

Fig.4 Various synthesis methods to prepare LixMy anodes materials
采用“先包覆后热熔合金”策略是一种拓展的高温热熔合成方法. 如南京大学鲁振达课题组报道的两步法制备LixSi-Li2O/TiyOz负极[70]、LixSn@PPY 负极[84]和LixSi/Cu 复合材料含锂负极[85]等. 其中LixSi-Li2O/TiyOz负极制备通过先将Si NPs包覆TiO2,然后与熔融Li 反应[图4(B)],其坚固的锂化TiO2致密保护层使其可暴露在干燥空气(相对湿度10%)中30 d后保留约87%的容量;LixSn@PPY负极则通过先对Sn负极进行聚吡咯(PPY)包覆,然后热熔锂化进行制备,其可在干燥空气(相对湿度10%)中5 d后保留约75%的容量;LixSi/Cu负极则使用低成本的微米硅作为原材料,首先通过工业常用的无电沉积方法进行镀铜包覆,然后与熔融的锂金属进行反应;均匀分布在LixSi/Cu复合材料中的Cu增强了LixSi的有效电接触,保持了其高的电化学活性,同时减少Li-Si合金体积变化引起的应力,从而实现充放电过程中电极保持结构完整,最终使所获得的材料表现出较好的电化学性能.
此外,可以通过氢化锂(LiH)等锂的化合物代替锂金属作为前驱体,与Si,P 等高温下发生反应,合成LixM材料. 如浙江大学刘永峰课题组[64]利用该反应[12LiH(s)+7Si(s)→Li12Si7(s)+6H2(g)]合成出的Li12Si7材料,用作锂离子电池负极材料时循环稳定性和倍率性能优于纯Si负极材料.
2.2 高能机械球磨合金法
高能机械球磨法利用球磨机的高速机械转动使球珠对原材料及原材料之间进行强烈的撞击、研磨和搅拌来制备合金材料. 尤其是常规方法难以获得的高熔点合金材料,并能够在一定程度上控制和优化合金颗粒的大小,如用该方法制备纳米材料;但同时也存在引入氮气、氧气等杂质的问题[100]. 该方法可用在多种合金基高容量含锂负极材料的制备中,但需要避免材料被氧化,引起爆炸或电化学性能失效等问题.
代表性研究主要有日本甲南大学Machida 等[86,88]采用机械球磨法制备亚稳态的Li4.4Si 二元合金(2001年)和Li4.4GexSi1-x(x=0~1.0,2004年)三元固溶体合金负极,并应用于全固态锂电池中;2014年美国科罗拉多矿业大学杨永安课题组[78,87]通过高能机械球磨方法使用己烷作为润滑剂合成了4种纯相的Li-Si合金(Li4.4Si,Li3.75Si,Li3.25Si和Li2.33Si),系统地研究了它们的化学稳定性和热稳定性,同时对碳包覆的Li-Si合金材料的电化学性能进行了研究,所制备的材料中Li4.4Si表现出最优的比容量和循环性;该课题组进一步于2017年使用球磨辅助表面氮化的工艺,在Li4.4Si的表面生成稳定的导电氮化层获得了Li4.4Si@LixNySiz负极[67],提升了电化学性能[图4(C)]. 此外,2017年南京大学周豪慎课题组[89]在氩气中采用高能机械球磨法合成Li21Si5负极,与载铂的多壁碳纳米管(Pt-MCNT)氧气正极匹配,评估了其在锂空电池中的电化学性能.
2.3 电化学锂化方法
近年来,以锂金属为对电极组装电池,通过控制电化学反应对工作电极进行锂化的方法在科学研究中被广泛使用. 如通过组装Li||Si电池,通过电化学反应可以使Si负极转变为Li-Si合金. 研究表明,电化学锂化方法合成的Li-Si 合金与直接通过化学合成的Li-Si 合金表现出不同的电化学储锂性能[78].电化学锂化方法需要预先将常规匀浆、涂布制备好的无锂负极(如Si/C,Sn和Al电极等)与锂对电极组装半电池,进行一定的充放电循环得到锂化后稳定的合金负极(LixSi/C等),再拆卸后在保护性气氛中用溶剂清洗和后续干燥处理,获得含锂合金负极,将其重新与正极(如S 和O2等)组装新的全电池[60~63,66,69,90,91]. 此方法因工艺较复杂而繁琐可以作为基础探索研究,但其规模化使用受限,大规模使用需要对其进行工艺改进.
代表性研究如2011 年斯坦福大学崔屹课题组[61]对硅纳米线(SiNW)进行电化学锂化制备LixSi 负极,并成功与硫/介孔碳复合正极匹配[图4(D)];2011年以色列巴伊兰大学Elazari和Aurbach等[62]将磁控溅射形成的无定形硅薄膜电极在恒电流下锂化至20 mV制备Li-Si合金负极,并与硫/碳正极匹配组装全电池等. 此外,通过将Si电极等与锂片接触,添加电解液进行短路,自发放电嵌锂合金的方法也是此类变体之一. 如2011 年Hassoun 和Scrosati 等[98]将Si/C 复合材料(硅含量70%)在外在压力(约100 kPa)和电解液[溶有1.2 mol/L 六氟磷酸锂(LiPF6)的碳酸乙烯酯/碳酸甲乙酯(EC-EMC)]存在条件下,与锂箔直接接触进行12 h的自发锂化反应,制备了LixSi/C复合含锂负极. 除了使用常规锂片作为对电极进行锂化沉积之外,2018年上海交通大学杨军课题组[91]报道了构筑Li3N||Si电池,利用Li3N对电极使Si负极进行电化学锂化制备LixSi负极的研究[图4(E)].
2.4 辊压机械合金法
基于锂的高活泼性,含锂负极的制备也可将原材料与锂在接触后通过施压/辊压等方式进行机械合金化反应,此外也可以辅助进行加热以加速其反应或控制晶相结构(低于熔点). 如2003 年Zaghib等[102]通过将锂箔与多孔铝金属(孔隙率50%)接触压制在一起,并于60~80 ℃下热处理1 h,制备了一种多孔膨胀Li-Al合金负极,由于其多孔结构和高的孔隙率,能够缓冲循环过程中的体积变化,从而具有较高的结构稳定性. 此外,2019年同济大学黄云辉课题组和麻省理工学院李巨课题组合作,报道了一种卷对卷(Roll-To-Roll)接触辊压机械合金方法[图4(F)][71],制备了LixSn,LixAl和LixSi/C等多种含锂负极箔材,并随后通过调控其合金的晶粒大小、形状、取向等金相组织,制备了改进的含锂负极材料Lix(3Ag0.5Cu96.5Sn)[92]. 该研究同时指出,不同于纯Sn 箔的无锂电极在循环中特定电压下催化电解液分解产生气泡和莱顿弗罗斯特气体膜现象引起库仑效率低、循环差等问题,该方法制备的新型LixSn含锂负极由于锂化后较低的初始负极电位,抑制了产气并促进了钝化的SEI形成,有效提升了初始库仑效率(从纯Sn 箔负极的20%提高至94%);在与LiFePO4,LiNi0.8Co0.1Mn0.1O2(NCM811)正极匹配时也展现出稳定的电化学循环性能,同时具备良好的空气稳定性.
2.5 化学溶剂还原合金法
化学还原法是传统制备合金超细粉体的有效和常用的方法之一[100]. 通过在特定溶剂中,选择合适的络合剂、还原剂,可以实现还原电位比较接近的金属元素的共还原,从而制得合金材料. 该方法简单易行,且对设备的要求较低,便于工业化生产. 由于锂的还原电位很低,目前在含锂负极材料的制备中研究极少. 2020年武汉大学王功伟课题组[93]报道了一种化学还原的方法制备Li-Al合金负极,通过将商用铝箔在特定溶液中浸泡,制备出Li-Al合金[图4(G)]. 该溶液由锂-二甲基芴(Li-DiMF)溶于醚类溶剂[如二甲氧乙烷(DME)、四氢呋喃(THF)]组成,具有极低的还原电势(0.22 Vvs. Li+/Li). 该化学还原方法制备的LiAl合金负极在溶液中预先形成了人造SEI,因而具有一定的多硫化物耐性和空气稳定性,与硫/氮掺杂碳正极(S-NC)匹配全电池,其电化学性能优于使用电化学锂化方法得到的负极组装而成的全电池.
2.6 其它合成方法及多种方法的综合利用
由于不同制备方法具备各自的优缺点,研究者常常结合多种方法,综合制备高容量合金基含锂负极材料,或对其进行复合、优化,以提高整体电化学性能. 如2015年Iwamura等[103]先将金属锂片和硅粉混合在750 ℃下氩气中进行热熔合金反应,冷凝后再次通过高能机械球磨方法制备更细的晶相Li21Si5粉末;其超高反应活泼性导致与常规黏结剂如聚四氟乙烯(PTFE)组装电池时在手套箱中发生剧烈的火花反应,引起电极材料失效,因而电极制备采用Li21Si5粉末与Cu粉按照质量比为5%(对应的体积比为0.4)混合压制成极片,其中铜粉形成刚性的多孔导电骨架,Li21Si5嵌入其中. 该电极实现了1007 mA·h·g-1的首次脱锂容量(理论Li21Si5锂含量的51%). 此外,2018 年北京工业大学宋晓艳课题组[99]结合放电等离子烧结工艺(SPS)和高能球磨方法,制备了一种非晶态Li21Si5与碳的核-壳结构复合材料负极(a-Li21Si5@C)负极. 所制备的材料在0.1 A/g 电流密度下可逆比容量为870 mA·h·g-1(基于Li21Si5@C计算,若基于Si计算则为2479 mA·h·g-1),并在100次循环后维持在583 mA·h·g-1;Li-Si合金薄膜的石墨化碳层外壳结构可以有效约束循环过程中的体积变化,并为电荷的快速传输提供多种途径,抑制材料表面与电解液之间的副反应.
3 高容量合金基含锂负极的全电池
高容量合金基含锂负极作为Si,Sn,P 和Al 等不含锂合金负极到锂金属负极之间的过渡,或作为两者的潜在替代选择,可应用在多个全电池体系中,如传统锂离子电池(匹配V2O5,FeF3,LiCoO2,甘共苦LiFePO4和LiNiCoMnO2等含锂或不含锂正极)、锂离子-硫电池(Li-ion-Sulfur)、锂离子-空气电池(Li-ion-O2)等,但由于电极制备难度高、电化学性能较差等多种问题,目前相关研究整体较少. 同时,基于不同负极体系的系统性研究也刚起步,主要以Li-Si 二元体系及其复合物为主,少量涉及Li-Sn,Li-Al,Li-P和Li-Ge等二元体系或更多元体系.
由于高容量合金基含锂负极的电极制作、全电池的组装与使用传统电池材料有区别,当前关于高容量合金基含锂负极的多数研究局限于对锂半电池. 随着研究的深入,近年来一些前沿研究实现了高容量合金基含锂负极与V2O5,S和O2等高容量不含锂正极的匹配. 但与之匹配的电解液、黏结剂等仍然是以后的努力方向. 以下主要介绍使用高容量含锂合金负极的全电池研究进展.
3.1 常规锂离子电池体系
目前有代表性的研究主要有:2003年Zaghib等[102]将接触热压获得的多孔膨胀Li-Al合金负极在聚氧化乙烯(PEO)和三氟甲烷磺酰亚胺锂盐(LiTFSI)组成的固态聚合物电解质(SPE)中与V2O5,FePO4和LiCoO2等正极材料匹配了全电池,电化学表现接近于对应的Li负极组配的全电池,由于Li-Al过电位约为0.27~0.42 V(vs.Li/Li+),故全电池平均电压比Li负极略低. 2004年日本甲南大学Machida等[86,88]球磨制备的Li4.4GexSi1-x(x=0~0.1)负极在无机非晶60Li2S·40SiS2(摩尔分数)固态电解质中,与LiCo0.3Ni0.7O2正极匹配,在64 μA/cm2电流下获得最大可逆比容量210 mA·h·g-1,稳定循环20次无明显衰减. 2012年浙江大学刘永峰课题组[64]用氢化锂(LiH)与Si反应并球磨合成的非晶Li12Si7活性材料在泡沫镍集流体上通过10 MPa压制成负极,在含有1 mol/L LiPF6的碳酸乙烯酯/碳酸二甲酯(EC/DMC 体积比为1∶1)电解液中与锂对电极组装半电池,在100 mA/g电流下可初始放电容量约为2988 mA·h·g-1(基于Si),并在循环20 次后容量保持率约70.7%,优于商业化的体硅,并指出以Li12Si7替代Si 作为初始活性材料,其预膨胀态可在电极层面上减少相对体积变化,同时非晶态也减缓了各向异性的膨胀/收缩.
2013年Tang 等[104]制备了LiSi 负极,研究了其储锂的电化学表现,在含有1 mol/L LiPF6的EC/DMC(体积比1∶1)电解液中,可在C/30倍率下实现初始容量870 mA·h·g-1,循环10次后约为805 mA·h·g-1.2014 年崔屹课题组[65]制备了Li2O 包覆的LixSi-纳米颗粒在1 mol/L LiPF6的EC/DMC(体积比1∶1)(含体积分数为10%的FEC,1%的VC)电解液中,在C/20(1C=4.2 A/g Si)倍率下材料的比容量达到了1310 mA·h·g-1,优于Si 纳米颗粒负极. 2015 年Iwamura 等[103]将制备的Li21Si5/Cu 负极在含有1 mol/L LiPF6的碳酸乙烯酯/碳酸二乙酯(EC/DEC 体积比为1∶1)电解液中,半电池首次脱锂比容量为1007 mA·h·g-1(Li21Si5中理论锂含量的51%),后续循环提高至1591 mA·h·g-1;与MnO2正极匹配的全电池第一次放电和充电容量分别为479 和304 mA·h·g-1(基于Li21Si5),在50 mA/cm2电流下循环10 次容量约为600 mA·h·g-1(基于整个电极);并指出最初制备的晶相Li21Si5在去锂化过程中变为多孔非晶硅,在随后的电化学循环锂化过程中变为非晶相锂硅合金;且相比于Si负极的巨大体积变化,以锂硅合金为负极,即使经过数次充放电循环,锂硅合金的原始颗粒尺寸几乎没有变化,因而其循环性要优于硅负极. 2017美国科罗拉多矿业大学杨永安课题组[78,87]用高能球磨法制备的Li4.4Si 负极[67]在含有1 mol/L LiPF6的EC/DEC(体积比1∶1)电解液中,半电池在358 mA/g 电流下首次放电容量为3306 mA·h·g-1,30 次循环保持约2100 mA·h·g-1以上,60 次循环保持1200 mA·h·g-1以上(基于Si),表面氮化处理后的Li4.4Si@LixNySiz负极可80 次循环容量保持1200 mA·h·g-1以上(基于Si),且Li4.4Si 基负极的首次循环库仑效率(约90%)皆远高于Si基负极(约40%~70%).
除块体(Bulk)、纳米(Nanosized)粉体制备的电极之外,2017年崔屹课题组[68]用涂布工艺制备出一种空气稳定性优异的自支撑LixM/石墨烯复合薄膜负极(Thin film,M=Si,Sn,Al)[图5(A)]. 以Li22Si5/石墨烯复合薄膜负极为例,其结构为Li22Si5团簇封装在石墨烯片间,厚度为19和42 μm的Li22Si5/石墨烯复合薄膜负极极片在半电池中首次脱锂面容量分别为3.8 和8.3 mA·h·cm-2,即体积比容量高达约2000 mA·h·cm-3,接近Li22Si5的理论值(2240 mA·h·cm-3)和锂金属的理论值(2061 mA·h·cm-3);质量比容量约为1600 mA·h·g-1(基于Li22Si5);在1 mA/cm2电流下循环400 次后容量保持约为98%,面容量达2.4 mA·h·cm-2,实现了优异的循环性和高的容量保持率. 该研究指出,高的电化学性能一方面源于石墨烯的高导电性(1400 S/cm),使电极整体获得良好导电性;另一方面活性材料Li22Si5处于全锂化膨胀态,与Si不同,避免体积膨胀等系列问题,将有利于电极层面结构完整. 此外在全电池研究中,制备的LixSi/石墨烯负极与LiFePO4匹配[图5(B),(C)],全电池在低倍率下容量与Li||LiFePO4电池接近,但在高倍率下表现出明显更优异的容量(LixSi/C||LiFePO4电池在10C倍率时约为91.7 mA·h·g-1,20C倍率时为84.0 mA·h·g-1,而Li||LiFePO4电池在10C倍率时约为70 mA·h·g-1,20C倍率时约为58 mA·h·g-1);在200 次循环后X 射线光电子能谱(XPS)与扫描电子显微镜(SEM)分析表明,Li22Si5负极结构保持完好,无厚的SEI 形成. 同时,制备的LixSi/石墨烯负极与V2O5和S 正极匹配实现了长循环的高比能全电池,如与V2O5正极匹配[图5(D),(E)]在1C倍率下(1C=441 mA/g基于V2O5)表现出高比容量365 mA·h·g-1及200次及以上稳定的长循环寿命(容量基于V2O5质量计,负极和正极的质量比为1∶4);当平均电压为2.5 V时,全电池能量密度约为510 W·h·kg-1. 此外,石墨烯表面层的疏水性和气体不渗透性阻止了高活性LixSi与气体分子的渗透反应,因而该含锂负极可在不同的环境条件下表现出良好的稳定性,如在干燥空气中14 d后仍保持原有容量的94.3%,呈现出高面积容量3.6 mA·h·cm-2,即使在高湿度(20%~60%相对湿度)空气中暴露3 d后,仍然保持3.1 mA·h·cm-2的高面积容量. 其高的空气稳定性增加了工艺操作安全性,降低了对工业电池制造环境的要求.
此外,箔材(Foil)含锂负极的研究逐渐兴起;如2019年黄云辉和李巨合作课题组机械辊压锂化制备的Sn 基系列含锂负极[71,76,92],优化后的50 μm 箔材电极Lix(3Ag0.5Cu96.5Sn)表现出比LixSn 更加优异的空气稳定性及循环、倍率性能,在匹配LiFePO4全电池(约2.65 mA·h·cm-2)中实现0.4C倍率下稳定循环200 次,容量保持率为95%,优于同厚度的50 μm 纯锂箔,也优于他们之前报道的70 μm LixSn箔(80 次循环后容量迅速衰减,120次循环后容量仅剩余82%);即使在5C高倍率环境下,其容量仍高达1.8 mA·h·cm-2;此外,Lix(3Ag0.5Cu96.5Sn)负极与更高电压的LiNi0.5Co0.2Mn0.3O2(NCM523)正极(3 mA·h·cm-2)匹配全电池稳定循环100次后容量为2.4 mA·h·cm-2,而Li||NCM523在40次循环后容量发生迅速衰减,在80 次循环容量降低至1.3 mA·h·cm-2;另外,该课题组进一步采用70 μm Lix(3Ag0.5Cu96.5Sn)负极,在极片面积为3 cm×2.8 cm软包电池中实现825 mA·h·cm-3的初始体积比容量,50 次循环后体积比容量为674 mA·h·cm-3,皆高于石墨负极(500 mA·h·cm-3),表现出一定的实际应用潜力.

Fig.5 Air-stable and freestanding lithium alloy/graphene foil anodes[68]
在LixSi基、LixAl基和LixSn基含锂负极之外,2020年本课题组[72]开发了一种电化学循环稳定性好、容量高、倍率性能优异的Li3P/C负极. 其首先通过升华冷凝的方法将红磷嵌入微米尺度高孔隙率的多孔碳中,获得孔隙不完全填充的磷/碳(P/C)复合材料,之后将其与熔融的锂均匀混合反应,制备出Li3P/C纳米复合材料. Li3P/C负极工作示意图见图6(A),在脱/嵌锂过程中活性材料Li3P体积收缩/膨胀被限域在材料孔隙结构内部,继而保持在材料和电极尺度的结构完整性,使SEI能够在Li3P/C整体颗粒表面稳定形成,在循环过程中不发生破裂和重新生成,有利于获得高的库仑效率,最终获得稳定的电化学循环性能;此外,碳框架不仅提供了材料的结构支撑,其连续的网络结构也提供了在材料内部电子快速传输的通道,同时疏水的碳限域Li3P结构也有助于一定程度上提高Li3P的空气稳定性;在多孔碳孔隙结构中的Li3P受孔隙尺寸的限制,Li3P活性粒子尺寸仅约为5 nm,小的一次活性物质颗粒尺寸有利于在充放电过程中的高材料利用率和高充放电倍率性能. 受益于其独特的微/纳米复合结构,Li3P/C负极展现出优异的电化学性能[图6(B)~(D)]和较高的空气稳定性,可在0.1C倍率下初始脱锂过程中实现791 mA·h·g-1的高可用锂离子容量(根据Li3P/C的整体质量计算,若按P计算,则约为2179 mA·h·g-1,接近P理论比容量2596 mA·h·g-1),在6C高倍率充放电中,也表现出75%的容量保持率[基于0.5C倍率下时容量计算]与优异的循环稳定性;分别在空气中暴露3和6 h后,第一次循环脱锂容量分别为608和389 mA·h·g-1,相应的容量保持率分别为80.9%和52.0%.
3.2 锂离子-硫电池体系
将LixM基含锂负极(M=Si,Sn,Al,P等)与高容量硫基正极匹配,全电池能量密度将显著提升. 但目前该锂离子-硫电池体系(Li-ion-S batteries,LISBs)的研究尚处于初始阶段,相应的电池体系也尚未形成统一的描述,如涉及到电池体系名称为锂离子-硫电池(Li-ion-Sulfur)、硅硫电池(Si-Sulfur)、锡硫电池(Sn-Sulfur)、锂化硅-硫电池(Si-lithiated-Sulfur,SLS)和无锂金属硫电池(Li-metal-free)等;其次使用的电解液体系、活性物质载量以及正负极质量比(NP比)等都不同(或未注明),较难对各项研究展开比较研究. 下面简单介绍部分代表性研究.
如前所述,2010年崔屹课题组[61]对硅纳米线进行电化学锂化制备的LixSi负极与硫/碳正极匹配组装电池,使用的电解液为1 mol/L 双三氟甲烷磺酰亚胺锂盐(LiTFSI)溶解于1,3-二氧戊环/二甲醚(DOL/DME体积比为1∶1),该电池实现了10次循环容量保持率为75%;2011年Elazari和Aurbach等[62]用电化学锂化无定形硅薄膜制备的Li-Si 合金负极与硫/碳正极构筑的全电池,在含有10%LiTFSI 和2%LiNO3的DOL/DME(体积比为1∶1)电解液中电池第二次循环比容量约为2840 mA·h·g-1(基于Si的质量计算),经过60次循环后可逆容量保持为380 mA·h·g-1以上(基于S计算):2011年Hassoun和Scrosati等[98]将Si/C 复合材料与锂箔添加电解液接触锂化制备的LixSi/C 纳米复合负极与硫/碳正极(S/C)匹配,在含有三氟甲磺酸锂(LiCF3SO3)的四乙二醇二甲醚(TEGDME)电解液中,在0.5 A/g电流下实现了可逆电化学反应[S8+8LixSi→8Li2S+8Li(x-2)Si],初始比容量达到600 mA·h·g-1(基于S计算). 2015年美国南加州大学Zhou 等[90]采用电化学锂化全氟磺酸(Nafion)包覆的多孔硅制备的Li-Si 负极与硫/碳正极匹配,在含有1 mol/L LiTFSI和5%LiNO3的DOL/DME(体积比为1∶1)电解液中100次循环后比容量为330 mA·h·g-1,能量密度为590 W·h·kg-1(以硫和硅的总质量计算),为现有商业化锂离子电池的2倍左右.
2017 年崔屹教授课题组[68]制备的自支撑LixSi/石墨烯复合薄膜负极与S 正极匹配,在含有1 mol/L LiTFSI 和0.4 mol/L LiNO3的DOL/DME(体积比为1∶1)电解液中,在1.3~2.6 V之间实现全电池比容量高达1086 mA·h·g-1(基于S),平均电压约为1.8 V,负极和正极的质量比为1.8∶1,能量密度约为490 W·h·kg-1;显示的2 个放电电压平台2.1 和1.7 V 对应于Li-S 放电平台(2.4 和2.1 Vvs.Li/Li+)和Li-Si 平台(0.4 Vvs.Li/Li+);在0.5C 倍率下(1C=1672 mA/g 基于S),110 次循环后容量保持为858 mA·h·g-1,库仑效率为99.5%,高于Li-S的98.8%.
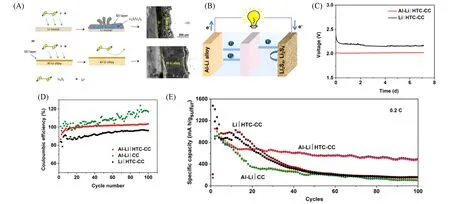
Fig.7 Li-Al alloy anodes for novel battery configuration[77]
此外,2018 年Wang 课题组[69]通过电化学锂化制备Li-Al 合金负极与硫化聚丙烯腈(SPAN)正极匹配,使用碳酸酯类电解液构筑全电池,其平均放电电压为1.5 V,在200 mA/g电流密度下实现高可逆容量550 mA·h·g-1(基于SPAN质量),200次循环容量保持率为83%;由于表面Al2O3层的存在,电极具备一定的空气稳定性. 该课题组[77]进一步沿用电化学锂化方法制备Li-Al合金负极,在多硫溶剂中展现出优于Li金属的无枝晶和高化学稳定性[图7(A)],可归因于Li-Al在电化学合金制备过程中预先形成的SEI的保护;将Li-Al与载有Li2S4的碳布正极(HTC-CC)构筑全电池[图7(B)],在1 mol/L LiTFSI[溶剂为四乙二醇二甲醚(TEGDME),无LiNO3添加剂]电解液中,自放电测试开路电压稳定在2.05 V,实现了在0.2C(基于硫的质量)倍率下1050 mA·h·g-1的高比容量,循环100次后容量保持约为500 mA·h·g-1,库仑效率接近100%[图7(C)~(E)]. 该研究指出,用Li-Al代替Li负极,工作电压有一定降低,但有效抑制了与多硫化物的副反应以及避免了锂枝晶的生长,提升了电化学循环性能.
2020年武汉大学王功伟课题组[93]通过化学还原法制备的Li-Al合金负极(命名为c-LiAl)与硫/氮掺杂碳正极(S-NC)匹配,全电池呈现出与电化学锂化的e-LiAl||S-NC相似的电压曲线,电池初始放电容量为854 mA·h·g-1,充电容量为769 mA·h·g-1,循环100 次后容量保持约为500 mA·h·g-1以上(负极正极面容量比约为1.07);该研究指出优异性能源于c-LiAl在化学还原制备时形成的人工SEI具有良好的耐多硫腐蚀能力及空气稳定性.
3.3 锂离子-空气电池体系
2012 年Hassoun 和Scrosati 等[63]首次报道了一类锂离子-空气电池(Li-ion-air batteries,LIOBs)新体系的雏形,通过将球形纳米结构Si-C 复合颗粒与锂箔接触自发进行电化学锂化制备了LixSi-C 含锂负极,在三氟甲烷磺酸锂盐(LiCF3SO3)溶于TEGDME 电解质中,与O2/C 正极匹配,以固定比容量1000 mA·h·g-1在200 mA/gcarbon电流下实现了稳定循环15次,首次证实了LixSi等高容量合金基含锂负极替代锂金属负极在空气电池中应用的可行性(图8),该研究表明,含锂合金负极相比于锂负极,全电池表现出更低的过电位和更好的循环性能,虽然含锂合金负极的运用在一定程度上降低了锂离子-空气电池的能量密度,但是避免了负极金属锂枝晶生长及负极空气腐蚀快速失活等问题,有望进一步提高空气电池的稳定性和安全性.

Fig.8 An initial prototype of lithium ion-air battery[63]
2015 年复旦大学王永刚课题组[105]通过电化学锂化方法将Al/C 复合电极进行锂化,制备了一种LixAl/C复合电极,在醚类(TEGDME基)电解液中,与O2-C正极匹配实现了100 mA/g电流密度下稳定循环20 次无明显容量衰减. 此外,由于碳层的保护作用,所制备的LixAl/C 复合电极中LixAl 具有优异于锂金属负极的抗空气腐蚀能力. 2016年南京大学周豪慎课题组[66]将商业化的Si 颗粒电化学锂化制备了Li-Si 负极,通过构筑稳定的SEI 膜,在提高含锂电极的循环稳定性的同时,可作为保护层结构有效地抑制了负极上的氧气腐蚀副反应,在TEGDME-LiTFSI 电解质中,以固定比容量1000 mA·h·g-1与500 mA/g 电流密度、1.5~4.0 V 电压区间,实现了100 次的超长循环性能,实际能量密度达到了678 W·h·kg-1. 2017 年该课题组[89]进一步通过在氩气中采用高能机械球磨法合成Li21Si5粉末,与Cu 粉均一混合在10 MPa下压制在铜箔上制备含锂电极,并在TEGDME-LiCF3SO3(摩尔比4∶1)电解质中与载铂的多壁碳纳米管氧气正极(Pt-MCNT)匹配,在同电流条件下实现了80次稳定循环. 2017年天津大学杨全红课题组[106]通过对商业化的Al箔电化学锂化,制备了Li-Al合金负极同时兼作为集流体,与预载Li2O2的含锂氧气正极匹配,在TEGDME-LiCF3SO3电解质中以100 mA/g 电流密度实现了100 次以上循环,其全电池最大能量密度达1178 W·h·kg-1,100次循环后依然保持1002 W·h·kg-1.
此外,2017 年复旦大学彭慧胜课题组[107]设计了一种固态同轴结构,以LixSi/CNT 混合纤维为含锂内负极,TEGDME 基聚合物凝胶为中间电解质,CNT 为外正极,开发出了一种高能量密度(约512 W·h·kg-1)和超高柔性(20000弯折有效)的锂空电池纤维,可在比容量500 mA·h·g-1实现了100次的稳定循环,平均放电电压2.1 V. 同年Aurbach等[95]也尝试对硬碳进行锂化处理,并用在锂离子-空气电池中,但能量密度优势不在. 2019年上海交通大学杨军课题组[96]采用静电纺丝法制备了一种自支撑的纤维状硅/碳阳极,在组装全电池时将其夹在隔膜和锂金属之间,加入电解液后电化学锂化生成Li-Si合金负极,之后在TEGDME 基聚合物凝胶电解质中装配O2电池. 由于负极LixSi 相比于Li 具有更低的活性和无枝晶特性,其全电池性能优于常规锂离子-空气电池.
总之,目前的关于锂离子-空气电池的研究仍然较少,处于雏形论证与概念探讨阶段,且含锂负极的制备多采用对常规Si/C等负极进行电化学锂化的方式,尚无其它合成方法的报道,整体缺乏深入研究. 此外,目前整体电池的循环性能较差,需要从电解液和电极结构设计等多角度出发,进一步提高电池的循环性能.
4 高容量合金基含锂负极的电化学性能调控与优化策略
高容量合金基含锂负极面临多个重要挑战(图2):(1)活性材料巨大体积变化引起的电极结构不稳定、电接触变差、SEI不稳定、库仑效率低和循环性能差等问题;(2)在嵌锂和脱锂后,材料本征变化的电子和离子导电性问题;(3)化学稳定性及空气稳定性差等问题. 因此,提高合金基含锂负极的电化学性能,需从材料、电极、电池等多个层面进行综合考虑与协同优化调控. 目前常见的研究策略主要有:
材料组分调控(引入其它元素、材料复合等). 通过调控组分引入合金元素,调控最终所制备的锂合金材料晶粒大小、晶粒形状、晶粒取向,这些对其电化学性能造成重要影响[108]. 此外,低体积效应或惰性组分的引入有助于缓解材料在充放电过程中的体积效应,提高电极的电化学循环性能和稳定性.如2014年Chumak等[109]报道了一类Lix(Al1-zZnz)基含锂多元合金负极,其中将LixAl中20%的Al用Zn替换,制备Lix(Al0.8Zn0.2)复合的含锂负极材料,与LixAl 合金相比,电化学稳定性有一定程度提升. 2020年同济大学李洒与麻省理工学院李巨课题组[76]合作报道了通过机械合金方法制备的Mn和Si掺杂的无长裂纹、超细纳米晶LixAl合金负极,并与NCM523和LiFePO4正极匹配,实现了比前期机械合金化制备的LixAl负极[110]更为优异的电化学性能,该研究指出Al中少量的Mn或Si的掺入会导致纳米沉淀物的齐纳钉扎(Zener Pinning),产生更致密的晶界网络与更细的晶粒尺寸,因此可显著降低机械辊压后LixAl箔的孔隙率,延缓其断裂,改善了在后续循环中的电极健康状态(SOH),同时减少了由于SEI的破裂和电解液渗入而引起的电子绝缘层的死晶粒团簇形成.
表面包覆与体相复合策略. 表面包覆可以物理隔离活性材料与空气/电解液,提高材料的环境稳定性、加工性和电化学性能,常见包覆材料涉及到碳族、氮族、氧族、氟族等非金属,以及如导电聚合物、纳米金属及氧化物等. 如崔屹教授课题组通过在含有适量氧的气氛中合金化反应一步制备了LixSi-Li2O核壳结构材料[65];以及使用固体、无毒的含氟聚合物(CYTOP)作为前驱体在250 ℃温度下加热原位释放氟气,在含锂负极材料表面形成一层均匀和致密的晶相LiF 涂层包覆,制备LixSi-LiF 负极材料[82],其在潮湿空气(相对湿度约40%)中暴露1 d后,容量保留率高达85.9%[82];杨永安等[67]氮化包覆制备的Li4.4Si-LixNySiz负极材料等. 此外还有“先包覆后合金化”(Coating-then-lithiation)策略,如南京大学鲁振达课题组报道的两步法制备LixSi-Li2O/TiyOz负极材料[70]、LixSi/Cu复合负极材料[85]、LixSn@PPY负极材料[84]等,在与锂反应形成锂合金前,首先对初始材料(如Si,Sn)引入表面包覆层,然后再进行合金化反应,获得的复合材料电化学性能和稳定性得到有效提升. 除包覆外,体相复合其它元素和组分也是提高含锂合金电极稳定性和电化学性能的途径. 早期研究中还引入了Cu[85],Cr[48]等惰性金属或Sn[45],Mg[111]等活性金属与Li-Si合金混合,充当骨架或基体、甚至辅助催化等作用,进一步改良提升合金基高容量含锂负极的电化学性能.
电极尺度界面保护策略(人工SEI构筑、保护层、涂层). 如2015年崔屹课题组[112]利用1-氟癸烷还原,对LixSi进行了表面改性处理构建人造“类SEI保护膜”,生成LiF和长疏水碳链的碳酸烷基锂组成的钝化层,进一步提升其空气稳定性和循环性能. 此外,如2016年南京大学周豪慎课题组[66]用商业化的Si颗粒电化学锂化制备Li-Si负极用于锂离子-空气全电池,通过构筑稳定的SEI膜,在提高含锂电极的循环稳定性的同时,可作为保护层结构有效地抑制负极上的氧气腐蚀副反应等.
电解液添加剂、电解质(液态、聚合物、全固态)、隔膜、黏结剂、集流体等设计等. 2015年日本横滨国立大学Watanab 等[113]报道了Li22Sn5负极在离子液体电解质中的电化学性能,电解质由Li[TFSA]、四氟甲基(G4)和氢氟醚溶剂(HFE)以1∶1∶6.2 的摩尔比组成,其中Li+和G4 形成了摩尔比为1∶1 的Li(G4)(+)络合物阳离子. Li22Sn5负极在该电解质中的首次放电比容量为500 mA·h·g-1;并与S正极构筑全电池实现了稳定充放电循环,且无严重副反应. 此外,Hassoun 等[114]报道了多硫化锂添加的PEO基电解质在LixSn-C||S-C匹配的高容量全电池中的使用,整体上进一步提升了电池的安全性.
5 总结与展望
当前,科学界已逐渐认识到高容量合金基含锂负极LixM有别于传统碳负极、高容量合金负极(非锂化态)和锂金属负极的独特优势,如具有数倍于石墨和含锂过渡金属氧化物的储锂比容量;其适当而合理的锂化电位,可在过充或快充中避免金属锂析出或枝晶形成,展现出安全性高的特性和可快充的前景;以及其作为全电池活性锂源提供者,可与不含锂的高容量正极材料(如S,O2,FeF3,V2O5和MnO2等)相匹配,有望构建下一代新型高比能电池体系等. 因此,近年来国内外研究者围绕LixSi 基、LixAl基、LixSn基和Li3P基等含锂负极的相关探索性研究已陆续展开. 然而,设计和制备性能优异的实用性可规模工业化的高容量含锂负极依然面临着多种严峻挑战,尤其是其合金基多电子脱嵌机理引起的大的体积效应、含锂态的高化学活泼性以及合成困难等引起的环境、化学稳定性和电化学稳定性等关键问题. 因此,下一步研究需要继续针对这些问题拓展思路,开发多种材料合成和电极制备方法,面向实际应用,研制多样的含锂负极,从粉体到薄膜和箔材电极等;同时探索与传统锂离子电池体系更加兼容的极片和电池工艺方法,如干法工艺极片制备等,针对不同的全电池体系,从电解液、黏结剂、添加剂、隔膜、集流体等进行综合设计与系统性创新;进一步采用更先进的合成和表征技术深入探究其中的科学机理,并综合运用更多重和新颖的策略方法,如体相复合、掺杂包覆、电极预处理、活性/惰性基体构筑、界面工程、电解液设计等,以更快获得下一代高比能锂离子电池.
