pH 对AZ31 镁合金表面磷酸钙转化膜性能的影响
2021-05-17左宏健贾素秋
左宏健,贾素秋*
(长春工业大学,吉林 长春 130000)
生物医用金属是目前常用于临床医学的材料,如钴基合金、钛及钛合金、不锈钢等。但由于它们的弹性模量与人骨的弹性模量不匹配,长期固定在人体内易引发炎症,且需要进行第二次手术取出植入物,增加了治疗成本和风险。镁合金的密度等同于天然骨,生物相容性良好,质量轻,易降解,成本也较低,具有相当优秀的发展潜力。但是镁合金在人体内极易溶解,腐蚀速率过快,常对其进行表面改性,以便广泛地应用于骨植入。表面改性不仅几乎不影响镁合金的强度,而且通过调整表面的成分和结构可控制其腐蚀速率。目前用于镁合金的磷酸盐转化膜主要有锰系、锌系、钡系、钙系等[1-6]。通过电化学反应在镁合金表面生成一层非金属、不导电、难溶的结晶型磷酸盐转化膜,可以降低镁在富含氯离子的人体生理环境中的腐蚀速率,防止镁合金腐蚀所产生氢气造成皮下气泡。钙系磷酸盐膜的研究起步相对晚一些,由于其良好的生物相容性,常被用作生物防护涂层[7]。本文研究了pH 对AZ31 镁合金Ca-P 转化膜的结构及耐蚀性的影响,并探究了成膜机制。
1 实验
1.1 基材及其前处理
材料为AZ31 镁合金,尺寸为20 mm × 10 mm × 4 mm。先用280 号、400 号、600 号、1000 号SiC 砂纸逐级打磨试样,再分别在去离子水、无水乙醇中超声清洗30 min,随即在50 °C 的20 g/L Na2CO3溶液中超声清洗30 min 以去除表面污染物,然后在过饱和的Ca(OH)2溶液中室温浸泡24 h,用去离子水清洗 以增加基体表面的形核点。
1.2 转化膜的制备
转化液由0.042 mol/L Ca(NO3)2和0.025 mol/L NH4H2PO4配成,钙磷比为1.68,使用HNO3和NaOH调节其pH 至4.5、5.0、5.5、6.0 和6.5。在室温下将预处理过的镁合金分别浸入不同pH 的转化液中,按pH 由低到高记为A、B、C、D 和E 组,48 h 后取出,用去离子水清洗表面后用冷风吹干。
1.3 表征与性能测试
使用JEM-5500LV 扫描电镜(SEM)和ZEISS SUPRA 40 场发射扫描电镜(FESEM)观察转化膜的形貌。使用D-MAXILA 型X 射线衍射仪(XRD)和EDAX-Falcon 能谱仪(EDS)确定膜层成分。
采用荷兰Ivium 电化学工作站测量试样的极化曲线以及电化学阻抗谱。腐蚀介质为0.9% NaCl 溶液;铂片电极作为辅助电极,饱和甘汞电极(SCE)作为参比电极,试样为工作电极(1 cm2,非工作表面用环氧树脂涂封)。电位扫描速率为5 mV/s,阻抗谱测试频率范围100 000 ~ 0.01 Hz,振幅0.014 14 V,测试电位自动确定。
镁合金作为生物植入材料若需应用于临床,应测试其在人体内的腐蚀情况。将在pH = 5.5 的转化液中制得的试样悬浮于37 °C 的仿生液(配方见表1)中,每隔24 h 更换一次仿生液,168 h 后取出并在空气中自然干燥,观察转化膜的腐蚀情况及溶液的沉淀情况。

表1 人体仿生液的配方 Figure 1 Composition of simulated body fluid (单位:g/L)
2 结果与讨论
2.1 转化膜的形貌
从图1 可见,所有试样上均形成了一层致密的转化膜,膜厚普遍在10 ~ 20 μm 之间,最厚处达30 μm。所有转化膜都完全覆盖了基体。膜层形貌与转化液pH 有很大的关联性:pH 较低时,膜层主要由片状结构组成,最长可达几百微米,较大的晶粒组织导致膜层厚度不均匀;随着pH 增加,片状组织逐渐被10 μm左右的球状结构取代,膜层表面变得更加平滑,厚度也更加均匀。
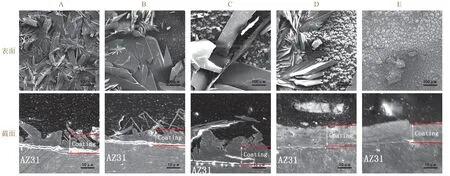
图1 不同p H 的转化液所制转化膜的SEM 照片 Figure 1 SEM images of conversion films prepared at different pHs
2.2 转化膜的成分
2.2.1 能谱分析
使用能谱仪分别对不同形貌的膜层进行微区扫描和点扫描,对膜层整体做面扫描,各组试样均得到类似的结果,如图2 和图3 所示。转化膜主要由Ca、P 和O 元素构成,3 种元素均匀地分布于膜层的不同区域,而H 元素由于原子序数低而无法检出,片状结构(区域1、点1)中的钙磷比约为1∶1,符合CaHPO4的元素构成。其中球状结构的膜层(区域2)除Ca、P、O 以外,还检出了少量Mg 元素,猜测这部分Mg 元素来源于转化初期形成的Mg(OH)2。
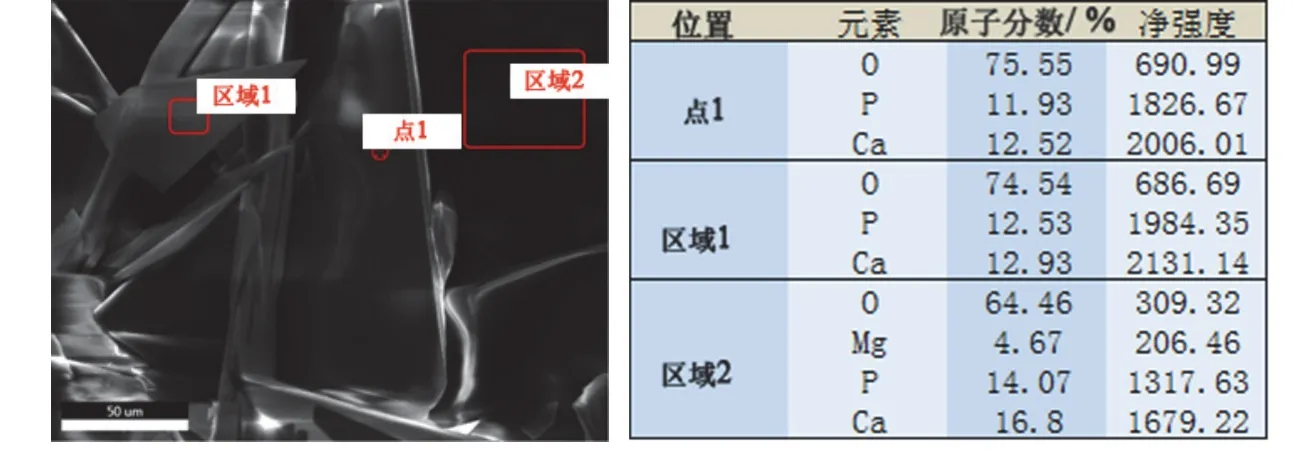
图2 转化膜不同位置的能谱分析 Figure 2 EDS analysis at different positions of conversion film
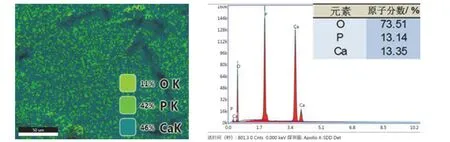
图3 转化膜的EDS 面扫描结果 Figure 3 EDS plane scan result of conversion film
2.2.2 XRD
从图4 可知,转化膜的衍射峰主要有11.6°、20.94°、29.28°、34.44°、47.92°、72.7°等,分别对应CaHPO4·H2O 和CaPO3(OH)·H2O。
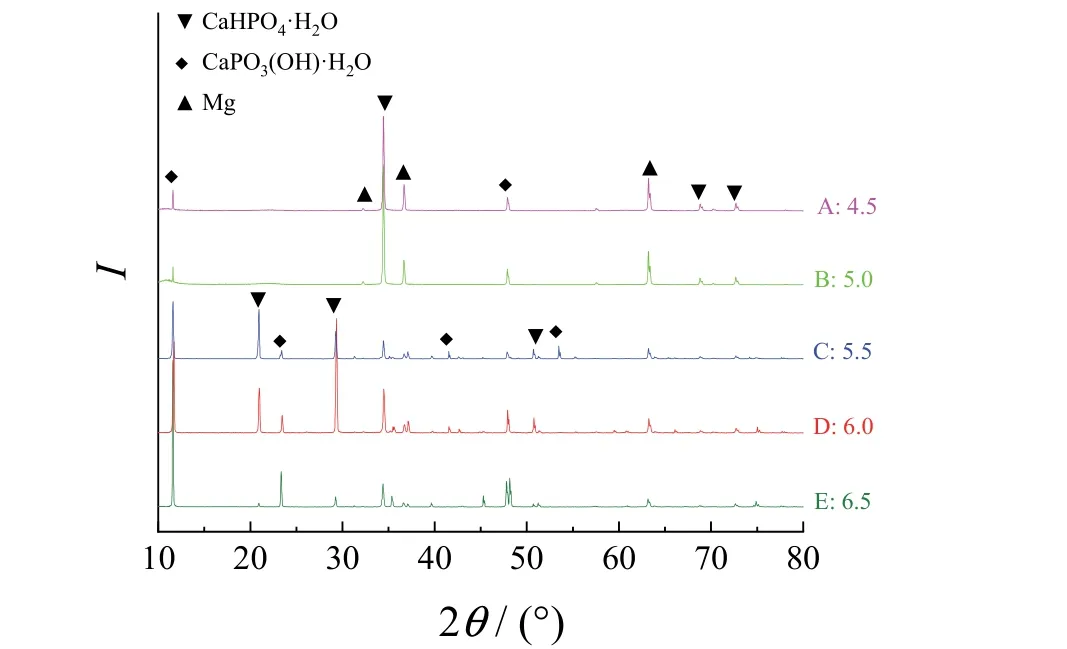
图4 不同pH 下所制转化膜的XRD 谱图 Figure 4 XRD patterns of conversion films prepared with different p H
为了探究膜层的生长过程,分析Mg 元素在转化膜中的存在形式,设计了如表2 所示的试验组:将9 组共18 个试样在不同pH 的转化液中浸泡一定时间后取出,用1000 号SiC 砂纸轻轻磨掉一部分转化膜。重复上述浸泡与磨的过程3 次,之后用XRD 分析转化膜的成分。

表2 探究转化膜生长过程的试验设置 Table 2 Conditions of experiments for exploring the growth of conversion film
18 个试样中有16 个检出了Mg(OH)2峰(18.527°、37.983°、50.785°和72.069°),图5 显示了其中较为典型的3 组(pH 6.0,转化时间1 h)、5 组(pH 5.5,转化时间2 h)和7 组(pH 5.0,转化时间4 h)样品的XRD 图谱,其中pH 较高的试样更容易检出Mg(OH)2,部分试样未检出Mg(OH)2的主要原因是打磨时力度稍大就会导致膜层过薄甚至暴露基体。据此有理由推测不同pH 条件下膜层生长初期均有Mg(OH)2形成。结合EDS 结果可知,成膜初期少量Mg 被氧化后以Mg(OH)2的形式与CaHPO4·H2O 一同附着在镁合金表面,二者共同组成了球状结构的转化膜。
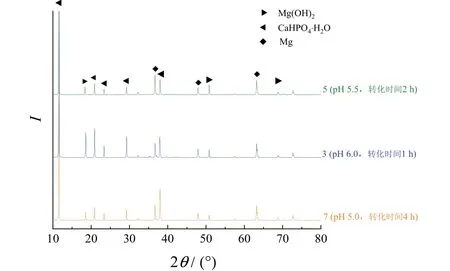
图5 生长过程中所得膜层的XRD 谱图 Figure 5 XRD patterns of conversion films obtained during the growth process
2.3 转化膜的耐蚀性
氯离子极性很强,易吸附在镁合金表面,令微小的局部区域内离子浓度过高,腐蚀产物形成一个疏松微小的包套,使其中的基体快速腐蚀[8]。磷酸盐膜层能将金属基材表面的活性降低到很小的程度,从而减弱后续的腐蚀反应。膜层还给金属表面各处提供了一个同等的电化学电位,抑制了局部的阴极反应和阳极“点蚀”,从而减少了电化学腐蚀[9]。
2.3.1 电化学测量
从图6 可知:C 组的阻抗谱曲线半径最大,其次为D 组,其余组的阻抗谱曲线半径相近。从表3 可知:C 组腐蚀电位(φcorr)最正,腐蚀电流密度( jcorr)也最低,B 组和D 组次之。这说明pH 为5.5 时形成的转化膜耐蚀性最好。
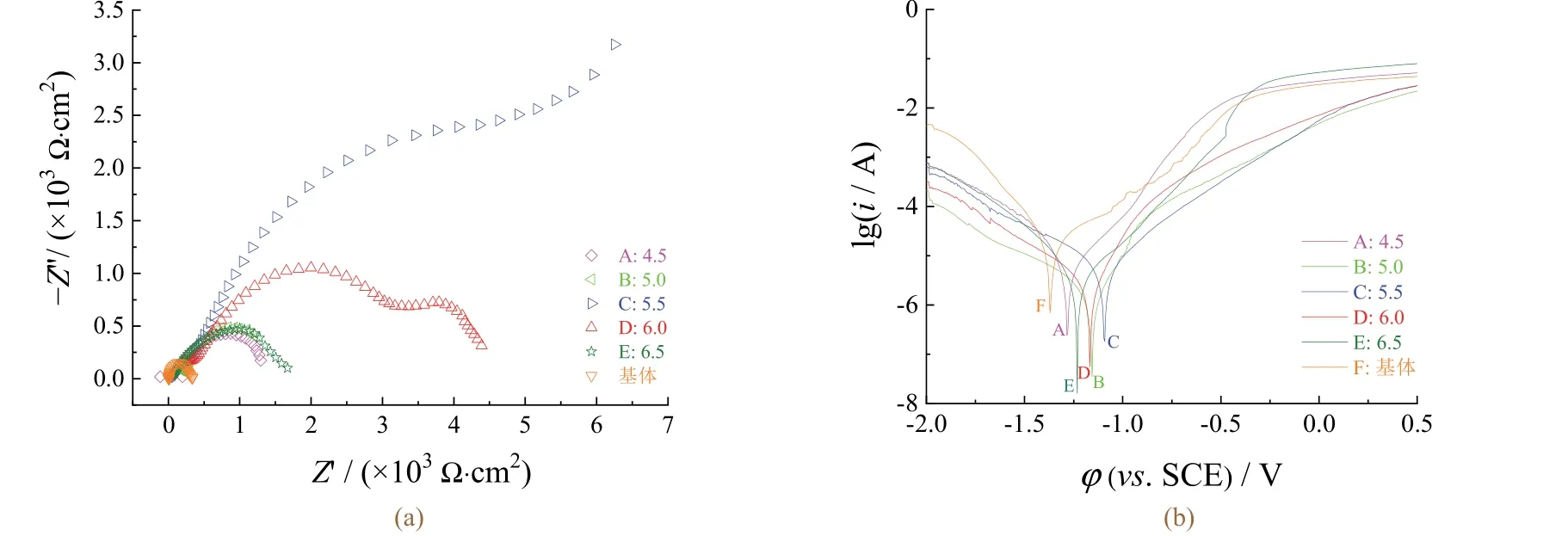
图6 基体与不同p H 下所得转化膜的电化学阻抗谱(a)和极化曲线(b) Figure 6 EIS plots (a) and Tafel curves (b) of substrate and conversion films obtained at different pHs
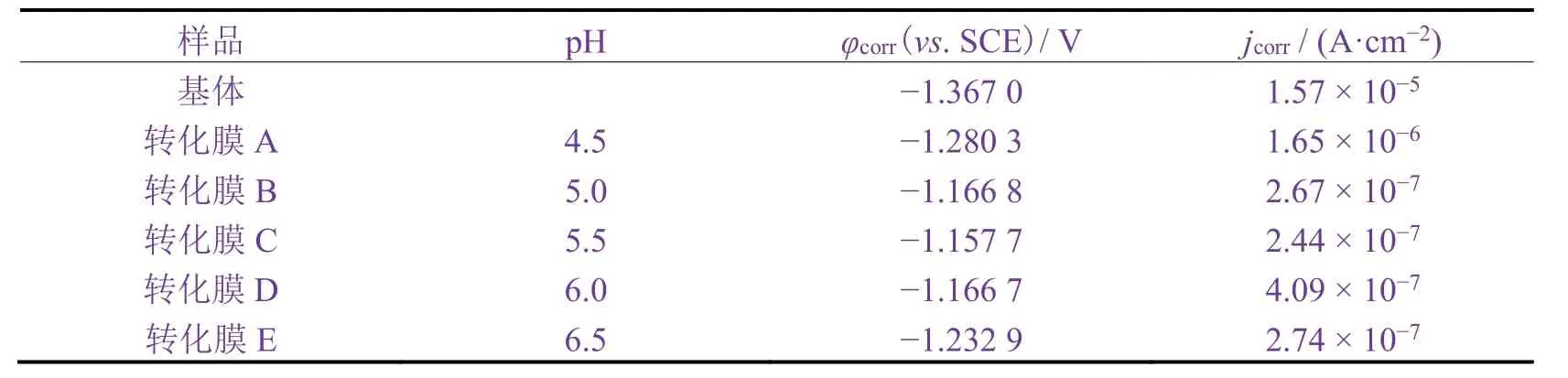
表3 基体与不同p H 下所得转化膜的腐蚀电位和腐蚀电流密度 Table 3 Corrosion potentials and corrosion current densities of substrate and conversion films obtained at different p Hs
2.3.2 人体仿生液浸泡试验
转化膜浸泡后的模拟体液依旧澄清且无沉淀生成。基体被严重腐蚀,表面可见大量点蚀坑。转化膜表面虽有明显的腐蚀痕迹,主要体现在表面较浸泡前更暗并失去光泽,但依旧完整,未出现大规模的开裂或脱落。使用扫描电镜进一步观察试样不同位置的腐蚀情况(见图7)时发现,膜层裂缝相较于浸泡前有扩大的迹象,转化膜受到一定程度的破坏,这导致了膜层表面失去光泽,但膜层整体依然完好,未暴露镁合金基体,同时在部分膜层表面观察到再结晶的趋势,说明膜层在人体仿生液中有一定的自愈合能力。这证明所制Ca-P 转化膜能够在一定程度上保护处于人体体液环境中的镁合金,减缓其腐蚀速率。

图7 在人体仿生液中浸泡168 h 后基体(a)与膜层不同位置(b、c、d)的形貌 Figure 7 Morphologies of substrate (a) and different positions (b, c, d) of conversion film after being immersed in simulated body fluid for 168 h
2.4 成膜机理
在磷化液中膜层形成的热力学动力是由金属基体的异质性和磷酸二氢铵的水解平衡运动引起的。镁合金浸入到Ca-P 转化液中后,首先由镁合金基体作为阴极发生析氢反应[2],如式(1)和式(2)所示。
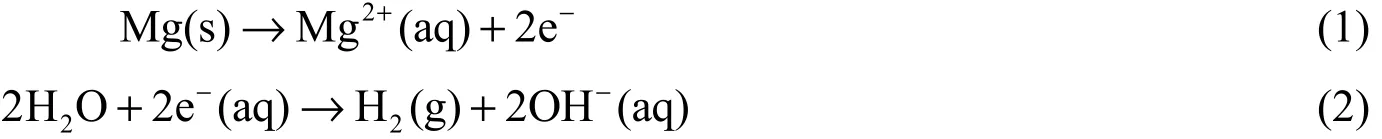
在析氢反应中,Mg 很快就形成了Mg2+,随着H+的消耗、Mg2+的生成,镁合金附近局部pH 升高,OH-浓度增加,反应生成的OH-参与式(3)和式(4)所示的反应。
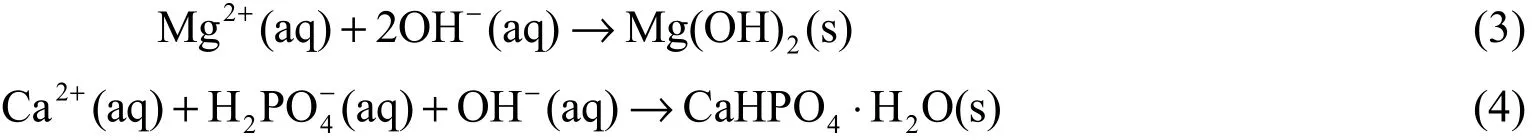
析氢反应开始之初,少量Mg(OH)2迅速附着于镁合金基体表面,形成一层1 ~ 2 μm 厚的薄膜[8]并阻止析氢反应进一步进行,反应(3)放缓,反应(4)逐渐占据主导地位,此时Mg(OH)2和CaHPO4一同附着在基体上形成球状转化膜。最终,沉淀与溶液处于反应(4)的动态平衡中。
镁合金基体加入转化液前,溶液中有少量CaHPO4·H2O 沉淀,pH 越高则沉淀量越多,因此不同pH 的转化液均为CaHPO4的过饱和溶液。成膜初期形成的球状膜为CaHPO4·H2O 的结晶和生长提供了良好的形核点,促进沉淀于烧杯底部的CaHPO4·H2O 溶解并在试样表面重新结晶[9],形成片状的膜层。片状膜层的形成会阻碍球状膜层的生长,而pH 越高,沉淀于烧杯底部的CaHPO4·H2O 越稳定,不利于CaHPO4·H2O在试样表面重新结晶。所以pH 较高(> 5.5)时更有利于球状结构的生长,反之则有利于片状结构的生长。
转化液pH 较低(< 5.0)时,H+在镁合金基体附近被迅速还原成H2,镁合金基体表面产生大量气泡,镁合金腐蚀速率过快,转化膜生长速率过快,而且对已形成的转化膜产生腐蚀作用,导致膜层疏松多孔且不均匀;pH 较高(> 6.0)时,溶液中大量的Ca2+和 H2PO−4提前沉淀于烧杯底部,溶液中离子浓度较低,不利于膜层形成。pH 适中(5.5)时生成的转化膜最为致密均匀,制得的膜层能更好地保护镁合金基体。
3 结论
以Ca(NO3)2和NH4H2PO4为原料,通过液相沉积法在镁合金表面制备Ca-P 转化膜,所制膜层由高纯度的CaHPO4和少量Mg(OH)2构成,可以显著提高AZ31 镁合金在人体环境中的耐蚀性。
Ca-P 转化膜由片状和球状两种形貌的结构组成:球状结构在成膜初期形成,主要由CaHPO4·H2O 和少量Mg(OH)2构成;片状结构完全由CaHPO4构成。pH 较高(> 5.5)时更有利于球状结构的生长,反之则有利于片状结构的生长。
