高强度聚焦超声联合GnRH-a对子宫腺肌症患者血清CA125、PGF2a、脂联素的影响
2021-05-17王小兰
王小兰 赵 洪 陈 行
1.福建省福清市妇幼保健院(350300);2.复旦大学附属华东医院 ;3.复旦大学附属妇产科医院
子宫腺肌症是一种临床常见的子宫良性疾病,临床主要表现为痛经加重、经量过多等[1]。目前子宫切除术是根治子宫腺肌症唯一的方法,但手术可能导致患者卵巢功能早衰、盆底韧带松弛等,使患者产生不良心理障碍,不能被有生育要求患者接受。高强度聚焦超声具有无创伤、痛苦小等优点,在治疗子宫腺肌症有较好临床疗效,但部分患者在治疗后出现了一定的不良反应及并发症,如肠道损伤、神经损伤等[2-3]。促性腺激素释放激素激动剂(GnRH-a)是治疗子宫腺肌症的常用药物,短期疗效明显停药易复发[4]。有文献报道[3],高强度聚焦超声联合GnRH-a治疗子宫腺肌症具有较好的临床效果。为进一步了解联合应用治疗子宫腺肌症的机制,本研究对患者血清糖链抗原199(CA125)、前列腺素2a (PGF2a)、脂联素(ADP)水平变化进行观察分析。
1 材料与方法
1.1 一般资料
选择2018年6月—2019年6月在本院接受治疗的子宫腺肌症患者122例。纳入标准:①经临床及MRI检测确诊为子宫腺肌症,病灶所在子宫肌层厚度≥3cm;②彩超显示腺肌病灶,高强度聚焦超声设备换能器焦点可达到病灶中心,且声通道安全;③患者有强烈治疗愿望及希望保留子宫的完整性。④对本研究知情并同意并配合治疗。排除标准:①合并高血压、糖尿病及肝、肾、心脏等重要脏器功能;②合并急性盆腔炎或慢性盆腔炎急性发作者;③近期使用过激素类药物;④膀胱充盈或无法俯卧1h以上;⑤有磁共振增强检测以及麻醉镇静禁忌者;⑥妊娠期、经期或绝经者。随机对照试验方法将入选患者分为观察组和对照组。本研究通过院伦理委员会批准后实施。
1.2 治疗方法
所以患者均采用聚焦超声肿瘤治疗系统[重庆海扶(HIFU)技术有限公司生产],超声换能器固有频率0.8MHz,焦距120mm,超声探头频率3.5 MHz。术前常规导泻灌肠等准备,给予芬太尼、咪唑安定镇静镇痛。取俯卧位,超声换能器置于下腹部位正下方,调整参数,使机载超声清楚显示出病灶,建立安全声通道,将焦点放在病灶中心,根据患者术中情况使用300~400W功率点扫描,同时根据实时灰度扩散情况调整焦点位置。当病灶内大部分区域出现可见的团块状灰度变化后停止治疗。治疗结束后对治疗区域进行降温等常规处理。观察组在治疗结束后第1次月经来潮的第1~2天给予皮下注射醋酸亮丙瑞林微球(上海丽珠制药有限公司)3.75mg,间隔28天注射1次,连续治疗3个周期。
1.3 观察指标
比较两组术前、术后6个月痛经与经量评分、子宫体积与其病灶体积;观察其血清CA125、PGF2a、ADP水平变化以及对卵巢功能指标血清卵泡刺激素(FSH)、黄体生成素(LH)及雌二醇(E2)的影响;观察术后6个月复发率和不良反应发生率。痛经评分采用VAS评分评定[5],总分10分,分值越高则疼痛感越强。经量评分根据本院自制问卷评定,总分5分,分值越高则表示经量越多。分别采集患者术前和术后6个月月经第3天时清晨空腹静脉血,全自动电化学发光分析仪检测血清CA125、FSH、LH及E2水平,使用酶联免疫吸附试验检测血清PGF2a、ADP水平。
1.4 统计学分析
数据选择SPSS18.0统计。计量资料比较采用t检验,计数资料采用χ2检验。当P<0.05时表示差异有统计学意义。
2 结果
2.1一般临床资料
两组一般资料比较无差异(P>0.05)。见表1。
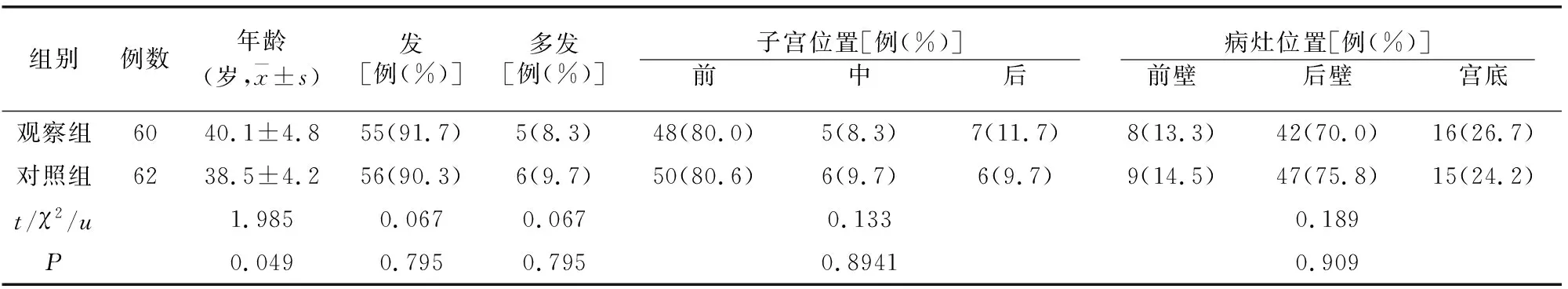
表1 两组一般资料比较
2.2 两组痛经和经量评分
痛经和经量评分,术前两组无差异(P>0.05),术后两组均降低且观察组低于对照组(P<0.05)。见表2。

表2 两组术前术后痛经和经量评分比较(分,
2.3 两组子宫体积与其病灶体积
子宫体积与病灶体积,术前两组无差异(P>0.05),术后两组均缩小且观察组小于对照组(P<0.05)。见表3。
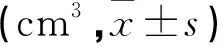
表3 两组术前术后子宫体积与病灶体积比较
2.4 两组血清CA125、PGF2a、ADP水平
术前,两组血清CA125、PGF2a、ADP水平比较无差异(P>0.05),术后血清CA125、PGF2a水平降低、APN水平增高,且观察组变化幅度高于对照组(P<0.05)。见表4。

表4 两组术前术后血清CA125、PGF2a、APN水平比较
2.5 两组卵巢功能指标
血清FSH、LH及E2水平术前两组无差异(P>0.05),术后观察组较术前降低且低于对照组(P<0.05)。见表5。

表5 两组术前术后卵巢功能指标比较
2.6 两组复发及不良反应
随访6个月,对照组有4例复发(6.5%),观察组未有复发(P<0.05)。对照组有25例出现下腹部疼痛,其中22例术后1天自行缓解,2例术后7天自行缓解,1例术后第一次月经来潮后缓解,表示疼痛均耐受;2例术后出现阴道出血;5例术中出现放射痛;10例术中皮肤有灼热感。以上不良反应通过对症治疗后均消失。观察组有5例出现不同程度的烦躁、出汗、失眠等症状,停药后自行消失。对照组不良反应发生率(62.9%)高于观察组(8.3%)(P<0.05)。
3 讨论
子宫腺肌症属一种特殊类型的子宫内膜异位症,目前发病机制尚未明确,但多项研究显示可能与输卵管结扎、人工流产、分娩等因素有关,上述操作造成子宫内膜或者浅肌层受损,使子宫内膜向子宫肌层侵袭性生长[6]。患者不愿切除子宫,使得保守治疗尤为重要。
高强度聚焦超声是一种新兴的保守治疗手段,治疗妇科良性疾病有确切疗效[7]。高强度聚焦超声技术通过体外投射超声能量在靶组织或器官内聚焦,利用超声能量沉积后所产生的热效应、空化效应等灭火病灶组织,从而使其凝固性坏死。有学者研究证实应用高强度聚焦超声治疗子宫腺肌症,不仅可有效使者腺肌病灶消融,还可缓解痛经等症状[8]。本研究结果显示,经高强度聚焦超声治疗后,患者痛经、经量得到一定好转,血清CA125、PGF2a、ADP也明显改善。有学者对行高强度聚焦超声治疗患者随访发现有较高的复发率[8],本研究结果也显示其复发率6.5%。有研究证实子宫腺肌症患者保守性手术后联合辅助药物可有效减少复发率[10],GnRH-a是临床常见的辅助用药。本研究通过高强度聚焦超声联合GnRH-a治疗后,不仅患者血清CA125、PGF2a、APN水平以及痛经、经量改善更为明显,且无患者复发,与相关结论一致[11]。
CA125在子宫内膜异位症等非恶性疾病中均存在一定阳性率,且临床证实子宫腺肌症患者血清CA125水平较正常者升高,而子宫切除术后血清CA125水平逐渐恢复正常[12]。国内外均有研究显示子宫腺肌症患者血清CA125水平与子宫大小明显相关[13-14]。高强度聚焦超声可灭活腺肌病灶组织使其凝固性坏死,而GnRH-a可通过抑制垂体,使机体处于低雌激素状态,从而增强疗效、缩小子宫体积。本研究结果显示,患者术前血清CA125水平显著升高,而联合治疗后水平明显降低,子宫体积缩小。说明高强度聚焦超声联合GnRH-a治疗子宫腺肌症具有一定的协同作用。
有文献报道血清PGF2a、ADP是反应子宫腺肌症病情变化的敏感指标[15]。PGF2a降低可促使宫腔松弛,从而改善痛经等症状;ADP通过抑制巨噬细胞分泌TNF-α,降低其炎症反应,同时可抑制新生血管形成。从本研究结果可见,联合治疗后患者血清PGF2a水平明显降低、ADP水平明显增高。且单纯使用高强度聚焦超声治疗不会影响其激素水平,而联合GnRH-α治疗后可有效降低其血清激素水平。
综上所述,高强度聚焦超声治联合GnRH-α治疗子宫腺肌症可有效缓解患者痛经、经量等症状,缩小子宫及病灶体积,同时可降低血清CA125、PGF2a水平,增高血清脂联素水平,是一种安全有效的治疗方法。
