紫苏子油O/W型纳米微乳的制备及其氧化稳定性
2021-05-15罗俊溢骆叶晴易孜成李威钢吴心成肖小年
易 醒,罗俊溢,骆叶晴,易孜成,李威钢,吴心成,肖小年*
(1 南昌大学 中德食品工程中心 南昌330047 2 南昌大学 中德联合研究院 南昌330047)
紫苏(Perilla frutescens)是一年生草本植物[1],在我国华中和西南一带大量栽培[2]。古典著作《名医附录》 中提到紫苏具有促进血液循环的作用,《本草纲目》中也记载紫苏具有祛寒散风、缓解中气的作用[1]。此外,紫苏子油具有抗氧化[3],抗肿瘤[4],抗菌以及抑制真菌[5],抗炎[6],抗过敏[7],抗抑郁[8-9]的作用,还具有降低总胆固醇和低密度脂蛋白所载胆固醇[10]的作用。紫苏子油中含有大量的α-亚麻酸(ω-3 脂肪酸),占脂肪酸总量的61.1%~64.0%[11-13],其次为亚油酸和油酸,含量差异不大,均占脂肪酸总量的15.0%左右,此外还有少量的三酰基甘油、甾醇和磷脂类物质[14],具有较高的食用价值。
紫苏子油中的不饱和脂肪酸含量较多,在存放过程中可能受微生物、重金属、氧气、温度等因素影响,使其不利于加工和食用。同时,紫苏子油直接食用时不具备良好的适口性,且不宜消化,降低了紫苏子油的生物利用度。为增加紫苏子油的生物利用度和贮藏稳定性,可将紫苏子油通过制备成O/W 纳米乳、固体脂质体、微胶囊等传递体系,以提高溶解性、稳定性和生物可及性[15]。O/W型纳米乳是由水、油和双亲性物质表面活性剂组成的热力学稳定的各向同性液体,乳液的平均粒径通常小于100 nm[16]。O/W 型纳米乳的制备方法通常分为2 种:高能乳化法(如微流控、高压均质化)和低能乳化法(如自发乳化和相转变乳化)。高能乳化法可能会破坏多不饱和油脂的化学稳定性[17],而低能法具有操作便捷,反应条件适宜等优势,因此低能乳化法更适合用于制备含生物脂质类的纳米乳剂,也是一种极具应用前景的低水不溶性生物活性化合物的制备技术[18-19]。同时,O/W纳米乳剂特别适用于食品,是因为它很容易与大多数食品体系中的其它成分兼容。
本研究中,主要使用低能乳化法将紫苏子油制备成O/W 纳米乳剂。首先选出适合制备微乳的表面活性剂,然后根据亲水亲油值(HLB)的可加性,将选出的表面活性剂间进行两两混合,制备出具有不同HLB 值的复合表面活性剂,选择肉豆蔻酸异丙酯(IPM)作为空白油相,通过伪三元相图筛选具有较大载油量的空白微乳配方,最后将空白微乳配方中的IPM 置换成紫苏子油或者将IPM与紫苏子油按比例混合制备紫苏子油纳米乳剂,研究紫苏子油纳米微乳的离心稳定性、氧化稳定性以及电位和粒径,为紫苏子油在食品加工中相关产品的研发提供借鉴。
1 材料与方法
1.1 原料与试剂
紫苏子油,荷泽中禾健元生物科技有限公司;肉豆蔻酸异丙酯(IPM)、Tween80、Span80、Tween20、Span20、EL-40,天津市恒兴化学试剂制造有限公司;无水乙醇 (C2H5OH)、聚乙二醇(PEG-400)、异辛烷、异丙醇、甲醇、正丁醇、硫氰酸铵、四水合氯化亚铁、六水合氯化铁、苏丹Ⅲ、亚甲基蓝均为分析纯级,天津市永大化学试剂有限公司;去离子水,实验室自制。
1.2 仪器与设备
T6-紫外分光光度计,北京普析通用仪器有限责任公司;TDL-5-A 离心机,厦门精艺兴业有限责任公司;Zetasizer Nano 激光散射粒度分析仪,英国Malven 公司;RH-DS25 磁力搅拌器,德国IKA 公司。
1.3 试验方法
1.3.1 表面活性剂的确定 选择表面活性剂Tween20、Span20、Span80、EL-40 和Tween80 (表1),与IPM 按9∶1 和8∶2 的质量比混合后,然后边搅拌(300 r/min、50 ℃)边滴加去离子水。仔细观察体系的外观状态,若体系从黏稠变稀薄并澄清透明或半透明则说明微乳形成。

表1 表面活性剂、助表面活性剂的HLB 值Table 1 The HLB value of surfactant and cosurfactant
1.3.2 空白微乳的筛选 根据HLB 值的可加性,将选出的表面活性剂两两混合,制备出不同HLB值的复配表面活性剂。将其与IPM 按不同比例预混合后,将蒸馏水逐滴加入预混料中。微乳制备成功后鉴定,根据伪三元相图中可形成微乳区域面积大小寻找最佳组合。

式中,Ma,Mb——表面活性剂a 和b 在复合表面活性剂中所占的质量比;HLBa,HLBb——表面活性剂a 和b 各自所对应的HLB 值[20]。
1.3.3 紫苏子油微乳的制备 根据空白微乳筛选出的配方,将IPM 替换成紫苏子油,或将IPM 与紫苏子油按比例混合,采用转相乳化法(50 ℃)制备微乳。
1.3.4 微乳的稳定性测定 将制备的纳米微乳体系在4 000 r/min 条件下离心15 min,选择未出现沉淀和分层且载油量最大的配方作为后续体外释放试验的最终配方。
1.3.5 微乳类型的鉴定 采用染色法鉴定微乳的类型。取微乳10 mL 于样品瓶中,分别滴入苏丹Ⅲ溶液(无水乙醇配制,0.1%体积分数)和亚甲基蓝溶液(蒸馏水配制,0.1%体积分数)5 μL,静置30 min,观察2 种染料在微乳中的扩散速度。
1.3.6 微乳的粒径和电位测定 使用激光散射粒度分析仪测定微乳制备12 h 后的平均液滴大小、粒径分布和电位,样品预先稀释100 倍。测定参数设置:紫苏子油折射率设为1.52,吸收率设为0.001,分散剂折射率设为1.33,样品的平衡时间为180 s。微乳平均粒径用d4,3来表示,且所有样品均重复测定3 次。

1.3.7 紫苏子油的氧化稳定性测定 将紫苏子油的过氧化值(POV)作为紫苏子油氧化稳定性的判定依据,紫苏子油的POV 值的测定参考Zhong 等[21]的方法。取360 μL 样品于离心管中,加入1.8 mL异辛烷/异丙醇(3∶1,体积比)混合溶液,振荡3 min,于5 000 r/min 离心30 min。取离心后的上清液600 μL,分别加入45 μL 硫氰酸铵溶液(3.94 mol/L)和新制Fe2+溶液(0.14 mol/L),再用甲醇/正丁醇(2∶1,体积比)混合溶液定容至10 mL,摇匀,在暗室中反应30 min 后,用分光光度计在510 nm波长处测定吸光值。使用600 μL 的异辛烷/异丙醇(3∶1,体积比)混合溶液作为空白对照。
先配制好100 μg/mL 的Fe3+溶液,分别取100,150,200,250,300,350,400 μL Fe3+标准溶液,再加45 μL 硫氰酸铵溶液(3.94 mol/L),用甲醇/正丁醇(2∶1,体积比)定容至7 mL,配制成1.43,2.14,2.68,3.57,4.29,5.00,5.70 μg/mL 的Fe3+标准溶液,振荡摇匀,在暗室中反应30 min 后,用分光光度计在510 nm 波长处测定吸光值。以甲醇/正丁醇(2∶1,体积比)混合溶液作为空白对照。

式中,A——样品的吸光度 (A=A样-A空);b——Fe3+标曲的截距;10——反应总体积(mL);k——Fe3+标曲的斜率;2——Fe3+与H2O2的反应摩尔比;56——Fe3+的摩尔质量(g/mol)。
固定紫苏子油的用量为0.25 g,根据筛选出的3 个最佳工艺配方(HLBTween80/Span20=14.0,HLBTween80/Span20=13.0 和HLBEL-40/PEG-400=13.5)制备微乳后,均加水稀释至10 mL,然后将制备的样品置于37 ℃烘箱中密封保存1,3,5,7,9,12,15 d,根据上述方法测定紫苏子油微乳在对应时间 (d) 下的POV 值。将单一的紫苏子油作为对照,平行3 次。
2 结果与分析
2.1 单一表面活性剂的筛选
表面活性剂的筛选结果如表2所示,选择的表面活性剂(SA)为Tween80 和EL-40 时,且SA∶Oil=9∶1(质量比)时,可形成澄清透明的微乳液,当表面活性剂为Span80、Span20、Tween20 时,形成白色乳状液,因为Span20 和Span80 的HLB 值小于9,Tween80、EL-40 和Tween20 的HLB 值都大于15,为了复配表面活性剂的需要,选择Tween80、EL-40、Span20 和Span80 作为本次试验的表面活性剂。
2.2 空白微乳的筛选
结果见表3和图1。当Tween80 和Span20 复配的HLB 值为9~12,且复合表面活性剂与IPM比值控制在8∶2 时,均不能形成微乳。当Tween80和Span20 复配的HLB 值为13~14,且复合表面活性剂与IPM 的质量比在8∶2 时,都可形成微乳,通过比较复配表面活性剂(Tween80/Span20)的HLB值在13 和14 时的微乳区域面积,发现当复合表面活性剂(Tween80/Span20)的HLB 值为14 时形成的微乳区域较大。当Tween80 和Span80 复配的HLB 值为13,且与IPM 的质量比在9∶1 时,可形成微乳,同时此组合形成的微乳区域在所有组合中的面积最小。当EL-40 和PEG-400 复配的HLB 值为13.5,且复合表面活性剂与IPM 的质量比在8∶2 时,可形成稳定的微乳体系。当EL-40和无水乙醇进行复配时,发现当HLBEL-40/无水乙醇=15时能形成稳定的微乳,然而该条件下形成的微乳区域较小。将制备的纳米微乳体系进行离心处理(4 000 r/min,15 min),不出现沉淀和分层,且将其继续稀释10 倍后,在稀释过程中保持澄清状态,因此选择Tween80/Span20 和EL-40/PEG-400 两个配方用于制备紫苏子油微乳。
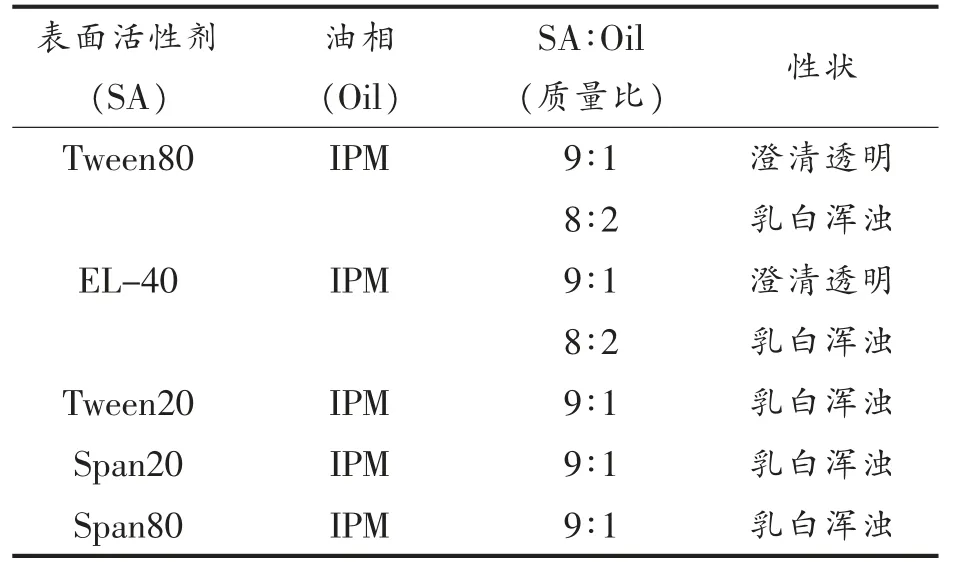
表2 单一表面活性剂筛选结果Table 2 Results of microemulsion by single surfactant

表3 空白微乳配方筛选结果Table 3 Results of blank microemulsion formula screening

图1 空白微乳筛选的伪三元相图Fig.1 Pseudo-ternary phase diagram of blank microemulsion formula screening
2.3 纳米微乳的制备
Tween80/Span20 制备的紫苏子油微乳在HLB=13.0 时,若将IPM 直接换成紫苏子油,则不能形成微乳,然而将IPM 与紫苏子油以3∶2 的质量比混合后可制备出微乳,可能是因为IPM 对紫苏子油具有一定的增溶作用(表4)。使用Tween80/Span20制备的紫苏子油微乳在HLB=14.0 时,将IPM 与紫苏子油质量比1∶1 混合后制备的微乳液载油量最高,此结论和筛选空白微乳时的结论一致,说明在相同条件下,空白微乳的筛选对紫苏子油的包载具有明确的指导意义。同理,以EL-40/PEG-400为表面活性剂制备的微乳与以Tween80 和Span20 制备的微乳情况相似。通过比较所制备的紫苏子油的微乳区域面积(图2),可得出SHLBTween80/Span20=14.0>SHLBTween80/Span20=13.0>SHLBEL-40/PEG-400=13.5。通过对所制备紫苏子油微乳的稳定性考察发现,其稳定性较好,因此Tween80/Span20 的表面活性剂组合最适合用于制备紫苏子油微乳。
2.4 微乳的类型鉴定
图3从左到右分别代表HLBTween80/Span20=13.0、HLBTween80/Span20=14.0、HLBEL-40/PEG-400=13.5 时的紫苏子油微乳体系,在制备好的紫苏油微乳中分别滴入苏丹Ⅲ溶液和亚甲基蓝溶液。结果表明,苏丹Ⅲ溶液一直滞留在微乳的表面,而亚甲基兰溶液慢慢扩散到整个微乳体系中,说明所制得的3 种微乳液都是O/W 型微乳。
2.5 微乳的粒径和电位
当复合表面活性剂Tween80/Span20 的HLB值为13 时制备的紫苏子油微乳,其液滴的平均粒径为458.6 nm,电位为-26.2 mV,PDI(聚合物分散系数)指数为0.517,此时形成的微乳粒径相对较大,PDI 较大,电位绝对值较小,可能是因为乳液滴间的静电屏蔽较小,微乳液滴间容易发生聚集(图4)。当Tween80/Span20 的HLB 值为14 时制备的紫苏子油微乳,其液滴的平均粒径为53.1 nm,PDI 为0.197,电位为-34.6 mV,此时形成的微乳粒径较小,乳滴间的静电屏蔽作用较大,可阻止乳滴间的桥连聚集,此时形成的微乳稳定性较好。当EL-40/PEG-400 的HLB 值为13.5 时制备的紫苏子油微乳,其液滴的平均粒径为69.16 nm,电位为-32.0 V,PDI 为0.281,此时形成的微乳的性质与Tween80/Span20 的HLB 值为14 时制备的微乳液相似,都具备较好的贮藏稳定性。

表4 紫苏子油微乳的制备Table 4 Preparation of perilla oil microemulsion
2.6 微乳的氧化稳定性
2.6.1 Fe3+标准曲线的绘制 对不同质量浓度Fe3+的测定结果如图5所示,结果表明,Fe3+在1.43~5.70 μg/mL 范围内线性良好。通过线性拟合可得,标准曲线的方程Y=0.1566x+0.0049,R2=0.9976。

图2 紫苏子油微乳的伪三元相图和实物图Fig.2 Pseudo-ternary phase diagram and photograph of perilla oil microemulsion

图3 紫苏子油微乳的类型鉴定结果Fig.3 Results of perilla oil microemulsion type identification
2.6.2 紫苏子油微乳的氧化稳定性分析 紫苏子油过氧化值(POV)可用于评估纳米乳剂中脂质氧化程度(图6)。通过试验可得,纳米乳液的过氧化值随贮藏时间的延长而上升。将贮藏15 d 后的纳米乳剂和紫苏子油相比,在37 ℃下贮存的紫苏子油过氧化值显著升高(P<0.05)。贮存15 d 后纳米乳剂的过氧化物值约为初始贮存阶段(1 d) 的3倍,而紫苏子油约为3.6 倍。通过比较不同配方制备的紫苏子油微乳的POV 值,发现3 种微乳的POV 值变化相似,且在贮藏15 d 后的POV 值均低于国家标准(9.85 mmol/kg)。表明紫苏子油制备成纳米乳液后可长期贮存,氧化稳定性较好。
3 结论
采用低能乳化法,以表面活性剂的HLB 值为指导对表面活性剂进行合理复配,再结合伪三元相图,筛选出性质稳定且载油量较大的微乳配方。表面活性剂组合为Tween80/Span20 和EL-40/PEG400 两种,当Tween80 和Span20 的HLB混=13~14 时,制备的空白微乳(以IPM 为油相)其微乳区域面积随混合表面活性剂HLB 值的增大而增大。同时,将该组合用于制备紫苏子油微乳时,发现在Tween80/Span20 复配表面活性剂的HLB值为14 时,制备出的微乳的区域面积最大;当EL-40 和PEG-400 的HLB混=13.5 时,也可制备稳定的空白微乳(以IPM 为油相)。将上述组合用于制备紫苏子油微乳时,Tween80/Span20 复配表面活性剂的HLB=14.0 时,制备出的微乳的区域面积最大,当EL-40/PEG-400 复配表面活性剂的HLB=13.5 时,制备出的微乳的区域面积最小。对所得紫苏子油微乳的类型进行鉴定可知,3 种配方工艺 (HLBTween80/Span20=13.0、HLBTween80/Span20=14.0、HLBEL-40/PEG-400=13.5)得到的微乳均为O/W 型乳剂,且3 种配方工艺制备的微乳的平均粒径分别为458.60,53.10,69.16 nm,电位为-26.2,-34.6,-32.0 mV,除了第1 种配方工艺,其它2 种配方制备的微乳粒径较小,电位的绝对值较大,再次佐证了所制备的微乳稳定性良好。最后,通过对比37 ℃贮存条件下的紫苏子油微乳和紫苏子油的POV 值,结果表明紫苏子油微乳具有较高的氧化稳定性。本研究制备的紫苏子油微乳在食品开发中的应用前景十分广阔,将具有生物活性的脂质运用在传递体系中,可能会产生各种生物功能效应,并可进一步研究如何增加紫苏子油微乳在胃肠体系中的生物利用度等问题。

图4 紫苏子油微乳的粒径和电位分析Fig.4 Particle size and Zeta potential analysis of perilla oil microemulsion

图5 Fe3+标准曲线结果Fig.5 Results of Fe3+ standard curve

图6 紫苏子油微乳在37 ℃下保存15 d 的过氧化值Fig.6 The peroxidation value of perilla oil microemulsion stored at 37 ℃for 15 days
