碳基含铁催化剂催化过氧化氢氧化去除对氯苯酚的试验研究
2021-05-12蔡博乔王蕾王红武
蔡博乔, 王蕾, 王红武
(1.同济大学 环境科学与工程学院, 上海 200092; 2.上海沁泰环境科技有限公司, 上海 201206)
对氯苯酚(4-CP)等酚类化合物是印染、 医药等行业废水中较为常见的有机污染物, 具有持久性、 致癌性等特点[1]。 铁基催化剂诱导芬顿反应处理废水已经被广泛应用于废水处理中。 Duan 等[2]利用共沉淀法制备了含有Fe3O4的磁性活性炭, Li等[3]、 王赫等[4]对废弃铁刨花进行了改性, Cheng等[5]利用水热还原法合成了介孔碳负载铁的催化剂。 尽管针对铁基催化剂的合成及改性等方面的研究较多, 但催化剂制备过程普遍较为复杂且成本较高。 因此, 低成本、 量产方便、 催化效果良好的催化剂吸引了研究者的关注。
本文针对自研发的一种成本低廉、 制作简便、可大规模量产的碳基含铁新型催化剂(HACO-P),开展其催化氧化性能研究。 以4-CP 为研究对象,在表征催化剂的形貌及结构的基础上, 分析单独HACO-P 型 催 化 剂 对4-CP 的 吸 附 作 用, 研 究HACO-P 型催化剂催化H2O2氧化4-CP 的效果,考察了污染物浓度、 催化剂投加量、 初始pH 值(pHini)及H2O2浓度对4-CP 降解效果的影响。
1 材料与方法
1.1 试验用水
试验中所使用的模拟废水为自行配制的不同浓度的4-CP 溶液。 当4-CP 质量浓度为2.0 g/L, 其TOC 质量浓度约为1 000 mg/L。
1.2 试剂及仪器
试 验 所 用4-CP、 Na2S2O3、 H2O2(30%)、 浓H2SO4等试剂均为分析纯, 所有溶液均使用超纯水配制。 试验仪器为: 高效液相色谱(HPLC, 安捷伦1260), 总有机碳分析仪(TOC-L CPH CN 200), 紫外分光光度计(TU1810 型)。
1.3 试验材料
HACO-P 型催化剂为自研发: 选取符合要求的活性炭粉末, 与氯化铁等溶液以2 ∶1 体积比进行混合, 加入氨水调节pH 值为7.0 ~8.0。 混合反应12 h 后去除固体混合物, 置于烘箱中105 ℃烘干,然后在500 ~600 ℃下真空加热反应8 h, 干燥冷却后用水洗净。 重复操作一次确保金属有效成分在活性炭表面分散。 制备完成的催化剂用去离子水清洗干燥后待用。
1.4 试验方法
1.4.1 催化氧化试验
试验在250 mL 锥形瓶中进行, 配制指定浓度的4-CP 溶液200 mL, 此时取样测定初始质量浓度(CO)。 采用磁力搅拌, 转速为200 r/min。 加入指定浓度HACO-P 型催化剂, 使用硫酸及氢氧化钠溶液调节初始pH 值至设定值, 待吸附30 min 后取样作为0 min 样品。 然后加入指定浓度的H2O2溶液, 分别在5、 15、 30、 60、 90、 120、 180、 240 min 时取2.0 mL 样品, 立即通过0.22 μm 水相针式聚醚砜滤头并加入50 μL 20 mol/L Na2S2O3溶液淬灭剩余的H2O2, 振荡混匀后将样品转移至4 ℃冰箱保存待后续分析。 对照组不添加催化剂或H2O2。所有试验均在室温下进行(约25 ℃)。
1.4.2 吸附试验
设定4-CP 初始质量浓度为0.1~4.0 g/L, 控制催化剂投加量为5.0 g/L, 取样测定水样中4-CP 浓度, 其余操作与1.4.1 节相同。
1.5 分析方法
利用扫描电子显微镜(SEM)、 X 射线衍射仪(XRD)、 X 射线光电子能谱(XPS)、 氮气吸附脱附(BET)对催化剂的表面形貌及元素组成、 比表面积等物理性质进行表征。
4-CP 采用高效液相色谱(HPLC)法测定, 分析条件为: 安捷伦XDB eclipse C-18(150 mm × 4.6 mm, 5 μm)色谱柱, 测定波长为280 nm, 流动相为甲醇和水, 比例为7 ∶3, 流速为0.8 mL/min。
TOC 浓度采用总有机碳分析仪测定。 总铁浓度采用电感耦合等离子体光谱仪测定。 H2O2浓度采用N,N-二乙基对苯二胺(DPD)分光光度法测定[6]。
2 结果与讨论
2.1 催化剂的表征结果

图1 HACO-P 催化剂的扫描电镜片Fig. 1 SEM photographs of HACO-P catalyst
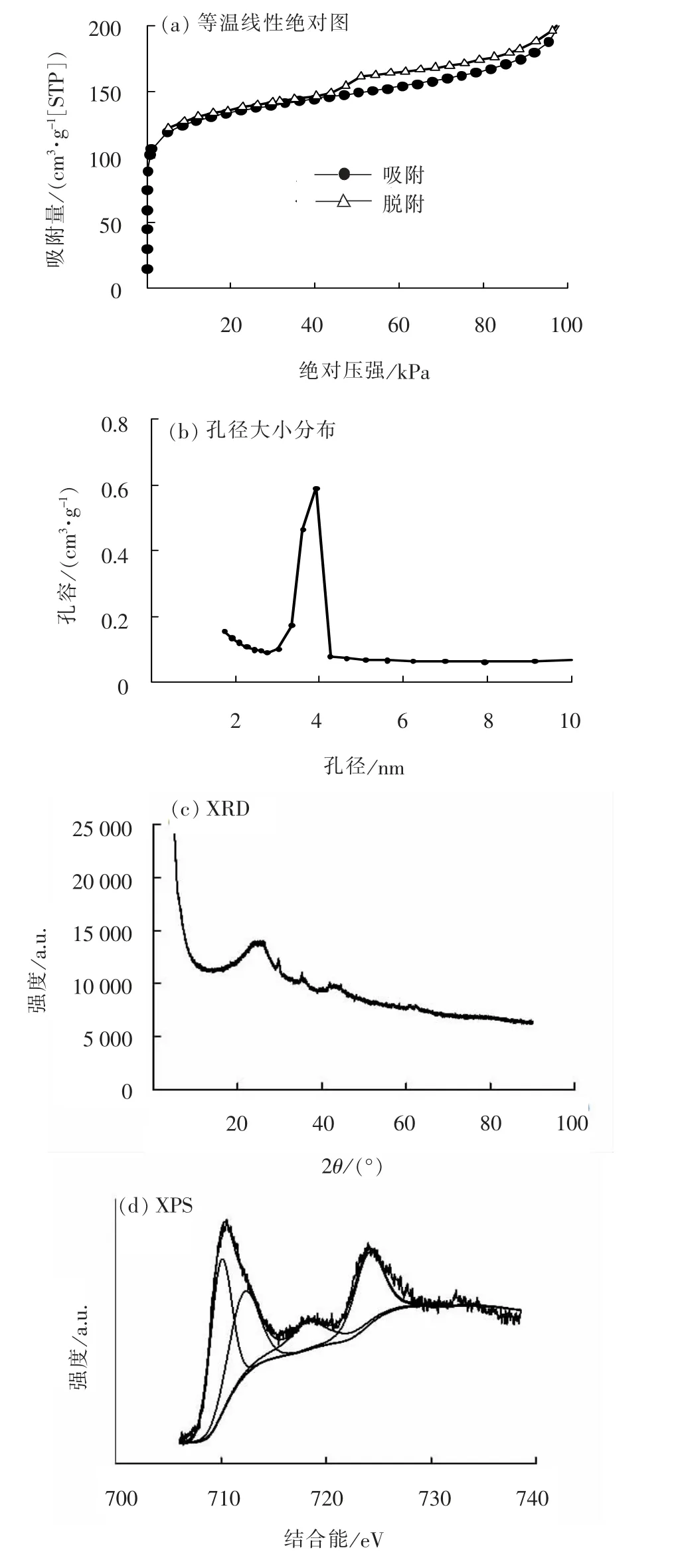
图2 HACO-P 催化剂比表面积、 XRD、 XPS 分析结果Fig. 2 Analysis results of HACO-P catalyst specific surface area, XRD and XPS
催化剂的表面形貌如图1、 图2 所示, 该催化剂表面分布着许多大小不同、 形状不规则且分散的块状物, 长度约为2 ~20 μm。 催化剂主要由碳(79.71%)、 氧(14.96%)、 铁(0.63%)、 钠、 镁、 铝、硅、 锰等元素组成, 含有丰富的介孔结构, 其比表面积达到了497.63 m2/g, 平均脱附孔径为2.42 nm,其中孔径分布曲线是根据BJH 方法[7]计算得到的N2脱附曲线。 XRD 分析结果(图2(c))表明催化剂含有的金属成分为FeO、 Fe2O3、 Fe3O4等铁氧化物及Mn3O4、 CaSiO3、 SiO2、 Na2SiO3等。 Fe2p 的XPS 分峰结果如图2(d)所示, 结合能为724.1 eV 的峰代表了Fe3O4的Fe2p1/2, 结合能为712.2 eV 的峰代表了Fe3+的Fe2p3/2, 结合能为718.3 eV 的峰则为Fe3+的卫星峰。 XPS 分峰结果表明催化剂中含有Fe2+及Fe3+, 与已报道的结果相一致[8-9]。
2.2 HACO-P 催化剂对4-CP 的吸附
HACO-P 催化剂具有介孔结构和较大的比表面积, 作为催化剂加入废水之后对于水中的污染物必然具有吸附作用。 为了明确催化氧化过程中催化剂的吸附作用对污染物去除效果的贡献, 考察了单独HACO-P 型催化剂(5.0 g/L)对不同初始浓度的4-CP 的吸附效果, 将溶液中残留的4-CP 浓度与初始浓度的比值对吸附时间作图, 结果如图3 所示。加入5.0 g/L 催化剂后, 溶液中4-CP 浓度迅速降低, 在5 min 后吸附速率逐渐减缓, 在30 min 时吸附已经基本达到平衡。 当4-CP 初始质量浓度为0.1 g/L 时, 4-CP 可全部通过吸附去除, 而随着4-CP 初始浓度增加, 催化剂吸附能力达到饱和, 4-CP 的吸附去除率逐渐下降。 4-CP 的吸附去除率与TOC 去除具有较好的相关性。
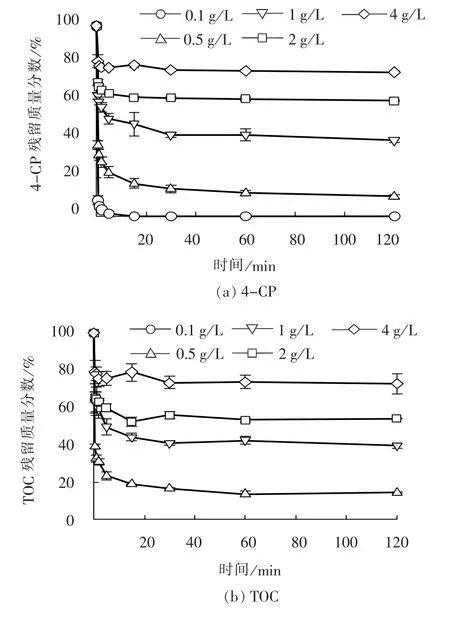
图3 吸附过程中4-CP 及TOC 残留质量分数Fig. 3 Residual mass fractions of 4-CP and TOC during adsorption.
2.3 吸附结果的等温线拟合
利用Langmuir(式(1))和Freundlich(式(2))等温模型对吸附数据进行拟合, 结果如图4 所示。 由图4 可知, 催化剂的吸附量随着4-CP 浓度增加而逐渐增加。
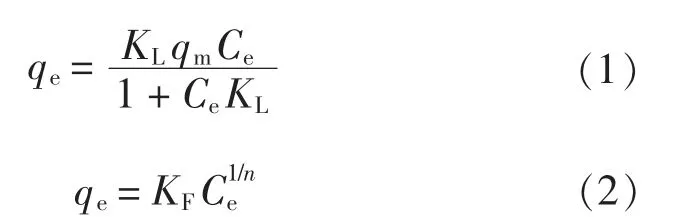
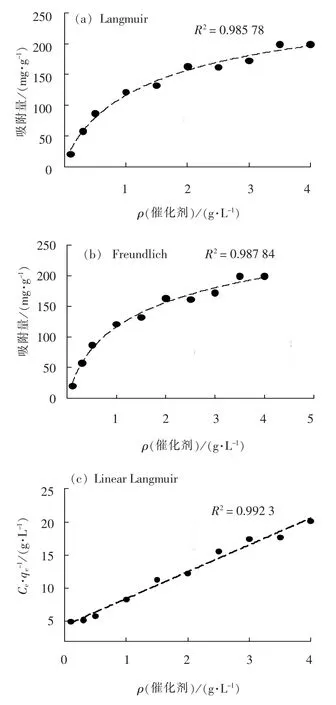

图 4 吸附数据的等温线拟合Fig. 4 Isotherm fitting of adsorption data
式中: KL是与焓相关的Langmuir 等温常数;qm是最大吸附容量, mg/g; KF是与吸附容量相关的Freundlich 常数, mg1-n·Ln/g; n 是与吸附强度有关的常数[2]。 Langmuir 和Freundlich 模型都能较好地描述HACO-P 催化剂对4-CP 的吸附过程, R2均超过了0.98。 Langmuir 模型拟合较好, 说明该吸附为单分子层吸附, 固体表面均匀, 被吸附分子相互间无作用力且吸附平衡为动态平衡, 此时qm为200 mg/g。 Freundlich 模型适用于异质表面, 并预测当液相中某些物质的浓度增加时, 吸附在固体表面上的离子物质的浓度会增加[10]; 模拟结果表明HACO-P 催化剂的n 值为1.792, 证明4-CP 较易被HACO-P 催化剂吸附, HACO-P 具有较好的吸附性能。 就线性模型来看, Langmuir 拟合略优于Freundlich 模型, R2分别是0.99 与0.97, 该结论与Duan 等[2]的研究结论相符。
2.4 HACO-P 催化剂投加量对试验结果的影响
在非均相催化氧化体系中, 催化剂投加量直接影响其对污染物的吸附效果, 同时也直接影响溶液中具有催化能力的活性成分的浓度, 因此, 在吸附平衡的基础上, 当H2O2投加量为3.4 g/L, 初始pH值控制为3.0 时, 考察了不同催化剂投加量下4-CP(2.0 g/L)的降解效果, 结果如图5 所示。 由图5 可知, 0 min 时吸附已达平衡, 此时溶液中4-CP 质量浓度已低于初始的2.0 g/L, 表明氧化开始前的30 min 内, 通过吸附去除的4-CP 的量随着催化剂投加量增加而逐渐增加, 吸附去除率从13% 增加到38%。 投加H2O2后, 催化氧化使4-CP 浓度迅速降低且降低速度与催化剂投加量呈正相关, 催化剂投加量高(>2 g/L)的试验组去除4-CP 的速率明显高于投加量低的试验组。 在整个过程中, 对照组亦观察到了约14.4%的4-CP 去除率, 这与Bao 等[8]的研究相一致, 说明单独H2O2对4-CP 的矿化能力很弱。 反应结束后, 所有试验组的pH 值均降到约1.8,对照组pH 值无明显变化, 这可能是因为HACO-P催化氧化过程产物中具有小分子有机酸(如甲酸、乙酸等), 它们的积累导致了pH 值的下降[11]。
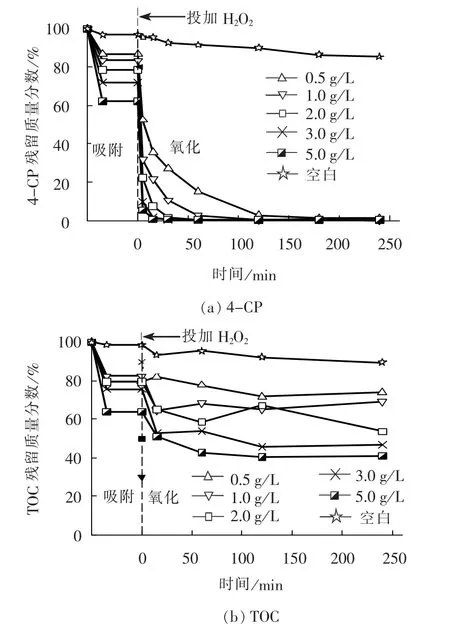
图5 不同催化剂投加量反应过程中4-CP 及TOC残留质量分数Fig. 5 Mass fraction changes of 4-CP and TOC residual during the reactions with different catalyst dosage
由图5(b)可知, 在0 min 前TOC 的去除原因为吸附, 且通过吸附去除的4-CP 随催化剂投加量增加而逐渐增加。 投加H2O2后TOC 得到去除的原因主要为氧化作用, 在催化剂投加量从0.5 g/L 变化至3.0 g/L 时, 能够一定程度上提高TOC 的去除率, 反 应2 h, TOC 去 除 率 可 从9.8% 提 升 至39.5%, 而将催化剂投加量继续提升至5 g/L, TOC的去除率反而略有下降, 为36.8%, 可见持续提高催化剂投加量无法持续提高4-CP 的矿化效果。 非均相反应必须在催化剂表面发生, 当催化剂投加量超过一定浓度后, 催化剂与H2O2的比例变高, 接触瞬间催化生成·OH, 由于·OH 存在时间极短,当其产生时间与有机物反应时间无法匹配时, 部分有机物还未来得及与·OH 接触, ·OH 即自我淬灭,因此催化剂投加量达到一定程度后继续增加催化剂投加量无法继续提高4-CP 的矿化效果。
2.5 初始pH 值对试验结果的影响
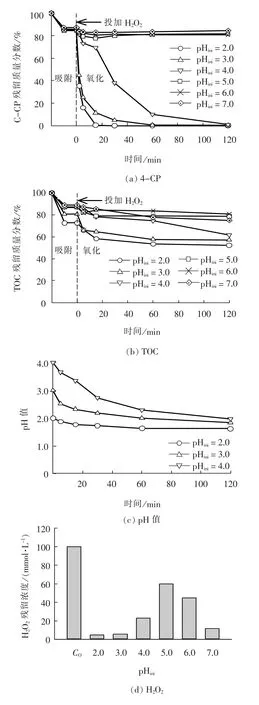
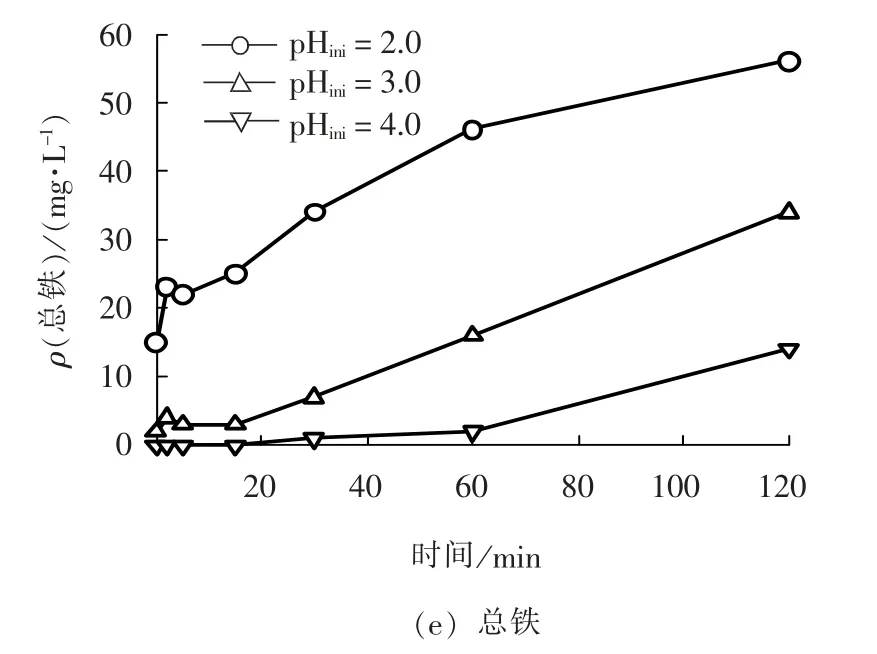
图6 初始pH 值对反应过程的影响Fig. 6 Effect of initial pH value on reaction
在催化剂投加量为2.0 g/L, H2O2投加量为3.4 g/L 条件下, 考察初始pH 值对试验结果的影响,结果如图6 所示。 当初始pH 值为2.0 ~4.0 时, 溶液中4-CP 转化速率逐渐下降, 结合TOC 的分析结果, 可知初始pH 值的降低能够一定程度上增加4-CP 的矿化率, 但大部分4-CP 只是被氧化为中间产物, 而非完全矿化。 当初始pH 值超过5.0 时,4-CP 的氧化去除则基本可以忽略。 图6(c)显示反应过程中体系pH 值随着反应的进行而逐渐降低,可佐证氧化过程中可能生成小分子有机酸, 而溶液pH 值降低, 催化剂表面的负载金属随之可更多地析出, 即pH 值越低, 溶液中的总铁浓度越高。H2O2残留浓度随着初始pH 值的增加而增加, 证实了pH 值可影响H2O2的利用效率。 在酸性条件下H2O2较稳定且催化氧化能力也更强, 初始pH 值为2 ~5 的时候随着pH 值的升高, H2O2自身稳定性降低且其催化氧化性能逐渐降低, 因此导致H2O2残留逐步升高, 初始pH 值超过5 后, H2O2的自我分解占主导[12]。
2.6 H2O2 投加量对试验结果的影响
为考察氧化剂浓度对催化氧化反应的影响, 在初始pH 值为3.0, HACO-P 催化剂投加量为2 g/L条件下, 考察H2O2投加量(1.7 ~17 g/L)对4-CP(2.0 g/L)去除效果的影响, 其中对照组未投加H2O2, 结果如图7 所示。 试验组4-CP 均在60 min内被完全转化。 随着H2O2投加量升高, 4-CP 转化速率越快, 当H2O2投加量大于8.5 g/L 时在5 min内即可转化绝大部分的4-CP。 H2O2投加量为17 g/L 时其反应速率低于13.6 g/L, 表明过高的H2O2浓度反而对芬顿反应有抑制作用, 主要原因为H2O2本身也是·OH 的淬灭剂, 过高浓度的H2O2能够与污染物竞争溶液中的·OH, 从而抑制了4-CP的氧化。
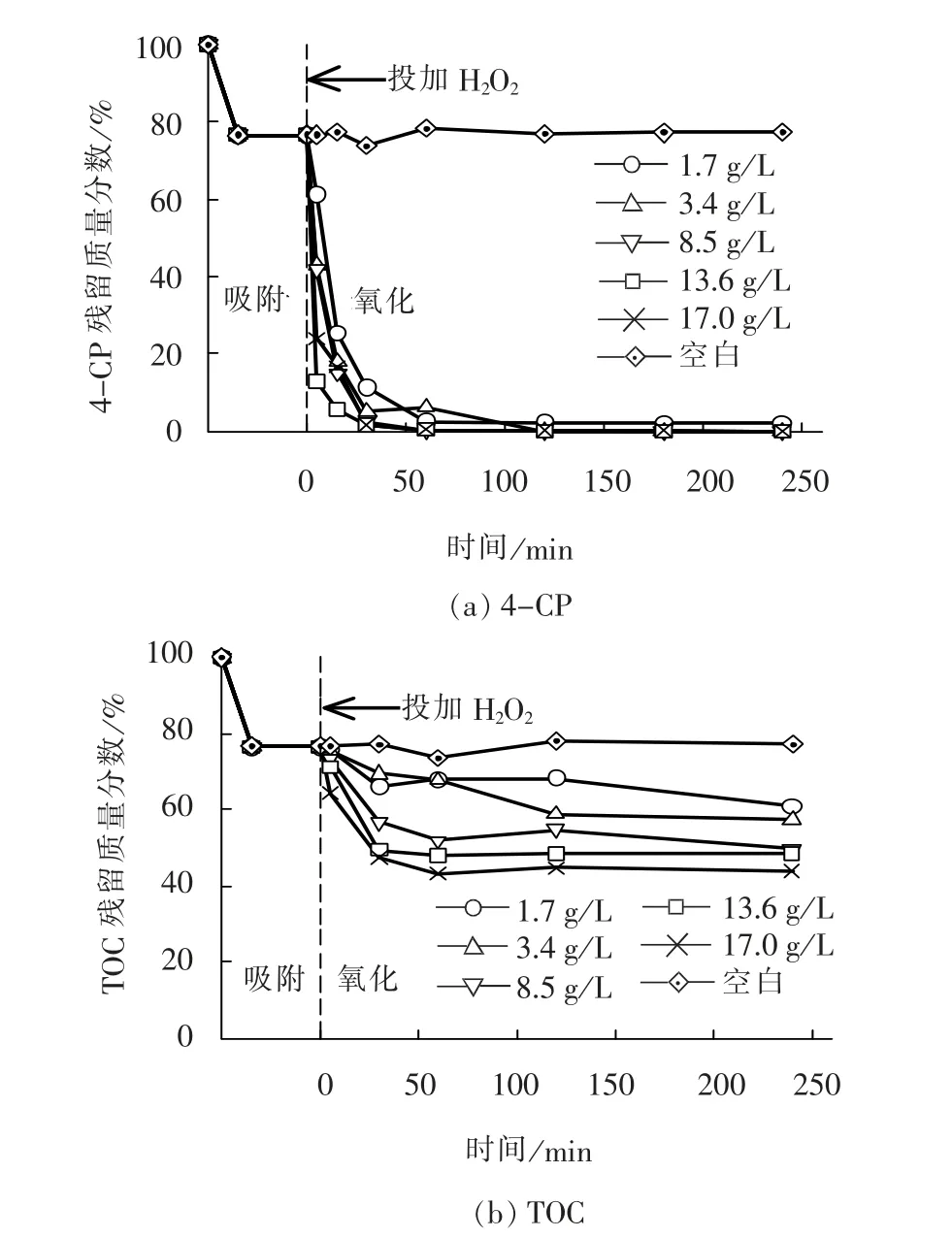
图7 H2O2 投加量对4-CP 及TOC 残留质量分数的影响Fig. 7 Effect of H2O2 dosage on 4-CP and TOC residual mass fractions
TOC 的去除率则随着H2O2浓度升高而不断增加, 但去除率均在60% 以下, 明显低于4-CP 的转化率, 表明仍有部分4-CP 只是被转化成为了其他物质而并没有被氧化完全。 如前文提到的, 当有机物被转化为小分子有机物如小分子酸等物质后,不易被吸附在催化剂表面, 因此即使提高H2O2浓度或延长反应时间, H2O2和有机物无法同时在催化剂表面出现, 故无法有效对小分子有机物进行氧化。
3 结论
HACO-P 型催化剂具有表面多孔、 比表面积大的特点, 利用Langmuir 和Freundlich 模型能够较好地拟合HACO-P 型催化剂对4-CP 的吸附, 其最大饱和吸附量为200 mg/g。 随着催化剂投加量的逐渐升高, 4-CP 去除速率也逐渐加快, 但存在一个最佳的催化剂投加量使得4-CP 的矿化度最好;较低的初始pH 值(2.0 ~5.0)更有利于4-CP 的氧化去除, 氧化过程中产生的小分子有机酸可导致pH值逐渐降低, 加速类芬顿反应的发生; 适当提高H2O2投加量对4-CP 的氧化及TOC 的去除具有明显促进作用, 但过高的H2O2浓度反而对芬顿反应有抑制作用。 综上, HACO-P 型催化剂具有良好的吸附性能和催化氧化活性, 具有商用前景。
