孕三烯酮联合自拟补肾化瘀方治疗肾虚血瘀型子宫内膜异位症疗效
2021-05-11李雅静
王 旺 毛 洁 陈 妍 左 婧 陈 琳 李雅静
南京中医药大学第二附属医院,江苏省第二中医院(南京,210000)
子宫内膜异位症(EMs)可导致不孕并伴局部浸润生长及转移等恶性肿瘤能力。多数研究认为,经血逆流、内膜种植、性激素紊乱及新生血管生成等共同参与其发病过程[1]。临床治疗EMs遵循在有效控制症状和抑制病变活动基础上,选择方便给药、可长期使用、毒副作用小的药物。孕三烯酮是治疗EMs常用激素类药物,能缓解症状但疗程长、不良反应多,可能使患者提前进入围绝经期。中医认为,EMs发病与脏腑失调、血液离经和血脉瘀阻相关[2]。肾藏精,主生殖,肾精亏虚则令胞脉、胞络、经络运行失常,血不循常道逆流于腹部,血滞成淤,故当以补肾填精,活血化瘀之法治之。本研究用自拟补肾化瘀方联合孕三烯酮治疗EMs,对患者用药前后性激素、血流变学、血清生化指标等进行观察,评估疗效并探索其可能药理学机制。
1 资料与方法
1.1 一般资料
采用方便抽样法,选择2017年11月-2020年11月本院妇科门诊及住院部收治的EMs患者。纳入标准:①经阴道B超、盆腔CT、实验室(癌抗原125、抗子宫内膜抗体)及术后病理检查确诊,符合EMs西医诊断标准[3];②符合《子宫内膜异位症中西医结合诊治指南》[4]中“肾虚血瘀”中医证型,主症:经行腹痛,腰骶胀痛;次症:月经量少、头晕失眠、性欲减退;舌脉向:舌黯淡,舌苔薄白,脉沉细;③年龄20~45岁;④开腹或腹腔镜手术治疗;⑤术后病理分型为深部浸润(或)卵巢型子宫内膜异位症;⑥近期无妊娠意愿;⑦患者及家属签署知情同意书。排除标准:①近3个月有激素类药物治史或行其他相关药物治疗;②合并子宫肌瘤或子宫腺肌症;③合并妇科恶性肿瘤;④存在肝、肾、心、脑及造血系统等严重基础疾病;⑤易过敏体质者或对本研究药物及成分过敏;⑥精神疾患不能配合治疗。研究经本院医学伦理委员会批准。
1.2 治疗方法
随机数字表法分组。对照组:口服孕三烯酮(华润紫竹药业有限公司,2.5mg),于术后首次月经来潮第1、4天服药,2.5mg/次,2次/周,连续用药3个月。观察组:在对照组用药基础上加用自拟补肾化瘀方,于术后首次月经来潮第1~5d用药。组方:取黄芪40g,丹参和菟丝子各20g,杜仲、五灵脂和川芎各15g,茯苓、赤芍、香附和牡丹皮各12g,桃仁9g,鸡内金、肉桂和甘草各6g。清水浸泡30min,武火煎沸后转文火煎熬,取汤汁400ml分2次服用,经期停服,连续用药3个月。
1.3 观察指标
1.3.1中医证候量化评分于用药前及用药后参照《中药新药临床研究指导原则》[5]中血瘀症的证候情况量化评分,中医症候包括经行腹痛、腰骶胀痛、头晕失眠、性欲减退按无、轻微、明显、严重分别计0、2、4、6分;月经量少按照未减少、轻微、明显减少分别计0、2、4分。
1.3.2实验室指标患者月经来潮第2~4d采集晨空腹静脉血分为3管。一管于室温下静置20min离心分离血清-80℃备用,酶联免疫吸附试验测定用药前后雌二醇(E2)、卵泡刺激素(FSH)、黄体生成素(LH)、血管内皮生长因子(VEGF)和基质金属蛋白酶-9(MMP-9)水平;一管采用放射免疫法测定癌抗原125(CA125)、前列腺素E2(PGE2)和前列腺素F2α(PGF2α)水平;一管用西斯美康XN-1000全自动血液分析仪测定用药前后全血高切黏度、全血低切黏度、血浆黏度和红细胞压积水平。
1.3.3痛经评分于用药前后参照疼痛视觉模拟评分(VAS)评估患者痛经程度,总分10分,0分表示无痛,10分表示剧痛。
1.3.4用药安全性及随访记录两组潮热、转氨酶升高、痤疮等不良反应,随访6个月统计复发率。
1.4 疗效评估标准
疗效评估标准[6],①痊愈:EMs症状和体征完全消失,影像学检查盆腔包块消失,中医症候评分减少≥90%;②显效:EMs症状和体征明显减轻,影像学检查盆腔包块消失,中医症候评分减少75%~89%;③有效:EMs症状和体征好转,影像学检查盆腔包块缩小,中医症候评分减少40%~74%;④无效:EMs症状和体征无明显改变或加重,影像学检查盆腔包块无变化或增大,中医症候评分减少<40%。总有效=痊愈+显效+有效。
1.5 统计学方法
2 结果
2.1 一般临床资料
观察组44例,年龄(32.3±4.6)岁(22~43岁),病程(17.3±3.1)月(6~29月);异位症分期(R-AFS)II期15例,III期19例,IV期10例。对照组44例,年龄(32.4±4.7)岁(23~45岁),病程(17.5±3.2)月(5~30月);R-AFSII期13例,III期22例,IV期9例。两组临床资料无差异(P>0.05)。
2.2 中医症候量化评分
用药前两组各项中医症候量化评分无差异(P>0.05),用药后各项评分均降低且观察组低于对照组(P<0.05)。见表1。

表1 两组用药前后中医症候量化评分对比(分,
2.3 性激素水平
E2、FSH、LH水平用药前两组无差异(P>0.05),用药后两组均下降且观察组降幅大于对照组(P<0.05)。见表2。
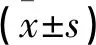
表2 两组用药前后性激素水平对比
2.4 血清生化指标
用药后对照组CA125、PGE2、PGF2α水平降低(P<0.05),VEGF和MMP-9水平与用药前无明显改变(P>0.05);观察组用药后CA125、PGE2、PGF2α、VEGF和MMP-9降低且均低于对照组(P<0.05)。见表3。
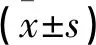
表3 两组用药前后血清生化指标对比
2.5 血液流变学指标
血液流变学指标用药前两组无差异(P>0.05);用药后两组均降低且观察组低于对照组(P<0.05)。见表4。
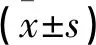
表4 两组用药前后血液流变学指标对比
2.6 痛经评分
用药前,痛经VAS评分观察组(5.61±1.06分)与对照组(5.54±1.04分)无差异(t=0.312,P=0.755);用药后观察组与对照组评分均降低(t=22.221、12.101,均P=0.000),且观察组(2.04±0.11分)低于对照组(3.52±0.38分)(t=24.816,P=0.000)。
2.7 临床疗效
治疗总有效率观察组高于对照组(χ2=5.899,P=0.015)。见表5。

表5 两组临床疗效对比[例(%)]
2.8 用药安全性及随访
不良反应发生率观察组与对照组无差异(χ2=0.693,P=0.405),复发率观察组低于对照组(χ2=6.506,P=0.011)。见表6。

表6 两组用药安全性及复发情况对比[例(%)]
3 讨论
EMs发病率为6%~10%,在慢性盆腔痛或不孕症女性中发病率为30%~50%[7]。EMs病变极具侵袭性和复发性,同时具备性激素依赖特征,故治疗困难。西医治疗EMs多以激素药物为主,以抑制排卵,减少周期性出血,促进异常子宫内膜萎缩。孕三烯酮属孕激素拮抗剂,能抑制EMs患者机体雌孕激素效应,并具备黄体酮对子宫内膜作用,促使子宫内膜及异位病灶细胞失活、退化,病灶萎缩。闫丽华[8]研究表明,孕三烯酮能较好控制EMs症状,患者停药后短期内月经可复朝,并使小病灶萎缩、消失,但易出现阴道干燥、痤疮、体重增加等不良反应。另外,长期使用激素会产生药物依赖性,停药后复发率高。
中医治疗妇科疾病积累了丰富经验,具有整体调节,辨证论治的独特优势。中医中并无EMs病名之记载,根据症状将其归入“癓瘕”、“痛经”、“无嗣”范畴,中医理论认为,EMs发病与肾脏相关。肾阳虚衰而血脉运行无力,血液凝滞而内滞为瘀,肾精亏虚则难养血脉,血脉涩行致血瘀。肾虚血瘀为其根本病机,基于“虚者补之,治必求本”原则,应以补肾填精,活血化瘀之法治之。
自拟补肾化瘀方由黄芪、川芎、丹参等中药组成,黄芪可补气固表,扶正活血;菟丝子为补肾之良药,能滋补肝肾,健脾固胎之功;丹参能活血祛瘀,通经止痛,三药共为君。川芎能补血活血,通经止痛;五灵脂有行血止痛之用;杜仲可补肝肾,安胎,与川芎和五灵脂共为臣药。茯苓有健脾利水,导滞化积之用;赤芍、牡丹皮、桃仁有清热凉血、活血散瘀止痛之效;香附可调经止痛;鸡内金有涩精止遗,软坚散结之效;肉桂可散寒止痛,温通经脉,上述中药共为佐药。甘草为使药,能补脾益气,缓急止痛,并有调和诸药之用。全方配伍,标本兼治,补先天肾气的同时,活血化瘀,调经止痛,散瘀滞,养胞宫。现代药理学表明,黄芪中异黄酮类活性成分能抑制VEGF表达,防止血管新生[9]。丹参有明显抗凝及改善血液微循环作用[10]。杜仲脾中环烯醚萜类成分通过激活雌激素受体α基因活性发挥调节雌激素作用[11]。五灵脂能抑制血小板聚集作用,可活血化瘀,多用于治疗淤血所致痛经[12]。孟广杰[13]等研究表明,赤芍与川芎配伍能降低血瘀模型大鼠全血高切黏度、全血低切黏度及血浆黏度,与牡丹皮配伍能抑制血小板聚集,延长血浆凝血酶时间,发挥活血作用。本研究结果显示,观察组经行腹痛、腰骶胀痛、月经量少、头晕失眠、性欲减退症候评分均低于对照组。说明在孕三烯酮用药基础上加用补肾、化瘀、活血类中药,能多靶点、多途径促进细胞凋亡,抑制血管新生及血小板聚集,从而进一步控制病情、改善症状。
现代医学研究认为,EMs是雌激素依赖性疾病,逆流入盆腔和腹腔内膜细胞在E2作用下可促进新生血管生成,使病灶形成[14]。罗芳[15]研究指出,性激素异常是引发EMs异位病灶出现周期性出血的诱因,使患者出现各种妇科疼痛症状,抑制局部高雌激素是控制EMs病情关键。本研究中,观察组用药后E2、FSH和LH水平均低于对照组。E2能抑制子宫内膜异位病灶细胞凋亡[16]。FSH和LH对评估生殖系统疾病疗效有重要意义。补肾化瘀方联合孕三烯酮治疗,能显著降低EMs患者性激素水平,推测与自拟补肾化瘀方中杜仲调节雌激素药理作用有关。本研究中,观察组用药后CA125、MMP-9、VEGF、PGE2和PGF2α水平均低于对照组。CA125与EMs发病密切相关。吴亚男[17]等研究证实,随着EMs患者R-AFS分期增加,血清CA125水平升高,可提示病情进展。异位内膜经过“黏附--侵袭--血管生成”生长为异位病灶,而血管生成为异位病灶定值、增值提供了有利条件。VEGF有促进子宫内血管新生作用,通过为异位内膜提供充足血氧而促进内膜生长[18]。细胞外基质降解有促进新生血管生成作用,MMP-9能促使基底膜、纤维连接蛋白和胶原降解,为异位子宫内膜细胞置入提供条件。机体内分泌系统紊乱,尤其是PGF2α水平异常升高是诱发EMs主要因素,并可导致全身血液循环障碍。孙阿梅[19]等研究指出,EMs患者PGE2和PGF2α多呈高表达,且水平异常升高与EMs所致痛经密切相关。用自拟补肾化瘀方联合孕三烯酮治疗EMs,能下调患者CA125、MMP-9、VEFG和前列腺素相关水平,推测与方中黄芪抑制血管新生作用有关,并在川芎、五灵脂、桃仁等活血化瘀类中药作用下促进异位内膜细胞凋亡,病灶萎缩。本研究中,观察组全血高切黏度、全血低切黏度、血浆黏度和红细胞压积与对照组比较明显降低。淤血浊液流注胞络胞脉之中,泛溢于子宫之外,发为EMs。有研究表明,机体微循环与血液流变学改变与淤血相关[20]。在孕三烯酮用药基础上加用补肾化瘀方中丹参、川芎和赤芍等中药可发挥活血化瘀之效,改善血液黏稠状态,加上杜仲调节性激素作用,使痛经症状得到明显缓解,本研究观察组用药后痛经评分低于对照组。本研究治疗总有效率观察组更高且疗效显著,分析原因是中西医联合治疗能发挥中药多靶点效应,标本兼治,二者起到协同增强作用提高疗效。转氨酶升高是孕三烯酮常见不良反应,本研究两组转氨酶升高占比均较其他不良反应高,就总体不良反应率两组未见差异,提示加用补肾化瘀方并未明显增加不良反应,用药安全。随访6个月,观察组复发率低于对照组,推测是联合用药药效持久,故减少了复发。
综上所述,临床用自拟补肾化瘀方合孕三烯酮治疗EMs能取得显著疗效,缓解患者痛经程度,其作用机制可能与自拟补肾化瘀方能进一步调节患者性激素指标,下调CA125、MMP-9、VEGF及前列腺素水平,改善血液流变学指标有关。
