SD大鼠正常胰腺MRI表现
2021-05-11李增晖张小明
梁 蕊,李增晖,张 菊,刘 佩,蒲 宇,朱 江,张小明*
(1.川北医学院附属医院放射科,四川 南充 637000;2.医学影像四川省重点实验室,四川 南充 637000;3.川北医学院药学院,四川 南充 637000)

图1 MRI 显示SD大鼠正常胰腺,绿色ROI为胰腺区域 A.T1WI; B.T2WI (①:肾脏;②:胰腺脾叶;③:脾脏;④:胃;⑤:肌肉;⑥:胰腺十二指肠叶)
胰腺是腹部重要脏器,胰腺疾病临床常见,其发病隐匿,难以早期诊断[1]。目前诊断胰腺疾病的常用影像学方法有超声、CT和MRI[2]。MRI具有极佳的软组织分辨率和多序列多参数成像等优势,可显示胰腺病灶位置、大小、信号特点等,评估胰腺疾病严重程度较超声及CT更为可靠、准确[3]。胰腺疾病基础研究常需采用相应动物模型。既往研究[4-6]发现大鼠胰腺分为3个解剖部分,即胃叶、脾叶及十二指肠叶,胃叶和脾叶沿胃背侧向脾脏和横结肠内脏表面延伸。MRI可用于评估大鼠胰腺形态及胰腺肿瘤、假性囊肿等病变[7]。本研究观察SD大鼠正常胰腺MRI表现,以期为研究胰腺疾病提供影像学基础。
1 材料与方法
1.1 动物 无特定病原体(specific pathogen free, SPF)级雄性SD大鼠9只,8~12周龄,体质量220~350 g,来自川北医学院实验动物中心[许可证编号:SYXK(川)2018-076]。本研究经实验动物学会福利伦理委员会批准(审批号:P20191226)。
1.2 仪器与方法 检查前停饲、停饮6~12 h[8]。扫描前10 min及扫描全程通过麻醉机(Midmark,Matrx VME2)给予异氟烷吸入麻醉(麻醉剂浓度1.50%~2.50%,氧流量500~700 ml/min)。将麻醉状态下的SD大鼠放入GE Discovery MR750 MR机,必要时加泡沫垫俯卧位保定,头先进,以大鼠专用线圈(Magtron,animal coil WK601)行MR扫描。序列及参数[9-12]:T1W,脂肪抑制快速扰相梯度回波序列,NEX 8,TR 105 ms,TE 3.5 ms,FOV 8.0 cm×8.0 cm,层厚1.0 mm;T2W,脂肪抑制快速自旋回波序列,NEX 8,TR 9 000 ms,TE 73.1 ms,FOV 8.0 cm×8.0 cm,层厚1.0 mm。
完成轴位、冠状位、矢状位平扫后,经大鼠尾静脉留置导管(Ⅱ-B,26 g×0.63in)以流率0.3 ml/s注射对比剂钆喷酸葡胺(Bayer AG,469.01 mg/ml) 0.2 mmol/kg体质量,行增强扫描,序列同平扫。

1.4 解剖和组织学观察 完成MR扫描后处死大鼠,观察正常胰腺位置、分布、形态及毗邻关系。分离并取出胰腺,常规固定后切片,行HE染色,观察胰腺组织内外分泌腺是否完整,有无出血、水肿及炎性细胞浸润等病理表现。
1.5 统计学分析 采用SPSS 25.0统计分析软件。符合正态分布的计量资料以±s表示,采用配对t检验进行比较。P<0.05为差异有统计学意义。
2 结果
9只大鼠中8只完成MR扫描,1只因麻醉死亡。
2.1 MRI表现 MRI显示大鼠胰腺位于胃、脾脏及左肾之间,分为胃叶、脾叶及十二指肠叶,汇合于胰腺结合部,轴位MRI可同时清晰显示胰腺脾叶及十二指肠叶,最大层面可见胰腺轮廓呈横置“Y”型。胰腺脾叶较厚,SI最高(5 272.50±438.20),紧贴脾脏内侧面;胰腺十二指肠叶较细长,SI为5 008.88±388.34,与十二指肠相连;胰腺胃叶薄而分散,SI最低(SI为4 660.63±335.00),向胃背侧延伸,与肠系膜及脂肪组织分界欠清。见图1、2。

图2 T1WI显示SD大鼠正常胰腺,绿色ROI为胰腺大致区域 A~C.分别为轴位、冠状位、矢状位平扫MRI图像;D~F.分别为轴位、冠状位、矢状位增强MRI (①:胰腺脾叶;②:肾脏;③:脾脏;④:肌肉;⑤:胃;⑥:肝脏;⑦:胰腺十二指肠叶;⑧:胰腺胃叶)
T1WI胰腺呈稍短T1信号,SI胰腺=4 980.50±1 087.21,邻近层面脾脏实质SI脾脏=4 493.75±833.65,同层面肌肉实质SI肌肉=3 651.13±525.33,SI胰腺高于SI脾脏(t=3.13,P=0.02)及SI肌肉(t=4.72,P<0.01)。SI胰腺/SI脾脏=1.11±0.09,SI胰腺/SI肌肉=1.36±0.20。
T2WI所示SI胰腺=(3 174.75±564.04)ms,邻近层面脾脏实质SI脾脏=4 274.63±949.57,同层面肌肉实质SI肌肉=2 694.13±566.70,SI胰腺低于SI脾脏(t=5.23,P<0.01)、高于SI肌肉(t=-4.04,P<0.01)。SI胰腺/SI脾脏=0.75±0.09,SI胰腺/SI肌肉=1.20±0.18。

增强前胰腺信号与同层面肌肉信号的CNR为9.97±6.57,增强后CNR升高至15.48±3.66(t=3.68,P<0.01),ΔCNR=5.52±4.24。
2.2 解剖及组织学表现 在大鼠腹部做“工”型开口,以镊子挑起胃后可见胰腺为淡粉色弥散器官(图3),呈倒置“Y”型或“三叶草”型,由胃叶、脾叶和十二指肠叶组成(7只大鼠胰腺有完整3个分叶,1只仅有脾叶及胃叶),汇合于胰腺结合部。胰腺结合部位在胆胰管周围,主要位于胆胰管和十二指肠降段之间。胰腺十二指肠叶位于空肠系膜起点和胆胰管之间,其周围可见十二指肠系膜;胰腺胃叶和脾叶体积较大,胃叶长径约(1.93±0.16)cm,脾叶长径约(1.54±0.13)cm,分别沿胃背侧及脾脏内侧表面延伸(图4)。
大鼠胰腺由外分泌腺和内分泌腺组成。低倍光镜下可见胰腺周围为疏松结缔组织,小叶间隔清晰;高倍光镜下胰腺腺泡及胰岛完整,少量导管及毛细血管显示;未见明显囊肿、钙化、水肿、出血、坏死、纤维化、肉芽组织及炎性细胞浸润,证实其为正常胰腺组织;见图5。
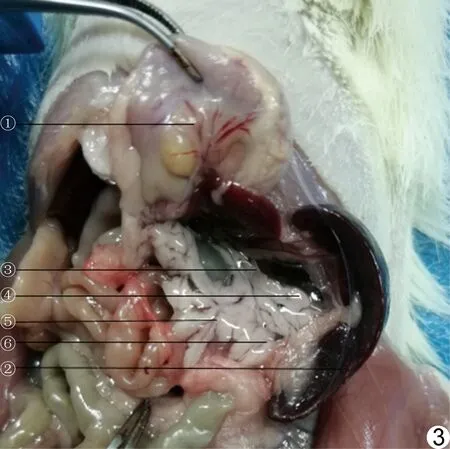
图3 SD大鼠腹部解剖图 腹部“工”型开口后腹腔视野显示胰腺形态、分布及位置毗邻 (①:胃;②:脾;③:胰腺胃叶;④:胰腺脾叶;⑤:胰腺十二指肠叶;⑥:胰腺结合部)
3 讨论
SD大鼠是胰腺疾病基础研究中常用实验动物。本研究观察SD大鼠正常胰腺MRI特点,旨在为MR研究大鼠胰腺疾病模型提供参考。

图4 SD大鼠胰腺经Bounin液固定后大体标本 (①:胰腺胃叶;②:胰腺脾叶;③:胰腺十二指肠叶;④:胰腺结合部)
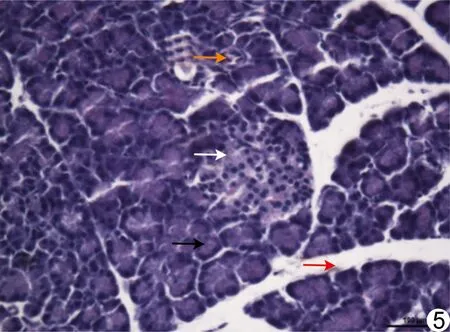
图5 SD大鼠正常胰腺组织病理图(HE,×400) 腺泡(黑箭)及胰岛(白箭)结构完整,毛细血管(橙箭)及小叶内导管(红箭)清晰可见
SD大鼠正常胰腺多由胃叶、脾叶和十二指肠叶组成,3叶不仅长度各异,SI亦有所不同。本组大鼠胰腺脾叶SI最高,原因可能为脾叶较厚、受部分容积效应影响小,腺泡细胞及其分泌的胰蛋白酶含量较多,同时脾叶内水含量高,氢质子含量亦高;十二指肠叶及胃叶SI依次降低,原因可能是十二指肠叶纤细,胃叶更加菲薄,受部分容积效应影响大,腺泡细胞含量依次减少,分泌胰蛋白酶亦减少,而系膜及结缔组织含量依次增加,水含量较少,氢质子含量亦少。胰腺3叶间胰腺导管分布不同也可能导致SI差异,因胰腺导管上皮细胞可分泌富含碳酸氢根的液体到管腔内,抑制不成熟胰蛋白酶原激活,并可将消化酶输出胰腺[13-14]。T2WI上,腹膜后有液体时,胰腺区域呈高信号,此时胰腺本身信号易被掩盖而不利于观察。本组多数大鼠胰腺呈横置“Y”型,其T1WI的SI于高于脾脏及同层肌肉,T2WI的SI低于脾脏但高于同层肌肉;增强后胰腺SI与脾脏SI相近,与同层肌肉SI差异具有统计学意义,可能与胰腺腺泡细胞含有丰富的内质网组织有关,亦可能与胰腺分泌液中蛋白含量高及存在某些顺磁性物质有关,有待进一步探索。MRI上述信号差异有助于区分胰腺与毗邻脏器、准确定位病灶。
本组8只大鼠中,7只胰腺有完整的3个分叶,1只胰腺仅有脾叶及胃叶,可能为解剖变异。肖波等[15]研究发现小型猪胰腺有3个分叶,呈倒“Y”字形或“人”字型。大鼠胰腺形态与小型猪胰腺相似,二者均与呈长条形的人类胰腺显著不同。物种之间胰腺形态学差异可能提示生物进化中胰腺结构由繁到简的过程。
本研究的主要不足之处:①样本量少;②SD大鼠胰腺组织过于分散,单层面MRI无法显示其整体形态,三维重建等后处理方法或可显示更清晰。总之,MRI显示大鼠正常胰腺效果良好,易于观察各叶形态、位置及SI。本研究初步认识大鼠正常胰腺MRI表现,可为SD大鼠胰腺疾病模型研究提供影像学基础。
