15例帕博利珠单抗致免疫相关性心肌炎的病例分析
2021-04-27黄光明贺盛发黄振光张宏亮
黄光明 贺盛发 黄振光 张宏亮
摘 要 目的:了解帕博利珠單抗致免疫相关性心肌炎发生的规律和特点,为临床合理用药提供参考。方法:以“帕博利珠单抗/可瑞达”和“心肌炎”“心脏毒性”,“Pembrolizumab/Keytruda”和“Cardiac toxicity”“Myocarditis”“Cardiotoxity”“Cardiotoxicity”等为中英文检索词,检索中国生物医学文献数据库、维普网、中国知网、万方数据、PubMed、Wiley Online Library、Embase等数据库中收录的帕博利珠单抗致免疫相关性心肌炎的个案报道,检索时限从建库起至2020年8月。剔除疑似病例文献和重复文献后,对纳入文献中患者性别、年龄、用药原因、既往病史、联合用药、用药剂量、不良反应(ADR)发生时间、临床表现、干预措施与转归等信息进行分析。结果与结论:共纳入15篇文献,其中英文13篇、中文2篇;涉及15例患者,其中男性12例、女性3例,平均年龄为71.35岁;临床诊断非小细胞肺癌4例,黑色素瘤4例,膀胱癌2例,尿路上皮癌、多发性骨髓瘤、胃癌、胸腺癌、鼻咽癌各1例;有6例患者记录了既往病史,其中5例无心脏疾病史,1例既往患有高血压、高血脂;有9例患者记录了联合用药情况;有12例患者详细记录了帕博利珠单抗的用药剂量和频次。93.3%患者的免疫性心肌炎出现在应用帕博利珠单抗第1~2周期用药后,平均发生时间为末次用药后15.5天;最常见临床症状为呼吸困难、乏力、头晕或晕厥等;9例患者心电图检查显示心脏传导阻滞;所有患者都使用了糖皮质激素处理;5例患者经住院治疗后死亡,其中1例患者在心肌炎控制后重启帕博利珠单抗治疗1周期,心肌炎复发并最终死于该ADR。结论:在患者使用帕博利珠单抗免疫治疗时,建议做好心脏功能相关基线检查和常规监测,一旦怀疑出现免疫相关性心肌炎,应及时完善心电图等心功能相关检查,并尽早使用大剂量糖皮质激素治疗,同时应警惕再次用药后心肌炎复发致死的风险。
关键词 免疫检查点抑制剂;帕博利珠单抗;免疫相关性心肌炎;不良反应;病例分析
中图分类号 R969.3 文献标志码 A 文章编号 1001-0408(2021)06-0729-07
ABSTRACT OBJECTIVE:To investigate the rules and characteristics of pembrolizumab-induced immune-related myocarditis, and to provide reference for rational drug use in clinic. METHODS: Using “pembrolizumab/keytruda”“myocarditis”“cardiotoxicity”“Pembrolizumab/Keytruda”“Cardiac toxicity”“Myocarditis”“Cardiotoxity”“Cardiotoxicity” as Chinese and English retrieval words, CBM, VIP, CNKI, Wanfang database, PubMed, Wiley Online Library and Embase database were searched on the case reports of pembrolizumab-induced immune-related myocarditis during the inception to Aug. 2020. After eliminating the suspected case literature and repetitive literature, gender, age, medication cause, medical history, drug combination, drug dosage, occurrence time of ADR, clinical manifestation, intervention measure and outcome of patients in the included literature were analyzed. RESULTS & CONCLUSIONS: A total of 15 literatures were included, involving 13 English literatures and 2 Chinese literatures. Totally 15 patients were involved, including 12 males and 3 females, with an average age of 71.35 years. There were 4 cases of non-small cell lung cancer, 4 cases of melanoma, 2 cases of bladder cancer, 1 case of urothelial cancer, 1 case of multiple osteosarcomas, 1 case of gastric cancer, 1 case of thymic cancer, 1 case of nasopharyngeal carcinoma. There were 6 patients with previous medical history, of which 5 had no history of heart disease and 1 had hypertension and hyperlipidemia; there were 9 patients recorded the combined use of drugs; the dosage and frequency of pembrolizumab were recorded in 12 patients. Immunological myocarditis of 93.3% patients occurred after the first to second cycle of pembrolizumab administration, and the average occurrence time was 15.5 days after the last administration. The most common clinical symptoms were dyspnea, fatigue, dizziness or syncope. 9 patients showed cardiac block on electrocardiogram. All patients were treated with glucocorticoids when they developed immune-associated myocarditis, and 5 patients died after hospitalization; another one patient was restarted with pembrolizumab for one cycle after control of immune-related myocarditis, but developed a recurrence of myocarditis and died of myocarditis ADR. It is suggested that baseline examination and routine monitoring of cardiac function should be done well when patients are treated with pembrolizumab. Once the patient is suspected to have immune-related myocarditis, they should timely improve the cardiograms and other cardiac function-related tests, and start the treatment of high-dose glucocorticoids as soon as possible, and are alert to the risk of death due to recurrence of myocarditis after readministration.
KEYWORDS Immune checkpoint inhibitors;Pembroli- zumab; Immune-related myocarditis; ADR; Case analysis
免疫检查点抑制劑(Immune checkpoint inhibitors,ICIs)是近年来在抗肿瘤领域中出现的一类新的治疗药物,主要包括细胞毒性T淋巴细胞相关抗原4(CTLA-4)、程序性死亡1(PD-1)和程序性死亡配体1(PD-L1)等[1]。帕博利珠单抗(Pembrolizumab)是一种针对PD-1的单克隆抗体,于2014年9月被美国FDA批准用于经伊普利单抗(Ipilimumab)治疗复发的不可切除或转移性黑色素瘤的二线治疗,并于2018年7月26日在我国上市,商品名为可瑞达。随着临床研究的广泛开展,帕博利珠单抗的适应证也扩展到晚期非小细胞肺癌、经典霍奇金淋巴瘤、晚期尿路上皮膀胱癌、头颈部鳞状细胞癌和微卫星不稳定性高的实体瘤等多种恶性肿瘤[2]。该药具有较强抗肿瘤作用,能提高患者生存质量、延长其生存时间,但在临床使用过程中也可能引发各种免疫相关性不良反应(ADR),如皮疹、肺炎、垂体炎、结肠炎、肝炎、心肌炎等,其中免疫相关性心肌炎的发生率虽然较低,但后果较为严重,甚至可能导致患者死亡[3]。为了解帕博利珠单抗致免疫相关性心肌炎发生的规律和特点,本研究对国内外已发表的帕博利珠单抗致免疫相关性心肌炎的ADR个案报道进行分析、总结,旨在为其临床合理使用提供参考。
1 资料来源与数据处理
检索中国生物医学文献数据库、维普网、中国知网、万方数据、PubMed、Wiley Online Library、Embase等数据库中收录的帕博利珠单抗致免疫相关性心肌炎的个案报道,中文检索词为“帕博利珠单抗/可瑞达”和“心肌炎”“心脏毒性”,英文检索词为“Pembrolizumab/Keytruda”和“Cardiac toxicity”“Myocarditis”“Cardiotoxity”“Cardiotoxicity”。文献发表范围为全世界,语种限定为中文和英文,检索时限均为建库起至2020年8月。剔除疑似病例文献和重复文献。
仔细阅读纳入文献,提取患者性别、年龄、用药原因、既往病史、联合用药、用药剂量、ADR发生时间、临床表现、并发症、心功能相关检查、干预措施与转归等有效信息,使用Excel 2013软件进行统计,分析该ADR的特点和规律。
2 结果
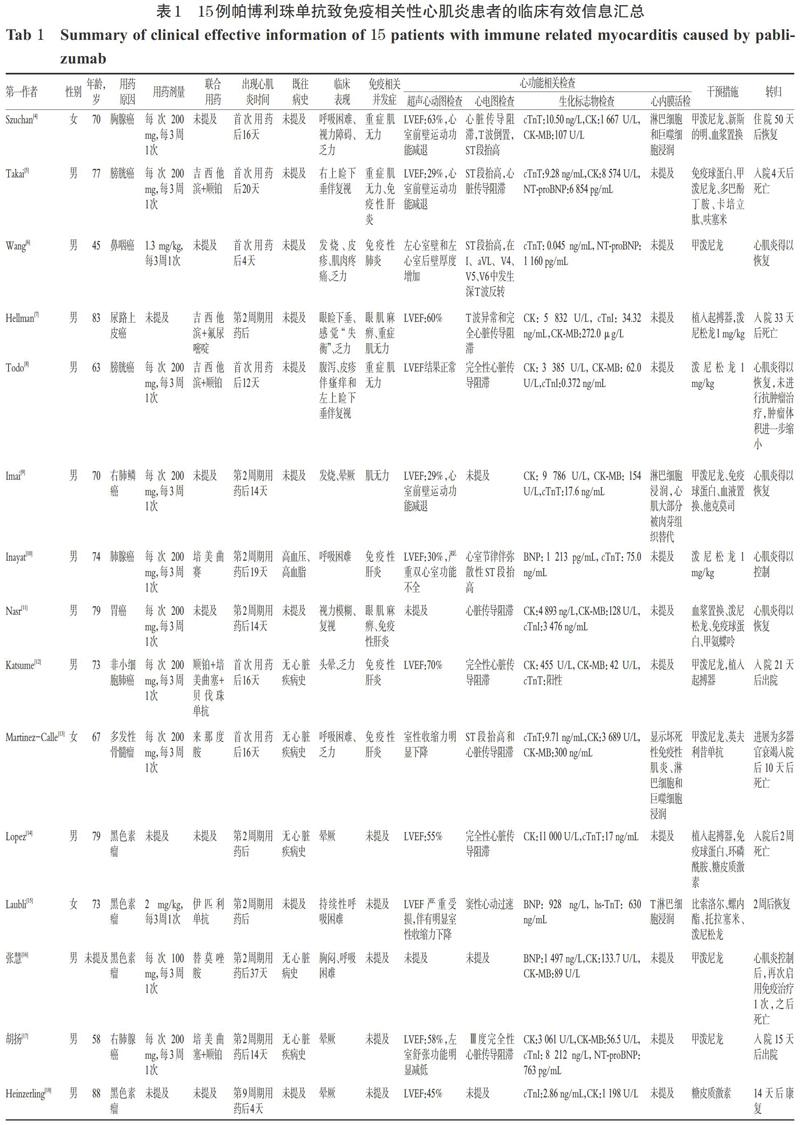
最终纳入文献15篇[4-18],其中英文文献13篇[4-15,18]、中文文献2篇[16-17];涉及患者15例,其临床有效信息见表1(表中,LVEF:左室射血分数;BNP:脑钠肽;CK:肌酸激酶;CK-MB:磷酸肌酸同工酶;cTnI:心肌肌钙蛋白I;cTnT:心肌肌钙蛋白T;hs-TnT:高敏心肌肌钙蛋白T;NT-proBNP:N端脑钠肽前体)。
2.1 性别和年龄
15例患者中,男性12例、女性3例。除1例仅提示为老年患者未记录具体年龄外,其余14例都详细记录了年龄,年龄分布为45~88岁,平均年龄为71.35岁,其中≥60岁的患者有12例、≥70岁的患者有10例。
2.2 用药原因和既往病史
15例患者临床诊断包含非小细胞肺癌4例,黑色素瘤4例,膀胱癌2例,尿路上皮癌、多发性骨髓瘤、胃癌、胸腺癌、鼻咽癌各1例。有6例患者记录了既往病史,其中5例患者无心脏疾病史,既往检查心功能正常;只有1例患者既往患有高血压、高血脂。
2.3 联合用药、用药剂量及ADR发生的时间
15例患者中,有9例记录了帕博利珠单抗联合用药情况,其中联合吉西他滨+顺铂2例,联合吉西他滨+氟尿嘧啶、培美曲塞、顺铂+培美曲塞+贝伐珠单抗、来那度胺、伊匹利单抗、替莫唑胺、培美曲塞+顺铂各1例。除3例患者未提及帕博利珠单抗用药剂量外,其余12例患者均详细记录了帕博利珠单抗的用药剂量和给药频次,其中给药剂量为每次200 mg的患者有9例,每次100 mg、1.3 mg/kg、2 mg/kg的患者各1例,给药频次均为每3周给药1次。15例患者中,有14例心肌炎发生时间在使用帕博利珠单抗第1~2周期(每3周为1个周期)用药后,其中有6例发生在首次用药后,8例发生在第2周期用药后;另有1例发生于第9周期用药后。有12例患者记录了末次用药与心肌炎发生的间隔时间,最早发生时间在末次用药后4天,最晚发生时间在末次用药后37天,平均发生时间为末次用药后的15.5天。
2.4 临床症状和实验室检查情况
15例心肌炎患者中,最常见临床症状包括呼吸困难(5例)、乏力(5例)、头晕或晕厥(5例)、眼睑下垂(3例)、复视或视力障碍(4例),还有部分患者伴有发烧、胸闷、肌肉疼痛、腹泻等。其他免疫相关并发症主要包括肌无力或重症肌无力、免疫性肝炎、眼肌麻痹、免疫性肺炎等。有13例患者报道了超声心动图检查情况,发现4例出现心室壁运动障碍,5例患者LVEF严重受损或不高于45%,其中有3例明确注明LVEF低于35%(重度收缩功能障碍)。有12例患者报道了心电图检查情况,发现有9例出现心脏传导阻滞,5例ST段抬高,还有部分患者出现窦性心动过速、T波异常等心律失常症状。所有患者都监测了cTnI或cTnT、CK、BNP等生化标志物,发现所有心肌炎患者心力衰竭相关生化标志物检测值都明显增高。另有4例患者报道了心肌活检情况,发现其心肌细胞遭到了淋巴细胞和巨噬细胞浸润。
2.5 干预措施与转归
15例患者在出现心肌炎时都及时给予了糖皮质激素(泼尼松龙或甲泼尼龙)治疗。此外,有5例患者除了使用糖皮质激素外还联合免疫球蛋白、环磷酰胺、他克莫司或英夫利昔单抗等免疫制剂治疗,其中仅有2例患者的心肌炎得到了控制;有3例患者接受了血浆置换等透析治疗,且心功能都得到了恢复;有3例患者接受了紧急起搏器放置的处理,结果有2例患者死亡。15例心肌炎患者中,有5例经住院治疗后仍死亡,其中有1例在心肌炎控制后重启帕博利珠单抗治疗1周期再次出现免疫相关性心肌炎并最终死于该ADR;另10例患者经住院治疗后,心肌炎得到了控制。
2.6 用药关联性
15例患者免疫相关性心肌炎发生时间与帕博利珠单抗用药时间顺序合理,根据我国药品ADR评价细则[19],其免疫相关性心肌炎与帕博利珠单抗的关联性评价均为“可能”。
3 分析与讨论
3.1 可能机制
帕博利珠单抗等ICIs引發免疫相关性心肌炎的具体机制尚不完全明确,可能与免疫激活和自身抗体的产生有关:在正常情况下,PD-L1与PD-1的相互作用会下调T淋巴细胞活性,阻止自身免疫;使用ICIs后,激活的T淋巴细胞除了识别肿瘤抗原外,还可与心脏等非靶器官的免疫检查点结合,促进非靶器官产生自身抗体,引起心肌炎症细胞浸润和心肌纤维化,从而导致心肌炎的发生[3]。在心肌组织中,上调PD-L1可作为细胞因子的保护机制,以减少心脏在应激和疾病状态下T淋巴细胞介导的炎症反应[20]。免疫检查点上调可能是T淋巴细胞侵袭的抑制信号,ICIs则抑制了心脏的这种自我保护机制,从而导致心肌炎的发生[21]。有研究发现,PD-1基因缺陷小鼠可因自身产生免疫球蛋白G(IgG)抗体而引起扩张型心肌病,导致严重的心肌收缩障碍;进一步分析发现,该自身抗体可与cTnI作用,使心肌细胞内Ca2+流动性增强,使心脏扩大、心室壁变薄并影响心肌细胞的功能[22]。另外,PD-1基因缺陷小鼠还可产生高滴度肌球蛋白抗体,导致心脏中CD4+、CD8+T淋巴细胞和髓样细胞浸润,引发致死性淋巴细胞浸润性心肌炎[23]。这进一步说明了PD-1等免疫检查点可能是导致自身免疫性疾病的重要因子。
3.2 年龄、病史、联合用药
已有研究报道,帕博利珠单抗引起的心肌炎发生率为0.06%~2.40%,易发生于老年患者[3]。年龄是心脏毒性的独立危险因素,大于60岁的患者更易发生[24-25]。本研究结果也显示,帕博利珠单抗致免疫相关性心肌炎患者中,60岁及以上患者占80.0%(12/15)。既往病史分析发现,大部分患者既往都无高血压、高血脂、心脏病等心血管疾病,提示心血管病史可能并不是该药导致免疫相关性心肌炎的独立危险因素。已有研究报道,培美曲塞、氟尿嘧啶、卡培他滨和金属铂类等传统化疗药物可诱发缺血性心脏病等心脏毒性[26-27]。贝伐珠单抗是一种抗血管内皮因子靶向药物,可引起充血性心力衰竭和室上性心动过速等心脏疾病,发生率为1%~10%[26]。ICIs联合其他化疗药物治疗可使患者发生致死性心肌炎的风险更高[28]。研究报道,多种ICIs联合用药、ICIs联合其他心脏毒性药物、心脏抗原在肿瘤中的表达、既往有自身免疫性疾病、遗传等都是导致免疫相关性心肌炎发生的危险因素[29]。本研究结果显示,属于两种ICIs联合用药的病例有1例,属于ICIs联合金属铂、氟尿嘧啶、培美曲塞等有心脏毒性药物的病例有6例。
3.3 给药剂量、发生时间
关于帕博利珠单抗给药剂量,其药品说明书中推荐剂量为200 mg,儿童剂量为2 mg/kg,每3周1次(即每3周为1个周期)。已有研究报道,帕博利珠单抗致腹泻、皮疹等免疫相关ADR与用药剂量无相关性,免疫性心肌炎与用药剂量是否有关尚无确切证据[30]。本研究中有9例患者明确指出给药剂量为每次200 mg,符合药品说明书推荐;另有3例患者的用药剂量较推荐剂量低。分析ADR发生时间发现,93.3%的患者(14/15)心肌炎出现在第1~2周期用药后,平均发生时间为末次用药后15.5天,这可能与帕博利珠单抗的半衰期长(t1/2为21~25 d)有关。Moslehi等[31]研究表明,在101例经ICIs治疗后发生严重心肌炎的患者中,出现严重心肌炎的中位时间是27 d(5~155 d),76%的患者心肌炎发生在用药前6周,64%的患者在心肌炎发作前仅接受过1次或2次ICIs治疗,总体病死率高达46%。另一项包含42例病例的研究显示,33%的患者的心肌炎发生在单剂ICIs治疗后,其中29%发生在两剂后[32]。这说明免疫性心肌炎更容易出现在用药早期,临床应在用药时尤其是用药早期予以重视。
3.4 临床表现和心功能检查特点
本研究结果显示,免疫相关性心肌炎的临床表现形式多样且不具有特异性,最常见的临床表现为呼吸困难、乏力、头晕或晕厥等。一项包括15例患者的研究报道指出,发生免疫相关性心脏毒性患者中,53.3%的患者同时发生了3~4级累及其他系统的ADR,其中最常见的是自身免疫性肝炎和肌炎[33]。cTnI/cTnT和CK水平是心肌损伤的敏感和特异性标志物[34]。Mahmood等[35]学者研究指出,100%的免疫相关性心肌炎患者都出现了cTnT不同程度的升高,66%的患者出现了NT-proBNP升高。另一项包含56例免疫相关心肌炎患者的研究显示,93.3%的患者出现cTnT升高,100%的患者CK、CK-MB、BNP及肌红蛋白出现升高[36]。本研究结果显示,所有患者的cTnI或cTnT、CK、BNP等生化标志物都出现明显增高,提示一旦患者怀疑为免疫相关性心肌炎,临床应及时完善心肌生化标志物等检查,以便进一步确诊和对症处理。
超声心动图和心电图变化是评估继发于心肌炎结构和功能变化的重要工具,可以排除心力衰竭、心包渗出和腔内血栓等其他原因[37]。一项包含42例免疫性心肌炎病例的研究显示,64%的患者及50%的死亡患者的LVEF在正常范围内,提示免疫相关性心肌炎患者的超声心动图和心电图表现并无特异性[32]。本研究显示,11例报道了LVEF结果的病例中,有54.5%(6/11)的患者LVEF在正常范围(50%~70%)内。Palaskas等[38]学者认为LVEF正常并不能排除免疫相关性心肌炎的诊断。有研究报道,免疫相关性心肌炎心电图变化同样不具有特异性[39]。但Atallah-yunes 等[32]学者的研究显示,有36%的免疫相关性心肌炎病例和64%的死亡病例与完全性心脏传导阻滞有关。本研究也发现,有60%(9/15)的病例和80%(4/5)的死亡病例与心脏传导阻滞有关。心内膜活检是心肌炎诊断的“金标准”,由于其高风险而很少使用。根据达拉斯标准,心肌炎的诊断是有或没有心肌坏死的淋巴细胞浸润[40]。本研究发现,有4例患者接受了心肌活检,均显示心脏被淋巴细胞和/或巨噬细胞浸润,这可能与继发于心肌组织细胞的传导系统的炎症变化有关[32]。因此,建议使用帕博利珠单抗的患者在治疗开始和随访时进行连续心功能相关检查,以便早期预防或及时干预相关ADR。
[10] INAYAT F,MASAB M,GUPTA S,et al. New drugs and new toxicities:pembrolizumab-induced myocarditis[J/OL]. BMJ Case Rep,2018[2021-02-24]. http://dx.doi.org/10. 1136/bcr-2017-223252.
[11] NASR F,EL RE,MAALOUF G,et al. Severe ophthalmoplegia and myocarditis following the administration of pembrolizumab[J]. Eur J Cancer,2018,91:171-173.
[12] KATSUME Y,ISAWA T,TOI Y,et al. Complete atrioventricular block associated with pembrolizumab-induced acute myocarditis:the need for close cardiac monito- ring[J]. Intern Med,2018,57(21):3157-3162.
[13] MARTINEZ-CALLE N,RODRIGUEZ-OTERO P,VILLAR S,et al. Anti-PD1 associated fulminant myocarditis after a single pembrolizumab dose:the role of occult pre-existing autoimmunity[J]. Haematologica,2018,103(7):e318-e321.
[14] LOPEZ EM,DUNN S,MAZIMBA S. Malignant arrhythmias in autoimmune myocarditis secondary to immune checkpoint blockade treatment[J]. J Am Coll Cardiol,2018,71(11):A2375.
[15] LAUBLI H,BALMELLI C,BOSSARD M,et al. Acute heart failure due to autoimmune myocarditis under pembrolizumab treatment for metastatic melanoma[J]. J Immunother Cancer,2015,3(1):11.
[16] 張慧,别自东,杜皓洁.帕博利珠单抗治疗转移性黑色素瘤致4级心肌炎1例[J].国际医药卫生导报,2019,25(19):3295-3297.
[17] 胡扬,李娇菊,孙雯娟,等.帕博利珠单抗致免疫性心肌炎1例[J].中国医院药学杂志,2020,40(14):1600-1602.
[18] HEINZERLING L,OTT PA,HODI FS,et al. Cardiotoxicity associated with CTLA4 and PD1 blocking immunotherapy[J]. J Immunother Cancer,2016,4:50.
[19] 卫生部.药品不良反应报告和监测管理办法[J].中国药事,2004,18(4):203-205.
[20] SURY K,PERAZELLA MA,SHIRALI AC. Cardiorenal complications of immune checkpoint inhibitors[J]. Nat Rev Nephrol,2018,14(9):571-588.
[21] TARRIO ML,GRABIE N,BU DX,et al. PD-1 protects against inflammation and myocyte damage in T cell-mediated myocarditis[J]. J Immunol,2012,188(10):4876- 4884.
[22] OKAZAKI T,TANAKA Y,NISHIO R,et al. Autoantibodies against cardiac troponin Ⅰ are responsible for dilated cardiomyopathy in PD-1-deficient mice[J]. Nat Med,2003,9(12):1477-1483.
[23] WANG J,OKAZAKI IM,YOSHIDA T,et al. PD-1 deficiency results in the development of fatal myocarditis in MRL mice[J]. Int Immunol,2010,22(6):443-452.
[24] ROMOND EH,JEONG JH,RASTOGI P,et al. Seven- year follow-up assessment of cardiac function in NSABP B-31,a randomized trial comparing doxorubicin and cyclophosphamide followed by paclitaxel(ACP)with ACP plus trastuzumab as adjuvant therapy for patients with node-positive,human epidermal growth factor receptor 2-positive breast cancer[J]. J Clin Oncol,2012,30(31):3792-3799.
[25] ADVANI PP,BALLMAN KV,DOCKTER TJ,et al.Long-term cardiac safety analysis of NCCTG N9831(al- liance)adjuvant trastuzumab trial[J]. J Clin Oncol,2016,34(6):581-587.
[26] 董爽,胡勝,欧武陵,等.免疫检查点抑制剂的心脏毒性及其机制[J].肿瘤防治研究,2018,45(11):858-863.
[27] 崔亚萌,齐新,魏丽萍,等.顺铂心脏毒性的研究进展[J].现代药物与临床,2017,32(2):351-355.
[28] JOHNSON DB,BALKO JM,COMPTON ML,et al. Fulminant myocarditis with combination immune checkpoint blockade[J]. N Engl J Med,2016,375(18):1749-1755.
[29] LYON AR,YOUSAF N,BATTISTI N,et al. Immune checkpoint inhibitors and cardiovascular toxicity[J]. Lancet Oncol,2018,19(9):e447-e458.
[30] RIBAS A,PUZANOV I,DUMMER R,et al. Pembrolizumab versus investigator-choice chemotherapy for ipilimumab-refractory melanoma(KEYNOTE-002):a randomised,controlled,phase 2 trial[J]. Lancet Oncol,2015,16(8):908-918.
[31] MOSLEHI JJ,SALEM JE,SOSMAN JA,et al. Increased reporting of fatal immune checkpoint inhibitor-associated myocarditis[J]. Lancet,2018,391(10124):933.
[32] ATALLAH-YUNES SA,KADADO AJ,KAUFMAN GP,et al. Immune checkpoint inhibitor therapy and myocarditis:a systematic review of reported cases[J]. J Cancer Res Clin Oncol,2019,145(6):1527-1557.
[33] JAIN V,BAHIA J,MOHEBTASH M,et al. Cardiovascular complications associated with novel cancer immunotherapies[J]. Curr Treat Options Cardiovasc Med,2017,19(5):36.
[34] JANARDHANAN R. Myocarditis with very high troponins:risk stratification by cardiac magnetic resonance[J]. J Thorac Dis,2016,8(10):E1333-E1336.
[35] MAHMOOD SS,FRADLEY MG,COHEN JV,et al. Myocarditis in patients treated with immune checkpoint inhibitors[J]. J Am Coll Cardiol,2018,71(16):1755- 1764.
[36] MIR H,ALHUSSEIN M,ALRASHIDI S,et al. Cardiac complications associated with checkpoint inhibition:a systematic review of the literature in an important emerging area[J]. Can J Cardiol,2018,34(8):1059-1068.
[37] NIEMINEN MS,HEIKKILA J,KARJALAINEN J. Echocardiography in acute infectious myocarditis:relation to clinical and electrocardiographic findings[J]. Am J Cardiol,1984,53(9):1331-1337.
[38] PALASKAS N,LOPEZ-MATTEI J,DURAND JB,et al.Immune checkpoint inhibitor myocarditis:pathophysiological characteristics,diagnosis,and treatment[J]. J Am Heart Assoc,2020,9(2):e13757.
[39] FUNG G,LUO H,QIU Y,et al. Myocarditis[J]. Circ Res,2016,118(3):496-514.
[40] ASNANI A. Cardiotoxicity of immunotherapy:incidence,diagnosis,and management[J]. Curr Oncol Rep,2018,20(6):44.
[41] 王汉萍,宋鹏,斯晓燕,等.危重及难治性免疫检查点抑制剂相关毒性反应诊治建议及探索[J].中国肺癌杂志,2019,22(10):605-614.
[42] MORRIS GS,GALLAGHER GH,BAXTER MF,et al.Pulmonary rehabilitation improves functional status in oncology patients[J]. Arch Phys Med Rehabil,2009,90(5):837-841.
[43] VARRICCHI G,MARONE G,MERCURIO V,et al. Immune checkpoint inhibitors and cardiac toxicity:an emerging issue[J]. Curr Med Chem,2018,25(11):1327-1339.
[44] THOMPSON JA,SCHNEIDER BJ,BRAHMER J,et al.NCCN Guidelines insights:management of immunotherapy-related toxicities,version 1.2020[J]. J Natl Compr Canc Netw,2020,18(3):230-241.
[45] 中国临床肿瘤学会指南工作委员会.中国临床肿瘤学会(CSCO)免疫检查点抑制剂相关的毒性管理指南:2019[M].北京:人民卫生出版社,2019:72-74.
[46] HAANEN J,CARBONNEL F,ROBERT C,et al. Management of toxicities from immunotherapy:ESMO Clinical Practice Guidelines for diagnosis,treatment and follow-up[J]. Ann Oncol,2018,29(Suppl 4):v264-v266.
[47] BRAHMER JR,LACCHETTI C,THOMPSON JA. Management of immune-related adverse events in patients treated with immune checkpoint inhibitor therapy:American Society of Clinical Oncology Clinical practice guideline summary[J]. J Oncol Pract,2018,14(4):247-249.
[48] KWON HJ,COTE TR,CUFFE MS,et al. Case reports of heart failure after therapy with a tumor necrosis factor antagonist[J]. Ann Intern Med,2003,138(10):807-811.
[49] 趙一贺,王虹剑,宋卫华.免疫检查点抑制剂相关心脏毒性的研究进展[J].中国循环杂志,2020,35(5):518-520.
[50] 张志仁.免疫检查点抑制剂及其心血管不良反应研究进展[J].药学进展,2018,42(7):492-499.
(收稿日期:2020-09-16 修回日期:2021-02-25)
(编辑:邹丽娟)
