采用UHPLC-MS和质量亏损过滤技术分析二苯乙烯苷在大鼠体内的代谢产物和代谢途径
2021-04-27梁幼玲史旭华白俊其黄志海徐文黄娟丘小惠
梁幼玲 史旭华 白俊其 黄志海 徐文 黄娟 丘小惠


摘 要 目的:分析二苯乙烯苷在大鼠体内的代谢产物并推测代谢途径。方法:将雄性SD大鼠随机分为血浆组(n=3)、尿液组(n=3)、胆汁组(n=3)和组织组(n=9),各组大鼠均单次灌胃二苯乙烯苷200 mg/kg,分别收集给药后10、30 min和1、1.5、2、4 h的血浆,给药后0~6 h的尿液,给药后0~4 h的胆汁以及给药后30 min和1、2 h(每个时间点3只)的心、肝、脾、肺、肾、胃组织样品,经甲醇沉淀蛋白后,采用超高效液相色谱-四极杆-静电场轨道阱高分辨质谱联用技术和质量亏损过滤技术联合分析、鉴定各样本中的代谢产物,推测代谢途径。结果:从血浆、尿液、胆汁、心、肝、脾、肺、肾、胃样品中分别检出6、7、11、1、5、1、3、4、4个代谢产物,包括Ⅰ相代谢(如水解、加氢、羟化)产物2个、Ⅱ相代谢(如葡萄糖醛酸结合和硫酸化)产物18个,其中葡萄糖醛酸结合产物有12个。结论:二苯乙烯苷在胆汁中的代谢产物种类居多,以Ⅱ相代谢产物二苯乙烯苷的葡萄糖醛酸结合产物为主;代谢途径主要涉及葡萄糖水解、加氢、羟化、葡萄糖醛酸结合、硫酸化反应等。
关键词 二苯乙烯苷;超高效液相色谱-四极杆-静电场轨道阱高分辨质谱联用技术;质量亏损过滤技术;代谢产物;大鼠
中图分类号 R969.1 文献标志码 A 文章编号 1001-0408(2021)06-0675-07
ABSTRACT OBJECTIVE: To analyze the metabolites of tetrahydroxystilbene glucoside (THSG) and speculate its metabolism pathway in rats. METHODS: Male SD rats were randomly divided into plasma group (n=3) , urine group (n=3), bile group (n=3), and tissue group (n=9). Each group was given single dose of THSG 200 mg/kg intragastrically. Plasma samples 10, 30 min and 1, 1.5, 2, 4 h after medication, the unrine 0-6 h after medication, the bile 0-4 h after medication, the tissue of heart, liver, spleen, lung, kidney and stomach 30 min and 1,2 h after medication (3 at each time point) were collected respectively. After precipitated with methanol, the metabolites of samples were analyzed and identified by UHPLC-Q-Exactive Orbitrap MS and mass loss filtration (MDF). Its metabolism pathway was speculated. RESULTS: In the blood, urine, bile, heart, liver, spleen, lung, kidney, stomach samples, 6, 7, 11, 1, 5, 1, 3, 4, 4 metabolites were detected, including two phase Ⅰ (hydrolysis, hydrogenation and hydroxylation) metabolites, 18 phase Ⅱ (glucuronic acid binding and sulfation) metabolites. There were 12 glucuronic acid binding products. CONCLUSIONS: Most of the metabolites of THSG are found in bile, mainly glucuronic acid binding products of phase Ⅱ metabolite THSG; main metabolic pathways involve glucose hydrolysis, hydrogenation, hydroxylation, glucuronic acid binding and sulfation.
KEYWORDS Tetrahydroxystilbene glucoside; UHPLC-Q-Exactive Orbitrap MS; Mass defect filter; Metabolite; Rats
二苯乙烯苷(Tetrahydroxystilbene glucoside,THSG)为多羟基茋类化合物,化学名为2,3,5,4′-四羟基二苯乙烯-2-O-β-D-葡萄糖苷,是中药何首乌中的特有成分[1]。现代研究表明,THSG具有抗衰老、降低胆固醇、提高免疫功能、防治动脉硬化、保肝、抗肿瘤等多重药理作用[2-3]。但THSG单体的体内代谢途径尚不清晰,故有必要对其代谢产物和代谢途径进行分析鉴定,为THSG的药效物质基础研究及代谢机制研究提供依据。
目前,液相色谱-串联质谱技术(LC-MS/MS)在探讨药物代谢特征、确定药物代谢物结构和代谢途径等领域中被广泛应用,已成为药物代谢分析研究的首选手段之一[4-6]。超高效液相色谱-四极杆-静电场轨道阱高分辨质谱联用技术(UHPLC-Q-Exactive Orbitrap MS)具有灵敏度高、分辨率高、快速准确等特点,在鉴定和辨识复杂生物样品的微量药物代谢产物时具有极大优势[7]。近年来,许多质谱数据挖掘技术如提取离子流技术、中性丢失过滤技术、产物离子过滤技术等得到较大程度的开发和应用[8]。其中,质量亏损过滤技术(MDF)是一种基于高分辨质谱数据的过滤技术,是以母体药物和核心亚结构作为过滤模板,对复杂生物基质中药物代谢产物进行快速检测的方法,能够有效去除干扰离子,在一定程度上可以排除假阳性结果,从而提高目标筛选的准确性[9]。由于MDF在代谢产物分析中的独特优势,使其得以快速发展,越来越多地被应用于药物代谢分析研究中[10-11]。基于此,本文采用UHPLC-Q-Exactive Orbitrap MS和MDF技術分析THSG在大鼠体内的代谢产物,推测代谢途径,为进一步阐明其药效物质基础和药理作用机制提供参考。
1 材料
1.1 主要仪器
本研究所用主要仪器包括Q Exactive PlusTM组合型四极杆Orbitrap质谱仪(美国Thermo Fisher Scientific公司)、Ultimate 3000型UHPLC系统(美国Dionex公司)、LSE型涡旋混合器(美国Corning公司)、LK/CSJ-20型超声清洗器(成都老肯科技股份有限公司)、5430R型高速冷冻离心机(德国Eppendorf公司)、RODI-220B1型纯水机(广州誉维生物科技仪器有限公司)、BT-125D型十万分之一电子天平[赛多利斯科学仪器(北京)有限公司]等。
1.2 主要药品与试剂
THSG对照品(批号HSW191102,纯度≥99.5%)购自桂林益天成生物科技有限公司,顺式二苯乙烯苷对照品(cis-THSG,批号P27A11F107214,纯度≥98%)购自上海源叶生物科技有限公司,肝素钠购自上海如吉生物科技有限公司,甲醇、乙腈(色谱级)均购自德国Merck公司,甲酸(色谱级)购自美国Thermo Fisher Scientific公司;其余试剂均为分析纯或实验室常用规格,水为超纯水。
1.3 动物
SPF级SD大鼠,雄性,体质量(220±20)g,购自南方医科大学实验动物中心,动物生产许可证号为SCXK(粤)2016-0041。
2 方法
2.1 溶液的配制
称取THSG对照品适量,加水溶解,稀释制成质量浓度为60 mg/mL的溶液,振荡混匀,避光,备用。
2.2 分组与给药
将18只雄性SD大鼠随机分为血浆组(n=3)、尿液组(n=3)、胆汁组(n=3)和组织组(n=9)。实验前,所有大鼠均于SPF级屏障环境适应性饲养1周,自由摄食、饮水;给药前禁食12 h,各组大鼠均单次灌胃THSG溶液200 mg/kg[12]。
2.3 生物样品采集与处理
2.3.1 血浆 分别在给药后10、30 min和1、1.5、2、4 h时采集血浆组大鼠眼眶血0.3 mL,置于涂有肝素钠的1.5 mL离心管中,于4 ℃下以3 000 r/min离心10 min,分离血浆,合并同一只大鼠不同时间点的血浆样品,混匀,于-80 ℃冰箱中保存。
2.3.2 尿液 尿液组大鼠饲养于代谢笼中,收集给药后0~6 h的尿液,于-80 ℃冰箱中保存。
2.3.3 胆汁 给药后,胆汁组大鼠腹腔注射乌拉坦(1 g/kg)麻醉,通过胆管插管手术收集给药后0~4 h的胆汁,于-80 ℃冰箱中保存。
2.3.4 组织 组织组大鼠分别于给药后30 min和1、2 h腹腔注射10%水合氯醛(0.04 mL/kg)麻醉,每个时间点各3只,分离心、肝、脾、肺、肾、胃,用生理盐水洗净,滤纸吸干水分,于-80 ℃冰箱中保存。
2.4 样品预处理
2.4.1 血浆样品 取血浆样品40 μL,加入4倍体积的甲醇涡旋混匀以沉淀蛋白,于4 ℃下以15 000 r/min离心30 min,取上清液5 μL进行分析。
2.4.2 尿液/胆汁样品 取尿液/胆汁样品100 μL,加入3倍体积的甲醇涡旋混匀以沉淀蛋白,于4 ℃下以15 000 r/min离心30 min,取上清液5 μL进行分析。
2.4.3 组织样品 取各组织样品,加入3倍量(g/mL)生理盐水,在冰浴下匀浆,超声(功率280 W,频率40 kHz)10 min,于4 ℃下以15 000 r/min离心30 min,取上清液100 μL,再加入3倍体积的甲醇涡旋混匀以沉淀蛋白,于4 ℃下以15 000 r/min离心30 min,取上清液5 μL进行分析。
2.5 液相条件
以Acquity UPLC HSS T3(100 mm×2.1 mm,1.8 μm)为色谱柱,以0.1%甲酸水溶液(A)-乙腈(B)为流动相进行梯度洗脱(0~2 min,10%B→15%B;2~4 min,15%B→20%B;4~8 min,20%B→30%B;8~10 min,30%B→40%B;10~11 min,40%B→60%B;11~12 min,60%B→70%B),流速为0.2 mL/min,柱温为35 ℃,自动进样器温度为4 ℃,进样量为5 μL。
2.6 质谱条件
以组合型四极杆Orbitrap质谱仪进行检测;离子源为加热型电喷雾离子源,离子源温度为350 ℃;碰撞能量为25、35、45 eV;鞘气流速为40 arb;辅助气为15 arb;喷雾电压为2.5 kV;辅助气温度为350 ℃;采集模式为负离子模式,质谱检测模式为全扫描/数据依赖二级扫描(Full mass/dd-MS2);Full mass分辨率为70 000,监测离子扫描范围为m/z 100~1 200;dd-MS2分辨率为17 500,动态排除时间为10.0 s。
2.7 数据处理方法
将样品质谱数据文件导入Compound Discovery 2.1软件,以THSG和THSG苷元(THS)为过滤模板,分别设定质量范围和质量亏损范围为50 Da和50 mDa,误差值<3 ppm,通过与空白生物样品比较,排除内源性因素干扰,得到处理数据集。结合体内药物代谢规律,根据精确相对分子质量的高分辨质谱信息、碎片离子信息并结合相关文献,筛选代谢产物相关信息,推测代谢途径[13]。
3 结果
3.1 THSG对照品的质谱裂解规律
在负离子模式下,THSG的准分子离子峰[M-H]-为m/z 405.119 45,推测分子式为C20H22O9,二级质谱图中出现碎片离子m/z 243.066 13、137.023 19、149.022 84、215.070 13、225.054 76、173.059 37、93.032 98。其中,主要碎片離子m/z 243.066 13(C14H12O4)系由THSG脱去一分子葡萄糖残基(C6H10O5)形成THS碎片离子峰,结合文献[14]报道,可推测THSG的质谱裂解途径,详见图1。
由图1可见,THSG中碎片离子m/z 225.054 76、215.070 13分别由m/z 243.066 13丢失1分子H2O、1分子CO形成,由于THS中没有直接脱去H2O和CO的基团,推测THS可能由于羟基取代苯环首先发生重排成醌式结构后,再脱去小分子基团形成较为稳定的碎片离子。m/z 149.022 84为脱去苯环后所形成的碎片离子,m/z 137.023 19为THS发生醌式重排后双键位置断裂且多个羰基基团脱去CO后形成的碎片离子。m/z 215.070 13脱去1分子C2H2O中性分子形成m/z 173.059 37。
3.2 THSG代谢产物的识别与鉴定
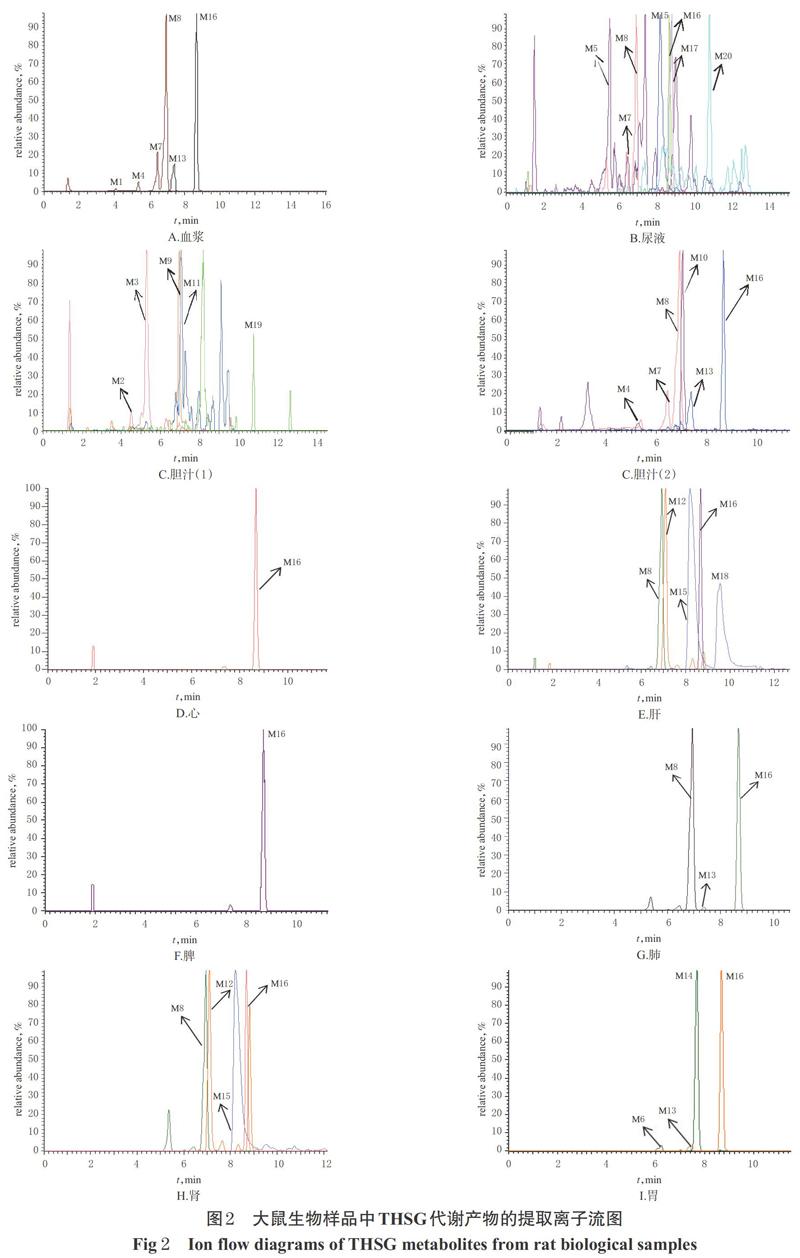
从大鼠血浆、尿液、胆汁、组织样品中共识别、鉴定出代谢产物20个,其中血浆、尿液、胆汁、心、肝、脾、肺、肾、胃样品中分别检出6、7、11、1、5、1、3、4、4个代谢产物,包括Ⅰ相代谢(如水解、加氢、羟化)产物2个、Ⅱ相代谢(如葡萄糖醛酸结合和硫酸化)产物18个,结果见图2(胆汁中的代谢产物出峰时间接近,峰形重叠不易辨别,故该样品以2张提取离子流图表示)、表1。
3.2.1 M13、M16 M16的准分子离子峰[M-H]-分别为m/z 405.118 38、405.118 74,保留时间及质谱裂解规律与原型化合物一致,因此将其鉴定为THSG。M13具有与原型化合物类似的二级碎片离子,但保留时间不同,推测其可能为THSG的同分异构体,经过与对照品对比,将M13鉴定为cis-THSG。
3.2.2 M11 M11的准分子离子峰[M-H]-为m/z 485.074 62,推测分子式为C20H22O12S,与原型化合物分子组成相比增加了80 Da(SO3)。其二级特征性碎片离子m/z 243.065 12、405.117 86,与THSG特征碎片离子基本一致,推测M11为THSG的硫酸化代谢产物。
3.2.3 M1、M4、M7、M8 M1、M4、M7、M8的准分子离子峰[M-H]-分别为m/z 581.149 90、581.150 15、581.150 70、581.150 21,推测分子式均为C26H30O15,均与原型化合物分子组成相比增加了176 Da。在二级质谱图中,均出现了碎片离子m/z 243.065 09、405.117 00,推测这4个化合物均为THSG的葡萄糖醛酸结合产物[15-16]。
3.2.4 M2、M3 M2、M3的准分子离子峰[M-H]-均为m/z 661.106 14,推测分子式均为C26H30O18S,其分子组成与M11(C20H22O12S)相比增加了176 Da(C6H8O6),与M1、M4、M7、M8分子组成(C26H30O15)相比增加了80 Da。其二级特征性碎片离子包括m/z 243.065 11、485.073 85等,推测M2、M3均为THSG的硫酸化及葡萄糖醛酸结合产物。
3.2.5 M9、M12、M17 M9、M12、M17的准分子离子峰
[M-H]-分别为m/z 419.097 02、419.097 84、419.098 91,推测分子式均为C20H20O10,其均较二级碎片离子m/z 243.065 06增加了176 Da,推测M9、M12、M17均为THS的葡萄糖醛酸结合产物。
3.2.6 M5 M5的准分子离子峰[M-H]-为m/z 595.130 49,推测分子式为C26H28O16。与M9、M12、M17分子组成(C20H20O10)相比增加了176 Da。其二级特征性碎片離子为m/z 243.066 07、419.097 93,推测M5为THS双葡萄糖醛酸结合产物。
3.2.7 M20 M20的准分子离子峰[M-H]-为m/z 325.039 15,推测分子式为C14H14O7S。其二级特征性碎片离子为m/z 245.081 36、230.057 80,其中相对丰度最强的为m/z 245.081 36的碎片,与m/z 243.065 06分子组成相比增加了2 Da,推测THSG进入大鼠体内后通过水解脱糖形成THS,THS(C14H12O4,[M-H]-为m/z 243.065 09)碳碳双键加氢进一步转化成碳碳单键生成dihydro-THS(C14H14O4,[M-H]-为m/z 245.081 36),因在所有组织及体液样品中均未检测到THS及dihydro-THS,笔者认为这两种成分在体内易进一步发生结合反应,根据一般药物代谢规律及生成的系列代谢产物[17-18],推测THS、 dihydro-THS可能是后续代谢产物的中间转化体。M20与dihydro-THS分子组成相比增加了80 Da(SO3),综上推测M20为THSG的水解-加氢-硫酸化代谢产物。
3.2.8 M6、M14、M19 M6、M14的准分子离子峰[M-H]-分别为m/z 421.113 04、421.112 95,推测分子式均为C20H22O10,与原型化合物的分子组成相比增加了16 Da。其均生成了相同的二级特征性碎片离子m/z 259.060 15(C15H16O4),与THS分子组成相比增加了16 Da,推测M6、M14均为THSG的羟化产物。M19的准分子离子峰[M-H]-为m/z 421.113 77,推测分子式为C20H22O10,与dihydro-THS分子组成相比增加了176 Da,其二级特征性碎片离子为m/z 245.117 13,推测M19为THSG的水解-加氢-葡萄糖醛酸结合产物。
3.2.9 M15、M18 M15、M18的准分子离子峰[M-H]-分别为m/z 323.022 25、323.022 22,推测分子式均为C14H12O7S,二者与THS分子组成相比增加了80 Da,且均生成了相同的二级碎片离子m/z 243.065 11,推测M15、M18均为THS的硫酸化代谢产物。
3.2.10 M10 M10的准分子离子峰[M-H]-为m/z 597.144 47,推测分子式为C26H30O16,与M6、M14分子组成相比增加了176 Da,二级特征性碎片离子为m/z 259.060 21、421.112 27,推测M10为THSG的羟化-葡萄糖醛酸结合产物。
3.3 THSG在大鼠体内的代谢途径分析
20个代谢产物涉及的代谢反应有葡萄糖水解、加氢、羟化、葡萄糖醛酸结合、硫酸化反应等,推测THSG在大鼠体内主要代谢途径见图3。
4 讨论
THSG为茋类化合物,是中药何首乌的特征成分。本课题组前期已对生、制何首乌提取液在大鼠体内的主要成分及其代谢产物进行了鉴定分析,结果显示大部分代谢物与THSG或大黄素有关,且以Ⅱ相代谢产物为主[12]。何首乌提取液中的成分十分复杂,仅进行化合物结构鉴定不能明确体内代谢产物的来源,化合物代谢途径判断结果亦较为模糊。因此,本研究以THSG单体给药,考察其在大鼠血浆、尿液、胆汁、组织中的代谢情况。结果显示,在大鼠不同部位检测到的代谢产物有一定差异,从血浆、尿液、胆汁、心、肝、脾、肺、肾、胃样品中分别检出了6、7、11、1、5、1、3、4、4个代谢产物,包括Ⅰ相代谢产物2个、Ⅱ相代谢产物18个。已有研究表明,THSG作为何首乌主要活性成分之一,因其具有多个活泼的羟基结构,较易发生Ⅱ相代谢反应,主要排泄途径是胆汁[19],本研究在胆汁中检测到的代谢产物种类居多,且除检测到的原型化合物外,以Ⅱ相代谢产物THSG的葡萄糖醛酸结合产物为主。
对于代谢产物的鉴定,关键在于裂解途径的分析与鉴定以及通过研究药物原型及其代谢产物的裂解过程,比较碎片离子和分子离子的差异[20-21]。对于大部分代谢产物而言,可采用质谱方法根据其一级、二级质谱初步推测代谢产物结构,但仅凭m/z无法判断具体结合位置,故可通过核磁共振及其他分析手段进一步研究确证。本研究将高分辨质谱产生的海量质谱数据通过MDF技术的过滤作用获得更精炼的数据集,从而挖掘出更多THSG潜在的体内代谢产物。MDF技术的优势在于可有效地去除干扰离子、简化质谱解析、提高筛选目标物的准确率[22]。
综上,本研究采用UHPLC-Q-Exactive Orbitrap MS和MDF技术对THSG在大鼠体内的代谢产物进行分析与鉴定,通过分析各部位生物样品中代谢产物的分子式、保留时间并结合一级、二级质谱信息,共鉴定出THSG的20个代谢产物,推测该化合物在大鼠体内的代谢途径主要涉及葡萄糖水解、加氢、羟化、葡萄糖醛酸结合、硫酸化反应等,为进一步研究THSG的代谢产物以及作用机制提供了重要信息。
参考文献
[ 1 ] 陈冰冰,姜爱玲,张岩.何首乌有效成分二苯乙烯苷的药理活性研究进展[J].中国临床药理学与治疗学,2016,21(6):710-715.
[ 2 ] WANG XM,ZHAO LB,HAN TZ,et al. Protective effects of 2,3,5,4′-tetrahydroxystilbene -2-O-β-D-glucoside,an active component of Polygonum multiflorum Thunb,on experimental colitis in mice[J]. Eur J Pharmacol,2008,578(2/3):339-348.
[ 3 ] CHEUNG FW,LEUNG AW,LIU WK,et al. Tyrosinase inhibitory activity of a glucosylated hydroxystilbene in mouse melan:a melanocytes[J]. J Nat Prod,2014,77(6):1270-1274.
[ 4 ] SANDOR R,MIDLIK A,SEBRLOVA K,et al. Identification of metabolites of selected benzophenanthridine alkaloids and their toxicity evaluation[J]. J Pharm Biomed Anal,2016,121:174-180.
[ 5 ] BUCK A,LY A,BALLUFF B,et al. High-resolution MALDIFT-ICR MS imaging for the analysis of metabolites from formalinfixed,paraffin-embedded clinical tissue samples[J]. J Pathol,2015,237(1):123-132.
[ 6 ] WANG GW,BAO B,HAN ZQ,et al. Metabolic profile of fructus gardeniae in human plasma and urine using ultra high-performance liquid chromatography coupled with high-resolution LTQ-orbitrap mass spectrometry[J]. Xenobiotica,2016,46(10):901-912.
[ 7 ] 趙文靖,黄漠然,尚展鹏,等.丹参酮Ⅰ和丹参酮ⅡA在大鼠体内的代谢物研究[J].中国中药杂志,2018,43(1):174-182.
[ 8 ] 侯艳婷,王晓明,张家伟,等.高分辨质谱数据MDF技术的进展[J].天津中医药,2016,33(12):765-768.
[ 9 ] MA SG,ZHU MS. Recent advances in applications of li- quid chromatography-tandem mass spectrometry to the analysis of reactive drug metabolites[J]. Chem Biol Interact,2009,179(1):25-37.
[10] XING J,ZANG M,ZHANG H,et al. The application of high-resolution mass spectrometrybased data-mining tools in tandem to metabolite profiling of a triple drug combination in humans[J]. Anal Chim Acta,2015,897:34-44.
[11] TAO JH,ZHAO M,WANG DG,et al. UPLC-Q-TOF/MS-based screening and identification of two major bio- active components and their metabolites in normal and CKD rat plasma,urine and feces after oral administration of Rehmannia glutinosa Libosch extract[J]. J Chromatogr Biomed Appl,2015,1001:98-106.
[12] HUANG J,ZHANG JP,BAI JQ,et al. Chemical profiles and metabolite study of raw and processed polygoni multiflori radix in rats by UPLC-LTQ-Orbitrap MSn spectrometry[J]. Chin J Nat Med,2018,16(5):375-400.
[13] ZHANG J,GUO Q,WEI M,et al. Metabolite identification and pharmacokinetic profiling of isoflavones from black soybean in rats using ultrahigh-performance liquid chromatography with linear-ion-trap-orbitrap and triple- quadrupole tandem mass spectrometry[J]. J Agric Food Chem,2018,66(49):12941-12952.
[14] 徐文.液质联用技术在两种中药成分分析中的应用[D].广州:广州中医药大学,2015.
[15] LIN LF,LIN HM,YIN XB,et al. Characterization of the constituents in rat plasma after oral administration of radix polygoni multiflori extracts by ultra-performance li- quid chromatography/quadrupole time-of-flight mass spectrometry[J]. Biomed Chromatogr,2015,29(10):1541- 1547.
[16] 郭忠会,贾志鑫,陈奎奎,等.基于UPLC-Q-TOF-MS分析何首乌提取物体内外成分[J].中国中药杂志,2018,43(13):2796-2805.
[17] 刘震,徐风,王静哲,等.哈巴苷在大鼠体内代谢产物的鉴定与分析[J].中国药房,2017,28(10):1310-1315.
[18] 張亚洲,王涛,邹树良,等.芹菜素在大鼠体内代谢产物的鉴定与分析[J].中国药房,2016,27(4):479-482.
[19] BUENZ EJ. Aloin induces apoptosis in Jurkat cells[J]. Toxicol In Vitro,2008,22(2):422-429.
[20] 徐叶.雷公藤甲素及其衍生物雷腾舒药物代谢研究[D].北京:中国科学院大学,2019.
[21] 林佩,陆建美,张光远,等.何首乌活性成分在肝L-02细胞中吸收及代谢产物的LC-MS/MS定性分析[J].中国药学杂志,2015,50(12):1048-1053.
[22] 刘洁,李月婷,陈奕君,等.高分辨质谱数据处理策略在中药体内外成分检测和表征中的应用进展[J].药学学报,2021,56(1):113-129.
(收稿日期:2020-11-11 修回日期:2021-02-01)
(编辑:邹丽娟)
